294 (24)

Cząsteczki te mieszczą się w lukach strukturalnych i każda z nich ma w swym otoczeniu, dwa aniony SO|“ i dwie cząsteczki wody otaczającej jony Cua+.
Od wody koordynacyjnej, sieciowej i zeolitycznej należy odróżnić jeszcze „wodę’* konstytucyjną., występującą w strukturach kryształów w postaci grup hydroksylowych. Przykładem struktur zawierających grupy OH- są wodorotlenki: Ca(OH)2» brucyt Mg(OH)2, hydrargilit Al(OH)3, sole zasadowe Hg(OH)Cł, Bi(0H)2N03 i kwasy tlenowe (np. H3BO3). W strukturze tych związków nie można wyróżnić rzeczywistych cząsteczek wody. Mówimy o „wodzie” konstytucyjnej, ale właściwie cząsteczek wody nie ma w strukturze. Utrata wody konstytucyjnej podczas prażenia powoduje całkowitą zmianę struktury kryształu.
5.1.6. Wiązania atomowe w kryształach
Wiązanie atomowe, zwane inaczej homeopolarnym łub kowalencyjnym, polega na istnie* niu wiążących par elektronów należących jednocześnie do dwóch sąsiadujących z sobą atomów. Zewnętrzne powłoki elektronowe atomów, związanych z sobą wiązaniem atomowym, zachodzą wzajemnie na siebie i niektóre elektrony należą jednocześnie do dwóch atomów. W wiązaniu atomowym nie następuje wymiana elektronów jak w wiązaniu jonowym, lecz ich uwspólnienie (por. § 5.1.4).
Istnieje grupa kryształów, w których atomy są związane z sobą wyłącznie wiązaniami atomowymi. Przykładem substancji krystalicznych o wiązaniach wyłącznie atomowych są: diament C (rys. 3.42), krzem Si, węglik krzemu SiC (karborund). W strukturze diamentu każdy atom węgla jest tetraedrycznie otoczony przez cztery inne atomy, przy czym atomy wiążą się z sobą przez wspólne pary elektronów (rys. 5.5).
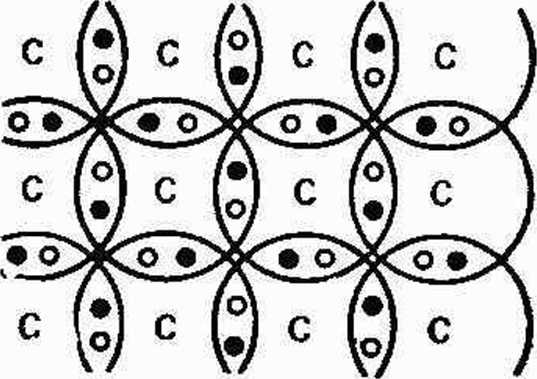
5.5. Wiązania mostkami elektronowymi w diamencie
Wiązania atomowe w krysztale, podobnie jak w cząsteczkach chemicznych, są kierunkowe. W diamencie skierowane są od środka do naroży regularnego czworościanu. Kąty między czterema kierunkami wiązań wychodzących z jednego atomu węgla wynoszą 109°28' (rys. 3.42). W kryształach atomowych, czyli w kryształach o wiązaniach wyłącznie atomowych, traci sens pojęcie cząsteczki chemicznej (podobnie jak w kryształach jonowych), gdyż nie możemy tu wyróżnić pojedynczych cząsteczek. Cały kryształ atomowy traktujemy jako jedną olbrzymią cząsteczkę. W sieciach krystalicznych o wiązaniach atomowych liczby koordynacyjne są zwykle .małe, gdyż są uzależnione od wartościowości pierwiastka (liczby dubletów elektronowych). Tetraedryczne struktury typu diamentu (strukturę taką wykazuje również krzem, german i cyna szara) są bardzo luźne i odpowia-
299
Wyszukiwarka
Podobne podstrony:
CB i rad 170 170 XI. BHP na niektóre odmiany raka. Wyniki te mieszczą się jednak w granicach błędu
img165 108 Wyróżnia się wiele odmian dyskusji, a każda z nich ma nieco inny przebieg i pozwala na ks
SWISSCONTRIBUTION ZADANIE 1 Klasa dzieli się na grupy. Każda z nich wybiera swojego lidera i tworzy
UCZĘ SIE LICZYĆ (30) Długie gąsienice proponują ci dodawanie. Każda z nich ma krótszą koleżankę, któ
50 51 1 1 Słonko się z gwiazdkami wita, Każdą z nich za rączkę chwyta. Wietrzyk się z chmurkami goni
DSCN8877 porcje. Ucząc się kilku definicji, każdą z nich na ogól opanowujemy oddzielnie. Jednak późn
W masowej produkcji wyrobów, składających się z wielu części, każdą z nich należy wykonać z
skanuj0189 (7) przyjąć, że struktury warstwowe są utworzone z cząsteczek kowalencyjnych rozciągający
więcej podobnych podstron