9
116 Enzymy
4.4. CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI ENZYMATYCZNEJ
Szybkość reakcji enzymatycznych zależy od stężenia substratu i enzymu oraz warunków, w jakich jest przeprowadzana (temperatura, pH, obecność aktywatorów, lub inhibitorów). W czasie badania wpływu danego czynnika na szybkość reakcji enzymatycznej, należy zadbać o to, żeby obserwowane zmiany szybkości reakcji wynikały jedynie ze zmiany wybranego czynnika, dlatego pozostałe powinny być niezmienne i optymalne dla danego enzymu.
Oznaczenie aktywności enzymu powinno być oparte na pomiarze początkowej szybkości reakcji - v0 (rozdział 4.2.). Należy podkreślić, że pomiar ilości produktu w dowolnym czasie trwania reakcji, bez sprawdzenia, że reakcja przebiega ze stałą szybkością, prowadzi do licznych błędów w oznaczaniu poziomu aktywności.
4.4.1. Wpływ stężenia substratu na szybkość reakcji enzymatycznej
Jednym z ważniejszych czynników, od którego zależy szybkość reakcji enzymatycznej jest stężenie substratu. Zależność ta ma charakter hiperboli: początkowo, wraz ze wzrostem stężenia substratu szybkość reakcji rośnie, a następnie osiąga stałą wartość (Rys. 4.6).
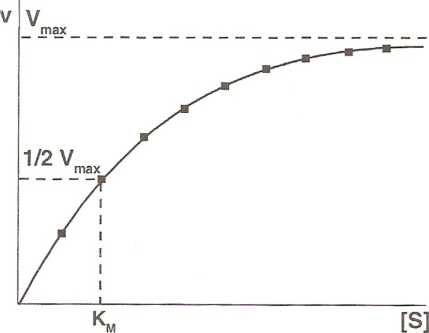
Rys. 4.6 Wykres zależności szybkości reakcji od stężenia substratu
Michaelis i Mentcn wykazali, że przyczyną obserwowanych zmian szybkości reakcji jest fakt powstawania w czasie reakcji enzymatycznej kompleksu cnzym-substrai (ES).
[e]+[s]ćz2 [es]—kł2~ > [e]+ [p]
k-t
[E] - stężenie enzymu, [S] - stężenie substratu, [ES] - stężenie kompleksu enzym-substrat, [Pj -stężenie produktu reakcji, k+|, k_i, k+2 - stałe szybkości odpowiednich reakcji.
W uproszczonym schemacie przebiegu reakcji enzymatycznej możemy wyróżnić kilka etapów: najpierw substrat łączy się z enzymem, w wyniku czego powstaje kompleks ES.
Wyszukiwarka
Podobne podstrony:
IMAG0331 (4) Czynniki wpływające na szybkość reakcji enzymatycznej S Stężenie enzymu - szybkość reak
DSC00033 (28) Czynniki wpływające na szybkość reakcji enzymatycznejStężenie enzymu Temperatura przeb
DSC00301 2 Czynniki wpływające na szybkoóć reakcji enzymatycznej f Stężenie substratu. . • Temperatu
DSC02178 4. Czynniki wpływające na szybkość reakcji . •/ rodzaj reagentów •/ stopień rozdrobnienia
CCF20120521�005 Czynniki wpływające na szybkość reakcji: Szybkość dyfuzji • Aby ot
Slajd16 < CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ PRZEPŁYWU POTENCJAŁU CZYNNOŚCIOWEGO WZDŁUŻ WŁÓKNA >O
zagadnienia Zagadnienia do egzaminu Enzymy, czynniki wpływające na ich aktywność i budowa. Substancj
116 Złożoność czynników wpływających na formowanie się odpływu w zlewni karpackiej wymaga szerokiego
DSC08250 (3) 1. Do czego służy olejek immersyjny >2.Wymienić czynniki wpływające na szybkość migr
DSC08469 (2) mm . Czynniki wpływające na szybkość >* irów
4. Wyjaśnij, co to jest rozpuszczalność. Podaj, jakie czynniki wpływają na szybkość
CCF20140528�016 Czynniki wpływające na szybkość wchłaniania ■ Właściwości substanc
Slajd15 < CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ PRZEPŁYWU POTENCJAŁU CZYNNOŚCIOWEGO WZDŁUŻ WŁÓKNA
WYKŁAD 2 enzymy cz 1 (25) AKTYWNOŚĆ ENZYMÓW MÓZE BYĆ REGULOWANACzynniki wpływające na szybkość re
więcej podobnych podstron