DSCN4041
Falowo-korpuskularny charakter elektronГіw
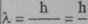
m-v p
ZaleЕјnoЕӣДҮ miДҷdzy korpuskulamД… i falowД… naturД… czД…stek podaЕӮ Louis de Broglie:
Rys. Schematyczne przedstawienie ruchu elektronu wokГіЕӮ jД…dra jako fali.
h = 6.626 s staЕӮa Plancka m - masa czД…stki
v - prДҷdkoЕӣДҮ poruszajД…cej siДҷ czД…stki

Fala de Broglie'*. odpowiadajД…ca jakoЕӣcigwo jakiemuЕӣ obiektowi o
skoЕ„czonych rozmiarach
Zasada Heisenberga
KonsekwencjД… dualistycznego (korpuskularno-falowego) charakteru materii jest zasada nieoznaczonoЕӣci Heisenberga, ktГіra stwierdza, Ејe nie jest moЕјliwe rГіwnoczesne okreЕӣlenie poЕӮoЕјenia i pДҷdu czД…stki z dowolnД… dokЕӮadnoЕӣciД…
Ax вҖў Ap > hj
Zasada nieoznaczonoЕӣci poЕӮoЕјenia i pДҷdu (takЕјe energii i czasu) gЕӮosi, Ејe nie jest moЕјliwe jednoczesne i dokЕӮadne wykonanie pomiarГіw wielkoЕӣci fizycznych, przy czym niepewnoЕӣДҮ tych oznaczeЕ„ wynika nie z niedoskonaЕӮoЕӣci aparatury badawczej, ale z natury mikroЕӣwiata. Oznacza to, Ејe nie moЕјna wyznaczyДҮ parametrГіw fizycznych, ktГіrych znajomoЕӣДҮ byЕӮaby rozstrzygajД…ca o falowej tub korpuskulamej naturze czД…stek.
Wyszukiwarka
Podobne podstrony:
DSCN4040 Chemia kwantowa Falowo-korpuskulamy charakter elektronГіw emisja elektronГіw i metali pod wpj
12 Obwody elektryczne prД…du przemiennego trГіjfazowego: WielkoЕӣci charakterystyczne i ich zaleЕјnoЕӣci.
26. Emisja ЕӣwiatЕӮa. 27. Dualizm falowo- korpuskulamy natury ЕӣwiatЕӮa. 28. Prom i en
img036 (3) ZALEЕ»NOЕҡCI MIДҳDZY ELEMENTAMI MACIERZY CHARAKTERYSTYCZNYCH
StaЕӮa MichaeЕӮisa (Km) jest charakterystyczna dla kaЕјdego enzymu i okreЕӣla zaleЕјnoЕӣДҮ miДҷdzy stДҷЕјeniem
8. Miary czasu i zaleЕјnoЕӣci miДҷdzy nimi. 9. Miary charakterystyc
CCF20111125�011 (3) 6.7. Moment elektromagnetyczny maszyny indukcyjnej6.7.1. ZaleЕјnoЕӣДҮ miДҷdzy mocД… i
DSC03056 (3) ZaleЕјno
12 Obwody elektryczne prД…du przemiennego trГіjfazowego: WielkoЕӣci charakterystyczne i ich zaleЕјnoЕӣci.
CHARAKTERYSTYKA PODSTAWOWYCH ELEMENTГ“W RYNKU - POPYTU, PODAЕ»Y I CENY. WZAJEMNE ZALEЕ»NOЕҡCI MIДҳDZ
Photo0010 2.1.2. Charakterystyki pomp tЕӮokowych CharakterystykД… pompy nazywamy zaleЕјnoЕӣДҮ miДҷdzy taki
NadzГіr UkЕӮad zaleЕјnoЕӣci miДҷdzy organami sprawujД…cymi funkcje administracji publicznej o charakterze
4. charakterystyk - zaleЕјnoЕӣci miДҷdzy wielkoЕӣciami, rozkЕӮadami
fytUGrx *---- i n Cto iwi wybranm przykЕӮadzie sens dualizmu falowo-korpuskularoego promieniowania
wiДҷcej podobnych podstron