DSCN4087 (2)
Wiązanie kowalencyjne spolaryzowane
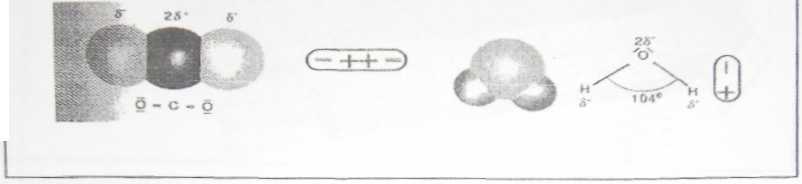
W cząsteczce C02 wszystkie wiązania pomiędzy atomem węgla
i atomami tlenu są spolaryzowane. C02 nie wykazuje charakteru dipolowego, ładunek dodatni ukryty jest we wnętrzu cząsteczki, a ładunki ujemne są po obu stronach cząsteczki, przez co nie powstaje dipol.
Cząsteczka H20 wykazuje wyraźną polarność i ma budowę nieliniową. Kąt pomiędzy wiązaniami powoduje, że oba dodatnie ładunki są zbliżone do siebie i tworzą dodatni biegun cząsteczki.
Wiązanie koordynacyjne
Jeżeli oba elektrony tworzące wiązanie kowalencyjne pochodzą od Jednego atomu, to wiązanie nazywa się koordynacyjne.

Budowa przestrzenna kationu NH
Wyszukiwarka
Podobne podstrony:
DSCN4086 (2) Wiązanie kowalencyjne spolaryzowane Cząsteczki z wiązaniami kowalencyjnymi spolaryzowan
Wiązanie kowalencuine spolaryzowane: * powstaje jeżeli tw*oizącc cząsteczkę
DSCN4081 (2) Wiązanie kowalencyjne A/yiązaipł© ko^^ńcy)ną-(at^rnowe)^^tęĘuje w cząsteczkach Każdy 2
DSCN4085 (2) Wiązanie kowalencyjne spolaryzowaneWiązanie kowalencyjne spolaryzowane Mechanizm powsta
Zdjęcie0217 Wiązania kowalencyjne spolaryzowane - polega na współużytkowania pary elektronów, ale ws
13 Proseminarium V Wiązania kowalencyjne spolaryzowane, jonowe i metaliczne Definicje i
P1050451 IWiązanie kowalencyjne spolaryzowane • Pośrednie między wiązaniem atomowym i jonowym. • Two
P1191307 9 Zdolność wiązania azotu cząsteczkowego mnin I - wszystkie gatunki drzewiaste 2. &nb
DSCN4082 (2) Wiązanie atomowe (kowalencyjne) Hz> Cl*, 02, N2 a* .-C-i ~ Sj
chemia mat bud032 Węglowodory Alkany Alkany są węglowodorami nasyconymi - wszystkie wiązania pomiędz
DSCN4078 (2) WIĄZANIA CHEMICZNE Charakter wi^/ama chemicznego i Jego wlnnolci zaletą od * &nbs
DSCN4080 (2) Wiązania chemiczne elektrony wspólne przesunięcie wspólnych elektronów w stronę Jednego
DSCN4088 (3) Wiązanie jonowe Jeżeli powstaje wiązanie jonowe, atomy dwóch łączących się pierwiastków
DSCN4089 (2) Wiązanie jonowe Każdy Jon Na* Jest otoczony przez 6 Jonów Cl Każdy Jon Cl Jest otoczon
DSCN4090 (2) Wiązanie metaliczne metale, stopy, i .związki międzymetaliczne Wiązanie metaliczne zwią
DSCN4092 I Wiązanie wodorowe Siły van der Waalsa < E„odolowc= 10-40 kJ/moK Ekov
Wykład 4W poszukiwaniu cząstek elementarnych & i Wszystkie substancje zbudowane są z pierwiastkó
więcej podobnych podstron