56814

Liczba wiązań chemicznych, jakie tworzy atom - to wartościowość pierwiastka w danym
związku chemicznym.
W stanie wolnym wartościowość pierwiastka wynosi 0; zależnie od rodzaju związku wartościowość tego samego pierwiastka może być różna.
Elektrony w cząsteczkach są opisywane za pomocą orbitali molekularnych czyli cząsteczkowych.


Orbitale molekularne powstają przez zbliżenie i „r się orbitali atomowych o podobnych energiach i symetrii względem osi łączącej dwa jądra atoi
Funkcję falową elektronu w cząsteczce A - B można więc traktować jako kombinację liniową funkcji falowych
opisujących orbitale atomowe:
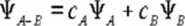
gdzie: cAl c„ - stałe
Rozwiązaniem funkcji falowej elektronu w cząsteczce są dwie funkcje własne: orbital wiążący a
oraz orbital antywiążący a*.
Orbitale te różnią s»ę energią, przy czym orbital wiążący charakteryzuje się mniejszą, a orbital antywiążący większą energią od energii wyjściowych orbitali atomowych.
Wyszukiwarka
Podobne podstrony:
DSC06739 RODZAJE WIĄZAŃ CHEMICZNYCH\J KOWALENCYJNE(ATOMOM E)—powstaje między gtnmami pierwiastko* ni
Plansze dydaktyczne CHEMIA(1) wiązania chemiczne w cząsteczkachwiązanie atomowe(KOWALENCYJNE) 0-0,4w
Wartosciowosc modulacji jest to Wartościowość modulacji jest to Wymierz odpowiedź a. &nb
Wykład 9 - WIĄZANIA CHEMICZNE W CZĄSTECZKACH WIELOATOMOWYCHWiązania i orbitale w cząsteczce BeH2 :_C
_wykład 8 WIĄZANIA CHEMICZNE_to jest WIĄZANIE CHEMICZNE? Wiązanie chemiczne: -
DSCN3972 S. Rzędowość reakcji chemicznej jest to: A. wartość stałej szybkości reak
Scan Pic0004 2 Utlenienie to reakcja chemiczna, w której jakiś atom (lub ich grupa) przechodzi z niż
DSC06745 WIĄZANIA n RZĘDU (WTÓRNE) SILAMI VAN DER WAALSA - (Energia wiązania £, “Nie jest to wiązani
więcej podobnych podstron