
Ilościowe oznaczenie glikogenu oraz badanie niektórych jego
właściwości
Cel ćwiczenia
Celem ćwiczenia jest zapoznanie się z podstawową wiedzą dotyczącą budowy,
funkcji i właściwości glikogenu jak również poznanie zasad najczęściej stosowanych
metod ilościowego oznaczania zawartości tego polisacharydu.
Wprowadzenie
Budowa glikogenu. Jest to silnie rozgałęziony polisacharyd zwierzęcy,
homopolimer zbudowany z reszt α-D-glukozy połączonych ze sobą wiązaniami α-1,4-
glikozydowymi, a w miejscach rozgałęzień α-1,6-glikozydowymi. Glikogen ma budowę
zbliżoną do składnika skrobi – amylopektyny, ale rozgałęzienia w jego cząsteczce są
liczniejsze i krótsze. Jedno rozgałęzienie przypada zwykle na 10-12 reszt glukozy.
Taka budowa cząsteczki glikogenu sprawia, że rozpuszcza się on lepiej w wodzie niż
amylopektyna. Wielkość cząsteczek glikogenu, jak też liczba i stopień rozgałęzień tego
wielocukru zależą od źródła, z którego został wyizolowany. Masa cząsteczkowa glikogenu
jest różna i waha się w granicach od kilkuset tysięcy do kilku milionów Da (masa
cząsteczkowa glikogenu w mięśniach ok. 1 000 000, a w wątrobie ok. 5 000 000 Da).
Występowanie i funkcje glikogenu
.
Jest to zapasowy polisacharyd odkładany w wątrobie
i w mniejszych ilościach w mięśniach. Zawartość glikogenu jest zależna od stanu
fizjologicznego organizmu, w wątrobie wynosi od 2 do 10%, a w mięśniach od 0,5 do
1,5% tkanki. Ze względu na dużą masę mięśni w porównaniu z masą wątroby w
organizmie przeważa jednak forma mięśniowa tego polisacharydu. Organizm ludzki może
zmagazynować nawet do 450 g glikogenu, z czego jedynie ok. 30 % znajduje się w
wątrobie. W komórce glikogen wraz z większością enzymów niezbędnych do jego syntezy
i degradacji jest zlokalizowany w postaci ziarnistości w cytoplazmie.
Glikogen w wątrobie służy przede wszystkim do utrzymania odpowiedniego poziomu
glukozy we krwi w przerwach pomiędzy posiłkami.
Glikogen w mięśniach stanowi
natomiast rezerwę glukozy wykorzystywanej do syntezy ATP podczas intensywnych
skurczów mięśni i nie bierze udziału w regulacji stężenia cukru we krwi.
Aktywność enzymów uczestniczących w syntezie i rozkładzie glikogenu podlega złożonej
regulacji przez hormony i inne czynniki.
Właściwości fizykochemiczne glikogenu. Podobnie jak pozostałe polisacharydy glikogen
należy do grupy nie zjonizowanych związków polarnych. Jako koloid hydrofilowy
rozpuszcza się w wodzie na zimno dając opalizujący roztwór. Możliwe jest to dzięki
występowaniu w jego cząsteczce licznych grup hydroksylowych, mogących łatwo tworzyć
wiązania wodorowe z cząsteczkami wody. W obecności soli nieorganicznych o znacznych
stężeniach oraz pod wpływem cieczy organicznych mieszających się z wodą glikogen
łatwo ulega wytrąceniu z roztworu. Dodanie do roztworu glikogenu soli obojętnej dobrze
zdysocjowanej, np. siarczanu amonowego lub chlorku sodowego, powoduje rozerwanie
wiązań wodorowych między grupami –OH polisacharydu a cząsteczkami wody
(dehydratacja), a samorzutnie tworzące się wewnątrz- i międzycząsteczkowe wiązania
doprowadzają do agregacji cząsteczek glikogenu i wytrącenia asocjatów z roztworu. Pod
wpływem rozpuszczalników organicznych, takich jak aceton czy alkohol, następuje
znaczne zmniejszenie stałej dielektrycznej roztworu (woda – 80, etanol – 24), co w
konsekwencji również prowadzi do zmniejszenia stopnia uwodnienia grup
1
hydroksylowych glikogenu i powoduje jego wytrącenie z roztworu. Glikogen z jodem
tworzy kompleks o barwie czerwonobrunatnej. Pozwala to na odróżnienie niektórych
polisacharydów (glikogen, skrobia) od innych, gdyż kompleksy takie mogą być
wytwarzane tylko przez cząsteczki o odpowiednio dużych wymiarach i uporządkowanej
strukturze. Boczne łańcuchy rozgałęzionej cząsteczki glikogenu tworzą układy spiralne, w
których środku występują wolne przestrzenie umożliwiające pomieszczenie cząsteczek
jodu. Charakterystyczna absorpcja jodu występuje jedynie w przypadku łańcuchów
zawierających, co najmniej 6 reszt polisacharydowych (jeden skręt spirali). Barwny efekt
jest tym silniejszy, im większe są cząsteczki polisacharydu, a więc im większa jest liczba
cząsteczek jodu związanego w kompleksie. Glikogen, jako polisacharyd nie wykazuje
właściwości redukujących. Stosunkowo łatwo ulega on hydrolizie kwasowej oraz
enzymatycznej z udziałem amylaz. Podczas zajęć laboratoryjnych hydroliza wiązań
glikozydowych będzie przeprowadzona w wysokiej temperaturze w obecności kwasu
solnego. Obecność uwolnionych w wyniku hydrolizy cukrów redukujących stanowi
podstawę najczęściej stosowanych metod oznaczeń ilościowych tego polisacharydu.
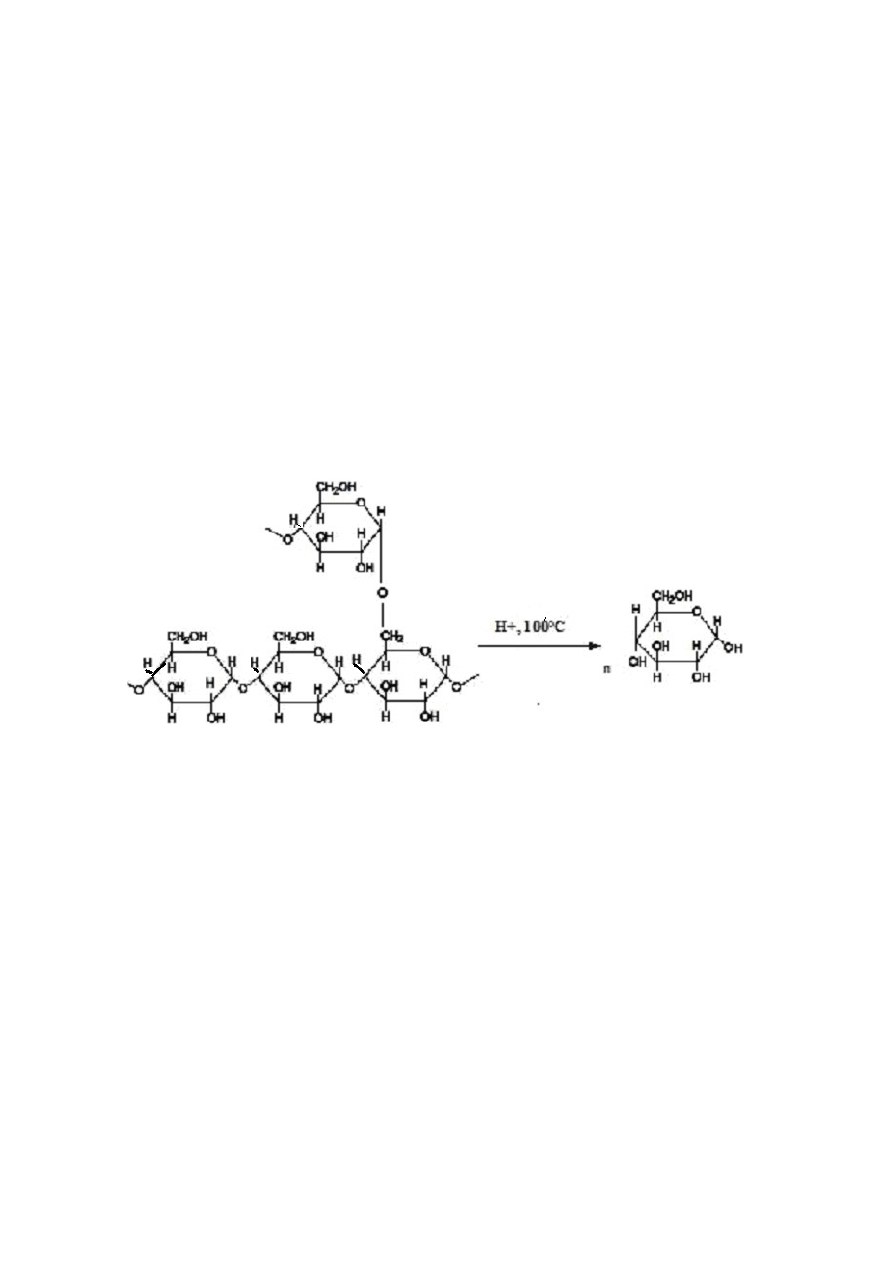
Rys. 1. Hydroliza kwasowa glikogenu
Zasada metody Somogyi i Nelsona (punkt a wykonania ćwiczenia).
G
lukoza redukuje w środowisku alkalicznym obecne w odczynniku miedziowym
(Somogyi) jony Cu
2+
do Cu
+
. Ilość powstałego w reakcji tlenku miedzi (I) oznacza się przy
użyciu odczynnika arsenomolibdenowego (Nelsona), który ulega redukcji do błękitu
molibdenowego. Natężenie powstałej niebieskiej barwy produktu jest proporcjonalne do
ilości wytworzonego Cu
2
O a tym samym do ilości powstałej podczas hydrolizy glikogenu
glukozy.
Zasada metody Benedicta (punkt b wykonania ćwiczenia). W środowisku alkalicznym
jony miedzi (II) ulegają pod wpływem glukozy redukcji do Cu(I), z roztworu wypada
żółty, pomarańczowy lub ceglastoczerwony osad tlenku miedzi(I). Z barwy i ilości osadu
można w przybliżeniu ocenić stężenie sacharydu w badanym roztworze.
Odczynniki
1. Roztwór glikogenu o stężeniu ok. 2 mg/1 ml.
2. Roztwór glikogenu o stężeniu 5 mg/ml.
2

3. Jod w jodku potasowym (10 g KI + 2,5 g I
2
w 1 l).
4. 2 M kwas solny.
5. 1 M wodorotlenek sodowy.
6. 2 M wodorotlenek sodowy.
7. Odczynnik Benedicta: 173 g cytrynianu sodowego i 100 g węglanu sodowego rozpuścić
w 800 ml ciepłej wody, uzupełnić wodą destylowaną do 850 ml. Przygotować
jednocześnie roztwór siarczynu miedziowego (17, 3 g w 100 ml wody destylowanej).
Zmieszać oba roztwory, całość uzupełnić wodą do 1000 ml.
8. Roztwór glukoamylazy o stężeniu dobranym do warunków ćwiczenia
9. Odczynnik Somogyi (miedziowy): rozpuścić 24 g bezwodnego węglanu sodu i 12 g
winianu sodowo-potasowego w 240 ml wody destylowanej. Dodać 4 g siarczanu miedzi
rozpuszczonego w 40 ml, po czym dodać 16 g kwaśnego węglanu sodu. Przygotować
równoległe roztwór siarczanu sodowego: rozpuścić 18 g bezwodnego siarczanu sodu w
500 ml wody, gotować, schłodzić. Zmieszać oba roztwory i uzupełnić wodą destylowaną
do 1000 ml.
10. Odczynnik Nelsona (arsenomolibdenowy): 25 g czterowodnego molibdenianu
amonowego rozpuścić w 450 ml wody destylowanej i ostrożnie dodać 21 ml stężonego
H
2
SO
4
. Oddzielnie rozpuścić 3 g kwaśnego arsenianu sodowego siedmiowodnego
(Na
2
HAsO
4
7H
2
O) w 25 ml wody destylowanej i przelać oba roztwory do kolby miarowej
na 500 ml. Uzupełnić do kreski wodą destylowaną.
Wykonanie
a) Oznaczanie stężenia glikogenu metodą Somogyi i Nelsona
Otrzymany w kolbie miarowej na 10 ml roztwór glikogenu (1) dopełnić wodą
destylowaną do kreski i wymieszać. Pobrać z kolby 2 ml roztworu do probówki, dodać 5
ml 2 M kwasu solnego (4), wymieszać i prowadzić hydrolizę glikogenu we wrzącej łaźni
wodnej przez 30 minut. Następnie próbę ochłodzić zimną wodą, zobojętnić hydrolizat
przez dodanie 5 ml 2 M wodorotlenku sodowego (6) i wymieszać. Do 2 probówek pobrać
po 1 ml uzyskanego hydrolizatu. Przygotować także próbę kontrolną, w której należy
zmieszać 0,5 ml 2 M kwasu solnego (4) i 0,5 ml 2 M wodorotlenku sodowego (6). Do
wszystkich trzech probówek odmierzyć po 1 ml odczynnika Somogyi (9), zamieszać i
wstawić do wrzącej łaźni wodnej dokładnie na 10 minut. Próby ochłodzić zimną wodą i
odmierzyć do nich po 1 ml odczynnika Nelsona (10), dokładnie wymieszać aż do
rozpuszczenia osadu tlenku miedzi (I) i ustania wydzielania pęcherzyków gazu (CO
2
).
Próby rozcieńczyć dodając po 7 ml wody destylowanej, wymieszać i po 10 minutach
zmierzyć w fotometrze absorbancję przy długości fali 520 nm wobec próby kontrolnej.
Odczyty z aparatu uśrednić a następnie odczytać z wcześniej przygotowanej krzywej
wzorcowej odpowiadające im stężenie glukozy.
b) Badanie niektórych właściwości glikogenu
1. Stopniowa hydroliza kwasowa glikogenu. Przygotować 8 probówek, do 4 z nich
odmierzyć po 1 ml 1 M wodorotlenku sodowego (5), a do 4 pozostałych po 1 ml wody.
Równolegle przygotować próbę do hydrolizy glikogenu: do probówki odmierzyć 10 ml
roztworu glikogenu (2) i 5 ml 2 M kwasu solnego, wymieszać i pobrać natychmiast po 1
ml tej mieszaniny do pierwszych probówek serii z 1 M wodorotlenkiem sodu oraz z wodą
(próby pobrane w czasie zerowym). Pozostałą część próby do hydrolizy umieścić we
wrzącej łaźni wodnej i po 5, 10 i 15 minutach pobierać po 1 ml mieszaniny do kolejnych
3
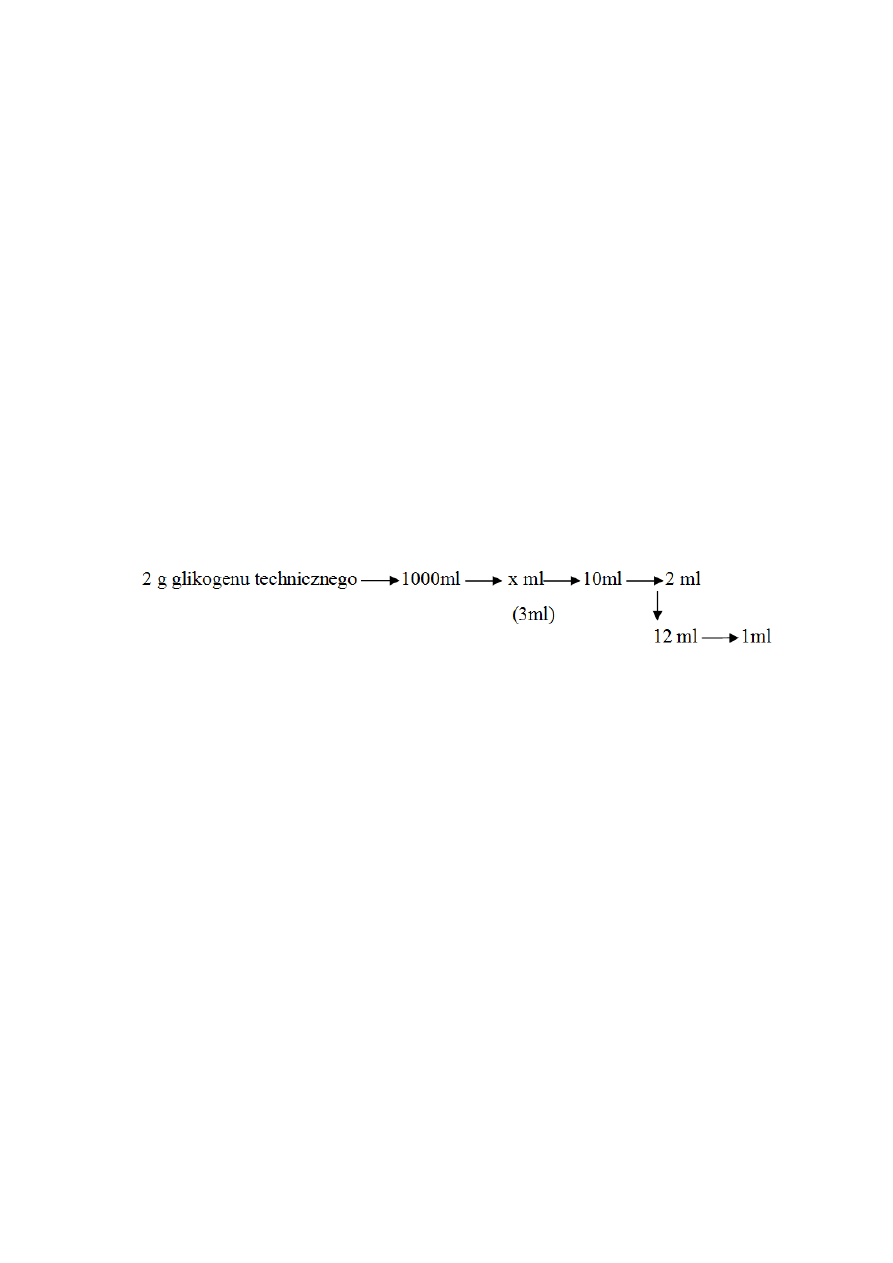
probówek serii z wodorotlenkiem sodowym i z wodą. Roztwory w probówkach z wodą po
pobraniu próby natychmiast potraktować 2 kroplami roztworu jodu w jodku potasu (3).
Następnie do probówek zawierających wodorotlenek sodowy i hydrolizat glikogenu dodać
po 1 ml odczynnika Benedicta (7), po wymieszaniu wstawić na dwie minuty do wrzącej
łaźni wodnej.
2. Hydroliza enzymatyczna glikogenu. Do probówki odmierzyć 2 ml glikogenu (2) i 1 ml
glukoamylazy (8), wymieszać i wstawić do łaźni wodnej o temp. 40°C na 10 minut.
Reakcję przerwać przez zakwaszenie 0,2 ml 2 M kwasu solnego (4), wymieszać.
Przygotować dwie probówki, do jednej z nich pobrać 1 ml tej mieszaniny, do drugiej 1 ml
glikogenu (2), do obu dodać po 1 ml odczynnika Benedicta (7), wymieszać i ogrzewać we
wrzącej łaźni wodnej przez 2 minuty.
Opracowanie wyników
W celu obliczenia czystości otrzymanego roztworu glikogenu należy na podstawie
średniej wartości absorbancji prób pełnych dokonać odczytu stężenia glukozy z krzywej
wzorcowej i uwzględnić podany podczas zajęć sposób rozcieńczenia preparatu glikogenu.
W obliczeniach należy także uwzględnić współczynnik 0,9 (162g/180g) pozwalający na
przeliczenie stężenia glukozy na stężenie glikogenu.
Przykładowe obliczenia na podstawie przedstawionego poniżej schematu rozcieńczenia
zadania kontrolnego:
2 g glikogenu technicznego (zawierającego zanieczyszczenia niecukrowe) rozpuszczono
w 1000 ml wody destylowanej; z tak przygotowanego roztworu studenci otrzymali w
formie zadania kontrolnego różne jego objętości (objętość podaje prowadzący ćwiczenia
po przyjęciu wyników absorbancji, w przedstawionym przykładzie 3ml) w kolbce
miarowej na 10ml, uzupełnionej do kreski wodą destylowaną.
Do hydrolizy pobrano 2 ml z kolby na 10 ml, po neutralizacji pH otrzymano mieszaninę o
objętości 12 ml, z której pobrano 1 ml do oznaczenia zawartości glukozy.
Przyjmijmy, ze średnia wartość absorbancji dla prób pełnych wyniosła 0,240 a odczytana
wartość z krzywej wzorcowej 90 μg glukozy, co po uwzględnieniu współczynnika 0,9 daje
nam 81 μg glikogenu.
Z analizy schematu rozcieńczenia otrzymanej próby wynika, skoro ze w 1 ml roztworu
pobranego do oznaczenia jest 81 μg glikogenu to w 12 ml 972 μg, tyle samo glikogenu
jest w 2 ml pobranego z kolby na 10 ml roztworu. W kolbie miarowej (10 ml) jest 4,86 mg
glikogenu i tyle samo w 3 ml wydanego zadania kontrolnego, zatem w 1000 ml:
3 ml –4,86 mg
1000 ml –x mg , x = 1620 mg=1,62 g, co odpowiada zawartości glikogenu w 1000 ml
przygotowanego roztworu glikogenu technicznego. Ze schematu rozcieńczeń wynika, że w
1000 ml rozpuszczono 2 g glikogenu technicznego, więc:
2,0 g – 100%
1,62 g – x%
Czystość glikogenu (%) w jego preparacie handlowym wynosi 81%.
4

B. 1. Należy dokonać obserwacji powstałego tlenku miedzi (I) w próbach, w których
przeprowadzono reakcję z odczynnikiem Benedicta. W próbach z wodą obserwować
stopniowy zanik barwy kompleksu glikogenu z jodem.
2. Dokonać obserwacji prób po reakcji z odczynnikiem Benedicta. Wyjaśnić potencjalne
różnice pomiędzy barwą tych prób.
Pytania
1. Do jakiej grupy związków należy glikogen? Omów występowanie i funkcje glikogenu.
2. Napisz fragment cząsteczki glikogenu. Wskaż i nazwij występujące tam wiązania.
3. W jaki sposób można dokonać hydrolizy glikogenu?
4. W jaki sposób można ilościowo oznaczyć glikogen? Podaj zasadę stosowanej na
ćwiczeniach metody.
5. Omów sposoby wytrącania glikogenu z roztworu.
6. Czy jod w kompleksie z glikogenem zmienia swoją wartościowość? Uzasadnij
odpowiedź.
7. Uzasadnij stopniową zmianę barwy roztworu glikogenu z odczynnikiem Benedicta i z
jodem w miarę reakcji: a) z kwasem solnym, b) z enzymem.
Literatura:
M. Somogyi. Notes on sugar determination. The Journal of Biological Chemistry,
Baltimore, 195: 19-23 (1952)
N. Nelson. A photometric adaptation of the Somogyi method for the determination of
glucose. The Journal of Biological Chemistry, Baltimore, 153: 375-381 (1944)
Krishnaveni, S., Theymoli Balasubramanian and Sadasivam, S. Sugar distribution in sweet
stalk Sorghum. Food Chemistry 15: 229-232 (1984).
5

6
Document Outline
- Ilościowe oznaczenie glikogenu oraz badanie niektórych jego właściwości
- Cel ćwiczenia
- Wprowadzenie
- Odczynniki
- Wykonanie
- a) Oznaczanie stężenia glikogenu metodą Somogyi i Nelsona
- b) Badanie niektórych właściwości glikogenu
- Opracowanie wyników
- Pytania
Wyszukiwarka
Podobne podstrony:
choroby spichrzania glikogenu i Nieznany
Glikogenogeneza i glikogenoliza
SUPERKOMPENSACJA ZASOBÓW MIĘŚNIOWEGO GLIKOGENU
Glikogen przemianyczII
Fosforylaza glikogenu
Glikogen przemiany
Regulacja glikogenozlizy w mieśniach, materiały farmacja, Materiały 3 rok, Od Ani, biochemia, bioche
7. Glikogenogeneza, Lekarski WLK SUM, lekarski, biochemia, węglowodany, Węglowodany-kolo
obrazy koncert jankiela
Metabolizm glikogenu, Notatki AWF, Biochemia
Glikogen główna postać transportowa u zwierząt, biochemia
Glikoglicerolipidy (budowa, występowanie oraz aktywność farmakologiczna)
10 03 dwa spojrzenia na koncert jankiela[1]
Koncert Jankiela
10) Ilościowe oznaczenie glikogenu oraz badanie niektórych jego właściwości
Glikogen, Fizjoterapia, Biochemia
Prognozowanie i Symulacje - Wyklady - Jankiewicz-Siwek - 2003 (25), ● STUDIA EKONOMICZNO-MENEDŻERSKI
Fosforylaza glikogenowa, Notatki AWF, Biochemia
jankiewicz
więcej podobnych podstron