W4
STREPTOMYCYNY
Rodzina antybiotyków:
Streptomycyna
Mannozylostreptomycyna
Dihydrostreptomycyna
Mannozylodihydrostreptomycyna
N-demetylostreptomycyna
Hydroksystreptomycyna
PROCES WYTWARZANIA STREPTOMYCYNY:
1967 r. -Singh et all opis procesu laboratoryjnego
Streptomyces griseus DTH2 - liofilizowane spory zmieszane z ziemią zostają umieszczone na płytkach Petriego lub butelkach Rouxa z agarem sojowym, inkubacja 2-3 tyg, w temp. 27°C
inokulum
I etap: kultury wegetatywne; 0,5-2 l kolby Erlenmayera, sojowe podłoże A
II etap: fermentator 5 l, sojowe podłoże B
proces właściwy- fermentator produkcyjny, podłoże B, pH 7-6,5-7,5, mieszanie, napowietrzanie (trofofaza, idiofaza)
oczyszczanie:
zawiesina pohodowlana
filtracja lub odwirowanie - przesącz (50 m3, 5,5 g/cm)
+ 50 m3 H2O
chromatografia jonowymienna
wymywanie związku EDTA, woda nasycona CO2, 2,5 M H2SO4
wodny roztwór siarczanu streptomycyny (2700 l, 90 g/cm)
dekoloryzacja na węglu aktywnym
zagęszczanie pod próżnią
suszenie
275 kg siarczanu streptomycyny 98% czystości
POSZUKIWANIE NOWYCH AMINOGLIKOZYDÓW
skrining + inżynieria genetyczna
mutageneza
modyfikacje chemiczne lub enzymatyczne
synteza chemiczna
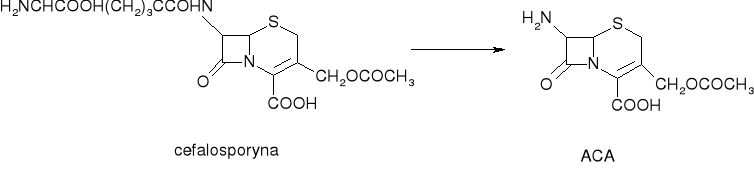
CEFALOSPORYNY
Antybiotyki β-laktamowe produkowane przez Cephalosporium (grzyb). Mechanizm działania analogiczny do penicylin (hamuje syntezę białka...). Poszczególne generacje cefalosporyn różnią się przenikalnością do OUN i odpornością w stosunku do β-laktamaz.
Proces wytwarzania FBC (Feed Batch Culture). W lecznictwie stosuje się ponad 50 cefalosporyn.
W4
CEFAMYCYNY
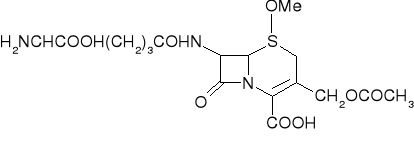
Cefamycyna C- Nocardia lactamdurans, Streptomyces clavuligerus; trwałe
Gram (-)- oporne na β-laktamazy
Cefoksytyna- zmodyfikowana cefamycyna (grupa tienacetylowa).
LINKOZAMIDY
Linkomycyna- Streptomyces lincolnensis, metylotioaminocukier + aminokwas, Gram (+) (Staphylococcus sp., Diplococcus sp. ) oraz beztlenowce; dobra przenikalność do tkanek i kości; działanie- hamowanie biosyntezy białka 50S.
ANTYBIOTYKI PEPTYDOWE
Blastycydyna S- Pyricularia oryzae, Streptomyces sp., rolnictwo
Bleomycyna, Bestatyna - terapia p/nowotworowa
Bleomycyna- hamowanie syntezy białek kwasów nukleinowych
Bestatyna- hamuje aminopeptydazy
ZWIĄZKI P/NOWOTWOROWE
Rośliny, mikroorganizmy, ssacze kultury tkankowe. Trudności przy procesie produkcji: toksyczność, wydzielanie, oczyszczanie; detoksyfikacja ścieków.
W4
Poszukiwanie i izolacja odpowiednich produktów- izolacja produktu.
Preskrining - linie P388 mysiej leukemii.
Testy in vitro sposób podania leku.
I faza badań klinicznych.
II faza badań klinicznych.
III i IV faza badań klinicznych.
Bezpieczeństwo przy produkcji leków cytotoksycznych- bariery biologiczne, filtry HEPA, czujniki, blokady, detoksyfikacja ścieków.
ANTRACYKLINY
Należą do najszerzej używanych związków p/nowotworowych.
Budowa: chromofor antrachinowy podstawiony jednym lub więcej cukrem.
Dannorubicyna (Daunomycyna)- Streptomyces coeruleorubidus
Doksorubicyna (Adriamycyna)- mutant; Streptomyces peucetius; szerokie spektrum działania
PROCES PRODUKCJI DAUNOMYCYNY
Streptomyces peucetius, glikozyd, 60-70 μg/ml daunomycyny, 5-15 μg/ml adriamycyny.
METODA I:
Skosy agarowe (10 dni, 26-27°C), kultury w kolbach (2 dni, mieszanie, napowietrzanie), 800 l fermentator (28°C, 67 h).
METODA II:
Kultury w 4 l kolbach (zamrożone mycelia, 28°C, 2,5 dnia), 100 l fermentator (30°C, 24h), 1000 l fermentator (12 dni), 10000 l fermentator (7-10 dni).
PROCES PRODUKCJI ADRIAMYCYNY
Agarowe skosy (26-27°C, 10 dni), homogenizacja zaszczepu i zawieszenie w wodzie, kultury w kolbach (48 h), wytrząsanie (28°C), 800 l fermentator (27°C, 67-145°C).
ANTYBIOTYKI NUKLEOZYDOWE
Najsilniejsze czynniki cytotoksyczne, hamują biosyntezę kwasów nukleinowych i białek, wykazują aktywność antybiotyczną, antywirusową, immunosupresyjną.
Produkcja: Streptomyces sp., Nocardia sp.
Enzymy cytotoksyczne:
L-asparaginaza- hamuje asparaginozależną biosyntezę białka i ewentualnie kwasów nukleinowych; limfocytowa leukemia u dzieci.
W4
CO JESZCZE BIOTECHNOLOGIA DAJE MEDYCYNIE?
PRZECIWCIAŁA MONOKLONALNE
diagnostyka, terapia chorób zakaźnych
badanie właściwości antygenowych białek
charakterystyka wirusów
transplantacja organów
KONIUGATY PRZECIWCIAŁO-LEK
indukowane wirusem komórki nowotworowe (limfoma myszy)
produkcja przeciwciał kozich (infekcja co 5 dni)
surowica- wysalanie 33% siarczanem amonu
frakcje immunoglobulin- odwirowanie, rozpuszczenie w buforze
trawienie pepsyną, 0,1 M octan sodu, pH 4,5, 16 h, 37°C
fragmenty (Fab)2
lek w postaci utlenionej, kowalencyjne wiązanie typu zasady Schiffa
redukcja i stabilizacja wiązania p/ciało-lek (HBr)
gotowy koniugat (2-10 moli leku / 1 mol p/ciała)
SIDEROFORY
Makroelementy - fosfor, wapń, magnez, potas, sód, żelazo.
Fe3+ - warunki tlenowe Fe2+ - warunki beztlenowe
Rola żelaza w organizmach żywych (mikroorganizmy)
Skład komórki |
niedobór żelaza powoduje zahamowanie wzrostu, zmniejszenie syntezy kwasów nukleinowych, hamowanie sporulacji, zmiany morfologii komórki |
Metabolizm |
procesy wymagające żelaza: CKT, transport elektronów, fosforylacja oksydacyjna, wiązanie azotu, biosynteza aminokwasów aromatycznych, fotosynteza |
Produkty metabolizmu |
biosynteza porfiryn, toksyn, witamin, antybiotyków, pigmentów, kwasów nukleinowych (regulowane żelazem) |
Białka i enzymy wymagające żelaza |
peroksydazy, dysmutazy nadtlenkowe, nitrogenazy, hydrogenazy syntaza glutaminy, cytochromy, ferrodoksyna, flawoproteiny |
Mikroorganizmy wykształciły specjalne mechanizmy umożliwiające pobieranie żelaza ze środowiska.
zewnątrz błona komórkowa wewnątrz
enterobaktyna ← enterobaktyna (synteza de novo)
↓Fe3+ ↓Fe2+
ferri-enterobaktyna → produkty hydrolizy
rozpuszczanie transport asymilacja
W4
CECHY SIDEROFORÓW
substancje niskocząsteczkowe (względna masa cząsteczkowa mniejsza 1500)
rozpuszczalne w wodzie
wiążą żelazo z wysoką swoistością i powinowactwem (stała stabilność 1030)
związki fenolowe lub hydroksomaty
enterobaktyna- bakteria jelitowe
ferichromy- grzyby
ferrioksoamina- promieniowce
egzochelina- bakteria śluzowe
Drobnoustroje wytwarzają siderofory zazwyczaj wtedy, gdy nikła dostępność żelaza ogranicza ich wzrost. Siderofory mogą posiadać aktywność antybiotyczną: sideromycyna, albomycyna, ferrimycyna. Produkcja przemysłowa sideroforów jest trudna. Siderofor produkowany na skalę przemysłową: deksterioksamina (Desferal) produkowany przez Streptomyces pilosus.
WYKORZYSTANIE SIDEROFORÓW
zatrucia żelazem- terapia chelatowa (cechy dobrego chelatora: łatwość produkcji, efektywność, specyficzność, toksyczność, dostęp do puli);
hemochromatoza
usuwanie toksycznych metali z organizmu
zastosowanie pozamedyczne: rolnictwo (Pseudomonas putida- pseudobaktyna; Rhizobium)
FERMENTACJA STEROLI
Steran- 4-pierścieniowy system cyklopentanoperhydrofenantrenu.
Hormony sterydowe - ważna funkcja metaboliczna.
Przemysł - leki.
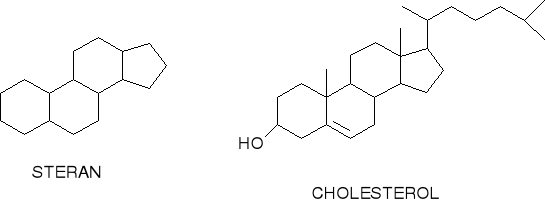
wypchnięte przez analogi półsyntetyczne
W4
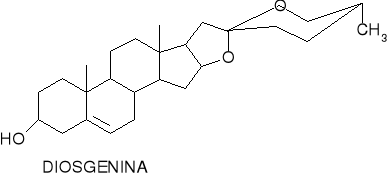
Analogi półsyntetyczne:
diosgenina (Discorea mexicana, Discorea composita)
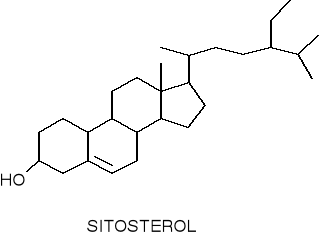
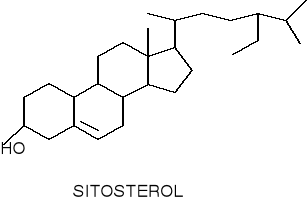
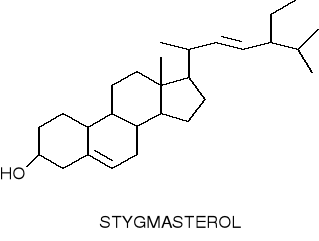
stygmasterol
β- i γ- sitosterole (nasiona soi, bawełny i trzciny cukrowej)
W4
MIKROBIOLOGICZNA KONWERSJA STEROLI OBEJMUJE:
dehydrogenację
epoksydację
estryfikację
izomeryzacje
hydrolizę acetali
hydrolizę estrów
hydrolizę epoksydów
hydroksylację
utlenianie alkoholi i ketonów
redukcja ketonów i podwójnych wiązań
REAKCJE O ZNACZENIU PRZEMYSŁOWYM
Hydroksylowanie w pozycji 11α i 11β, np. hydroksylowanie progesteronu w pozycji 11α
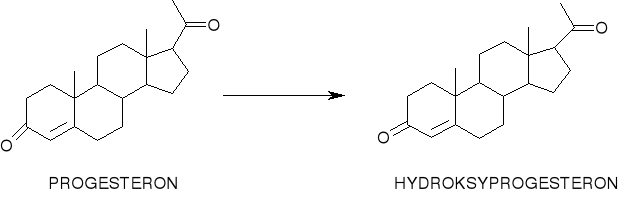
produkty uboczne: 6-α-, 11-β-dihydroksyprogesteron
Rhizopus arrhizus, Rhizopus nigricans, Aspergillus ochraceus
W4
Currularia lunata, Cunninghamella blakestleeana
MECHANIZM REAKCJI HYDROKSYLOWANIA- polega na wprowadzeniu jednego atomu tlenu cząsteczkowego do substratu przy udziale specyficznych oksygenaz i redukcji drugiego do H2O.
steroid steroid OH
enzym-FeO2+ enzym - Fe2+
NADP+ NADPH + H+
H2O O2
Dehydrogenacja w pozycji Δ1
Arthrobacter simplex, Bacillus sphaericus, Nocardia restricus, Septomyxa affinis, Fusarium solani
W4
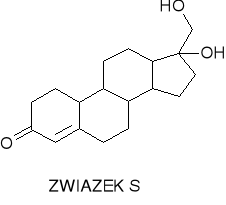
hydroksylowanie w pozycji 16-α.
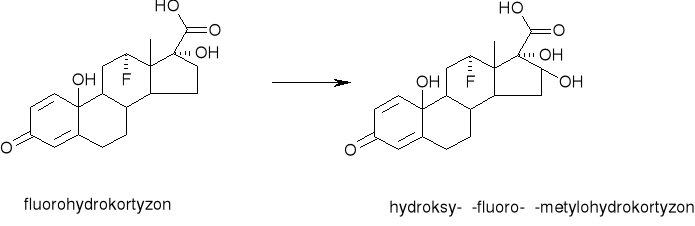
Streptomyces argenteolus
Modyfikacje łańcuchów bocznych.
Nocardia sp., Streptomyces sp., Arthrobacter sp., Mycobacterium sp.
Grupa ketonowa (C-17) oraz grupa karboksylowa (C-20).
PROCES FERMENTACJI STEROIDÓW
Produkty o znaczeniu komercyjnym:
kortyzon
hydrokortyzon
testosteron
testolakton
flokortolon
preolnizon
preolnizolon
BIOTECHNOLOGIA SZTUCZNYCH KOMÓREK
Błony komórki sztucznej:
półprzepuszczalna
grubość 0,002 μm - 1,8 nm
uzyskuje się w procesie emulsyfikacji a następnie polimeryzacji międzyfazowej (silastik, octan celulozy, nylon polietyloaminowy, materiały biodegradowalne).
Zamykanie systemów enzymatycznych wymagających systemu regeneracji kofaktora:
heksokinaza i kinaza pirogronianowa (regeneracja ATP)
glukoza → glukozo-6P
fosfoenolopirogronian → pirogronian
dehydrogenaza alkoholowa i dehydrogenaza jabłczanowa (NAD+ → NADH)
ureaza, dehydrogenaza glutaminianowa, dehydrogenaza glukozo-6P (mocznik → amoniak → α-ketoglutaran)
W4
Sztuczne komórki zawierające komórki biologiczne i inny materiał biologiczny:
sztuczne organy
powierzchnia wymiany 33 ml śr 0,1 mm → 2 m 2
przepuszczalność 0,002 μm → 20 μm
detoksyfikatory krwi
sztuczna wątroba
sztuczna nerka
substytuty krwi
NOWE TRENDY BIOTECHNOLOGII DLA MEDYCYNY
1990 r.- Humane Genome Project USA
Functional Genomics, FunctIonal Proteomics
technologia rekombinacji DNA
inżynieria białka - wykorzystanie organizmów transgenicznych
systemy ekspresji:
prokariotyczny system ekspresji Escherichia coli
eukariotyczny system ekspresji (Sacharomyces cerevisiae, Pichia pastoris)
systemy ekspresji oparte na hodowlach komórek ssaków (chomik, małpa)
hodowle owadzie (system bakulowirusa, Drosphilla melanogaster)
ekspresja heterologicznych białek w gruczołach mlecznych ssaków (myszy, króliki, owce, kozy, krowy)
systemy roślinne
szczepionki (rekombinowane szczepionki antygenowe, hybrydowe szczepionki wirusowe i bakteryjne, antyidiotopowe, hybrydowe, białkowe, antygenowe syntetyczne peptydy)
terapia genowa
strategia antysensu i rybozymowa
metody diagnostyczne
10
Wyszukiwarka
Podobne podstrony:
W4 Proces wytwórczy oprogramowania
W4 2010
Statystyka SUM w4
w4 3
W4 2
W4 1
w4 skrócony
w4 orbitale molekularne hybrydyzacja
in w4
w4 Zazębienie ewolwentowe
TM w4
IB w4 Aud pełny
W4 Mitochondria i chloroplasty
Psychiatria W4 28 04 2014 Zaburzenia spowodowane substancjami psychoaktywnymi
W4
MSG W4
więcej podobnych podstron