GR. 23T1 Zespół nr 6 |
Ćwiczenie: 11 |
Data: 11.04.2011 |
1. Klimek Magdalena 2. Mądro Marcelina 3. Brandys Iwona 4. Trębacz Wojciech |
Temat: Wyznaczanie stałej szybkości reakcji zmydlania estru metodą konduktometryczną |
Ocena: |
Wstęp teoretyczny.
Katalizatorami w reakcji hydrolizy estrów są kwasy lub zasady. Prowadzenie reakcji przy katalizatorze którym jest kwas prowadzi do otrzymania estrów na drodze równowagowej z kwasów i alkoholi. Reakcja przebiegająca przy udziale zasady jest reakcja nieodwracalna, zasada w tej reakcji bierze udział i należy dostarczy jej w ilościach stechiometrycznych, przykładem może być reakcja octanu etylu z zasada potasowa
CH3COOC2H5 + KOH = CH3COOK + C2H5OH
Wraz z postępem reakcji suma ilości jonów nie zmienia się, ponieważ jony OH- zastępowane są przez jony octanowe. Oba rodzaje jonów w znacznym stopniu różnią się ruchliwością. Różnicę tą wykorzystujemy w doświadczeniu. Jony OH- odznaczają się bardzo dużą ruchliwością, zastępowanie ich znacznie mniej ruchliwymi jonami octanowymi powoduje zmniejszenie przewodnictwa elektrycznego roztworu. W doświadczeniu dokonujemy pomiaru zmian przewodnictwa z upływem czasu. Początkowo w mieszaninie znajdują się tylko jony OH- i K+ w stężeniu równym początkowym stężeniom.
Przewodnictwo właściwe κ będzie równe wtedy:
![]()
gdzie:
λ - przewodnictwo graniczne,
C0 - stężenie początkowe.
Zadania do wykonania.
Wyznaczyć stałą C, czyli przewodnictwo właściwe w czasie t = ∞
Sporządzić wykres 1/(B-C) od czasu t, gdzie B - przewodnictwo właściwe w czasie t
Wyznaczyć stałą szybkości reakcji.
Wykonanie ćwiczenia.
W zadanej temperaturze T = 313K za pomocą konduktometru dokonujemy pomiaru przewodnictwa mieszaniny reakcyjnej.
W obliczeniach stosujemy wzór:
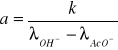
gdzie:
k - stała szybkości reakcji,
a - współczynnik kierunkowy prostej (a = tg α)
α - kąt nachylenia prostej do osi x.
Obliczenia i pomiary.
T = 303 [K]
C0,ZASADY - 0.12 [mol/dm3]
C0,ESTRU - 0.12 [mol/dm3]
W celu wyznaczenia przewodnictwa na końcu reakcji C kreślimy wykres:
C = 0,1235 ![]()
Wyznaczamy rzędowość reakcji na podstawie wykresów:
Z powyższych wykresów wynika, że jest to reakcja drugorzędowa. Stała szybkości tej reakcji wyliczamy ze wzorów:
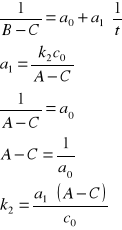
Odczytujemy wartości z równania prostej a0 = 1,1545 a1 = 0,0002. Zatem:
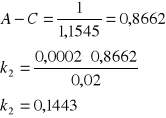
Stała szybkości reakcji wynosi k2 = 0,00144 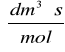
Wnioski.
Z przeprowadzonego pomiaru wynika, że reakcja zmydlania estrów jest reakcją drugorzędową. Świadczy o tym prostoliniowy przebieg zależności 1/(B-C) od t. Dodatkowo zależność ln(B-C) = f(t) nie wykazuje prostoliniowości, co również potwierdza drugorzędowy przebieg reakcji.
Wyszukiwarka
Podobne podstrony:
Gr, xBURDEL gł 2rok;)
aaaaaaaa, xBURDEL gł 2rok;)
lista na fizyczna, xBURDEL gł 2rok;)
sprawozdanie-wzorcowanie przyrządów, xBURDEL gł 2rok;)
PEHA, xBURDEL gł 2rok;)
chromatografia poprwiona, xBURDEL gł 2rok;)
wyswietlacz, xBURDEL gł 2rok;)
FIZYCZ~5, xBURDEL gł 2rok;)
destylacja, xBURDEL gł 2rok;)
Obiegi termod, xBURDEL gł 2rok;)
Elementy technologii chemicznej B8, xBURDEL gł 2rok;)
ćw3, xBURDEL gł 2rok;)
ustny maszyny, xBURDEL gł 2rok;)
sacharoza obliczenia, xBURDEL gł 2rok;)
więcej podobnych podstron