WYZNACZANIE ΔG, ΔH ORAZ ΔS REAKCJI CHEMICZNEJ
Pomiary SEM ogniw elektrochemicznych dostarczają nie tylko danych dotyczących współczynnika aktywności, lecz również cennych informacji o termodynamicznych właściwościach jonów w roztworach wodnych w stanie standardowym o aktywności jednostkowej.
Normalne potencjały elektrod umożliwia obliczenie zależność:
![]()
Ponadto dodatkowych informacji dostarczają pomiary zależności SEM ogniw elektrochemicznych od temperatury.
Zależność termodynamiczna:
![]()
lub 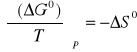
przekształca się po podstawieniu
![]()
we wzór określający entropię
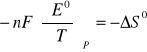
lub 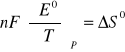
Znając wartość entropii można, korzystając z równania
![]()
obliczyć entalpię reakcji w danej temperaturze.
Pomiary siły elektromotorycznej i jej współczynnika termodynamicznego umożliwiają, więc określenie wartości ΔG, ΔH i ΔS dla przebiegającej w ogniwie reakcji. Ta metoda wyznaczania wielkości termodynamicznych jest często bardziej dogodna niż bezpośrednie pomiary kalorymetryczne.
Mierząc SEM ogniw i określając ich zależność od temperatury można uzyskać dane termodynamiczne dla reakcji powstawania jonów roztworze.
Wyszukiwarka
Podobne podstrony:
10.6 inne, Wyznaczanie 10.6L, Wyznaczanie G , H oraz S reakcji chemicznej
Kopia (10) WYZNACZANIE MODUŁU SZTYWNOŚCI METODĄ DYNAMICZNĄ
10 najstraszniejszych miejsc na Ziemi, W ஜ DZIEJE ZIEMI I ŚWIATA, ●txt RZECZY DZIWNE
10 Klasyfikacja osnów realizacyjnych oraz osnów budowlano montażowych
10 WYZNACZANIE STOSUNKU Cp Cv DLA POWIETRZA METODĄ CLEMENTA DESORMESA(1)
10 Wyznaczanie odksztalcen w belkach zginanych d, WYNIKI LABORATORYJNE
LAB 10, Wyznaczanie ogniskowych soczewek za pomoc˙ ˙awy optycznej
10 2 wyznaczenie pracownika
cw 10 - Wyznaczanie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego, Sprawozdania jakieś, F
10) Ilościowe oznaczenie glikogenu oraz badanie niektórych jego właściwości
10 Wyznaczanie odksztalcen w belkach zginanych a, Budownictwo PG, sem4, MDwAK, Metody doświadczalne
Ćw 10-Wyznaczanie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego
10, Wyznaczanie wilgotności powietrza za pomocą psychrometru Assmanna, NAZWISKO: NAJUCH
Laboratorium 10 - Wyznaczanie charakterystyki licznika Geigera - Műllera wstęp
10 Wyznaczanie odksztalcen w belkach zginanych a, POLITECHNIKA GDAŃSKA
Ćw. nr 10 Wyznaczenie n pryzmatu, Studia, Fizyka
80 Nw 10 Wyznaczanie srednic
Ćw 10 Wyznaczanie przyspieszenia ziemskiego za pomocą wahadła rewersyjnego
więcej podobnych podstron