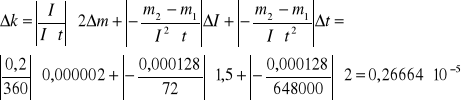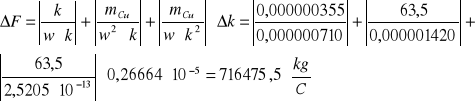Sprawdzanie praw elektrolizy Faradaya
I. Zagadnienia do samodzielnego opracowania:
Przepływ prądu przez elektrolity.
Pierwsze i drugie prawo Faradaya.
Atomy niektórych pierwiastków mają takie właściwości, że przy zbliżaniu się do atomów innego pierwiastka mogą mu oddać jeden lub kilka elektronów. Wskutek tego z obojętnych elektrycznie atomów powstają jony, przy czym jedne z nich, a mianowicie te, które oddały elektron lub elektrony i pozostały z nadmiarem ładunku dodatniego są naładowane elektrycznie dodatnio, a te które je przejęły, są naładowane ujemnie. Równocześnie między jonami wystąpi przyciąganie elektryczne, wiążące je w cząsteczkę związku.
W roztworach wodnych dysocjacji elektrolityczne ulegają: kwasy, zasady i sole, przy czym tworzące się jony wodoru i metali są dodatnie (kationy), jony zaś grupy wodorotlenowej OH lub reszty kwasowej (np. Cl-, NO3-) - ujemne (aniony).
Stosunek liczby cząstek ulegających dysocjacji, do całkowitej liczby cząstek zawartych w roztworze nazywamy stopniem dysocjacji elektrolitu, przy czym jego wartość wzrasta ze stopniem temperatury i maleje ze wzrostem stężenia roztworu. Zjawisko dysocjacji występuje również po stopieniu związku jonowego.

Po wprowadzeniu do elektrolitu CuSO4 płyt metalowych (elektrod) i podłączeniu ich ze źródłem napięcia rozpoczyna się, pod wpływem wytworzonego pola elektrycznego, uporządkowany ruch jonów. Jony ujemne (SO4- -) poruszają się z niewielką prędkością w kierunku dodatnio naładowanej elektrody, zwanej anodą A, dodatnie zaś (Cu- -) w kierunku ujemnie naładowanej elektrody, zwanej katodą K. Ponieważ jony są - podobnie jak elektrony w metalach - nośnikami ładunków elementarnych, zatem ich uporządkowany ruch jest równoznaczny z przepływem prądu elektrycznego.

Przyrządy: analityczna waga laboratoryjna, elektrody miedziowe z zamocowaniem, amperomierz, zasilacz, sekundomierz.
Połączyłem obwód według schematu:
Sprawdziłem poprawność obwodu elektrycznego zamykając obwód na krótki czas. Równocześnie regulowałem natężenie prądu w obwodzie, tak by nie przekraczał 0,5A/dm2. Natężenie prądu wyznaczyłem w oparciu o powierzchnię elektrody.
Wyjąłem katodę, oczyściłem starannie papierem ściernym, wypłukałem wodą. Wyznaczyłem masę m1 katody korzystając z analitycznej wagi laboratoryjnej.
Umieściłem ponownie katodę w elektrolicie, włączyłem prąd uruchamiając jednocześnie zegar. Utrzymałem stałą wartość natężenia prądu przez czas t = 30 minut.
Po upływie tego czasu przerwałem przepływ prądu. Opłukałem katodę wodą, osuszyłem i wyznaczyłem masę m2 katody. Masę wydzielonej miedzi obliczyłem ze wzoru m = m2 - m1. Przekształcając wzór m = k I t obliczyłem równoważnik elektrochemiczny miedzi. 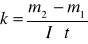
Z układu okresowego pierwiastków odczytałem masę atomową miedzi mCu, wartościowość miedzi w = 2 i ze wzoru wyrażającego II prawo Faradaya obliczyłem stałą Faradaya: 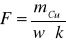
Wyniki umieściłem w tabelce:
Δm = Δm1 = Δm2 = 0,000001kg
ΔI = ± 1,5 mA (zakres - 300; klasa - 0,5)