
1.Temat ćwiczenia
Wyznaczanie potencjału wydzielania wodoru
2.Cel ćwiczenia
Celem ćwiczenia jest doświadczalne przebadanie krzywych prądu – napięcie (metodą galwaniczną) dla wydzielania
wodoru na platynie i na Miedzie oraz wyznaczenie nadnapięcia wydzielania wodoru na Pt i Cu.
3.Pomiary
NaOH Cu
0,1 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,43
0,54 0,94 1,31 1,37
1,4 1,42 1,44 1,46 1,47 1,48 1,49
1,5 1,51 1,53 1,53 1,53 1,53 1,54 1,55 1,55 1,56 1,56 1,57 1,58
NaOH Cu
0,01 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,61
0,72 0,82 1,35 1,44 1,49 1,53 1,57
1,6 1,63 1,65 1,69 1,71 1,74 1,76 1,79 1,81 1,83 1,86 1,89 1,91 1,93 1,95 1,97
2
NaOH Pt
0,1 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,5
0,8
1 1,04 1,07
1,1 1,12 1,14 1,15 1,17 1,18 1,19
1,2 1,21 1,22 1,23 1,24 1,25 1,26 1,27 1,28 1,29
1,3 1,31 1,32
NaOH Pt
0,01 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,46
0,73 1,04 1,12 1,17 1,23 1,27 1,31 1,35 1,37
1,4 1,44 1,46
1,5 1,52 1,55 1,57 1,58 1,61 1,64 1,66 1,67 1,71 1,73 1,75
H2SO4 Cu
0,1 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,5
0,56 0,62 0,68 0,71 0,73 0,75 0,76 0,77 0,78 0,78 0,79
0,8
0,8
0,8
0,8
0,8 0,81 0,81 0,82 0,82 0,83 0,83 0,83 0,83
H2SO4 Cu
0,01 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,8
0,84 0,86 0,88
0,9 0,92 0,94 0,97 0,99 1,01 1,04 1,05 1,07 1,08 1,09 1,09
1,1
1,1 1,11 1,12 1,13 1,15 1,17 1,18 1,19
H2SO4 Pt
0,1 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,3
0,32 0,33 0,34 0,35 0,36 0,37 0,38 0,39
0,4 0,41 0,42 0,43 0,44 0,45 0,45
4,6 0,47 0,48 0,48 0,49
0,5
0,5 0,51 0,51
H2SO4 Pt
0,01 N
mA
0,2
0,4 0,6
0,8
1
1,2
1,4
1,6
1,8
2
2,2
2,4
2,6
2,8
3
3,2
3,4
3,6
3,8
4
4,2
4,4
4,6
4,8
5
mV
0,44
0,47 0,48
0,5 0,53 0,56 0,58 0,61 0,63 0,66 0,68
0,7 0,72 0,74 0,76 0,78 0,79 0,81 0,83 0,85 0,87 0,89
0,9 0,92 0,94

4.Obliczenia
Wartośd potencjału wydzielania
[V] - 1,6 dla NaOH Cu 0,1N
[V] - 2,1 dla NaOH Cu 0,01N
[V] - 1,4 dla NaOH Pt 0,1N
[V] - 1,8 dla NaOH Pt 0,01N
[V] - 0,85 dla
Cu 0,1N
[V] - 1,24 dla
Cu 0,01N
[V] - 0,54 dla
Pt 0,1N
[V] – 1 dla
Pt 0,01N
[V] -1,874 dla NaOH Cu 0,1N
[V] - 2,374 dla NaOH Cu 0,01N
[V] - 1,674 dla NaOH Pt 0,1N
[V] - 2,074 dla NaOH Pt 0,01N
[V] - 1,124 dla
Cu 0,1N
[V] - 1,514 dla
Cu 0,01N
[V] - 0,814 dla
Pt 0,1N
[V] - 1,274 dla
Pt 0,01N
T – 299,14 K – temp. Pokojowa w Kelwinach
E = - 0,0290524 [V]
E ≈ - 0,029 [V]

[V] - 1,874 dla NaOH Cu 0,1N ; η [V] wynosi 1,903
[V] - 2,374 dla NaOH Cu 0,01N; η [V] wynosi 2,403
[V] - 1,674 dla NaOH Pt 0,1N; η [V] wynosi 1,703
[V] - 2,074 dla NaOH Pt 0,01N; η [V] wynosi 2,103
[V] - 1,124 dla
Cu 0,1N; η [V] wynosi 1,153
[V] - 1,514 dla
Cu 0,01N; η [V] wynosi 1,543
[V] - 0,814 dla
Pt 0,1N; η [V] wynosi 0,843
[V] - 1,274 dla
Pt 0,01N; η [V] wynosi 1,303
Wartośd średnia nadpotencjału η dla Cu:
1,7505 [V]
Wartośd średnia nadpotencjału η dla Pt:
[V]
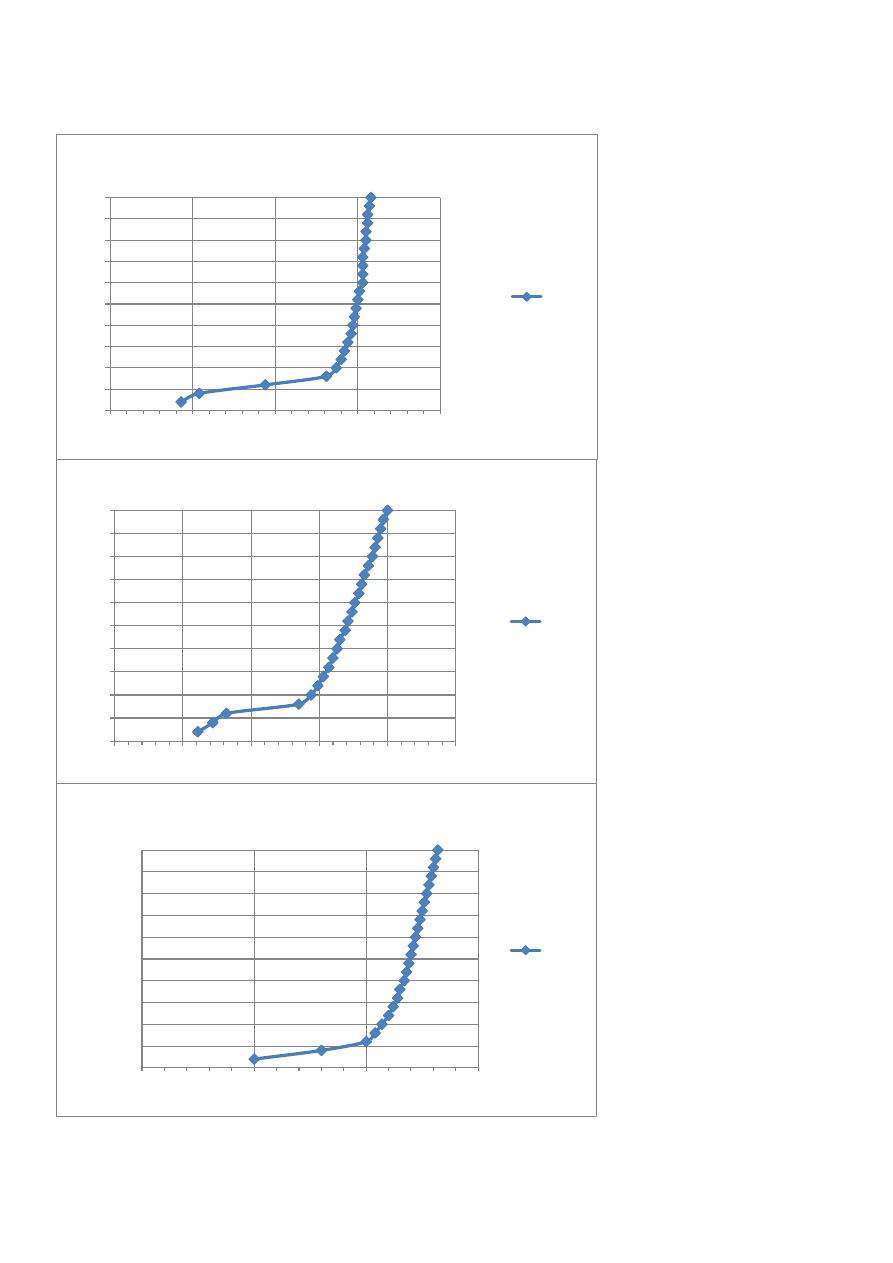
5.Wykresy
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,5
1
1,5
2
Serie1
π[mV]
I[mA]
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,5
1
1,5
2
2,5
Serie1
π[mV]
I[mA]
NaOH CU 0,01N
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,5
1
1,5
Serie1
π[mV]
I[mA]
NaOH Pt 0,1N
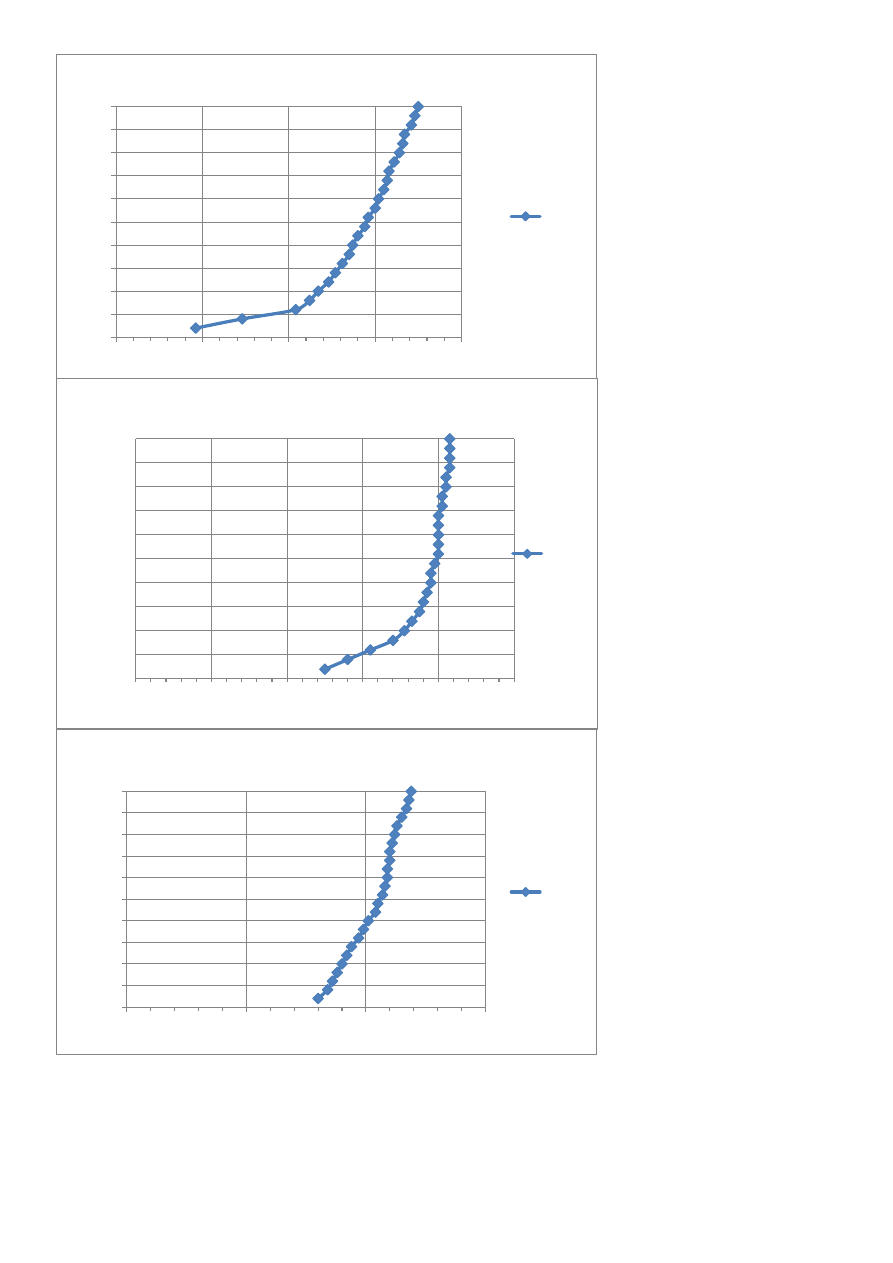
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,5
1
1,5
2
Serie1
π[mV]
I[mA]
NaOH Pt 0,01N
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,2
0,4
0,6
0,8
1
Serie1
π[mV]
I[mA]
H2SO4 Cu 0,1N
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,5
1
1,5
Serie1
π[mV]
I[mA]
H2SO4 Cu 0,01N
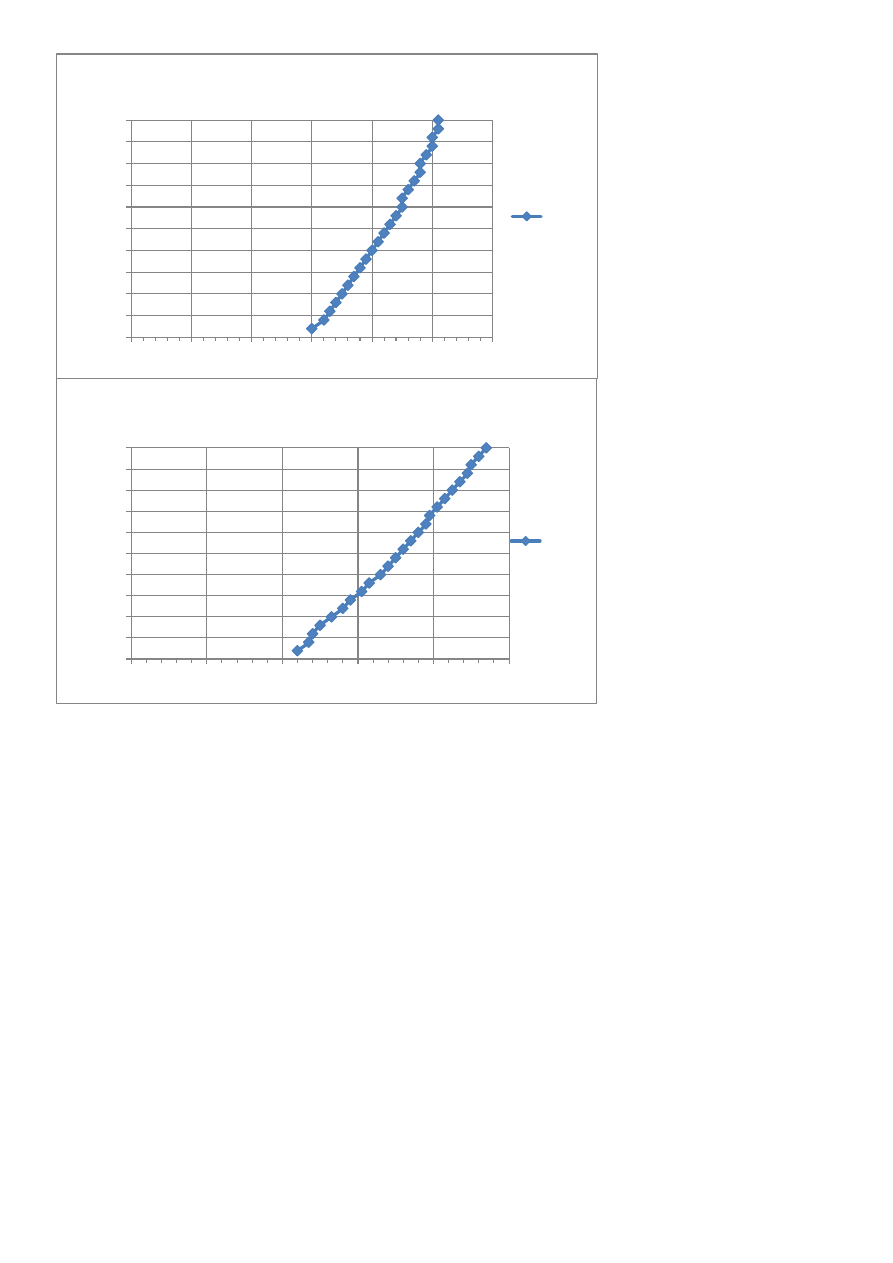
6.Wnioski.
- można zauważyd że ze wzrostem prądu potencjał rośnie
-wartośd średnia nadnapięcia η dla Cu wynosi: 1,7505 [V] , dla Pt [V]
-Z wykonanego doświadczenia jestem w stanie stwierdzid, że reakcje elektrodowe zachodzące podczas
przepływu prądu elektrycznego przez bardzo rozcieoczone roztwory wodne prowadzą do wydzielenia
wodoru. O wydzieleniu wodoru świadczą małe bąbelki, które zauważono podczas wykonywanego
doświadczenia.
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,1
0,2
0,3
0,4
0,5
0,6
Serie1
π[mV]
I[mA]
H2SO4 Pt 0,1N
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
0
0,2
0,4
0,6
0,8
1
Serie1
π[mV]
I[mA]
H2SO4 Pt 0,1N
Wyszukiwarka
Podobne podstrony:
metrologia cw 4 protokol
Cw 1 protokół pomiarów i obliczeń
Cw 4, Protokol
metrologia cw 1 protokol
Cw 1 Protokol
Cw 2 Protokol
Cw 9 Protokół
C - Statystyczna analiza wyników pomiarów, cw 1, Protokół z ćwiczenia: Statystyczna analiza wyników
Cw 2, Protokol
Cw 5, Protokol
Cw 3, Protokol
ćw 3 Protokół izolacji DNA genomowego
Cw 3 Protokol
Cw 3 protokół pomiarów i obliczeń
AP - Ćw - Protokół Sekcji Zwłok - SGGW, weterynaria 3 rok WROC, semestr 6, Apy 2 sem
metrologia cw 6 protokol
metrologia cw 3 protokol
Cw 4 Protokol
więcej podobnych podstron