Fizyka kwantowa
dotyczy świata mikroskopowego
wiele wielkości jest skwantowanych,
tzn. występuje w całkowitych
wielokrotnościach pewnych minimalnych
porcji zwanych kwantami
Foton, kwant światła
Zjawiska świadczące o kwantowej naturze
światła:
zjawisko fotoelektryczne – energia
kwantów - równanie Einsteina
efekt Comptona - pęd fotonów
widma emisyjne atomów
prawidłowy opis promieniowania
termicznego z postulatem kwantyzacji
energii świetlnej - prawo Plancka
Zjawisko fotoelektryczne
Wiązka światła wybija elektrony z powierzchni metalu
z falowej teorii wynika:
elektron nie opuści metalu dopóki amplituda fali E
o
nie
przekroczy określonej wartości krytycznej
energia emitowanych elektronów wzrasta proporcjonalnie
do E
o
2
liczba emitowanych elektronów powinna zmniejszyć się ze
wzrostem częstotliwość światła
wyniki eksperymentalne:
progowego natężenia nie zaobserwowano
energia elektronów okazała się niezależna od wielkości E
o
zauważono zależność energii elektronów od częstotliwości
Teoria Einsteina
światło o częstości
ν
stanowi zbiór pakietów
energii zwanych fotonami lub kwantami z
których każdy posiada energię h
ν
h to uniwersalna stała Plancka = 6.626×10
–34
Js
kwanty światła (fotony) zachowują się podobnie
do cząstek materialnych (przy zderzeniu foton
może być pochłonięty, a cała jego energia
przekazana jest elektronowi).
maksymalna energia kinetyczna elektronu
opuszczającego metal o pracy wyjścia W
o
wynosi
o
W
h
K
−
ν
=
max
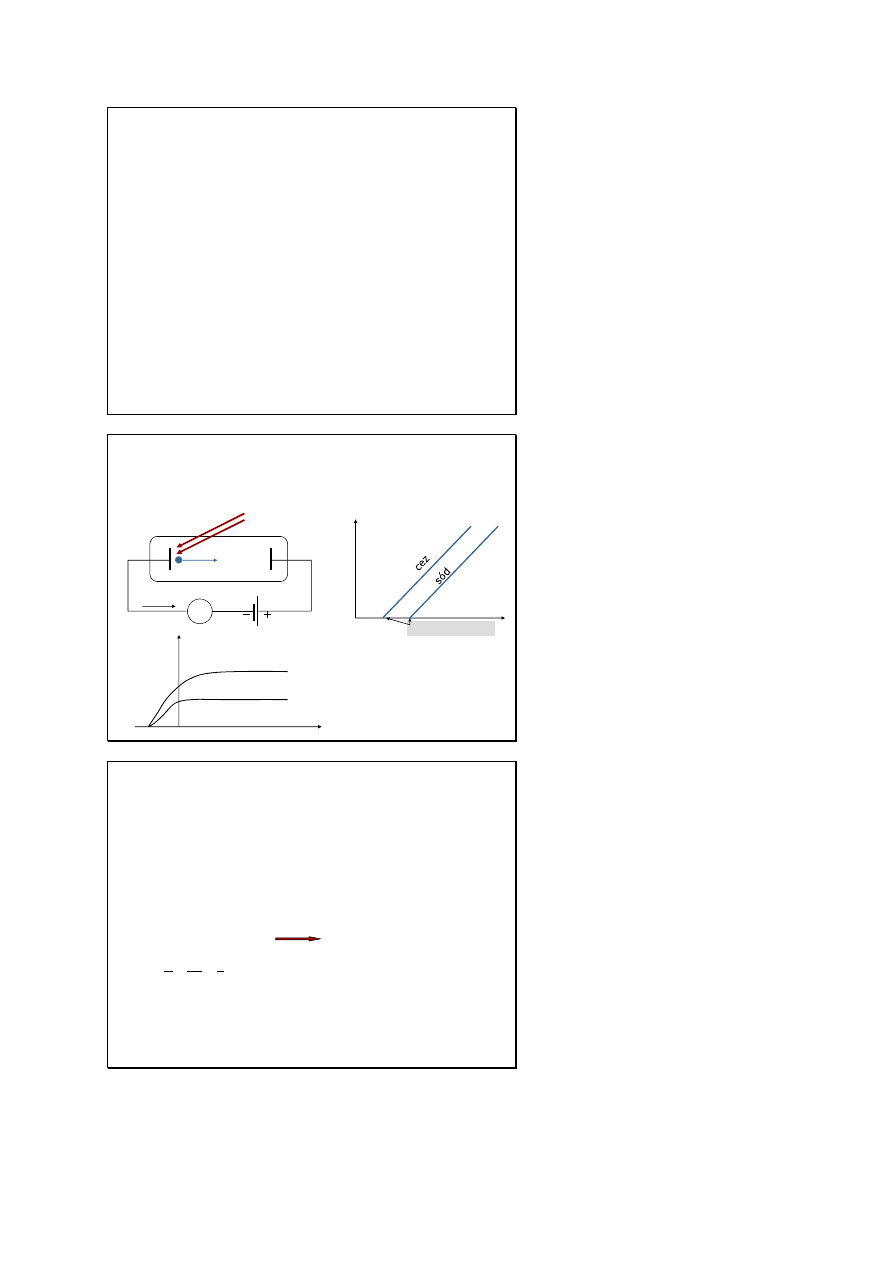
Doświadczenia
fotoelektryczne
j
A
U
j
U
U
h
I
o
2I
o
liczba emitowanych elektronów
(prąd j) rośnie ze wzrostem
natężenia światła I
o
maksymalna energia elektronów
K
max
=U
h
nie zależy od natężenia
światła I
o
, rośnie ze wzrostem
częstotliwości ν
o
W
h
K
−
ν
=
max
o
o
W
h
=
ν
max
K
ν
o
ν
częstość progowa
0
K
T
materiał
tarczy:
Pęd fotonu
Foton, oprócz energii E=h
ν, posiada również pęd p
Zgodnie z teorią relatywistyczną wszystkie cząstki
które posiadają energię muszą posiadać pęd,
nawet jeśli nie mają masy spoczynkowej
λ
ν
h
c
h
c
E
p
=
=
=
pc
E =
( )
(
)
2
2
2
2
c
m
pc
E
o
+
=
0
=
o
m
Kierunek pędu fotonu jest zgodny z kierunkiem
rozchodzenia się fali elektromagnetycznej
Foton nie ma ładunku elektrycznego ani momentu
magnetycznego, ale może oddziaływać z innymi cząstkami
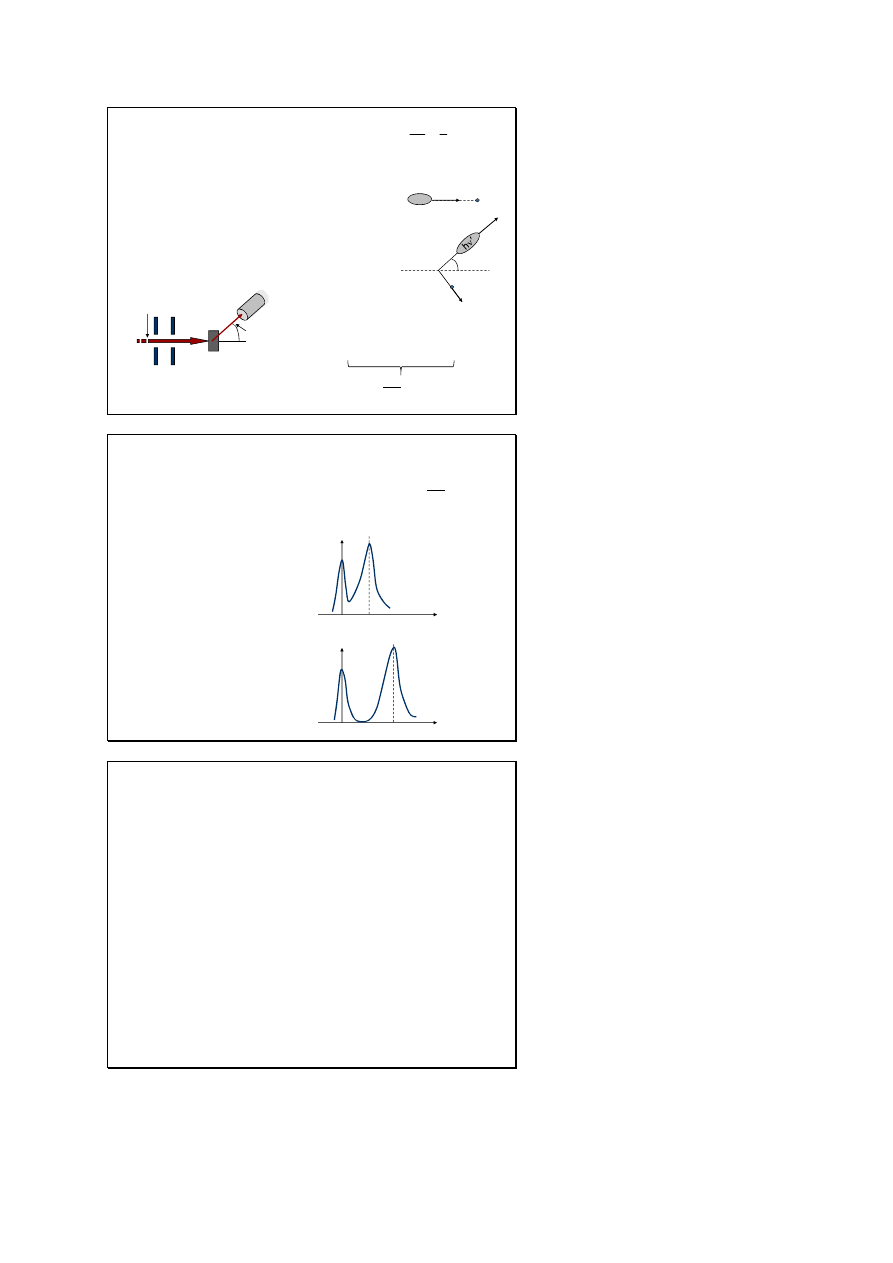
Efekt Comptona
Rozpraszanie fotonów na swobodnych elektronach:
wiązka promieniowania rentgenowskiego o długości
fali
λ rozpraszana przez grafitową tarczę zmieniała
swą długość w zależności od kąta rozpraszania
θ .
W klasycznym podejściu długość fali wiązki
rozproszonej powinna być taka sama jak padającej.
θ
detektor
szczeliny
kolimujące
λ
'
λ
tarcza
grafitowa
wiązka
rozproszona
promieniowanie
rentgenowskie
pr
hν
'
pr
e
p'
r
θ
przed zderzeniem
po
e
e
z prawa zachowania energii
i pędu przed i po zderzeniu
e
E
h
h
'
'
+
=
ν
ν
e
p
p
p
'
' r
r
r
+
=
(
)
θ
−
=
λ
−
λ
cos
'
1
mc
h
λ
ν
h
c
h
p
=
=
pc
E
=
Wyniki doświadczenia
Comptona
przesunięcie comptonowskie
Δλ=λ’-λ zwiększa się wraz ze
wzrostem kąta rozpraszania
obecność wiązki o nie
zmienionej długości fali
wynika z rozproszenia na
elektronach związanych
im większa masa cząstki tym
mniejsze przesunięcie Δλ
efekt Comptona potwierdza
korpuskularny charakter
światła – fotony obdarzone
energią i pędem
λ
λ’
I
o
długość fali
ϕ=90°
λ
λ’
I
o
długość fali
ϕ=135°
(
)
θ
−
=
λ
−
λ
cos
'
1
mc
h
Widma emisyjne atomów
pochodzenie dyskretnych linii
spektralnych można wyjaśnić w
oparciu o dwa założenia:
pojęcie fotonu
istnienie poziomów energetycznych
atomu
Model Bohra
elektrony poruszają się w atomach nie
promieniując energii, po takich orbitach
kołowych, że moment pędu elektronu jest równy
całkowitej wielokrotności stałej
przejścia elektronu z orbity o energii E
n
na
orbitę, gdzie energia wynosi E
m
, towarzyszy
emisja lub absorpcja fotonu o częstości
określonej wzorem
h
n
mv
r =
ν
=
−
h
E
E
m
n
n = 1, 2, 3..
h
1913r. – 13 lat przed sformułowaniem
równania Schrodingera
Widmo atomu wodoru
wzbudzenie atomu – przejście elektronu na
wyższy poziom energetyczny
po czasie 10
-8
s samorzutny powrót do stanu o
niższej energii i emisja fotonu o długości λ
jonizacja atomu – przejście elektronu na
najwyższy poziom energetyczny o zerowej
energii (elektron swobodny)
(energia jonizacji = E
0
)
⎟
⎠
⎞
⎜
⎝
⎛
−
=
−
=
ν
=
λ
2
2
1
1
1
n
m
R
hc
E
E
c
m
n
R – stała Rydberga
c
me
R
o
3
2
3
4
64
h
ε
π
=
E
1
E
2
E
3
E
∞
jonizacja
wzbudzenie
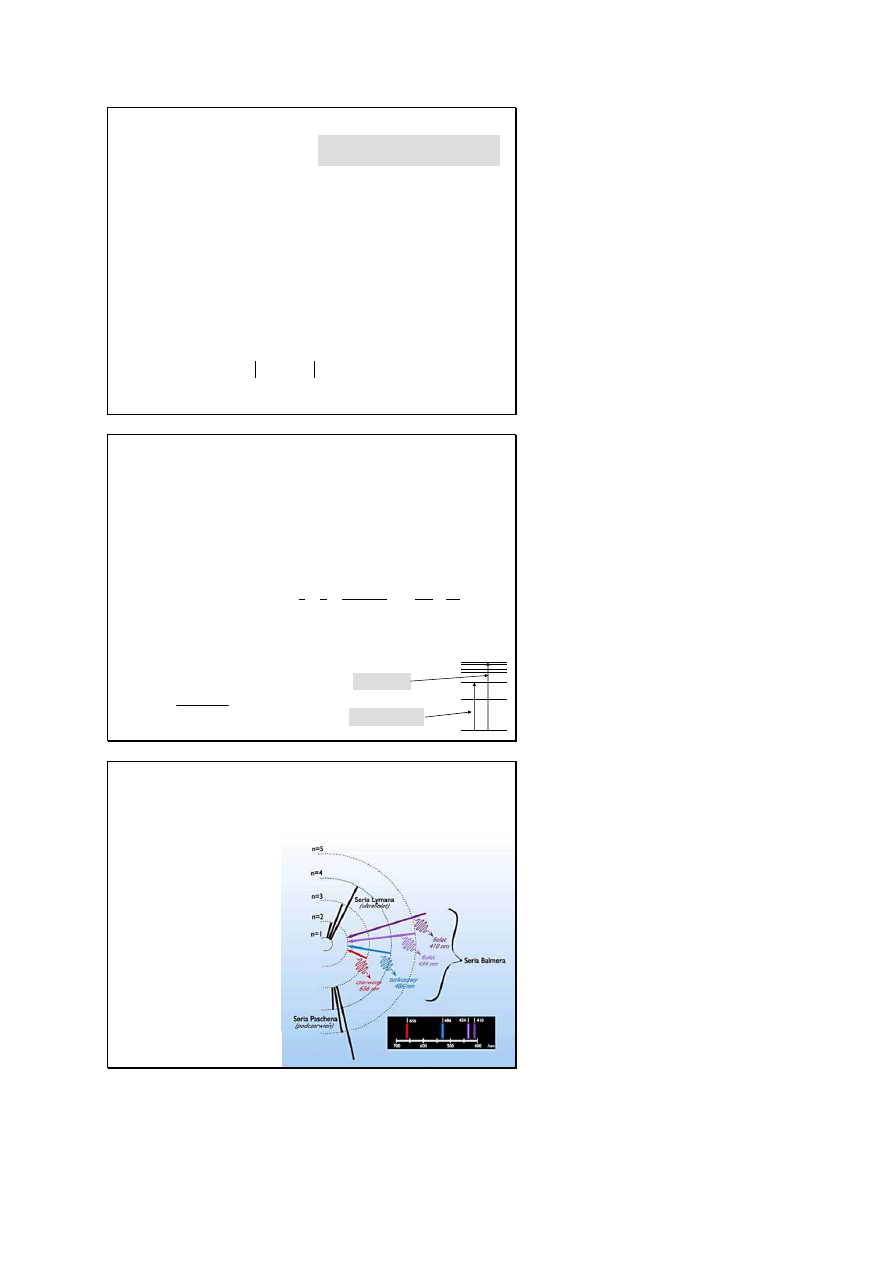
Serie widmowe
seria Lymana
seria Balmera
seria Paschena
seria Bracketta
seria Pfunda
BohrModel.swf
Promieniowanie termiczne
model ciała doskonale czarnego
prawa promieniowania termicznego
prawo Kirchhoffa
prawo Stefana-Boltzmanna
prawo przesunięć Wiena
prawo Rayleigha-Jeansa - klasyczne
prawo Plancka - kwantowe
Jak teoria fotonów wyjaśnia ciągłe widmo
promieniowania emitowanego przez gorące,
nieprzezroczyste ciała?
Podstawowe definicje
Promieniowaniem termicznym
(zwanym też cieplnym lub
temperaturowym) nazywamy promieniowanie wysyłane przez
ciała ogrzane do pewnej temperatury - jest wynikiem drgań
ładunków elektrycznych
Zdolność emisyjna
ciała e(ν,T)dν definiujemy jako energią
promieniowania wysyłanego w jednostce czasu z jednostki
powierzchni o temperaturze T, w postaci fal elektromagne-
tycznych o częstościach zawartych w przedziale od ν do ν + dν.
Zdolność absorpcyjna
, a, określa jaki
ułamek energii padającej na
powierzchnię zostanie pochłonięty.
Zdolność odbicia
, r, określa jaki ułamek
energii padającej zostanie odbity.
(
) (
)
1
=
ν
+
ν
T
r
T
a
,
,
Ciało doskonale czarne
Promień
świetlny
Powierzchnia
o dużej zdolności
absorpcyjnej
Ciało doskonale czarne
(c.d.cz.) całkowicie
absorbuje promieniowanie termiczne.
a =1 i r =0
Stosunek zdolności emisyjnej do
zdolności absorpcyjnej jest dla
wszystkich powierzchni jednakowy i
równy zdolności emisyjnej c.d.cz.
Prawo Kirchhoffa
:
(
)
(
)
(
)
T
T
a
T
e
,
,
,
ν
ε
=
ν
ν
Ponieważ zawsze a≤1, więc i e(ν,T) ≤ ε(ν,T), tzn.
zdolność emisyjna każdej powierzchni nie jest większa
od zdolności emisyjnej ciała doskonale czarnego.
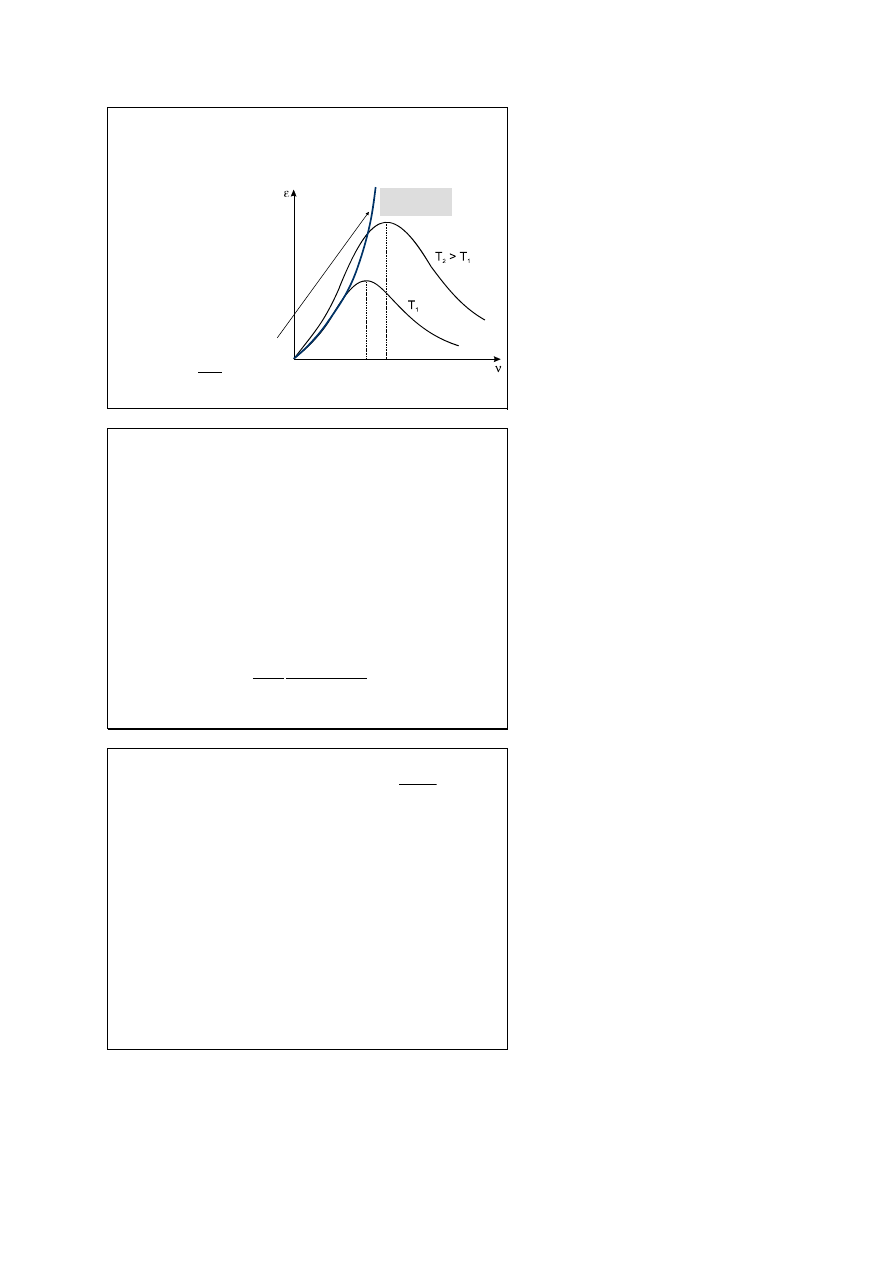
Prawa promieniowania
c.d.cz.
ν
max
1
ν
max
2
Prawo Stefana-Boltzmanna
4
T
E
σ
=
T
b ⋅
=
ν
max
Prawo przesunięć Wiena
(
)
kT
c
T
2
2
2
πν
=
ν
ε ,
Prawo Rayleigha-Jeansa
Stała Stefana-Boltzmanna
σ = 5.67×10
–8
Wm
–2
K
–4
Stała Wiena
b = 5.877×10
10
s
–1
K
–1
katastrofa
nadfioletowa
Prawo Plancka
Hipoteza Plancka: elektryczny oscylator harmoniczny
stanowiący model elementarnego źródła promieniowania, w
procesie emisji promieniowania może tracić energię tylko
porcjami, czyli kwantami ΔE, o wartości proporcjonalnej do
częstości ν jego drgań własnych.
ν
=
Δ
h
E
gdzie stała Plancka h = 6.626×10
–34
Js
zdolność emisyjna c.d.cz. jest funkcją częstości i temperatury
(
)
(
)
1
1
2
2
3
−
ν
ν
π
=
ν
ε
kT
h
c
h
T
/
exp
,
i pozostaje w bardzo dobrej zgodności z doświadczeniem
Wnioski
Postulat
Plancka
(energia
nie
może
być
wypromieniowana w sposób ciągły), doprowadził
do teoretycznego wyjaśnienia promieniowania
ciała doskonale czarnego.
Z
prawa
Plancka
wynika
prawo
Stefana-
Boltzmanna i prawo przesunięć Wiena.
Porcje energii promienistej emitowanej przez
ciało wynoszące h
ν
zostały nazwane kwantami
lub fotonami.
Hipoteza
Plancka
dała
początek
fizyce
kwantowej, a stała h występuje obecnie w wielu
równaniach fizyki atomowej, jądrowej i ciała
stałego.
(
)
ν
ν
ε
d
T
E
∫
∞
=
0
,
(
)
0
=
∂
∂
ν
ν
ε
T
,

Jak światło może być
jednocześnie falą i cząstką
opisy światła: falowy i korpuskularny
są uzupełniające się
potrzeba obu tych opisów do
pełnego modelu świata, ale do
określenia konkretnego zjawiska
wystarczy tylko jeden z tych modeli
dlatego mówimy o dualizmie
korpuskularno-falowym światła
Falowa natura cząstek
Promień świetlny jest falą,
ale energię i pęd przekazuje
materii w postaci fotonów.
Dlaczego innych cząstek np.
elektronów nie traktować jako
fal materii ?
Hipoteza de Broglie’a
W 1924 r. Louis de Broglie przypisał elektronom o pędzie p
długość fali λ
– długość fali de Broglie’a
p
h
=
λ
Słuszność hipotezy de Broglie’a została potwierdzona w 1927 r.
przez Davissona i Germera, którzy wykazali, że wiązka
elektronów ulega dyfrakcji tworząc typowy obraz interferencyjny
Promieniowanie i materia wykazują dwoistą falowo-korpuskularną
naturę – nazywamy to dualizmem korpuskularno-falowym
m
s
m
kg
s
J
p
h
27
6
34
10
6
6
1
10
1
0
10
63
6
−
−
−
⋅
=
⋅
⋅
⋅
⋅
=
=
,
,
,
λ
dla pyłku unoszonego
przez wiatr
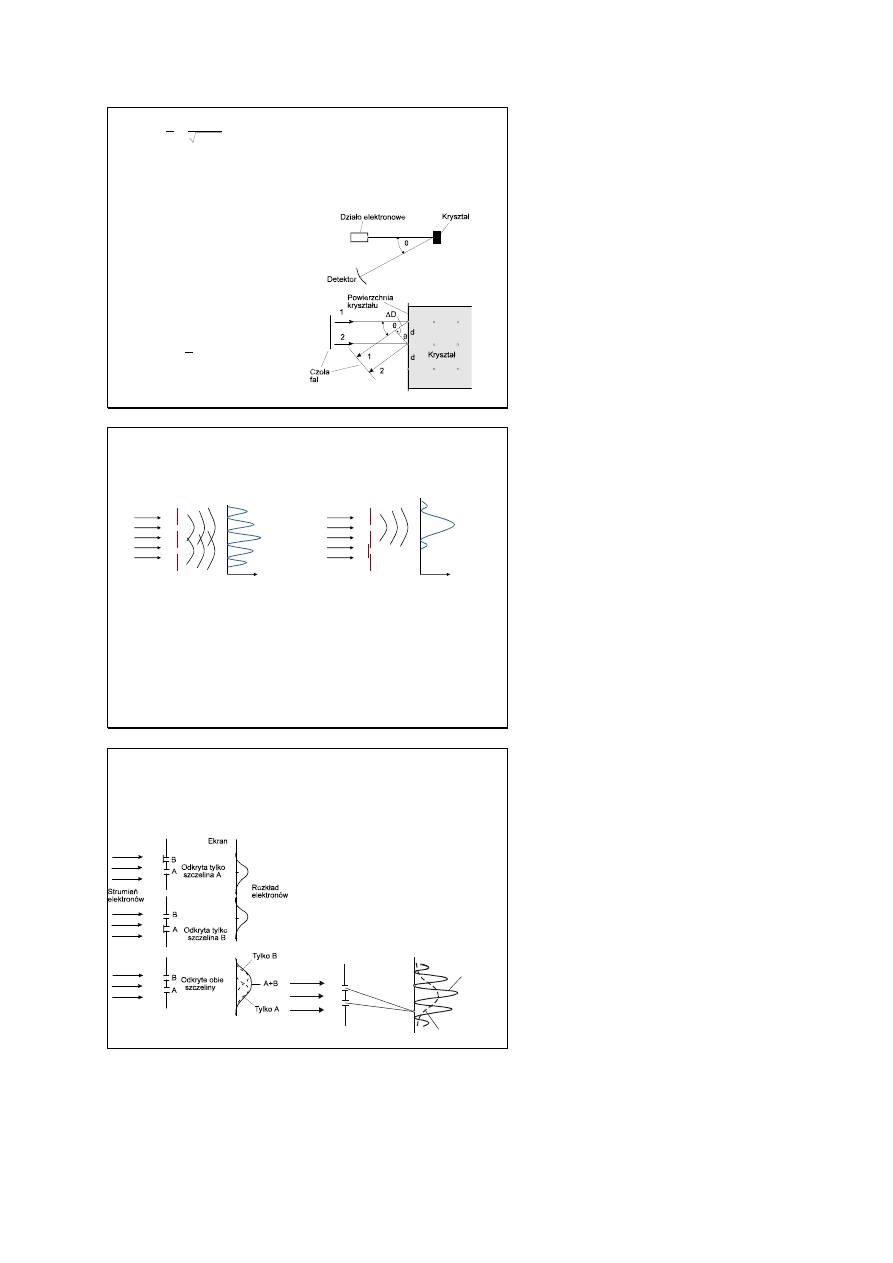
Dyfrakcja elektronów
mK
h
p
h
2
=
=
λ
Dla elektronów o K=1000eV
λ=4×10
–11
m
θ
= sin
d
p
h
Znając kąt θ przy którym
obserwuje się pierwsze
maksimum można określić
stałą Plancka
ΔD = d sinθ
ΔD =λ
θ
=
sin
pd
h
Doświadczenie Davissona - Germera
(dyfrakcja elektronów)
Jak elektron przechodzi
przez szczelinę?
• Pojedyncze elektrony padające na dwie szczeliny
dają obraz dyfrakcyjny w postaci szeregu prążków
• zasłonięcie jednej szczeliny (B) powoduje zmianę
obrazu dyfrakcyjnego
• skąd elektron wie, że szczelina B jest zasłonięta?
• fakt, że obraz dyfrakcyjny może zostać utworzony
przez różne nieoddziałujące ze sobą elektrony
świadczy o tym, że każdy elektron przechodzi
przez obie szczeliny i interferuje sam ze sobą
A
B
wiązka
elektronów
A
B
wiązka
elektronów
Fale prawdopodobieństwa
r
1
r
2
A
B
P
1
P
2
Rozkład
klasyczny
Rozkład
obserwowany
Rozkład elektronów na ekranie powinien być
sumą rozkładów dla każdej szczeliny oddzielnie
- obserwujemy obraz interferencyjny dla
dwóch szczelin
Do wyjaśnienia tego paradoksu musimy
stworzyć nowy formalizm matematyczny:
fale materii traktować jako fale
prawdopodobieństwa wytwarzającą na ekranie
obraz „prążków prawdopodobieństwa”
klasycznie
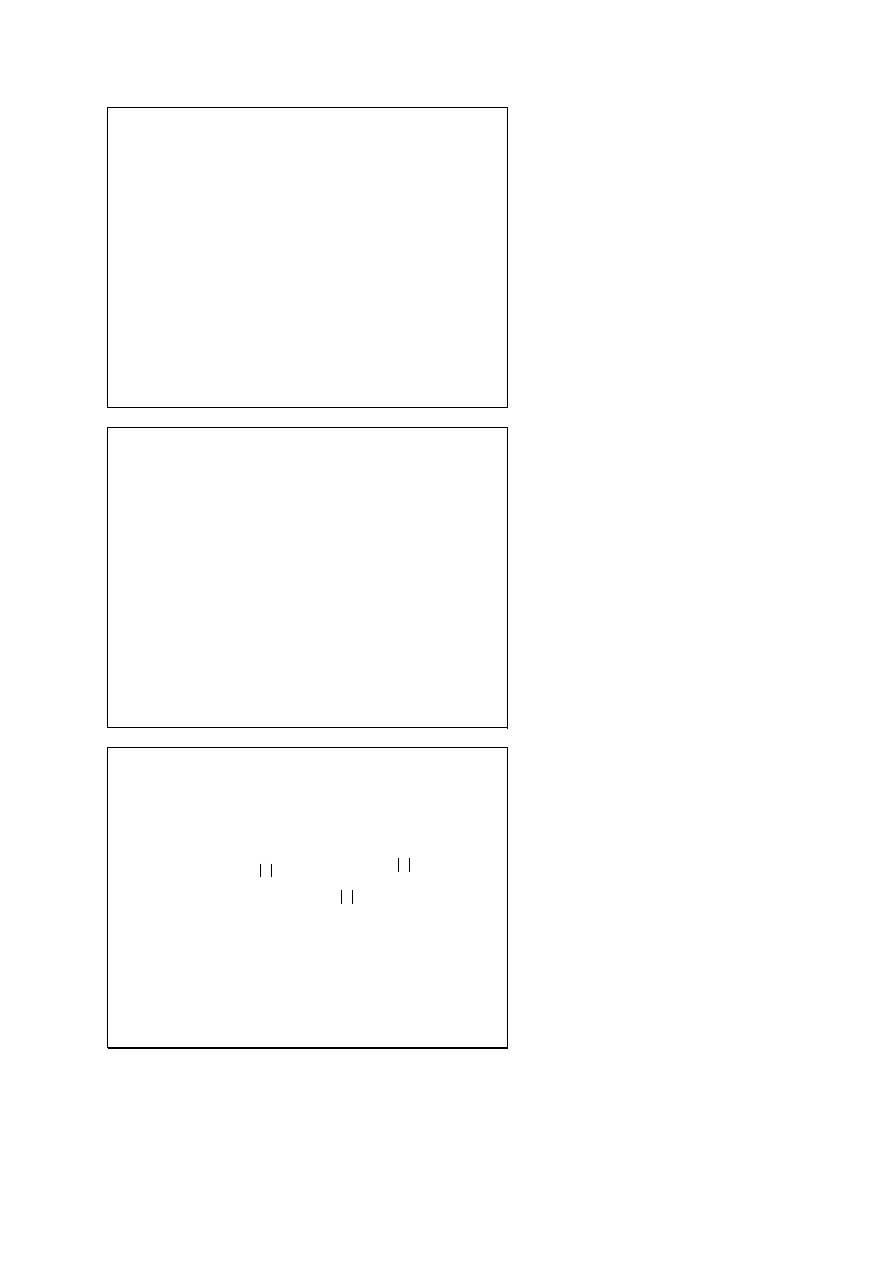
Mechanika kwantowa
dział mechaniki zajmujący się
ruchem mikrocząstek, których
stan opisany jest funkcją falową
będącą rozwiązaniem równania
Schrodingera
Funkcja falowa
Formalizm matematyczny za pomocą którego usuwa się te
paradoksy, przypisuje każdej cząstce materialnej funkcję
falową
Ψ (x,y,z,t) będącą funkcją współrzędnych i czasu
Znajdując rozkład natężenia w obrazie dyfrakcyjnym
można określić prawdopodobieństwo, że elektron padnie w
określonym miejscu ekranu
Kwadrat amplitudy funkcji falowej jest proporcjonalny do
gęstości prawdopodobieństwa znalezienia elektronu w
danym elemencie obszaru
Właściwości funkcji falowej
Prawdopodobieństwo znalezienia się elektronu
w objętości dV=dxdydz wynosi
gdzie
warunek unormowania
funkcji falowej
zasada superpozycji Ψ = Ψ
1
+ Ψ
2
funkcja falowa powinna być ograniczona |Ψ|<∞
funkcja falowa Ψ nie stanowi bezpośrednio obserwowanej
wielkości. Fale klasyczne i fale odpowiadające cząstkom
podlegają równaniom matematycznym tego samego typu.
Lecz w przypadku klasycznym amplituda fali jest
bezpośrednio obserwowana, a dla funkcji falowej Ψ– nie.
1
2
=
Ψ
∫
dV
V
dxdydz
PdV
2
Ψ
=
∗
Ψ
⋅
Ψ
=
Ψ
2
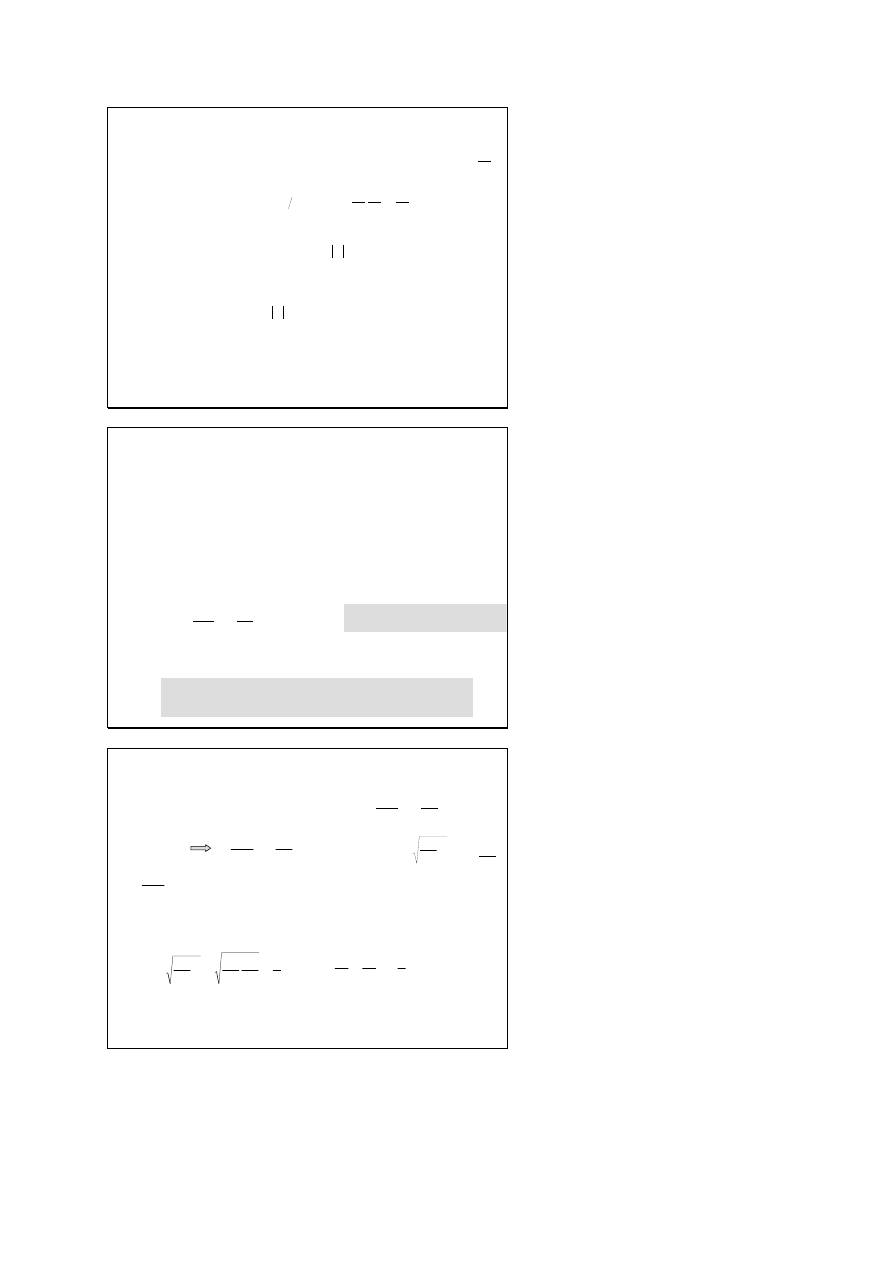
Postać funkcji falowej
o
o
o
k
h
h
p
π
λ
π
π
2
2
2
=
=
o
o
h
p
λ
=
o
o
k
p
h
=
π
2
o
o
h
=
h
Funkcja falowa cząstki o pędzie p
o
poruszającej się wzdłuż osi x,
odpowiada równaniu fali o długości λ
o
i wektorze falowym k
o
(
)
t
x
k
A
o
ω
−
=
Ψ
cos
Rzeczywista postać funkcji falowej jest niewłaściwa bo istniałyby
punkty, gdzie nie można cząstki zaobserwować. Lepsza zespolona
(
)
t
x
o
k
i
Ae
ω
−
=
Ψ
(
)
(
)
(
)
(
)
2
2
A
Ae
Ae
t
x
k
i
t
x
k
i
o
o
=
=
Ψ
Ψ
=
Ψ
−
−
−
∗
ω
ω
(
)
t
x
k
A
o
ω
−
=
Ψ
2
2
2
cos
Pokazaliśmy, że jeżeli pęd cząstki posiada określoną wartość, to
cząstkę można znaleźć z jednakowym prawdopodobieństwem w
dowolnym punkcie przestrzeni. Inaczej mówiąc,
Z hipotezy de Broglie’a:
jeżeli pęd cząstki
jest dokładnie znany, to nic nie wiemy o jej miejscu położenia.
Równanie Schrodingera
( )
[
]
Ψ
−
−
=
Ψ
x
U
E
m
dx
d
2
2
2
2
h
stacjonarne, jednowymiarowe
równanie Schrödingera
W sytuacjach stacjonarnych, gdy potencjał nie zmienia się w czasie,
zmienne przestrzenne i czas można rozseparować i zapisać funkcję
falową w postaci:
(
)
(
)
t
i
e
z
y
x
t
z
y
x
ω
−
Ψ
=
Ψ
,
,
,
,
,
Postać przestrzennej funkcji falowej, dla przypadku jednowymia-
rowego, wyznaczamy z równania Schrödingera:
gdzie: m – masa cząstki, E – całkowita energia mechaniczna cząstki,
U(x) – energia potencjalna w danym obszarze
równania Newtona – fale dźwiękowe i fale w strunach
równania Maxwella – fale świetlne
równanie Schrödingera – fale materii (funkcja falowa)
Równanie Schrodingera dla
cząstki swobodnej
( )
[
]
Ψ
−
−
=
Ψ
x
U
E
m
dx
d
2
2
2
2
h
Ψ
−
=
Ψ
E
m
dx
d
2
2
2
2
h
E
m
k
2
2
h
=
( )
0
=
x
U
Ψ
−
=
Ψ
2
2
2
k
dx
d
( )
ikx
ikx
Be
Ae
x
−
+
=
Ψ
oznaczając
którego rozwiązaniem jest
przyjmując B=0 (cząstka porusza się w kierunku dodatnich x)
(
)
( )
(
)
t
kx
i
t
i
Ae
e
x
t
x
ω
ω
−
−
=
Ψ
=
Ψ ,
funkcją falową cząstki swobodnej jest fala płaska o długości λ
określonej zależnością de Broglie’a
p
h
p
k
=
=
=
h
π
π
λ
2
2
m
p
E
2
2
=
tylko
kinetyczna
h
h
h
p
m
p
m
E
m
k
=
=
=
2
2
2
2
2
2
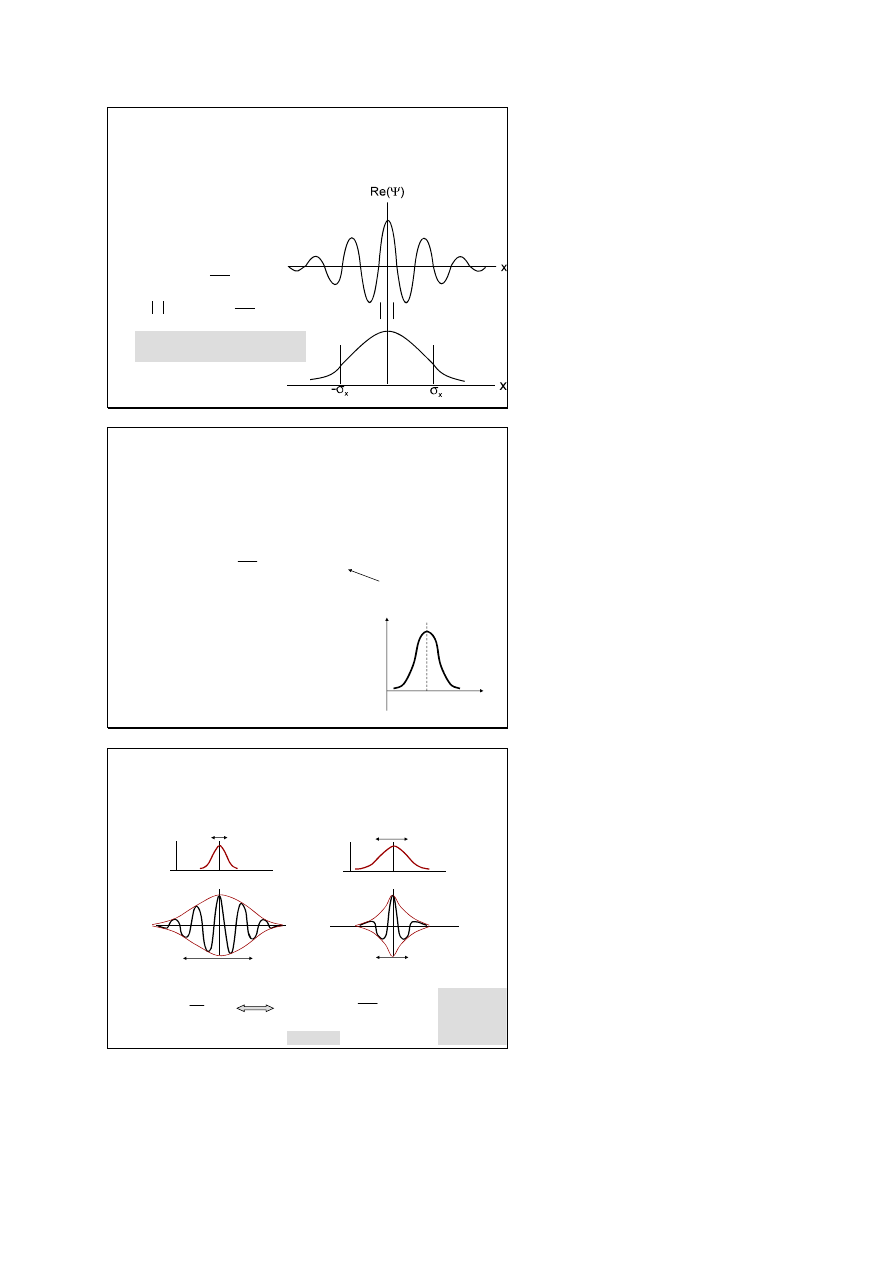
Paczki falowe materii
Dla cząstki znajdującej się w t=0 w
określonym obszarze przestrzeni
kwadrat modułu funkcji falowej
przyjmuje postać funkcji Gaussa
( )
(
)
x
ik
x
A
x
o
x
exp
exp
,
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
σ
−
=
Ψ
2
2
4
0
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
σ
−
=
Ψ
2
2
2
2
2
x
x
A exp
Ψ
2
Tak zlokalizowana funkcja
nazywana jest paczką falową
Elektron jako paczka falowa
przechodzi przez obie szczeliny
Superpozycja fal
monochromatycznych
(
)
( )
( )
∫
∞
∞
−
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
=
Ψ
dk
ikx
k
B
x
ik
x
o
x
exp
exp
exp
2
2
4
σ
Paczka falowa powstaje w wyniku superpozycji fal o różnych
długościach, którym odpowiadają różne wartości pędu
współczynniki Fouriera
Amplitudy tych fal B(k), zwane
współczynnikami Fouriera,
posiadają również postać funkcji
Gaussa wokół wartości k
o
Pomiędzy funkcją falową Ψ(x),
a współczynnikami Fouriera B(k)
istnieje ścisły związek
k
B(k)
k
o
Δk
niemożliwe jest jednoczesne dokładne określenie wartości
współrzędnej i pędu cząstki
Zasada nieoznaczoności
czym szerszy zakres k odpowiadający większemu rozrzutowi
Δp
x
, tym
paczka falowa jest przestrzennie węższa (mniejsze
Δx)
x
p
x
Δ
=
Δ
h
k
x
Δ
=
Δ
1
h
≥
Δ
Δ
x
p
x
B(k)
k
k
o
Re (Ψ)
x
B(k)
k
k
o
Re (Ψ)
x
k
p
x
Δ
=
Δ
h
Δk
Δx
Δx
gdy
Δ p
x
=0,
to
Δ x = ∞
cząstka
swobodna

Zasada nieoznaczoności w pociągu
2
λ
=
Δl
t
n
t
l
v
λ
=
=
λ
n
l =
n
v
t
t
l
v
2
2
=
=
Δ
=
Δ
λ
2
2
λ
n
l
x
=
=
Δ
4
λ
v
v
x
=
Δ
⋅
Δ
4
λ
p
p
x
=
Δ
⋅
Δ
chcemy zmierzyć prędkość pociągu wiedząc, że każdy wagon ma długość λ
minęło nas n wagonów w ciągu czasu t
pokonana przez pociąg droga wynosi
średnia prędkość
pociągu wynosi
im większy przedział czasu tym pomiar prędkości dokładniejszy, ale maleje
dokładność położenia pociągu w chwili pomiaru
w mechanice kwantowej pociąg to paczka falowa o długości fali λ
rozciągająca się na obszar l = n
λ
p
h
=
λ
h
≈
=
Δ
⋅
Δ
4
h
p
x
λ
Znaczenie zasady
nieoznaczoności Heisenberga
Δt=1/Δω
Δx=1/Δk
szerokość
paczki
falowej
k
p
h
=
h
=
Δ
⋅
Δ
p
x
ω
h
=
E
h
=
Δ
⋅
Δ
t
E
Działanie S można określić z dokładnością stałej Plancka
Zasada nieoznaczoności określa granice możliwości naszych
pomiarów.
Jest jednym z fundamentalnych twierdzeń mechaniki kwantowej:
• wyjaśnia dyfrakcję na szczelinie
• energie cząstek są zawsze większe od zera
• elektron nie spada na jądro atomowe
h
h
=
ΔS
Prędkość grupowa paczki
dk
d
v
g
ω
=
E
=
ω
h
p
k =
h
( )
m
k
2
2
h
h =
ω
m
p
E
2
2
=
m
k
dk
d
h
=
ω
v
m
p
m
k
dk
d
v
g
=
=
=
=
h
ω
v
v
g
=
Paczka falowa przemieszcza się z prędkością równą
prędkości cząstki
klasycznie
relatywistycznie
2
2
2
2
c
p
E
E
o
+
=
dp
pc
dE
E
2
2
2
=
v
mc
mv
c
E
p
c
dp
dE
dk
d
v
g
=
=
=
=
=
2
2
2
ω
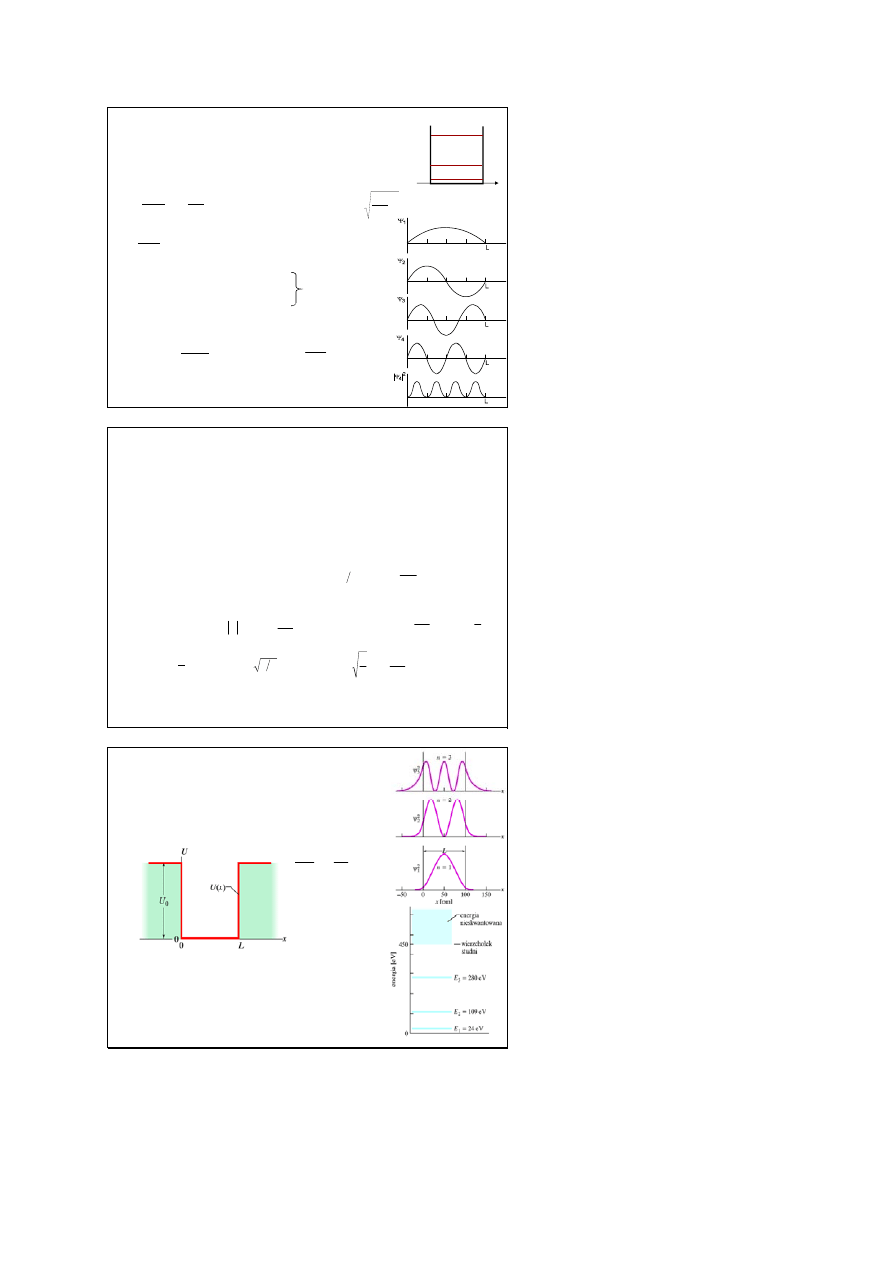
Równanie Schrodingera dla
nieskończonej jamy potencjału
wartości energii E
n
nazywamy wartościami własnymi
odpowiadające im funkcje falowe Ψ
n
– funkcjami
własnymi
( )
[
]
Ψ
−
−
=
Ψ
x
U
E
m
dx
d
2
2
2
2
h
E
m
k
2
2
h
=
( )
0
=
x
U
Ψ
−
=
Ψ
2
2
2
k
dx
d
( )
ikx
ikx
Be
Ae
x
−
+
=
Ψ
( )
( )
0
0
=
Ψ
=
Ψ
L
0
=
+ B
A
0
=
+
−ikL
ikL
Be
Ae
(
)
0
=
−
−ikL
ikL
e
e
A
( )
0
=
kL
sin
π
= n
kL
2
2
2
2
2mL
n
E
n
h
π
=
( )
⎟
⎠
⎞
⎜
⎝
⎛
=
Ψ
L
x
n
C
x
n
π
sin
0
L
U=0
U=∞
warunki brzegowe
E
1
E
2
E
3
U=∞
n=1,2,3...
Ai
C
2
=
Wnioski
energia jest skwantowana, występują dyskretne wartości
(poziomy) energii (n – liczba kwantowa)
cząstka nie może posiadać energii zerowej – wynika z
zasady nieoznaczoności
stałą C wyznaczamy z warunku unormowania
dla obiektów klasycznych poszczególne poziomy są tak
bliskie, że nierozróżnialne
L
x =
Δ
L
p h
≥
Δ
0
2
2
>
=
m
p
E
h
≥
Δ
Δ
p
x
1
0
0
2
2
=
⎟
⎠
⎞
⎜
⎝
⎛
=
Ψ
⋅
Ψ
∫
∫
dx
x
L
n
C
dx
L
L
π
sin
*
2
0
2
L
dx
x
L
n
L
=
⎟
⎠
⎞
⎜
⎝
⎛
∫
π
sin
1
2
2
=
L
C
L
C
2
=
( )
⎟
⎠
⎞
⎜
⎝
⎛
=
Ψ
x
L
n
L
x
n
π
sin
2
Elektron w skończonej
studni potencjału
studnia potencjału o głębokości U
o
( )
[
]
Ψ
−
−
=
Ψ
x
U
E
m
dx
d
2
2
2
2
h
równanie
Schrodingera
rozwiązujemy dla
trzech obszarów
wyniki zbliżone jak dla nieskończonej studni, lecz:
•fale materii wnikają w ściany studni
•energie dla każdego stanu są mniejsze niż w ∞
•elektron o energii większej od U
0
nie jest
zlokalizowany, jego energia nie jest skwantowana
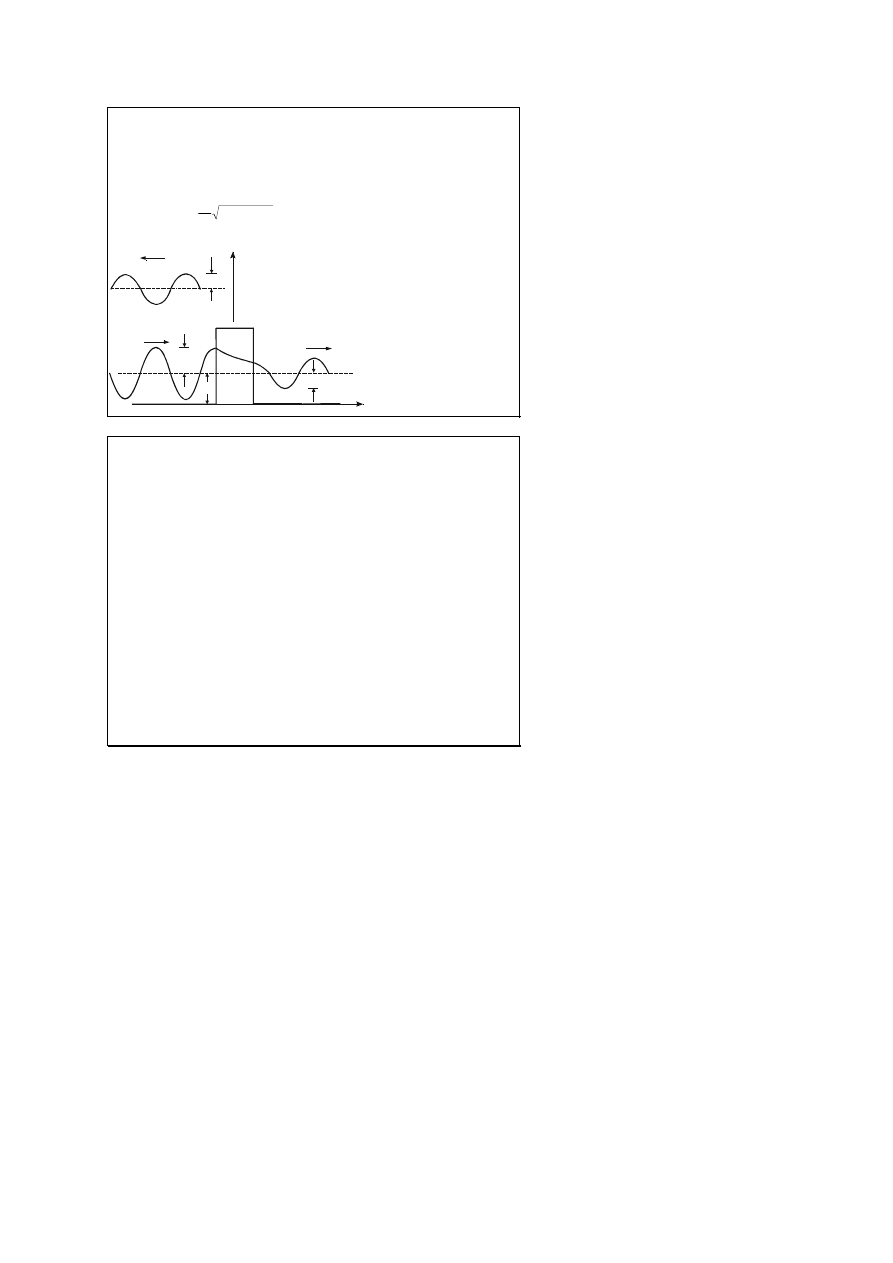
Efekt tunelowy - przenikanie
cząstki przez barierę potencjału
E
A
1
B
1
A
3
U >E
o
0 l
Ψ(x)
x
prawdopodobieństwo
przejścia przez barierę
potencjału zależy od L i U
o
szybko maleje ze
wzrostem jej szerokości i
wysokości
wg. mechaniki klasycznej
przenikanie przez barierę
jest niemożliwe
energia cząstki, w
odróżnieniu od jamy
potencjału nie jest
skwantowana
(
)
E
U
m
L
o
e
T
−
−
≈
2
2
h
Przykłady efektu
tunelowego
Dioda tunelowa (efekt tunelowy w złączu
p-n) Nagroda Nobla 1973r
Esaki - tunelowanie w półprzewodnikach
np. diody tunelowe
Giaever - tunelowanie w nadprzewodnikach
Josephson – złącze Josephsona, szybki
przełącznik kwantowy
Skaningowy Mikroskop Tunelowy
Binning i Rohrer Nagroda Nobla 1986r
Wyszukiwarka
Podobne podstrony:
fizyka kwantowa i J5NRKIZME7MPW Nieznany
05 Komunikacja aplikacji z ser Nieznany
05 rozdzial 04 nzig3du5fdy5tkt5 Nieznany (2)
CERN FIZYKA CZASTEK ELEMENTARNY Nieznany
Fizyka 1 id 175686 Nieznany
Lab 05 Obliczenia w C id 257534 Nieznany
05 Elewacje A1id 5681 Nieznany (2)
05 Pielegnowanie konczyn dolnyc Nieznany (2)
%9cwiat%b3o+a+fizyka+kwantowa FIE44NASQGDAHUBJ53IEAGGJG3WCSRIMILDMGMI
Fizyka 5 id 175251 Nieznany
7 05 2013 grammaire contrastive Nieznany (2)
Moje fizyka id 306511 Nieznany
05 Wykonywanie zabiegow agrotec Nieznany (2)
probabilistyczna natura wiata czyli chaos jako nauka fizyka kwantowa magia
05 Sporzadzanie rysunku technic Nieznany
więcej podobnych podstron