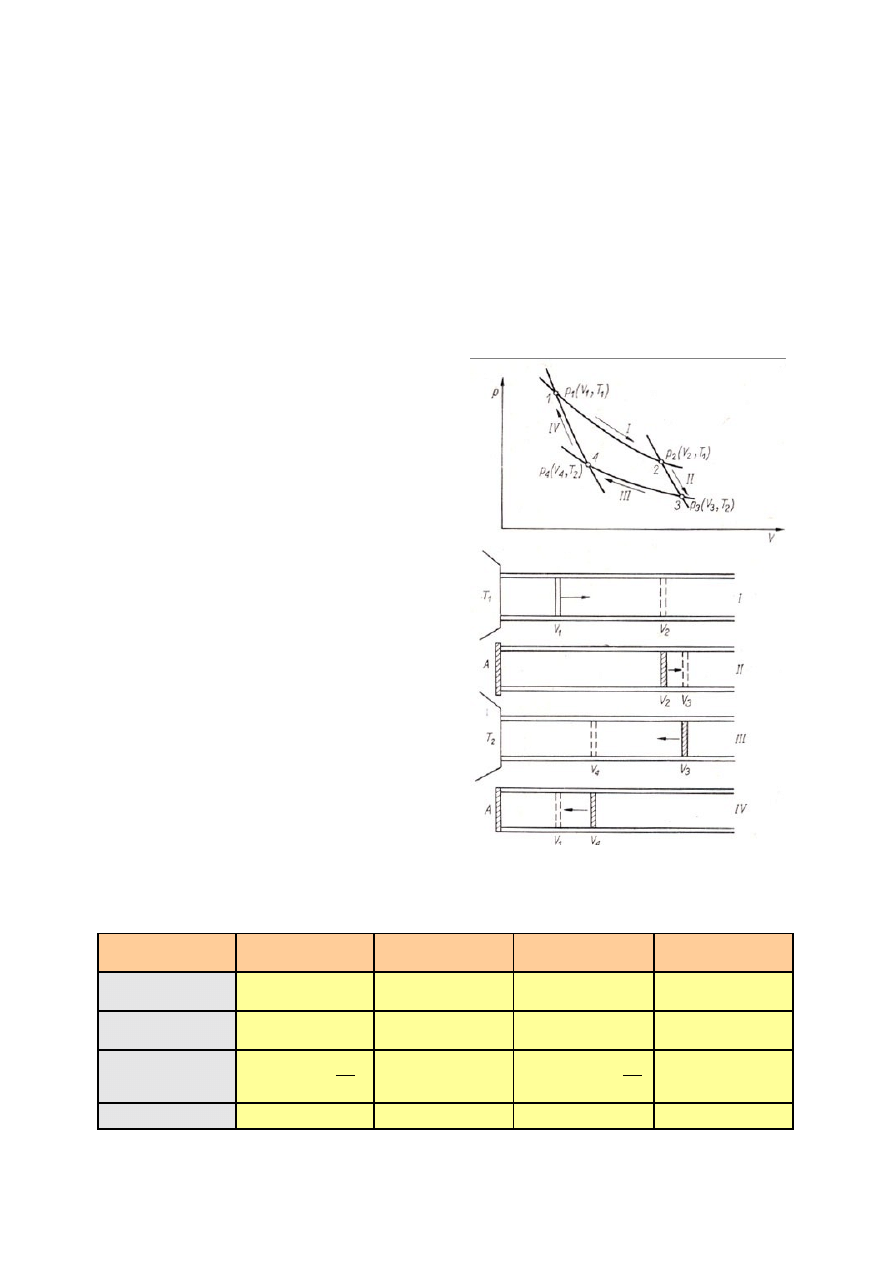
Cykl Carnota
Rozważania poniższe dotyczą maszyny cieplnej wyidealizowanej, w której procesy
przebiegają odwracalnie. Nie ma tu strat ciepła spowodowanych tarciem lub uchodzeniem
przez ściany izolujące. Maszyna ta wykonuje cykl zamknięty Carnota, tzn. po pewnej liczbie
przemian wraca z powrotem do stanu wyjściowego. Ciałem, które podlega procesowi
cyklicznemu, jest gaz doskonały.
Cykl Carnota składa się z 4 kolejnych procesów:
I. Rozprężania izotermicznego w temperaturze T
l
.
II. Rozprężania adiabatycznego przy zmianie temperatury od T
l
do T
2
.
III. Sprężania izotermicznego w temperaturze T
2
.
IV. Sprężania adiabatycznego przy zmianie temperatury od T
2
do T
l
.
Po przejściu tych czterech procesów gaz wraca
do stanu wyjściowego. Rysunek 1 przedstawia
wykres cyklu Carnota we współrzędnych p, V;
poniżej wykresu są pokazane położenia tłoka w
zbiorniku gazu na początku i na końcu każdego
procesu. Zbiornik gazu ma ścianki i tłok z
osłony adiabatycznej, tzn. nie przepuszczającej
ciepła, doskonale zaś przepuszczająca ciepło
podstawa może być ustawiona na zbiorniku
ciepła o temperaturze T
1,
zwanym grzejnicą, lub
na zbiorniku o temperaturze niższej T
2
, zwanym
chłodnicą, albo też na osłonie adiabatycznej A.
Punkty 2 i 3 cyklu Carnota mogą być dowolnie
obrane, byleby leżały na izotermach
odpowiadających temperaturom T
l
i T
2
,
natomiast punkt 4 o współrzędnych p
4
, V
4
, T
4
nie może być dowolnie obrany na izotermie,
ponieważ wartości p
4
i V
4
są wyznaczone przez
wartości p
l
, V
1
, T
1
punktu początkowego 1 oraz
temperaturę T
2
. Zmiany objętości gazu i jego
temperatury oraz wielkość pracy wykonanej
przez gaz i ilość ciepła pobranego w
poszczególnych procesach cyklu zestawione są
w Tabeli 1.
Tabela 1
Proces
Rozprężanie
izotermiczne
Rozprężanie
adiabatyczne
Sprężanie
izotermiczne
Sprężanie
adiabatyczne
Zmiana
objętości
2
1
V
V
→
3
2
V
V
→
4
3
V
V
→
1
4
V
V
→
Zmiana
temperatury
.
1
const
T
=
2
1
T
T
→
.
2
const
T
=
1
2
T
T
→
Wykonana
praca
2
1
1
ln
V
V
RT
W
=
(
)
1
2
2
T
T
c
W
V
−
=
3
4
2
3
ln
V
V
RT
W
−
=
(
)
2
1
4
T
T
c
W
v
−
=
Ciepło pobrane
1
Q
0
2
Q
0
Dla procesów adiabatycznych (II i IV) możemy zapisać następujące związki:
Rysunek 1 Cykl Carnota: a) Wykres cyklu, b)
położenie tłoka na początku i na końcu każdego
procesu

1
1
1
2
1
4
1
1
2
2
1
3
T
V
T
V
T
V
T
V
−
−
−
−
=
=
χ
χ
χ
χ
.
Dzieląc stronami otrzymujemy:
1
1
2
1
4
3
−
−
=
χ
χ
V
V
V
V
czyli:
.
1
2
4
3
V
V
V
V
=
*
Praca wykonana w procesie III wynosi:
3
4
2
3
ln
V
V
RT
W
−
=
,
.
ln
4
3
2
3
V
V
RT
W
=
Korzystając z * możemy zapisać:
,
ln
2
1
2
3
V
V
RT
W
−
=
czyli:
.
3
1
W
W
−
=
Podczas cyklu gaz pobrał z grzejnicą o temperaturze T
1
ciepło Q
1
i oddał do chłodnicy o
temperaturze T
2
ilość ciepła Q
2
oraz wykonał pracę W
1
+W
2
, a pobrał W
3
+W
4
.
Widzimy, że suma prac w procesach adiabatycznych jest równa 0. Zatem suma prac
pobranych i wykonanych w cyklu Carnota, wynosi:
(
)
.
ln
2
1
2
1
3
1
V
V
T
T
R
W
W
W
−
=
+
=
Z I zasady termodynamiki dla przemiany izotermicznej mamy
,
Q
W
−
=
czyli:
1
2
1
1
1
ln
Q
V
V
RT
W
−
=
=
i analogicznie:
2
2
1
2
3
ln
Q
V
V
RT
W
−
=
−
=
stąd:
(
)
(
)
.
ln
2
1
2
1
2
1
3
1
Q
Q
V
V
T
T
R
W
W
W
+
−
=
−
=
+
=
Ponieważ V
1
< V
2
, więc W
1
jest ujemne, W
3
– dodatnie, W zaś ujemne, gdyż T
1
> T
2
. Zatem
Q
1
jest dodatnie, Q
2
jest ujemne i oznacza ciepło oddane. Rezultatem cyklu jest więc praca W
wykonana przez gaz kosztem pobranego ciepła
.
2
1
Q
Q
−
Ponieważ
2
1
W
W
>
bo
2
1
T
T
>
,
więc
,
2
1
Q
Q
>
czyli ciepło pobrane jest większe od oddanego.
Wprowadzamy definicję wydajności (sprawności) cyklu jako stosunek ciepła
2
1
Q
Q
−
zamienionego na pracę do całkowitego ciepła pobranego
:
1
Q
.
1
2
1
Q
Q
Q
−
=
η
Dla silnika Carnota można również zapisać:

(
)
,
ln
ln
2
1
1
2
1
2
1
1
V
V
RT
V
V
T
T
R
W
W
−
=
=
η
czyli:
.
1
2
1
T
T
T
−
=
η
I twierdzenie Carnota:
Wszystkie maszyny termodynamiczne odwracalne pracujące między tymi samymi
temperaturami mają tę samą sprawność.
II twierdzenie Carnota
Silnik nieodwracalny nie może mieć większej sprawności od silnika odwracalnego.
Wyszukiwarka
Podobne podstrony:
Cykl Carnota
00518 Termodynamika D part 3 2008 cykl Carnota, zasady termodynamiki(1)
8 Cykl koniunkturalny
Cykl życiowy komórki
cykl Przyjaciel zwierząt 1
Cykl Krebsa
ITIL v3 Cykl życia usług IT
cykl Ekolog 1
Cykl koniunkturalny
Jak radzić sobie z agresywnymi uczniami, cykl VII artererapia
cykl i jego fazy 2., Ściągi Ekonomia
d druku BIBLIOGRAFI1, cykl VII artererapia, Karolina Sierka (praca dyplomowa; terapia pedagogiczna z
Wskazówki do pracy teraputycznej, cykl VII artererapia
cykl coricha, INNE KIERUNKI, biologia
więcej podobnych podstron