
IL
USTRACJA JANA BRENNING
54
ÂWIAT NAUKI KWIECIE¡ 2004
B
ia∏e Êlady na lusterku. Ig∏a i ∏y˝eczka. Wielu narkomanów ju˝ na sam widok narkotyku lub akce-
soriów do jego za˝ywania odczuwa przyjemny dreszczyk oczekiwania. A ju˝ w chwil´ po za˝y-
ciu przychodzi prawdziwa rozkosz: fala ciep∏a, jasnoÊç umys∏u, wizja, ulga, poczucie bycia p´p-
kiem Êwiata. Na jeden krótki moment wszystko jest tak, jak byç powinno. Ale po wielokrotnym
za˝ywaniu Êrodków uzale˝niajàcych – czy to heroiny czy kokainy, whisky czy te˝ amfetaminy – coÊ
si´ zaczyna psuç.
Dawka zapewniajàca do niedawna eufori´ ju˝ nie wystarcza i za˝ywajàcy musi sobie „daç w ˝y-
∏´” lub powàchaç, ˝eby poczuç si´ po prostu normalnie; bez tego wpada w depresj´, a nawet cho-
ruje. To wtedy rodzi si´ przymus brania. Bioràcy jest ju˝ uzale˝niony. Utraci∏ kontrol´ i odczuwa
silny g∏ód narkotyczny nawet wtedy, gdy rozkosz mija, a na∏óg zaczyna si´ negatywnie odbijaç
na zdrowiu, finansach i stosunkach z najbli˝szymi.
Neurobiolodzy wiedzà od dawna, ˝e mechanizm euforii narkotycznej polega na pobudza-
jàcym dzia∏aniu Êrodka chemicznego, jakim jest narkotyk, na cz´Êç mózgu zwanà uk∏a-
dem nagrody: skomplikowany obwód sk∏adajàcy si´ z komórek nerwowych, czyli neuro-
nów, powsta∏ych w procesie ewolucji po to, byÊmy po spo˝yciu posi∏ku lub po akcie
seksualnym – czynnoÊciach niezb´dnych do przetrwania i przekazania genów potom-
stwu – odczuli przyp∏yw zadowolenia. Kiedy si´ ten uk∏ad oszuka, przynajmniej na po-
czàtku, samopoczucie si´ poprawia i rodzi si´ ch´ç powtórzenia czynnoÊci spra-
wiajàcej tak wielkà przyjemnoÊç.
Ale z najnowszych badaƒ wynika, ˝e za˝ywanie narkotyków przez d∏u˝szy czas
zmienia struktur´ i funkcjonowanie neuronów sk∏adajàcych si´ na uk∏ad na-
grody i ˝e zmiany te utrzymujà si´ przez wiele tygodni, miesi´cy, a nawet lat
od ostatniej dzia∏ki. Co gorsza, zmiany te zmniejszajà przyjemnoÊç, jakà
za˝ywajàcy czerpie ze sta∏ego przyjmowania narkotyku, zwi´kszajàc
zarazem g∏ód owej substancji i zakleszczajàc cz∏owieka w destrukcyjnej
m
ó
z
g
Zniewolony
Narkomania powoduje
d∏ugotrwa∏e zmiany
w mózgowych obwodach
uk∏adu nagrody.
Poznanie szczegó∏ów tego
procesu mo˝e przyczyniç si´
do wynalezienia nowych
metod leczenia uzale˝nieƒ
m
ó
z
g
Eric J. Nestler i Robert C. Malenka

SUBSTANCJE UZALE˚NIAJÑCE wyp∏ywajà na uk∏ad nagrody w mózgu
w taki sposób, ˝e ten bardziej sobie ceni narkotyki ni˝ cokolwiek innego
na Êwiecie. Jest to jedna z istotnych przyczyn rozwoju uzale˝nienia.
spirali coraz wi´kszych dawek i coraz
wi´kszego zaniedbywania obowiàzków
szkolnych lub zawodowych i rodzin-
nych. Lepsze zrozumienie mechanizmu
tych zmian na poziomie neuronalnym
powinno dopomóc w tworzeniu coraz
skuteczniejszych metod przeciwdzia∏a-
jàcych uzale˝nieniom, tak by ludzie, któ-
rzy wpadli w szpony Êrodków uzale˝-
niajàcych, mogli wydrzeç im swój mózg
i swoje ˝ycie.
Narkotyki warte grzechu
ÂWIADOMOÂ
å
, ˝e ró˝ne narkotyki powo-
dujà uzale˝nienie, poniewa˝ oddzia∏ujà
na te same drogi nerwowe, zawdzi´czamy
przede wszystkim badaniom na zwierz´-
tach rozpocz´tym przed mniej wi´cej 40
laty. Majàc po temu sposobnoÊç, szczury,
myszy i naczelne b´dà si´ga∏y po te same
substancje, których i ludzie sk∏onni sà
nadu˝ywaç. Zwierz´ta doÊwiadczalne
pod∏àcza si´ do kroplówki, a nast´pnie
uczy naciskaç trzy przyciski: jeden daw-
kujàcy do˝ylnie narkotyk, drugi dawku-
jàcy stosunkowo nieciekawy roztwór so-
li fizjologicznej i trzeci wydajàcy suchà
karm´. Po kilku zaledwie dniach zwierz´-
ta sà ju˝ uzale˝nione: ochoczo dawkujà
sobie kokain´, heroin´, amfetamin´ i in-
ne popularne narkotyki.
Co wi´cej, w koƒcu zaczynajà zdra-
dzaç objawy uzale˝nienia. Zamiast wy-
konywaç normalne czynnoÊci ˝yciowe,
na przyk∏ad jeÊç i spaç, aplikujà sobie
narkotyki. Niektóre zwierz´ta robià to
bez opami´tania, a˝ zdychajà z prze-
m´czenia lub niedo˝ywienia. W przypad-
ku substancji najsilniej uzale˝niajàcych,
jak kokaina, zwierz´ta wi´kszoÊç okresu
czuwania poÊwi´cajà na zdobywanie co-
raz wi´kszych iloÊci narkotyku, nawet je-
Êli pozyskanie jednej dzia∏ki wymaga kil-
kuset naciÊni´ç przycisku. I tak jak ludzie,
którzy odczuwajà silny g∏ód, kiedy widzà
akcesoria zwiàzane z narkotykiem lub
miejsca, w których uda∏o im si´ go zdo-
byç, równie˝ zwierz´ta wolà przebywaç
w otoczeniu, które kojarzy im si´ z nar-
kotykiem – w tej cz´Êci klatki, w której
naciÊni´cie przycisku zawsze skutkuje
chemicznà rekompensatà.
Po odstawieniu substancji zwierz´ta
szybko zaprzestajà czynnoÊci prowadzà-
cych do uzyskania chemicznego zaspo-
kojenia. Ale pami´ç o przyjemnoÊci zo-
staje. Szczur, który nie bra∏ narkotyku na-
wet przez kilka miesi´cy, natychmiast
wznawia naciskanie przycisku, kiedy tyl-
ko da mu si´ skosztowaç kokainy lub
umieÊci si´ go w klatce, która kojarzy mu
si´ z narkotycznà euforià. Niektóre ro-
dzaje stresu psychicznego, na przyk∏ad
okresowe nieoczekiwane ra˝enie pràdem
stopy, sprawiajà, ˝e szczur b∏yskawicznie
rusza na poszukiwanie narkotyku. Ten
sam rodzaj bodêców – kontakt z ma∏ymi
dawkami narkotyku, skojarzenie z nar-
kotykiem, stres – uruchamiajà g∏ód i na-
wroty na∏ogu u ludzi uzale˝nionych.
Za pomocà opisanej tu metody samo-
dawkowania i innych podobnych technik
eksperymentalnych uda∏o si´ odtworzyç
map´ obszarów mózgu poÊredniczàcych
w zachowaniach zwiàzanych z uzale˝nie-
niami i odkryç kluczowà rol´, jakà w tych
zachowaniach odgrywa uk∏ad nagrody.
Narkotyki biorà ten uk∏ad we w∏adanie,
56
ÂWIAT NAUKI KWIECIE¡ 2004
n
Substancje uzale˝niajàce – kokaina, alkohol, opiaty, amfetamina – przejmujà kontrol´
nad naturalnym uk∏adem nagrody w mózgu. Stymulacja tej drogi wzmacnia zachowanie,
powodujàc, ˝e cokolwiek si´ zrobi, b´dzie chcia∏o si´ to zrobiç jeszcze raz.
n
Wielokrotny kontakt z tymi substancjami prowadzi do d∏ugotrwa∏ej adaptacji w sk∏adzie
chemicznym i strukturze mózgu, modyfikujàc sposób przetwarzania informacji
przez pojedyncze neurony wchodzàce w sk∏ad uk∏adu nagrody i ich wzajemne interakcje.
n
Lepsze zrozumienie mechanizmów, za których poÊrednictwem d∏ugotrwa∏y kontakt
z substancjami uzale˝niajàcymi powoduje zmiany w mózgu osoby uzale˝nionej,
pomog∏oby w wynalezieniu nowych, skuteczniejszych metod korygowania aberracji
komórkowych i molekularnych le˝àcych u pod∏o˝a wszystkich uzale˝nieƒ.
Przeglàd /
Ewolucja uzale˝nieƒ
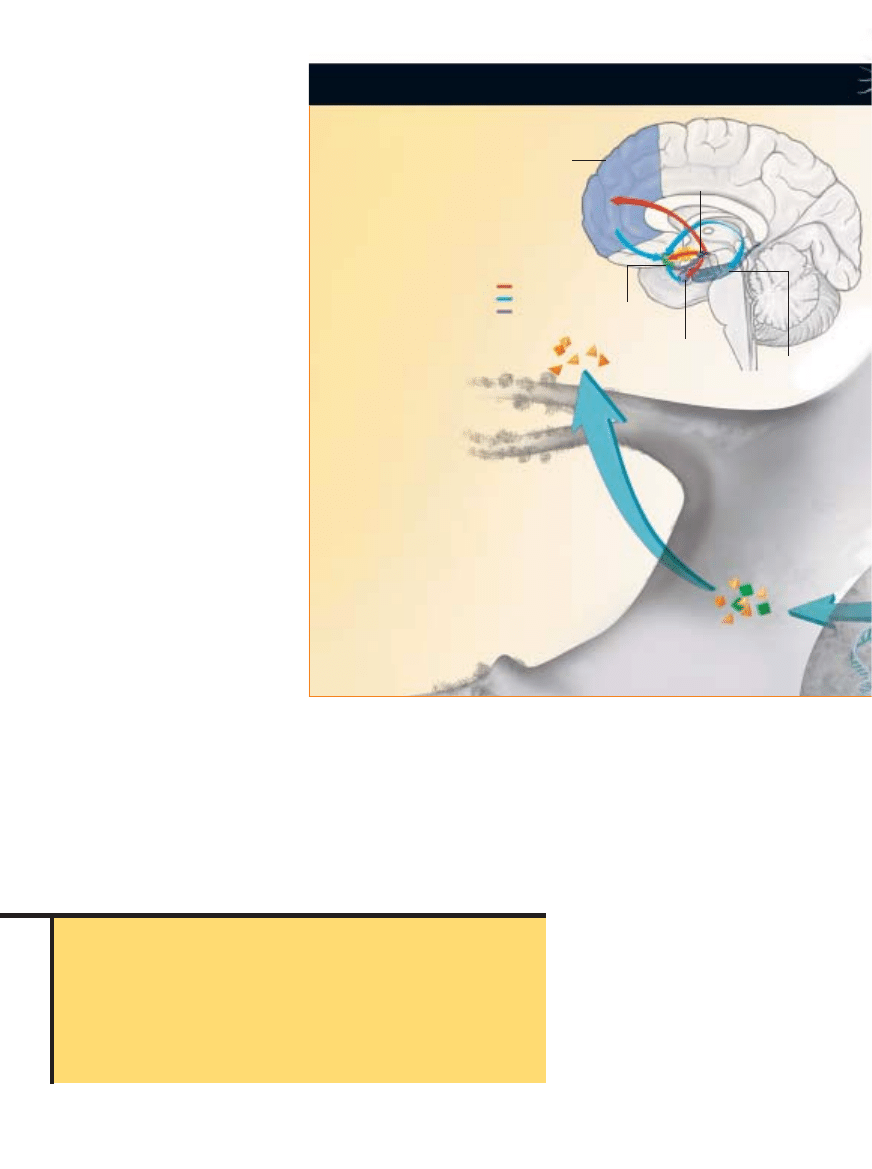
MÓZG UZALE˚NIONY
D¸UGOTRWA¸E ZA˚YWANIE
substancji uzale˝niajàcych
powoduje, ˝e zmieniajà si´
czynnoÊç i struktura kluczowej
cz´Êci mózgowego uk∏adu
nagrody: dróg prowadzàcych
z neuronów produkujàcych
dopamin´ w polu brzusznym
nakrywki (VTA – ventral
tegmental area) do komórek
wra˝liwych na dopamin´
w jàdrze pó∏le˝àcym (NA
– nucleus accumbens).
Zmiany te, zapoczàtkowane
po cz´Êci przez pokazane
z prawej strony rysunku
mechanizmy molekularne, majà
silny wp∏yw na powstawanie
tolerancji, uzale˝nienia i g∏odu,
czynników podsycajàcych
na∏ogowe si´ganie po narkotyki
i powodujàcych nawroty
nawet po d∏ugich okresach
abstynencji. Kolorowe strza∏ki
na schemacie mózgu pokazujà
niektóre drogi nerwowe
∏àczàce jàdro pó∏le˝àce i VTA
z innymi obszarami mózgu
czyniàcymi narkomana
szczególnie wra˝liwym
na miejsca, przedmioty
i sytuacje przypominajàce
dawnà eufori´, nara˝ajàcymi
go na nawroty pod wp∏ywem
stresu i uniemo˝liwiajàcymi
kontrol´ nad g∏odem
narkotycznym.
Kora
przedczo∏owa
Pole brzuszne
nakrywki (VTA)
Jàdro
pó∏le˝àce
(NA)
Dynorfina
Do
VTA
Cia∏o
migda∏owate
Komórka wra˝liwa
na dopamin´
w jàdrze pó∏le˝àcym
Hipokamp
Uwalniane
neuroprzekaêniki:
Dopamina
Glutaminian
GABA
4
Bia∏ko zwane
dynorfinà
przesy∏ane jest do
VTA, gdzie hamuje
uwalnianie dopaminy
i t∏umi uk∏ad nagrody,
powodujàc, ˝e narkoman
musi przyjmowaç
coraz wi´ksze
dawki narkotyku,
by odczuwaç
rozkosz.
3
Te geny uruchamiajà
produkcj´ bia∏ek
odpowiedzialnych za
tolerancj´ i uzale˝nienie
stymulujàc go do dzia∏ania z si∏à i wy-
trwa∏oÊcià znacznie wi´kszà od jakiejkol-
wiek naturalnej nagrody.
Jednym z kluczowych elementów
uk∏adu nagrody jest mezolimbiczny
uk∏ad dopaminergiczny: grupa komórek
nerwowych po∏o˝ona w polu brzusznym
nakrywki (VTA – ventral tegmental area),
w pobli˝u podstawy mózgowia i wysy-
∏ajàca po∏àczenia do miejsc docelowych
w p∏acie czo∏owym – przede wszystkim
do po∏o˝onej poni˝ej kory czo∏owej
struktury nazywanej jàdrem pó∏le˝àcym
(u cz∏owieka okreÊlanym równie˝ jako
dno prà˝kowia). Neurony VTA porozu-
miewajà si´ ze sobà w ten sposób, ˝e wy-
dzielajà chemiczny neuroprzekaênik
– dopamin´ – z zakoƒczeƒ aksonalnych
d∏ugich dróg wst´pujàcych do recepto-
rów znajdujàcych si´ na neuronach jàdra
pó∏le˝àcego. Droga dopaminergiczna
z VTA do jàdra pó∏le˝àcego odgrywa
krytycznà rol´ w uzale˝nieniach: zwie-
rz´ta, którym uszkodzono te obszary
mózgu, przestajà si´ interesowaç sub-
stancjami uzale˝niajàcymi.
Reostat nagrody
DROGI UK
¸ADU NAGRODY
nale˝à do ewo-
lucyjnie najstarszych. Nawet ma∏o skom-
plikowany nicieƒ Caenorhabditis elegans
ma bardzo podstawowà postaç tego
uk∏adu. Unieruchomienie od czterech
do oÊmiu kluczowych neuronów zawie-
rajàcych dopamin´ powoduje, ˝e zwie-
rz´ to mija oboj´tnie „kupk´” bakterii,
swojà ulubionà potraw´.
U ssaków uk∏ad nagrody jest bardziej
z∏o˝ony i ÊciÊle powiàzany z kilkoma in-
nymi obszarami mózgu, których za-
daniem jest zabarwianie doÊwiadczeƒ
emocjami i kierowanie reakcji osobnika
ku bodêcom nagradzajàcym, takim jak
po˝ywienie, seks i kontakty spo∏eczne.
I tak cia∏o migda∏owate pomaga oceniç,
czy dane doÊwiadczenie jest przyjem-
ne czy przykre i czy nale˝y je powtórzyç,
czy te˝ przeciwnie – trzeba go unikaç,
pomaga te˝ w tworzeniu nowych po-
∏àczeƒ mi´dzy doÊwiadczeniem a inny-
mi bodêcami; hipokamp uczestniczy w
rejestracji wspomnieƒ dotyczàcych dane-
go doÊwiadczenia – kiedy ono nastàpi∏o,
jakie by∏y okolicznoÊci; okolice czo∏owe
kory mózgu zaÊ odpowiedzialne sà za ko-
ordynacj´ i przetwarzanie wszystkich
tych informacji, i ustalenie, jak ostatecz-
nie nale˝y si´ zachowaç. Tymczasem dro-
ga z VTA do jàdra pó∏le˝àcego pe∏ni ro-
l´ reostatu nagrody: „informuje” inne
oÊrodki mózgowe o wielkoÊci nagrody,
jakà mo˝na uzyskaç za okreÊlone zacho-
wanie. Im wi´ksza nagroda, tym wi´ksze
prawdopodobieƒstwo, ˝e organizm do-
brze to konkretne zachowanie zapami´-
ta i b´dzie je powtarza∏.
KWIECIE¡ 2004 ÂWIAT NAUKI
57
TERESE WINSL
OW
1
2
3
4
5
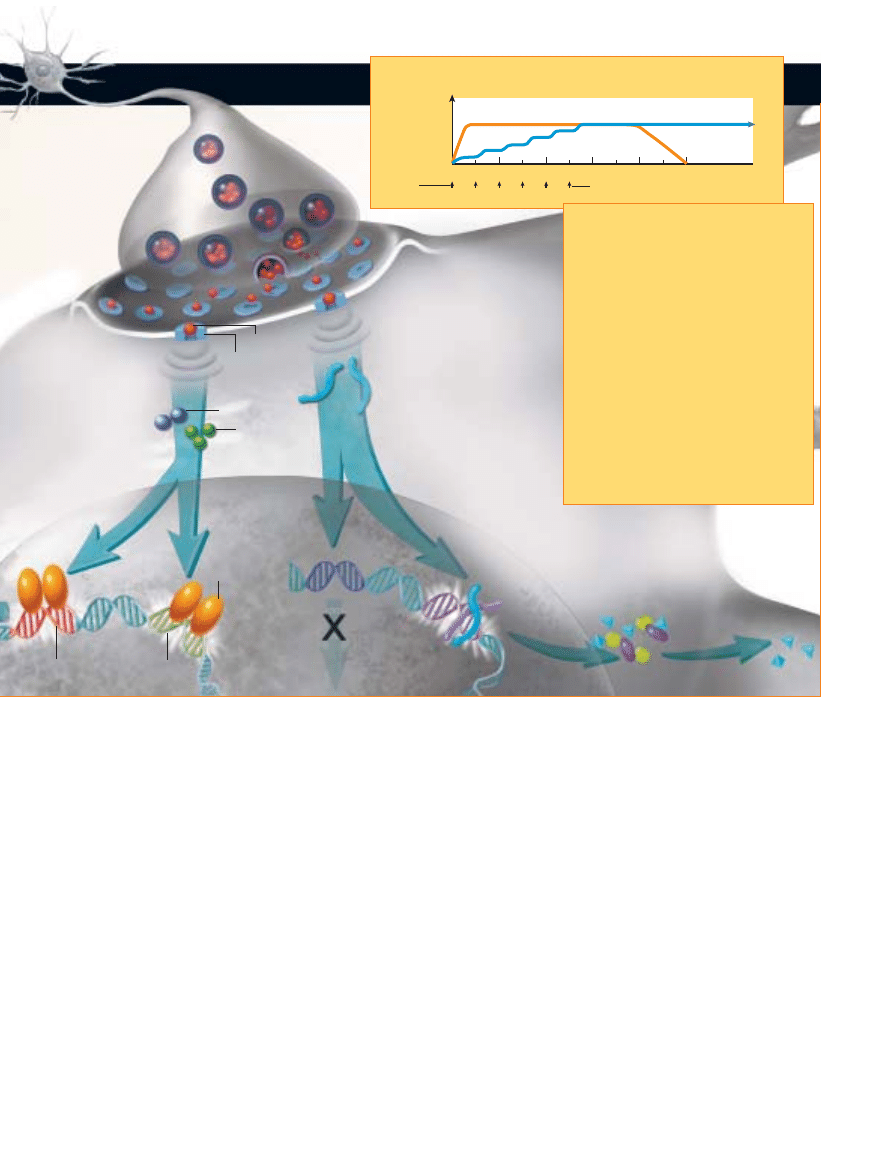
O TYM, CZY MA SI¢ dobrà tolerancj´
na narkotyk, czy – przeciwnie – jest si´ naƒ
szczególnie wra˝liwym, decyduje po cz´Êci
poziom aktywnego CREB i ∆FosB w komórkach
jàdra pó∏le˝àcego. Z poczàtku dominuje
CREB, prowadzàc do tolerancji i, w razie
braku narkotyku, do poczucia dyskomfortu,
który uÊmierzyç mo˝e tylko wi´ksza dawka
tej substancji. Ale je˝eli nie b´dzie
podtrzymywany przez kolejne dawki,
poziom CREB spadnie w ciàgu kilku dni.
Inaczej rzecz si´ ma z poziomem ∆FosB,
który raz podwy˝szony utrzymuje si´
na wzniesionym poziomie jeszcze przez
wiele tygodni po ostatnim kontakcie
z narkotykiem. A zatem spadkowi poziomu
CREB towarzyszy niebezpieczne, d∏ugotrwa∏e
dzia∏anie ∆FosB uwra˝liwiajàce na narkotyk,
które z czasem zaczyna dominowaç.
Komórka nerwowa VTA
produkujàca dopamin´
CREB:
èród∏o tolerancji
Delta FosB:
Klucz do g∏odu
Dopamina
Receptor
dopaminowy
∆FosB
cAMP
Ca
2+
Jàdro
CREB
Gen dynorfiny
Brak dynorfiny
Gen aktywowany
przez ∆FosB
CDK5
Geny aktywowane przez CREB
1
Sygnalizacja dopaminy
zwi´ksza iloÊç cyklicznego
AMP (cAMP) i koncentracj´
jonów wapnia (Ca
2+
)
1
Aktywowana dopamina
prowadzi do produkcji
bia∏ka delta FosB (∆FosB)
2
∆FosB hamuje syntez´
dynorfiny i aktywuje
specyficzne geny (odmienne
od genów w∏àczanych
przez CREB)
3
Aktywowane geny
powodujà produkcj´
bia∏ek odpowiedzialnych
za zwi´kszenie reaktywnoÊci
na narkotyki i na
wspomnienia o wczeÊniej
u˝ytych narkotykach
4
Bia∏ko CDK5 mo˝e
powodowaç zmiany
strukturalne trwale
uwra˝liwiajàce neurony
jàdra pó∏le˝àcego
na narkotyki i zwiàzki
narkotykopodobne
2
Wzrost ten szybko
aktywuje bia∏ko zwane
CREB. Aktywowane CREB
wià˝e si´ z DNA
i aktywuje okreÊlone
geny
CZAS ROBI SWOJE
Poziom
aktywnoÊci
CREB
Kontakt
z narkotykiem
Liczba dni
Ostatni kontakt z narkotykiem
∆FosB
Wi´kszoÊç naszej wiedzy na temat
mózgowego uk∏adu nagrody pochodzi z
eksperymentów na zwierz´tach, ale z ba-
daƒ wykonanych w ciàgu ostatnich 10
lat na ludziach technikà obrazowania
mózgu wynika, ˝e analogiczne drogi ner-
wowe kontrolujà mechanizm nagrody
cz∏owieka – zarówno naturalny, jak i
wzbudzony przez narkotyki. Dzi´ki zasto-
sowaniu takich technik, jak funkcjonal-
ny rezonans magnetyczny (fMRI) czy
emisyjna tomografia pozytonowa (PET),
czyli technik pomiaru zmian w przep∏y-
wie krwi zwiàzanych z aktywnoÊcià neu-
ronów, badacze mogli zobaczyç, jak u
kokainistów rozÊwietla si´ jàdro pó∏le-
˝àce, gdy zaproponuje im si´ dzia∏k´ ko-
kainy do powàchania. Kiedy tym samym
narkomanom poka˝e si´ nagranie wi-
deo przedstawiajàce kogoÊ, kto wàcha
kokain´, lub fotografi´ przedstawiajàcà
bia∏e Êlady na lusterku, jàdro pó∏le˝àce
reaguje podobnie, razem z cia∏em mig-
da∏owatym i kilkoma innymi obszarami
mózgu. Te same obszary mózgu o˝ywa-
jà u na∏ogowych hazardzistów, którym
pokazano zdj´cia automatów do gier.
Mo˝na z tego wnioskowaç, ˝e droga
VTA–jàdro pó∏le˝àce odgrywa równie
krytycznà rol´ w innych uzale˝nieniach
nawet bez udzia∏u narkotyków.
Dopamin´ prosz´
JAK TO MO
˚LIWE
, ˝e najrozmaitsze sub-
stancje uzale˝niajàce, niemajàce ˝ad-
nych wspólnych cech strukturalnych
i wp∏ywajàce na organizm w bardzo ró˝-
ny sposób, wywo∏ujà podobnà reakcj´
w mózgowym uk∏adzie nagrody? Jak to
si´ dzieje, ˝e kokaina, Êrodek pobudza-
jàcy, silnie przyÊpieszajàcy akcj´ serca,
i heroina, Êrodek uspokajajàcy i prze-
ciwbólowy, pod pewnymi wzgl´dami tak
ró˝ne, podobnie oddzia∏ujà na uk∏ad na-
grody? Odpowiedê jest prosta. Wszyst-
kie narkotyki, poza dzia∏aniem innego
rodzaju, powodujà, ˝e jàdro pó∏le˝àce
otrzymuje du˝à dawk´ dopaminy, a cza-
sem tak˝e odbiera sygna∏y naÊladujàce
dopamin´.
W stanie pobudzenia komórka ner-
wowa znajdujàca si´ w VTA wysy∏a b∏y-
skawicznie sygna∏ elektryczny, który
biegnie aksonem – „infostradà” si´gajà-
cà zakoƒczeniem jàdra pó∏le˝àcego.
Sygna∏ ów powoduje uwolnienie do-
paminy z czubka aksonu do maleƒkiej
przestrzeni – szczeliny synaptycznej –
oddzielajàcej koƒcówk´ aksonu od neu-
ronu znajdujàcego si´ w jàdrze pó∏-
le˝àcym. Receptor znajdujàcy si´ na
neuronie jàdra pó∏le˝àcego wychwytuje
dopamin´ i przekazuje jej sygna∏ dalej
do komórki. Aby póêniej sygna∏ wy∏à-
czyç, neuron znajdujàcy si´ w VTA usu-
wa dopamin´ ze szczeliny synaptycznej
i odzyskuje jà do póêniejszego, wtórne-
go u˝ytku, kiedy zajdzie taka potrzeba.
Kokaina i inne substancje pobudzajà-
ce wy∏àczajà czasowo bia∏ko odpowie-
dzialne za powrót neuroprzekaênika
do koƒcówek neuronów VTA, pozosta-
wiajàc w szczelinie synaptycznej nad-
miar dopaminy, która nadal oddzia∏uje
na jàdro pó∏le˝àce, natomiast heroina
i inne opiaty wià˝à si´ z neuronami
w VTA, które zwykle wy∏àczajà inne neu-
rony tam si´ znajdujàce, odpowiedzial-
ne za produkcj´ dopaminy. Opiaty t´ blo-
kad´ komórkowà likwidujà, uwalniajàc
w ten sposób komórki wydzielajàce dopa-
min´ i powodujàc dalszy nap∏yw dopa-
miny do jàdra pó∏le˝àcego. Opiaty gene-
rujà te˝ silny sygna∏ nagrody, oddzia∏ujàc
bezpoÊrednio na jàdro pó∏le˝àce.
Ale wp∏yw narkotyków nie ogranicza
si´ do dostarczania dodatkowego zastrzy-
ku dopaminy powodujàcego eufori´ i po-
Êredniczàcego mi´dzy pierwotnà nagrodà
a wzmocnieniem. Z czasem, po wielo-
krotnym za˝ywaniu, narkotyki urucha-
miajà stopniowo proces adaptacji w uk∏a-
dzie nagrody, prowadzàc do uzale˝nienia.
Korzenie uzale˝nienia
WCZESNE FAZY UZALE
˚NIENIA
charaktery-
zujà si´ tolerancjà na narkotyk i zale˝no-
Êcià od tej substancji. Po ciàgu narkotycz-
nym narkoman potrzebuje wi´kszej ni˝
poprzednio dawki narkotyku, by uzyskaç
ten sam efekt – takà samà popraw´ na-
stroju, taki sam poziom koncentracji itd.
Zjawisko tolerancji prowokuje eskalacj´
brania, prowadzàc do uzale˝nienia, czy-
li potrzeby objawiajàcej si´ bardzo przy-
krymi reakcjami emocjonalnymi, a nie-
kiedy i fizycznymi, na brak narkotyku.
Powodem wykszta∏cenia si´ zarówno to-
lerancji, jak i uzale˝nienia jest cz´ste za-
˝ywanie narkotyku, które jak na ironi´
t∏umi niektóre fragmenty uk∏adu nagrody.
U podstaw tego strasznego st∏umie-
nia tkwi czàsteczka chemiczna zwa-
na CREB. Jest ona czynnikiem trans-
krypcyjnym, bia∏kiem regulujàcym
ekspresj´ (aktywnoÊç) genów, a co za
tym idzie ca∏okszta∏t zachowania komó-
rek nerwowych. Wprowadzenie do orga-
nizmu narkotyku powoduje wzrost st´-
˝enia dopaminy w jàdrze pó∏le˝àcym,
58
ÂWIAT NAUKI KWIECIE¡ 2004
HANS C. BREITER
Massachusetts General Hospital
(obrazy mózgu i wykr
es)
;
pr
zedruk z S. D. NORRHOLM i in
.; NEUROSCIENCE, vol. 116, ©2003,
za zgodà ELSEVIER
(mikr
ofotografie)
2.0
1.5
2.5
1.0
0.5
5
10
Czas (minuty)
Za˝ycie
Euforia
G∏ód
IntensywnoÊç doznaƒ
15
20
0
0.0
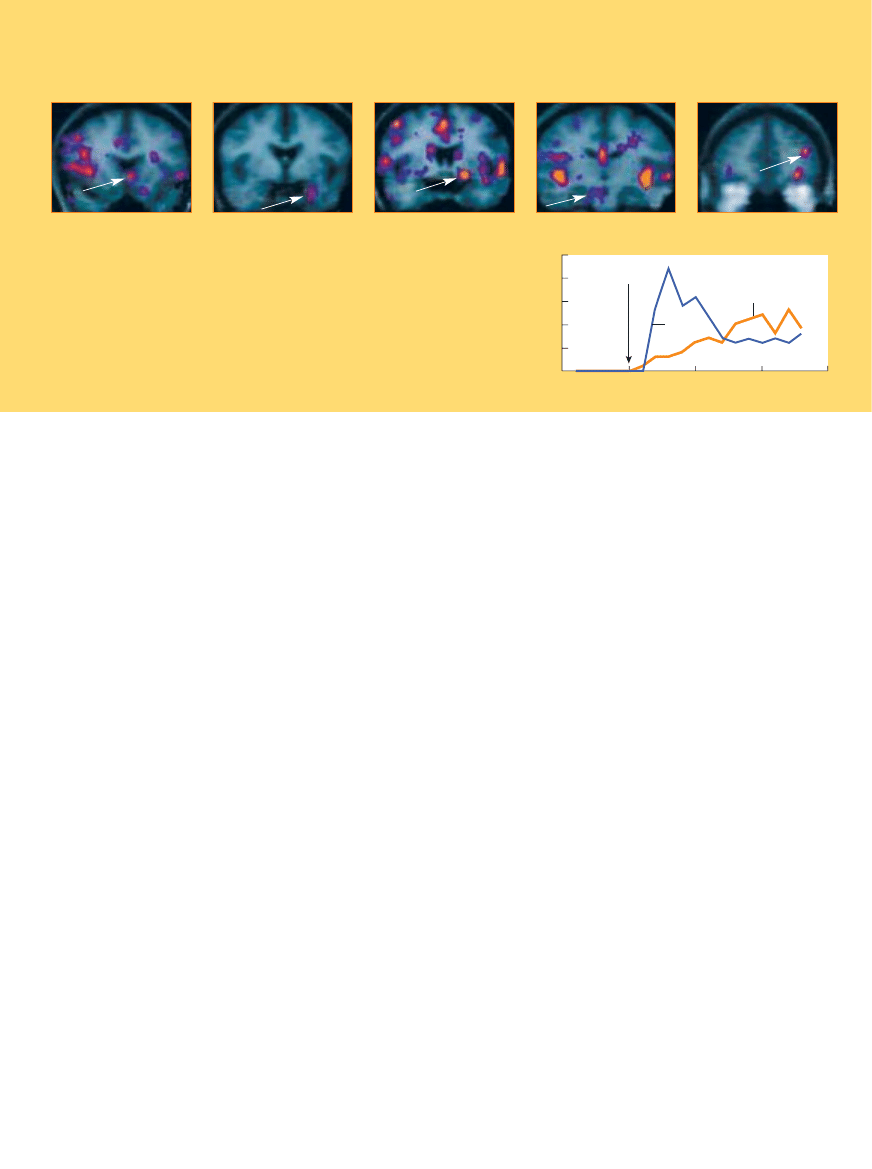
BARWNE PLAMY na obrazach mózgu kokainistów (powy˝ej) potwierdzajà
wyniki badaƒ na zwierz´tach, wskazujàce, ˝e przyj´cie narkotyku powoduje
natychmiastowe g∏´bokie zmiany w aktywnoÊci wielu rejonów mózgu, ∏àcznie
z widocznymi na rysunku; punkty najjaÊniejsze oznaczajà najwi´ksze zmiany.
Podczas skanowania osoby badane szacowa∏y swój poziom euforii i g∏odu w skali
od zera do trzech. Jak si´ okaza∏o, wa˝nà rol´ w powstawaniu euforii po za˝yciu
kokainy odgrywajà VTA i SLEA, natomiast cia∏o migda∏owate i jàdro pó∏le˝àce
majà wp∏yw zarówno na powstanie euforii, jak i g∏odu narkotycznego,
który wzmaga si´ w miar´ opadania euforii (wykres).
Jàdro pó∏le˝àce
Cia∏o migda∏owate
Cz´Êç podsoczewkowa
cia∏a migda∏owatego (SLEA)
Pole brzuszne nakrywki
Kora przedczo∏owa
CO NOWEGO WNIOS¸A TECHNIKA OBRAZOWANIA

a to z kolei pobudza komórki wra˝liwe
na dopamin´ do wzmo˝onej produkcji
ma∏ej czàsteczki sygnalizacyjnej, cyklicz-
nego AMP (cAMP), która ze swej stro-
ny aktywuje CREB. Z chwilà aktywacji
CREB wià˝e si´ z konkretnà grupà ge-
nów, uruchamiajàc produkcj´ bia∏ek ko-
dowanych przez te geny.
D∏ugotrwa∏e za˝ywanie narkotyków
podtrzymuje stan aktywacji CREB,
zwi´kszajàc tym samym ekspresj´ jej
genów docelowych, z których cz´Êç ma
zakodowane bia∏ka t∏umiàce uk∏ad na-
grody. CREB na przyk∏ad kontroluje
produkcj´ dynorfiny, naturalnej czàstecz-
ki o dzia∏aniu podobnym do dzia∏ania
opium. Dynorfina syntetyzowana jest
przez podgrup´ neuronów w jàdrze pó∏-
le˝àcym, tworzàcà p´tl´, po której sub-
stancja ta zwrotnie hamuje neurony znaj-
dujàce si´ w VTA. Indukcja dynorfiny
za pomocà CREB hamuje wi´c uk∏ad
nagrody w mózgu i zwi´ksza tolerancj´
na narkotyk, sprawiajàc, ˝e dotychczaso-
wa dawka jest odczuwana jako mniej-
sza nagroda. Wzrost poziomu dynorfi-
ny przyczynia si´ te˝ do pog∏´bienia
uzale˝nienia, poniewa˝ hamuje drog´
nagrody, pozostawiajàc pozbawionà nar-
kotyku osob´ w stanie depresji, przez co
nie czerpie ona ju˝ przyjemnoÊci z za-
chowaƒ ongiÊ przyjemnych.
Ale CREB to jeszcze nie wszystko. Ten
czynnik transkrypcyjny wy∏àcza si´ po kil-
ku dniach od odstawienia narkotyku.
A zatem to nie CREB odpowiada za d∏u-
gotrwa∏y wp∏yw narkotyku na mózg –
za zmiany w tym narzàdzie powodujà-
ce, ˝e narkoman wraca do narkotyków
nawet po kilku czy kilkudziesi´ciu latach
abstynencji. G∏ównà przyczynà takich
nawrotów jest uwra˝liwienie, zjawisko
wzmacniania wp∏ywu narkotyku.
Choç brzmi to niewiarygodnie, praw-
da jest taka, ˝e kontakt z narkotykiem
zwi´ksza tolerancj´ i uwra˝liwia zara-
zem. Wkrótce po za˝yciu aktywnoÊç
CREB jest du˝a i zawiaduje tolerancjà:
przez kilka dni narkoman musi przyjmo-
waç coraz wi´ksze dawki narkotyku, by
oszukaç uk∏ad nagrody. Ale po odstawie-
niu narkotyku aktywnoÊç CREB spada.
Kiedy tak si´ dzieje, spada te˝ tolerancja
i pojawia si´ uwra˝liwienie, urucha-
miajàc intensywny g∏ód, który powo-
duje przymus poszukiwania narkotyku
za wszelkà cen´. Jedno liêni´cie lub jed-
no wspomnienie wystarczy, by cz∏owiek
znów si´gnà∏ po narkotyk. Ten g∏ód
utrzymuje si´ nawet po d∏ugotrwa∏ej abs-
tynencji. Aby zrozumieç mechanizm
uwra˝liwienia, musimy poszukaç zmian
molekularnych trwajàcych d∏u˝ej ni˝ kil-
ka dni. Jednym z podejrzanych jest inny
czynnik transkrypcyjny: delta FosB.
Mechanizm nawrotu
DZIA
¸ANIE CZYNNIKA
delta FosB u osób
uzale˝nionych bardzo si´ ró˝ni, jak si´
wydaje, od dzia∏ania CREB. Z badaƒ
na myszach i szczurach wynika, ˝e w od-
powiedzi na d∏ugotrwa∏e przyjmowanie
narkotyków st´˝enie delta FosB roÊnie
stopniowo i progresywnie w jàdrze pó∏-
le˝àcym i innych rejonach mózgu.
A poniewa˝ jest to bia∏ko niezwykle
stabilne, jego aktywnoÊç w komórkach
nerwowych utrzymuje si´ przez wiele
tygodni, a nawet miesi´cy po podaniu
narkotyku. UporczywoÊç ta powoduje,
˝e czynnik delta FosB podtrzymuje
zmiany w ekspresji genu d∏ugo po od-
stawieniu narkotyku.
Badania prowadzone na zmutowa-
nych myszach produkujàcych nadmiar
czynnika delta FosB w jàdrze pó∏le˝à-
cym wskazujà, ˝e w razie przed∏u˝onej
indukcji tej czàsteczki zwierz´ta stajà si´
nadwra˝liwe na narkotyki. Myszy te
przejawia∏y du˝à sk∏onnoÊç do nawro-
tów po odstawieniu narkotyków i ich
póêniejszym ponownym udost´pnieniu,
z czego wynika, ˝e to prawdopodobnie
st´˝enie delta FosB odpowiada za d∏u-
gotrwa∏y wzrost wra˝liwoÊci uk∏adu na-
grody u cz∏owieka. Co ciekawe, myszy
wytwarzajà delta FosB tak˝e w jàdrze
pó∏le˝àcym w odpowiedzi na powtarzal-
ne nagrody nieb´dàce narkotykami, ta-
kie jak nadmiar ruchu w kole aktywno-
Êci czy nadmiar cukru. Niewykluczone
wi´c, ˝e czynnik ten odgrywa ogólniejszà
rol´ w rozwoju zachowaƒ kompulsyw-
nych w stosunku do szerokiej gamy bodê-
ców nagradzajàcych.
Wyniki najnowszych badaƒ odkrywa-
jà ràbka tajemnicy mechanizmu utrzy-
mywania si´ nadwra˝liwoÊci nawet
po powrocie st´˝enia delta FosB do nor-
my. Wiadomo, ˝e d∏ugotrwa∏y kontakt
z kokainà i innymi narkotykami uzale˝-
niajàcymi pobudza receptorowe wypust-
ki dendrytyczne jàdra pó∏le˝àcego do
tworzenia dodatkowych w´z∏ów, zwa-
nych kolcami dendrytycznymi, zwi´k-
szajàcych liczb´ po∏àczeƒ z innymi
neuronami. W przypadku szczurów do
tworzenia si´ dodatkowych w´z∏ów
dochodzi nawet po kilku miesiàcach
po odstawieniu narkotyku. Odkrycie to
sugeruje, ˝e byç mo˝e to w∏aÊnie delta
FosB odpowiada za zwi´kszenie liczby
kolców. Dokonujàc wysoce spekulatyw-
nej ekstrapolacji wyników tych odkryç,
KWIECIE¡ 2004 ÂWIAT NAUKI
59
ERIC J. NESTLER i ROBERT C. MALENKA badajà molekularne podstawy narkomanii. Nestler,
profesor i kierownik katedry na Wydziale Psychiatrii University of Texas Southwestern Medical Cen-
ter w Dallas, wybrany zosta∏ na cz∏onka Instytytu Medycyny w 1998 roku. Malenka, profesor psy-
chiatrii i nauk o zachowaniu w Stanford University School of Medicine, wczeÊniej by∏ dyrektorem
Center for the Neurobiology of Addiction w University of California w San Francisco. Wspólnie ze
Stevenem E. Hymanem, pracujàcym obecnie w Harvard University, Nestler i Malenka napisali
podr´cznik zatytu∏owany Molecular Basis of Neuropharmacology (McGraw-Hill, 2001).
O
AUTORACH
MIKROFOTOGRAFIE neuronów jàdra pó∏le˝àcego u zwierzàt majàcych kontakt z lekami
niepowodujàcymi uzale˝nienia pokazujà, ˝e wypustki dendrytów majà normalnà liczb´
kolców dendrytycznych (z lewej i poÊrodku). U zwierzàt uzale˝nionych od kokainy natomiast
na wypustkach dendrytycznych powstajà dodatkowe kolce, sprawiajàc, ˝e dendryt nabiera
bardziej krzaczastego wyglàdu (z prawej). Przypuszczalnie ta zmiana strukturalna powoduje,
˝e neurony stajà si´ bardziej wra˝liwe na sygna∏y p∏ynàce z VTA i innych miejsc, przez co roÊnie
wra˝liwoÊç na narkotyk. Z najnowszych badaƒ wynika, ˝e byç mo˝e jakàÊ rol´ w powstawaniu
nowych kolców dendrytycznych odgrywa delta FosB.
mo˝na pokusiç si´ o hipotez´, ˝e dodat-
kowe po∏àczenia wygenerowane dzi´ki
aktywnoÊci czynnika delta FosB wzmac-
niajà przep∏yw sygna∏ów mi´dzy po∏à-
czonymi komórkami na wiele lat i w∏a-
Ênie ta wzmo˝ona sygnalizacja sprawia,
˝e mózg jest nadmiernie wra˝liwy
na bodêce narkotyczne. Koniec koƒców
byç mo˝e to zmiany w dendrytach stano-
wià kluczowà form´ adaptacji, która
czyni na∏óg tak nieprzejednanym.
Nauka na∏ogu
DO TEJ PORY
koncentrowaliÊmy si´ na
zmianach powstajàcych pod wp∏ywem
narkotyków zwiàzanych z gospodarkà
dopaminowà w mózgowym uk∏adzie na-
grody. Przypomnijmy jednak, ˝e w uza-
le˝nieniu biorà udzia∏ i inne rejony
mózgu, a mianowicie cia∏o migda∏owa-
te, hipokamp i kora czo∏owa, i ˝e rejony
te komunikujà si´ wzajemnie z VTA i jà-
drem pó∏le˝àcym. Wszystkie te rejony
przemawiajà do uk∏adu nagrody, uwal-
niajàc neuroprzekaênik zwany glutami-
nianem. Kiedy narkotyk zwi´ksza
uwalnianie dopaminy z VTA do jàdra
pó∏le˝àcego, zmienia zarazem sposób
reagowania VTA i jàdra pó∏le˝àcego
na glutaminian na wiele dni. Z badaƒ
na zwierz´tach wynika, ˝e zmian´ wra˝-
liwoÊci na glutaminian w uk∏adzie na-
grody zwi´ksza zarówno iloÊç uwalnia-
nej w VTA dopaminy, jak i reakcja jàdra
pó∏le˝àcego na dopamin´, przez co ro-
Ênie aktywnoÊç CREB i delta FosB oraz
wzmaga si´ niekorzystne dzia∏anie tych
czàsteczek. Wydaje si´ ponadto, ˝e zmia-
na wra˝liwoÊci na glutaminian wzmac-
nia drogi nerwowe ∏àczàce Êlady pami´-
ciowe doÊwiadczeƒ narkotycznych z
wysokà nagrodà i pot´guje tym samym
dà˝enie do zdobycia narkotyku.
Mechanizm zmiany wra˝liwoÊci neu-
ronów wchodzàcych w sk∏ad szlaku na-
grody na glutaminian pod wp∏ywem nar-
kotyków nie jest jeszcze do koƒca wyja-
Êniony, ale mo˝na ju˝ sformu∏owaç hi-
potez´ roboczà, znajàc wp∏yw glutami-
nianu na neurony hipokampa. Tam
pewne typy bodêców o krótkotrwa∏ym
dzia∏aniu zwi´kszajà wra˝liwoÊç komór-
ki na glutaminian na wiele godzin. Zja-
wisko to, noszàce nazw´ d∏ugotrwa∏ego
wzmocnienia synaptycznego (LTP – long-
-term potentiation), sprzyja tworzeniu
wspomnieƒ i, jak si´ wydaje, czynnikiem
poÊredniczàcym w jego powstaniu jest
przetaczanie niektórych bia∏ek wià˝à-
cych glutaminian z magazynów we-
wnàtrzkomórkowych, gdzie pozostajà
w uÊpieniu, do b∏ony komórki nerwowej,
gdzie reagujà na uwolniony do synapsy
glutaminian. Narkotyki wp∏ywajà na ów
proces przetaczania receptorów glutami-
nianowych w szlaku nagrody. Istniejà te˝
wyniki Êwiadczàce o tym, ˝e substancje
te wp∏ywajà tak˝e na syntez´ niektórych
receptorów glutaminianowych.
60
ÂWIAT NAUKI KWIECIE¡ 2004
TERESE WINSL
OW
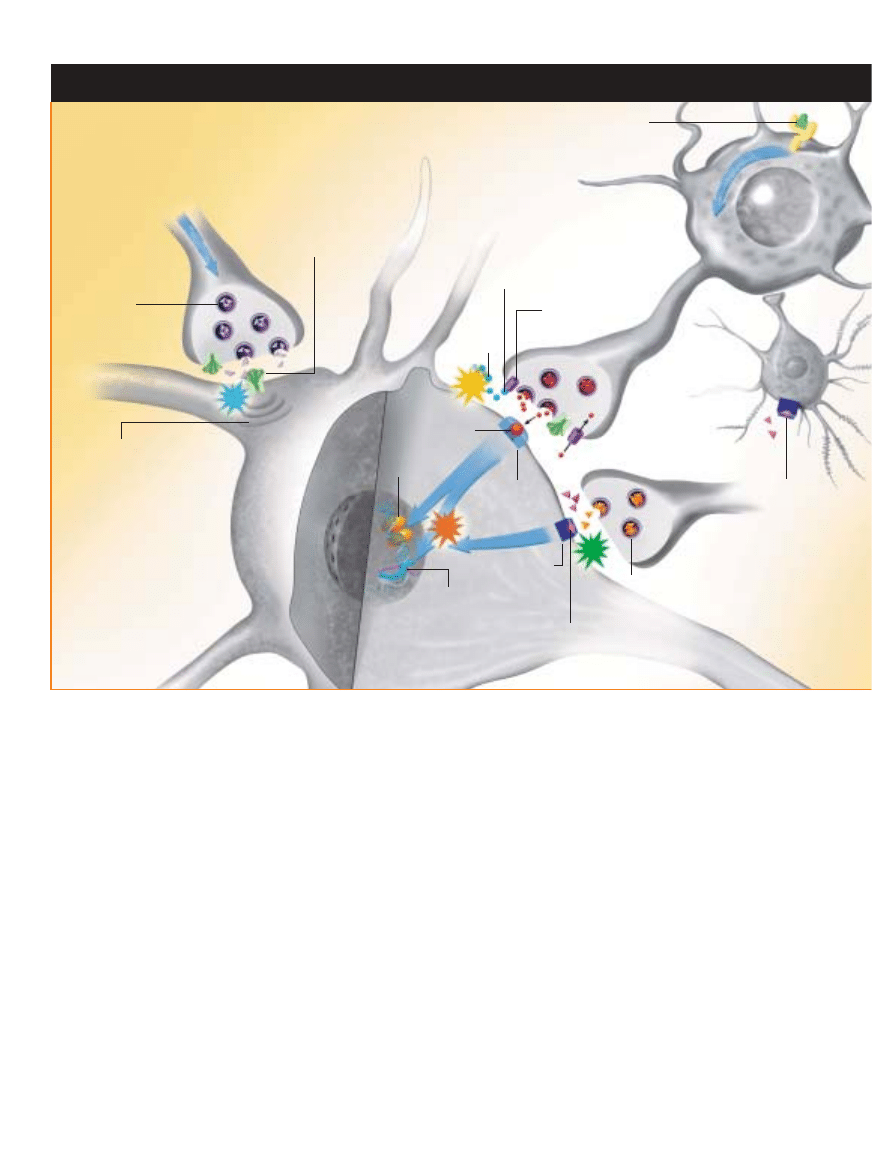
NARKOTYKI RÓ˚NE, EFEKT TEN SAM
RÓ˚NE NARKOTYKI trafiajà do ró˝nych punktów docelowych w mózgu,
ale wszystkie, wprost lub nie wprost, nasilajà sygnalizacj´ dopaminowà
w jàdrze pó∏le˝àcym, powodujàc uzale˝nienie. Poznanie tych punktów
pozwoli na opracowanie odpowiednich terapii (ramka obok).
KOKAINA
i inne pokrewne
Êrodki pobudzajàce albo
blokujà wychwyt dopaminy,
albo wzmagajà jej uwalnianie
przez zakoƒczenia komórek
VTA, powodujàc wzrost
sygnalizacji dopaminowej
w jàdrze pó∏le˝àcym
NIKOTYNA
pobudza
komórki VTA do
uwalniania dopaminy
OPIATY I ALKOHOL
wzmagajà uwalnianie
dopaminy, t∏umiàc
neurony, które
w przeciwnym
razie oddzia∏ywa∏yby
hamujàco na neuro-
ny uwalniajàce
dopamin´
Projekcje z kory,
cia∏a migda∏owatego
i hipokampa
WIELE NARKOTYKÓW
, w tym
kokaina, amfetamina i morfina,
oraz alkohol, modyfikuje reakcj´
jàdra pó∏le˝àcego i komórek VTA
na glutaminian w sposób trwa∏y,
nasilajàc wspomnienia
wczeÊniejszych doÊwiadczeƒ
z narkotykami nawet
po odstawieniu Êrodków
uzale˝niajàcych i przyczyniajàc
si´ tym samym do powstania
g∏odu narkotykowego
Glutaminian
Receptor
glutaminianowy
PrzenoÊnik
dopaminy
Neuron VTA
uwalniajàcy
dopamin´
Receptor
dopaminowy
Receptor
opiatowy
Dopamina
Kokaina
CREB
∆FosB
Neuron jàdra
pó∏le˝àcego
Naturalny
odpowiednik
opium
OPIUM
oraz jego naturalne
i syntetyczne odpowiedniki
naÊladujà niektóre oddzia∏ywania
dopaminy na komórki w jàdrze pó∏le˝àcym
Neuron
hamujàcy
w VTA

Wszystkie omówione dotychczas
zmiany w uk∏adzie nagrody pod wp∏y-
wem narkotyków wzmagajà ostatecznie
tolerancj´, zale˝noÊç, g∏ód, nawroty i ca-
∏y splot zachowaƒ towarzyszàcych na-
∏ogowi. Wiele szczegó∏ów tego procesu
nadal okrytych jest tajemnicà, ale o in-
nych mo˝emy si´ ju˝ wypowiadaç z du-
˝à dozà pewnoÊci. Podczas d∏ugotrwa∏e-
go przyjmowania narkotyków i wkrótce
po ich odstawieniu dominujà zmiany
st´˝eƒ cyklicznego AMP i aktywnoÊci
neuronów szlaku nagrody. Zmiany te
obni˝ajà wra˝liwoÊç na narkotyk, zwi´k-
szajà poziom depresji i os∏abiajà moty-
wacj´, wzmagajàc tym samym toleran-
cj´ i zale˝noÊç. Po d∏u˝szej abstynencji
natomiast dominujà zmiany w poziomie
aktywnoÊci czynnika delta FosB i sygna-
lizacji glutaminianu. To w∏aÊnie te zmia-
ny sprawiajà, ˝e narkoman znowu si´ga
po narkotyki, poniewa˝ pod ich wp∏y-
wem wra˝liwoÊç na efekty dzia∏ania nar-
kotyku po przerwie w braniu jest wi´k-
sza i uruchamiajà si´ u niego silne re-
akcje na wspomnienie dawnych stanów
odurzenia i nawet na bodêce wspomnie-
nia te wywo∏ujàce.
Zmiany w CREB, delta FosB i sygnali-
zacji glutaminianu odgrywajà wi´c pod-
stawowà rol´ w powstawaniu uzale˝nieƒ,
ale na pewno nie jedynà. W miar´ post´-
pu badaƒ neurobiolodzy z pewnoÊcià od-
kryjà nowe, wa˝ne zmiany molekularne
i komórkowe w uk∏adzie nagrody i w in-
nych zwiàzanych z tym uk∏adem obsza-
rach mózgu – zmiany, które pomogà od-
kryç prawd´ o uzale˝nieniach.
Wspólna terapia?
ODKRYCIE
tych molekularnych zmian –
poza tym, ˝e pozwala lepiej zrozumieç
biologiczne pod∏o˝e narkomanii – stwa-
rza nowe wyzwania dla biochemicznej
terapii uzale˝nieƒ. A zapotrzebowanie
na nowe metody leczenia jest ogromne.
Wiadomo ju˝ powszechnie, ˝e uzale˝-
nienia siejà wielkie spustoszenie w orga-
nizmie i psychice. Uzale˝nienia sà tak-
˝e jednym z najwa˝niejszych êróde∏
chorób somatycznych. Alkoholicy choru-
jà na marskoÊç wàtroby, palacze na ra-
ka p∏uc, a heroiniÊci, korzystajàc ze
wspólnych igie∏, rozsiewajà wirusa HIV.
Ka˝dego roku koszty uzale˝nieƒ, mie-
rzone uszczerbkiem na zdrowiu i spad-
kiem wydajnoÊci, si´gajà w Stanach
Zjednoczonych ponad 300 mld dolarów.
To dlatego uzale˝nienia sà jednym z naj-
wi´kszych problemów spo∏ecznych.
Gdyby definicj´ uzale˝nienia rozszerzyç
na inne rodzaje zachowaƒ kompulsyw-
nych, takich jak nadmierne objadanie
si´ i hazard, koszty by∏yby jeszcze wi´k-
sze. Gdyby istnia∏y terapie korygujàce
wszelkie aberracyjne, na∏ogowe reakcje
na nagrody – czy to w postaci kokainy
lub sernika, czy te˝ dreszczyku, jaki da-
je wygrana w totolotka – korzyÊç dla
spo∏eczeƒstwa by∏aby ogromna.
Stosowane dziÊ terapie uzale˝nieƒ sà
w wi´kszoÊci przypadków nieskuteczne.
Jest ju˝ kilka leków uniemo˝liwiajàcych
narkotykowi dotarcie do celu. Ârodki te
nie leczà jednak uzale˝nionego mózgu
ani nie likwidujà silnego g∏odu narko-
tycznego. Inne interwencje medyczne
naÊladujà efekt narkotyku, t∏umiàc g∏ód
na tyle, by wytràciç narkomana z na∏ogu.
Ale wszystkie te chemiczne substancje
tylko zast´pujà jeden na∏óg drugim.
I choç inne formy terapii pozamedycz-
nej – na przyk∏ad popularne programy
12 kroków – pomagajà wielu ludziom
wziàç si´ w karby i uporaç z uzale˝nie-
niem, liczba nawrotów jest du˝a.
Uzbrojonym w nowà wiedz´ na temat
biologicznych mechanizmów uzale˝nieƒ
badaczom byç mo˝e uda si´ kiedyÊ wy-
naleêç lek kompensujàcy d∏ugotrwa∏y
wp∏yw substancji uzale˝niajàcych na t´
cz´Êç mózgu, która zawiaduje mechani-
zmem nagrody. Specyfiki wchodzàce w
konkretne interakcje z receptorami wià-
˝àcymi glutaminian lub dopamin´ w jà-
drze pó∏le˝àcym czy preparaty chemicz-
ne blokujàce wp∏yw CREB lub delta FosB
na geny docelowe w tej okolicy mog∏yby
os∏abiç uzale˝nienie od narkotyku.
Musimy te˝ nauczyç si´ rozpoznawaç
tych ludzi, u których ryzyko uzale˝nie-
nia jest najwi´ksze. I choç nie mo˝na
bagatelizowaç roli czynników psycholo-
gicznych, spo∏ecznych i Êrodowiskowych,
badania rodzin o podwy˝szonym ryzyku
uzale˝nienia Êwiadczà, ˝e u ludzi zagro-
˝enie to jest w oko∏o 50% uwarunkowa-
ne genetycznie. Nie zidentyfikowano
jeszcze konkretnych genów odpowie-
dzialnych za t´ podatnoÊç, ale gdyby uda-
∏o si´ wczeÊniej rozpoznaç jednostki
szczególnie podatne, mo˝na by odpo-
wiednie terapie wycelowaç w t´ w∏aÊnie
populacj´.
Poniewa˝ w uzale˝nieniach du˝à ro-
l´ odgrywajà tak˝e czynniki emocjonal-
ne i spo∏eczne, nie ∏udêmy si´, ˝e ten
zespó∏ chorobowy uda si´ opanowaç
wy∏àcznie Êrodkami farmakologiczny-
mi. Miejmy jednak nadziej´, ˝e terapie
przysz∏oÊci os∏abià dzia∏anie pot´˝nych
si∏ biologicznych – uzale˝nienia i g∏odu
– które na∏óg nap´dzajà, i zwi´kszà dzi´-
ki temu skutecznoÊç oddzia∏ywaƒ psy-
chospo∏ecznych oraz pomogà naprawiç
szkody, jakie uzale˝nienie poczyni∏o
w organizmie i psychice cz∏owieka.
n
KWIECIE¡ 2004 ÂWIAT NAUKI
61
Incentive-Sensitization and Addiction. Terry E. Robinson i Kent C. Berridge; Addiction, tom 96,
nr 1, s. 103-114; I/2001.
Molecular Basis of Long-Term Plasticity underlying Addiction. Eric J. Nestler; Nature Reviews
Neuroscience, tom 2, nr 2, s. 119-128; II/2001.
Addiction: From Biology to Drug Policy. Wydanie II. A. Goldstein; Oxford University Press, 2001.
National Institute on Drug Abuse Information on Common Drugs of Abuse:
www.nida.nih.gov/DrugPages/
JEÂLI CHCESZ WIEDZIEå WI¢CEJ
MO˚LIWOÂCI
LECZENIA
Hipotetyczny Êrodek antykokainowy
móg∏by os∏abiç sygnalizacj´
dopaminowà w jàdrze pó∏le˝àcym,
uniemo˝liwiajàc kokainie
blokowanie wychwytu dopaminy
przez zakoƒczenia neuronów VTA.
Hipotetyczny Êrodek o szerokim
spektrum dzia∏ania hamowa∏by
efekty dopaminy, zapobiegajàc
kumulowaniu si´ CREB lub
∆FosB albo aktywacji genów
docelowych tych moleku∏.
Hipotetyczny Êrodek o szerokim
spektrum dzia∏ania móg∏by zapobiec
niekorzystnym zmianom sygnalizacji
glutaminianu, zachodzàcym
w komórkach jàdra pó∏le˝àcego
pod wp∏ywem d∏ugotrwa∏ego
za˝ywania narkotyków.
Dost´pne ju˝ na rynku Êrodki
b´dàce antagonistami opiatów
(np. naltrekson) blokujà receptory
opiatów. Stosowane sà w leczeniu
alkoholizmu i nikotynizmu,
poniewa˝ alkohol i nikotyna
uwalniajà w mózgu w∏asne
moleku∏y podobne do opium.
Wyszukiwarka
Podobne podstrony:
200405 Świat Nauki maj 2004 Niedoceniane komórki mózgu
ŚWIAT NAUKI I MEDIÓW ZDERZENIE CYWILIZACJI
Świat Nauki 07 2008 PL
swiat nauki bakterie
ŚWIAT NAUKI 06 2006
ŚWIAT NAUKI 06 2006
200309 Świat Nauki wrzesien 2003 Maly Wielki Mózg
M Cahill Dwie Płcie, Dwa Mózgi (Świat Nauki nr 5 2005 pdf chomikuj)
200011 Świat Nauki listopad 2000 Tajemnice meskiej erekcji
Świat Nauki 07 2008 PL
ŚWIAT NAUKI I MEDIÓW ZDERZENIE CYWILIZACJI
Grafika z komputera, szkoła, technik informatyki, INFORMATYKA-all, Informatyka-20 września 2004, Kom
2004 07 Wspaniały świat POV Raya [Grafika]
Jak krok po kroku wprowadzać dzieci o specjalnych potrzebach edukacyjnych w świat zabawy i nauki eb
swiat porty 2004(1)
więcej podobnych podstron