
Rodzaje geometrycznych defektów sieci krystalicznych
Defekty punktowe – na przykład nie obsadzone położenie atomowe (wakancja).
Defekty liniowe – nazywane dyslokacjami mają podstawowe znaczenie w odkształceniu plastycznym materiału krystalicznego.
Defekty powierzchniowe – są dwuwymiarowymi zaburzeniami struktury krystalicznej.
Hartowanie
Rodzaj obróbki cieplnej, której celem jest uzyskanie struktury o większej twardości.
Polega na ogrzewaniu stali do temperatury stanu austenicznego, wygrzewaniu w tej temperaturze w celu uzyskania jednakowej temp. W
całej masie, a następnie bardzo szybkim chłodzeniu.
Rodzaje hartowanie: zwykłe, stopniowe, izotermiczne, powierzchniowe
Odpuszczanie - cel przebieg zagrożenia
Rodzaj obróbki cieplnej stali wcześniej zahartowanej, w celu usunięcia naprężeń hartowniczych oraz zmiany właściwości fizycznych
zahartowanej stali, a przede wszystkim zmniejszenie twardości, a podniesienie poziomu udarności.
Polega na ogrzaniu stali zahartowanej do odpowiedniej temperatury, wygrzewaniu w tej temperaturze, a następnie ochłodzeniu. W czasie
odpuszczania całość lub część martenzytu zawartego w zahartowanej stali rozpada się, wydzielając bardzo drobne ziarna cementytu.
Rodzaje materiałów inżynierskich charakterystyka
Metale i ich stopy(stopy żelaza, miedzi aluminium, niklu, tytanu):
o
Sztywność
o
Ciągliwość
o
Odporność na pękanie
o
Dobra przewodność elektryczna i cieplna
o
Stopy mają dużą wytrzymałość(czyste metale nie)
o
Mała odporność chemiczna
o
Łatwo uleją korozji
Materiały ceramiczne i szkła(tlenki i związki chemiczne metali z takimi pierwiastkami jak C, N, P i S):
o Wytrzymałość szczególnie na ściskanie
o Odporne na korozję
o Odporność na wysokie temperatury – materiały ogniotrwałe
o
Obojętne dla środowiska
o Nadprzewodniki
o
Słaba przewodność cieplna
o
Słaba przewodność elektryczna
o
Słaba ciągliwość
o
Słaba odporność na pękanie
o Wysoka temperatura topnienia
Polimery(tworzywa sztuczne, materiały wielocząsteczkowe złożone z merów):
o
odporność na korozję
o
estetyczny wygląd bez dodatkowej obróbki
o
mała gęstość (lekkie)
o
łatwo formowalne w skomplikowane kształty
o
mały współczynnik tarcia
o
ciągliwe (tylko termoplastyczne)
o
są izolatorami
o
mogą przewodzić prąd elektryczny
o
mała sztywność
o niska temperatura topnienia
o
duże odkształcenia sprężyste
o
pełzanie przy temperaturze normalnej
o kruche (tylko termoutwardzalne)
o
silna zmiana właściwości od temperatury
o
szkodliwe dla środowiska
Kompozyty(składają się z co najmniej dwóch materiałów należacych do stopów, materiałów ceramicznych lub polimerów):
o
Właściwości kompozytów nigdy nie są sumą, czy średnią właściwości jego składników. Najczęściej jeden z
komponentów stanowi lepiszcze, które gwarantuje jego spójność, twardość, elastyczność i odporność na ściskanie, a
drugi, tzw. komponent konstrukcyjny zapewnia większość pozostałych własności mechanicznych kompozytu.
Półprzewodniki:
o
Nie są dobrymi przewodnikami ani dobrymi izolatorami
o
Dodanie do półprzewodnika małej ilości niektórych pierwiastków zmienia gwałtownie ich właściwości elektryczne
o
Służą do wytwarzania złożonych obwodów elektrycznych, np. wielowarstwowych układów scalonych o wysokim stopniu
integracji
o
Powszechnie stosowanymi półprzewodnikami pierwiastkowymi są Si i Ge
o
Niektóre związki chemiczne są również półprzewodnikami, np. arsenek galu GaAs
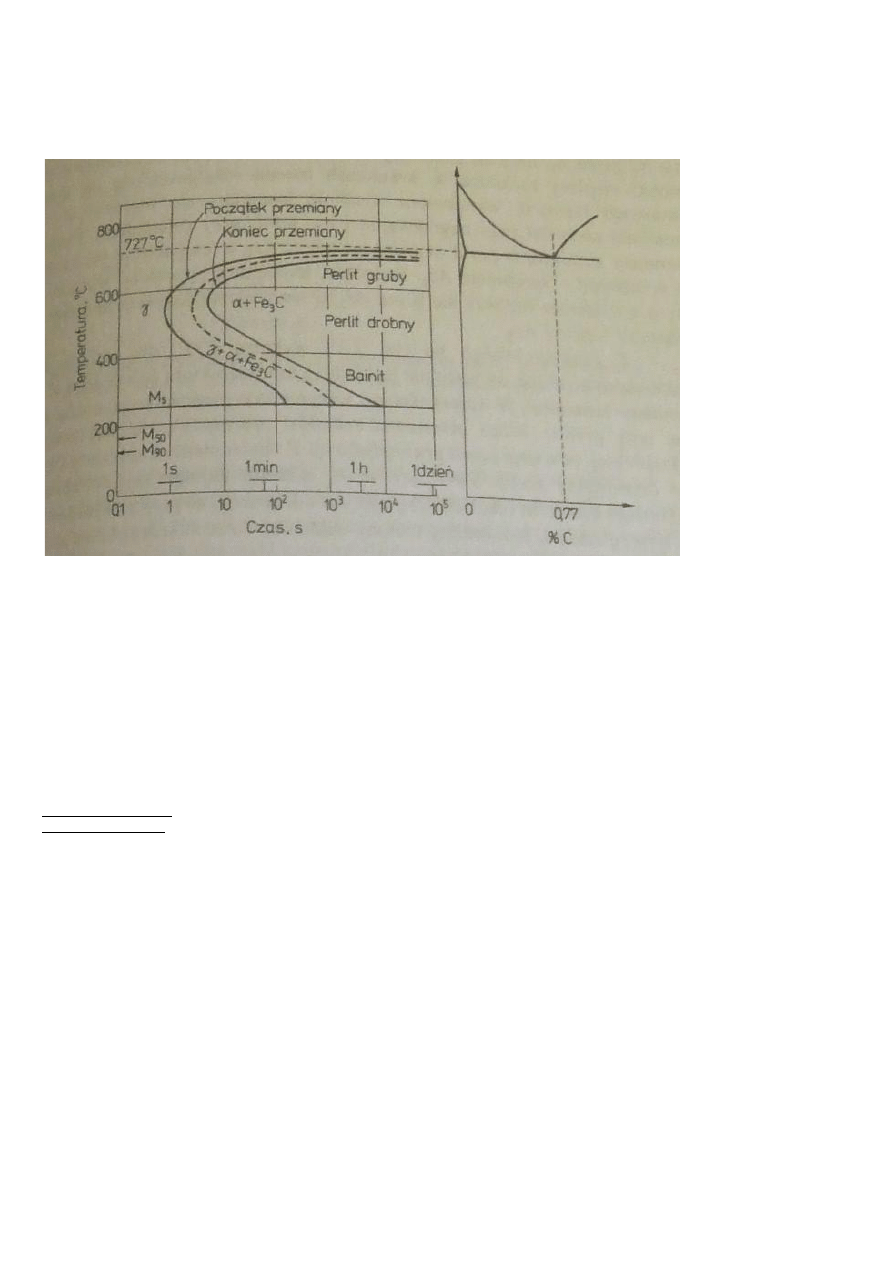
Wykresy CTP
Wykres CTP (CTP: czas-temperatura-przemiana) – graficzna prezentacja danych, dotycząca obróbki cieplnej materiałów inżynierskich.
Wyróżnia się wiele rodzajów tego typu wykresów, m.in.:
CTPc – prezentujący zmianę struktury przy ciągłym chłodzeniu materiału
CTPi – prezentujący zmianę struktury przy chłodzeniu materiału z wytrzymaniem izotermicznym
Wykres CTPi dla stali eutektoidalnej(przechłodzenia austenitu):
Przemiana perlityczna(dyfuzyjna) - przemiana fazowa (termiczna) austenitu w perlit zachodząca w wyniku powolnego chłodzenia stali
(poniżej temperatury 727 °C) nagrzanej do temperatury austenitu. Jest to przemiana dyfuzyjna, związana z przegrupowaniem atomów węgla,
zachodząca przez zarodkowanie i wzrost zarodków; zarodkowanie heterogeniczne na cząstkach cementytu, płytkach ferrytu, a w austenicie
na granicach jego ziaren; kolejno tworzenie płytek cementytu i ferrytu.
Przemiana martenzytyczna - jest przemianą bezdyfuzyjną i zachodzi przy dużym przechłodzeniu austenitu. Izotermiczna przemiana austenitu
w martenzyt zachodząca w wyniku gwałtownego chłodzenia nagrzanej do temperatury austenitu stali węglowej. W wyniku tej przemiany
powstaje martenzyt czyli przesycony roztwór węgla w żelazie α.
Przemiana bainityczna - fazowa przemiana termiczna w bainit, pośrednia między przemianą perlityczną a przemianą martenzytyczną,
polegająca na przechłodzeniu austenitu do temperatury z zakresu 500-300°C, w której nie zachodzi już dyfuzja pierwiastków metalicznych,
zachodzi zaś jeszcze dyfuzja węgla.
Struktury jednofazowa i dwufazowa. Wygląd i właściwości.
Struktura jednofazowa to jednolity układ posiadający w całej swojej objętości takie same własności chemiczne i fizyczne.
Struktura dwufazowa – składa się z dwóch układów oddzielonych od siebie wyraźną granicą, na której przynajmniej niektóre makroskopowe
własności chemiczne lub fizyczne ulegają zmianie.
Umocnienia i ulepszenia cieplne. Podobieństwa i różnice.
Umocnienie - ograniczenie ruchu dyslokacjom
Rodzaje umocnień:
Roztworowe - wewnętrzne pola naprężeń wokół rozpuszczonych atomów oddziałują wzajemnie z polami naprężeń wokół
dyslokacji co zmniejsza ruchliwość dyslokacji.
Odkształceniowe – dyslokacje z przecinających się płaszczyzn poślizgu przeszkadzają sobie wzajemnie w ruchu poślizgowym, co
prowadzi do ich spiętrzenia i gromadzenia się.
Wydzieleniowe lub cząstkami fazy dyspersyjnej – wykorzystuje się cząstki innych faz. Cząstkami takimi mogą być wydzielenia.
Przez rozdrobnienie ziarna – granica plastyczności jest odwrotnie proporcjonalna od pierwiastka z wielkości ziarna materiału
Ulepszanie cieplne – jest obróbką cieplną polegającą na połączeniu hartowania z wysokim (lub średnim) odpuszczaniem.
Ulepszanie cieplne prowadzi do:
wzrostu właściwości plastycznych (udarności, wydłużenia do zerwania, przewężenia),
wzrostu wytrzymałości na rozciąganie,
wzrostu odporności na pękanie
spadku twardości
Żelazo alfa i gamma
Żelazo α – zakres do 912°. Posiada strukturę krystaliczną RPC. Od 1394° Fe α(δ). Poniżej 770° jest ferromagnetykiem, powyżej
paramagnetykiem.
Żelazo γ – zakres od 912° do 1394°. Posiada strukturę krystaliczną RSC.
Ferryt – jest międzywęzłowym roztworem węgla w żelazie α lub δ. Charakteryzuje go niska zawartość węgla, niska wytrzymałość i
twardość, natomiast duża plastyczność i udarność.
Austenit – jest międzywęzłowym roztworem węgla w żelazie γ. Rozpuszczalność węgla wynosi od 0,8% w 727° do 2.1% w 1148°.
Cementyt – jest węglikiem żelaza o rombowej strukturze krystalicznej. Zawartość węgla jest stała i wynosi 6,67%, co czyni go twardym lecz
kruchym.
Perlit – jest produktem eutektoidalnej przemiany austenitu. Jest więc mieszaniną ferrytu i cementytu, zawierającą 0,8% węgla. Posiada
budowę pasemkową(na przemian ferryt i cementyt) co sprawia, że ma większą twardość i wytrzymałość przy gorszych właściwościach
plastycznych, bez objawów kruchości.
Ledeburyt – jest produktem przemiany eutektycznej. Powstaje z cieczy o zawartości 4,3% węgla i składa się z austenitu i cementytu.
Reguły faz
s = n – f +2
s- liczba stopni swobody(liczba zmiennych niezależnych, których zmiana nie powoduje zmiany liczby faz)
n – liczba składników
f – liczba faz
Reguła dźwigni
W celu określenia udziałów poszczególnych faz w obszarze dwufazowym należy przez punkt stanu poprowadzić linię poziomą aż do
przecięcia się z najbliższymi liniami wykresu. Długości odcinków między punktami stanu i punktami przecięcia się liniii poziomej z liniami
ograniczającymi obszar występowania faz są odwrotnie proporcjonalne do udziałów tych faz w stopie.
Sieć krystaliczna i typy sieci
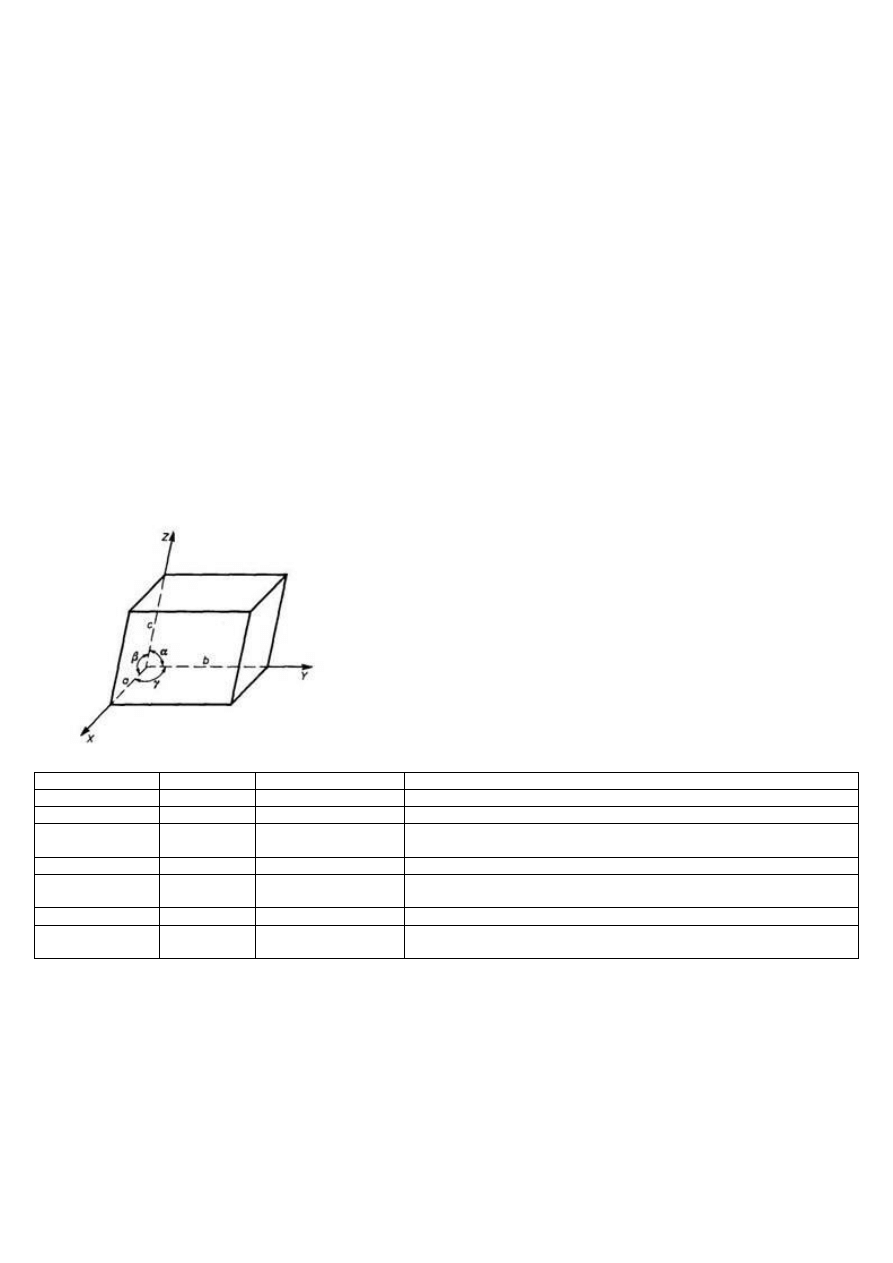
Komórka elementarna - najmniejsza, powtarzalna część struktury kryształu, zawierająca wszystkie rodzaje cząsteczek, jonów i atomów,
które tworzą określoną sieć krystaliczną. Komórka elementarna powtarza się we wszystkich trzech kierunkach, tworząc zamknięta sieć
przestrzenną, której główną cechą jest symetria. Komórka elementarna ma zawsze kształt równoległościanu
Układ
Jedn. osiowe
Kąty między osiami
Możliwe sieci Bravais'go
Regularny
a = b = c
α = β = γ = 90°
prymitywna (P), przestrzennie centrowana (I), ściennie centrowana (F)
Tetragonalny
a = b ≠ c
α = β = γ = 90°
prymitywna (P), przestrzennie centrowana (I)
Rombowy
a ≠ b ≠ c ≠ a
α = β = γ = 90°
prymitywna (P), przestrzennie centrowana (I), ściennie centrowana (F),
centrowana na podstawach (C)
Jednoskośny
a ≠ b ≠ c ≠ a
α = γ = 90°; β ≠ 90°
prymitywna (P), centrowana na podstawach (C)
Trójskośny
a ≠ b ≠ c ≠ a
α ≠ β ≠ γ ≠ α
α, β, γ ≠ 90°
prymitywna (P)
Heksagonalny
a = b ≠ c
α = β = 90°; γ = 120°
prymitywna (P)
Trygonalny
(romboedryczny)
a = b ≠ c
(a = b = c)
α = β = 90°; γ = 120°
(α = β = γ ≠ 90°)
prymitywna (P)
Stopy metali nieżelaznych
Stopy metali nieżelaznych, stopy, w których żelazo nie stanowi głównego składnika i może być najwyżej składnikiem stopowym.
Najliczniejszą grupę wśród stopów metali nieżelaznych stanowią:
- stopy miedzi
- stopy niklu
- stopy cynku
- stopy cyny
- stopy aluminium
- stopy magnezu

Podstawowe właściwości mechaniczne:
przy obciążeniu statycznym:
o
moduły sprężystości E (Younga) i G (Kirchhoffa)
o
granica plastyczności Re
o
wytrzymałość na rozciąganie Rm (granica wytrzymałości)
o
odporność na pękanie
o
twardość
o
ciągliwość
udarność – przy obciążeniach dynamicznych (impact load)
wytrzymałość zmęczeniowa – przy obciążeniach cyklicznie zmiennych
odporność na pełzanie – przy podwyższonej temperaturze
pełzanie – zwiększające się z czasem odkształcenie plastyczne pod wpływem naprężenia, występujące nawet przy naprężeniach
mniejszych od granicy plastyczności
Metody kształtowania metali i stopów:
odlewanie ciekłego metalu do formy
obróbka plastyczna, bezubytkowa (walcowanie, kucie, wyciskanie, ciągnienie, tłoczenie, zginanie, wykonywanie otworów)
łączenie (przy użyciu dodatkowych elementów), spajanie (spawanie, lutowanie, zgrzewanie)
zagęszczanie proszku metalowego i spiekanie
obróbka ubytkowa, wiórowa (toczenie, struganie, frezowanie, wiercenie, szlifowanie, polerowanie)
Właściwości drewna:
Mała gęstość
Trwałość
Sprężystość
Wytrzymałość
Mała rozszerzalność i przewodność cieplna
Podatność na obróbkę mechaniczną
Suche ma małą przewodność elektryczną
Jest zdrowe – ludzkość od początku współistnieje z drzewami
Wiązania silne (pierwotne) – związane z przechodzeniem lub uwspólnianiem elektronów przez atomy
Jonowe - istotą jest elektrostatyczne oddziaływanie między jonami o różnoimiennych ładunkach. Dwa etapy powstawania
wiązania:
o
przejście elektronu z jednego atomu do drugiego:
NaCl: energia jonizacji Na (uwolnienia elektronu) 5,1eV; uwolniony elektron przechodzi do Cl, wyzwala się
przy tym energia 3,8eV
o
powstanie jonów „+” i „-” czyli atomów elektrycznie nieobojętnych:
w przypadku NaCl: powstają jony Na+ i Cl-
Wiązanie jest stabilne jeżeli energia potrzebna do zerwania wiązania jonowego jest większa niż energia wyzwolona przy powrocie
elektronu do atomu macierzystego
Kowalencyjne - istotą jest istnienie pary elektronów, które są współdzielone w porównywalnym stopniu przez oba atomy tworzące
to wiązanie.
Metaliczne - wiązanie w substancjach metalicznych między dodatnio naładowanymi zrębami atomowymi (rdzeniami), osadzonymi
w węzłach sieci przestrzennej, pozostającymi w równowadze z gazem elektronowym, wypełniającym przestrzeń sieciową.
Znacznie słabsze wiązania wtórne
Van der Waalsa - wzajemne oddziaływania elektrostatyczne pomiędzy dipolami cząsteczkowymi, pomiędzy cząsteczkami
pozbawionymi momentów dipolowych lub atomami (tzw. oddziaływania dyspersyjne). Przyczyną wystąpienia oddziaływania van
der Waalsa są trwałe oraz wyindukowane momenty dipolowe w cząsteczkach lub - w przypadku oddziaływań dyspersyjnych -
chwilowe asymetrie rozkładu ładunku w cząsteczce lub atomie.
Mostki wodorowe - wiązanie wytworzone pomiędzy atomem wodoru, połączonym kowalencyjnie z atomem X, a atomem Y,
posiadającym swobodną parę elektronów i należącym zazwyczaj do innej cząsteczki. Oba atomy, X i Y, muszą odznaczać się
dużą elektroujemnością.
Polimorfizm - zjawisko występowania różnych odmian krystalograficznych tej samej substancji chemicznej. Występuje ono wtedy, gdy ta
sama substancja może występować w dwóch lub nawet kilku formach krystalicznych.
Alotropia – zjawisko występowania, w tym samym stanie skupienia, różnych odmian tego samego pierwiastka chemicznego różniących się
właściwościami fizycznymi i chemicznymi. Odmiany alotropowe pierwiastka mogą różnić się między sobą strukturą krystaliczną lub liczbą
atomów w cząsteczce. Każda odmiana alotropowa jest trwała w pewnym zakresie temperatury i ciśnienia. Zmiana tych warunków może
spowodować określoną przemianę alotropową. To pojęcie węższe od Polimorfizmu i dotyczy wyłączenie czystych pierwiastków.
Krystalizacja, proces tworzenia się i wzrostu kryształu z cieczy przechłodzonej, roztworu przesyconego lub przesyconej pary (fazy
gazowej).
Aby jednak rozpoczęła się krystalizacja, muszą najpierw powstać bardzo małe zalążki nowej fazy (zarodki krystalizacji), albo należy je do
krystalizatora wprowadzić (zaszczep krystalizacji).
Krystalizację stosuje się do oczyszczania substancji, wydzielania substancji z mieszanin lub rozdzielania mieszanin na składniki
(krystalizacja frakcjonująca) i do otrzymywania monokryształów.
Wyszukiwarka
Podobne podstrony:
Baza pytań egzaminacyjnych z odpowiedziami teoria 1 05 2013
Andragogika egzamin 1 część 7 pytan, Uczelnia
EP @ pytań na egzamin z odpowiedziami
egzamin odpowiedzi do pytan, Wykłady, Usługi w biznesie, Międzynarodowe Stosunki Gospodarcze, MSG, M
odpowiedzi na kilka pytan egzaminacyjnych, Krioterapia , Krioterapia jest metodą leczenia zmian skór
Biofizyka - egzamin - część 1, pytania rachunkowe i odpowiedzi
Wstęp do Religioznawstwa - egzamin, odpowiedzi Inne odpowiedzi do pytań ze skyptu 2
Biofizyka Odpowiedzi do pytan egzamin 2009 3
EP 40 pytań na egzamin z odpowiedziami
Biofizyka egzamin część 1 pytania rachunkowe i odpowiedzi
Biofizyka egzamin część 3 pytania rachunkowe i odpowiedzi
Test, Test Pytania Odpowiedzi Ochrona Własności Intelektualnej, ZESTAW PYTAŃ EGZAMINACYJNYCH Z PRAWA
WSP- Odpowiedzi do pytan egzaminacyjnych - Kopia, Dokumenty - Bezpieczeństwo Narodowe, 2 semestr (AR
Odpowiedzi do pytań egzaminacyjnych z chemii ogólnej i fizycznej
Odpowiedzi do pytań egzaminacyjnych
odpowiedzi na kilka pytan egzaminacyjnych, derma - opracowania, DERMATOLOGIA - PYTANIA EGZAMINACYJNE
Biofizyka Odpowiedzi do pytan egzamin 2009 3
więcej podobnych podstron