
ANALIZA LEKÓW
MIEJSCOWO ZNIECZULAJĄCYCH
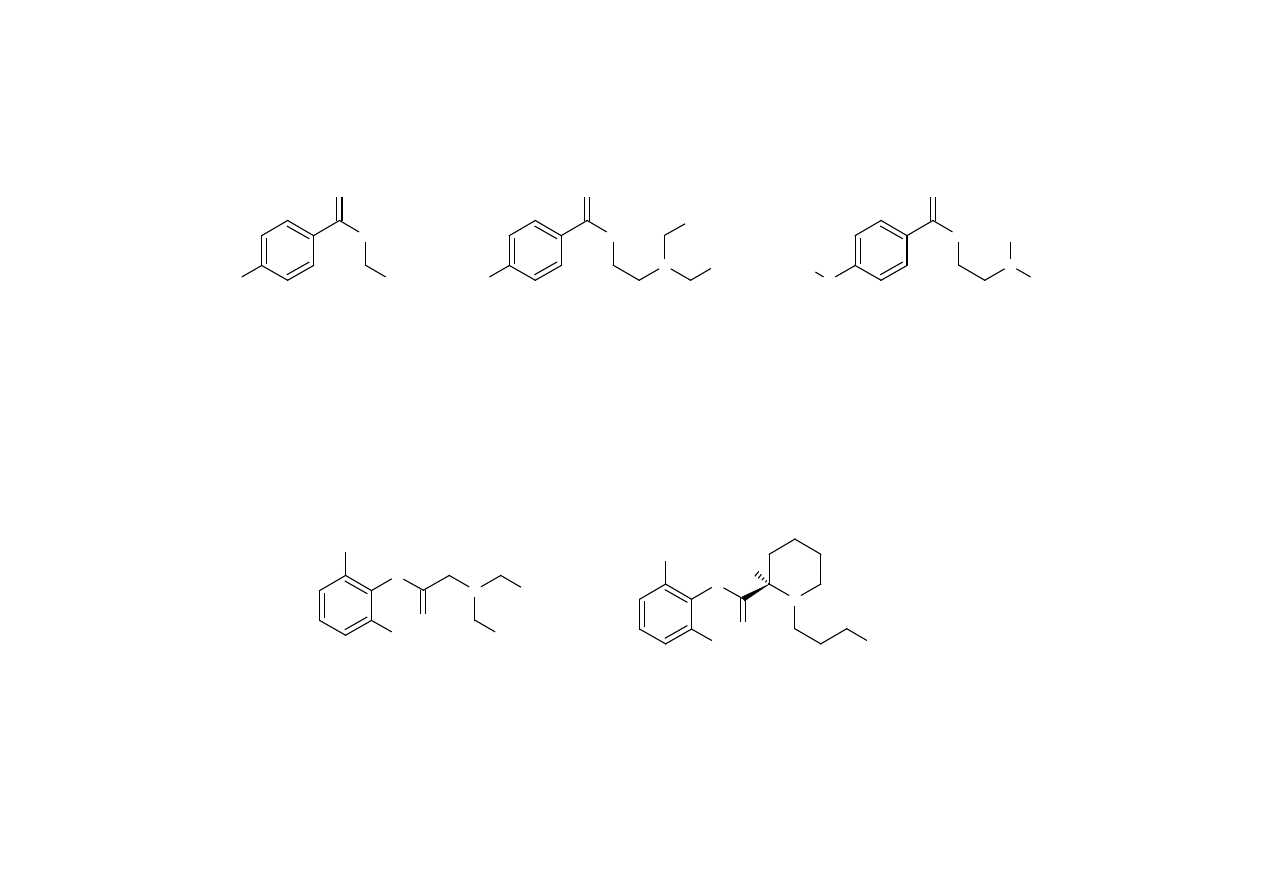
ZWIĄZKI O BUDOWIE ESTROWEJ
ZWIĄZKI O BUDOWIE AMIDOWEJ
Procaini hydrochloridum FPVI
Prokainy chlorowodorek
C
13
H
21
ClN
2
O
2
m.cz. 272.77
Tetracaini hydrochloridum FPVI
Tetrakainy chlorowodorek
C
15
H
25
ClN
2
O
2
m.cz. 300.83
Benzocainum FPVI
Benzokaina
C
9
H
11
NO
2
m.cz. 165.19
N
H2
O
O
CH3
N
H
2
O
O
N
CH3
CH3
* HCl
N
H
O
O
N
H
9
C
4
CH
3
CH
3
* HCl
i enancjomer
N
H
O
CH
3
CH
3
N
CH
3
CH
3
N
H
O
CH
3
CH
3
N
CH
3
H
* HCl, * H
2
O
Bupivacaini hydrochloridum FPVI
Bupiwakainy chlorowodorek
C
18
H
29
ClN
2
O *H
2
O
m.cz. 342.89
Lidocaini hydrochloridum FPVI
Lidokainy chlorowodorek
C
14
H
23
ClN
2
O *H
2
O
m.cz. 288.82
* HCl, * H
2
O
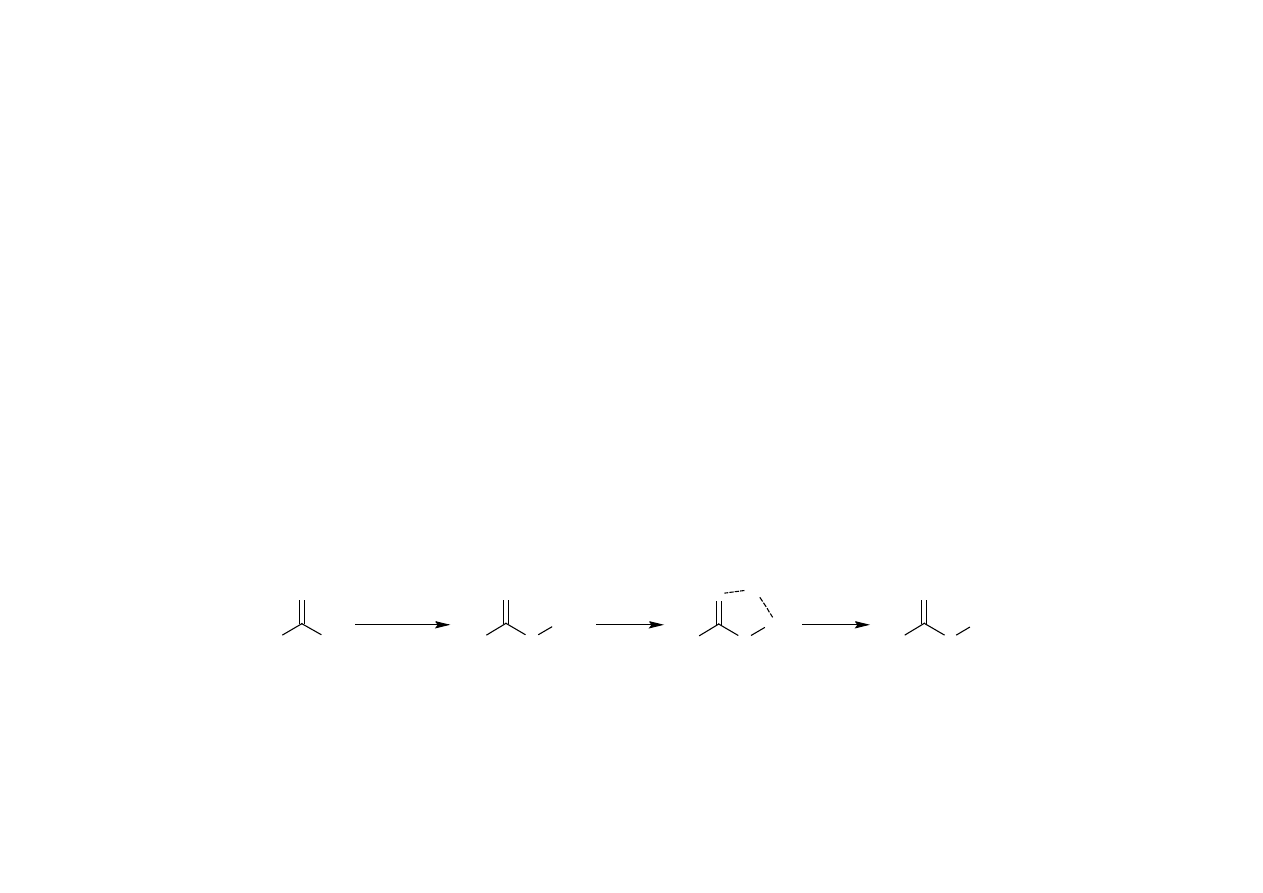
1. Reakcje z odczynnikami na zasady organiczne
prokainy HCl
ANALIZA JAKOŚCIOWA
tetrakainy HCl
lidokainy HCl
bupiwakainy HCl
2. Reakcja na jon chlorkowy
prokainy HCl
tetrakainy HCl
lidokainy HCl
bupiwakainy HCl
3. Tworzenie kwasów hydroksamowych
prokainy HCl
tetrakainy HCl
O
R
1
OR
2
O
R
1
O
NH
2
O
R
1
N
H
OH
O
R
1
O
NH
2
Ni
2+
Ni
2+
Ni
2+
NH
2
OH
-R
2
OH
4. Reakcja na grupę aminową I-rzędową aromatyczną
benzokaina
prokainy HCl
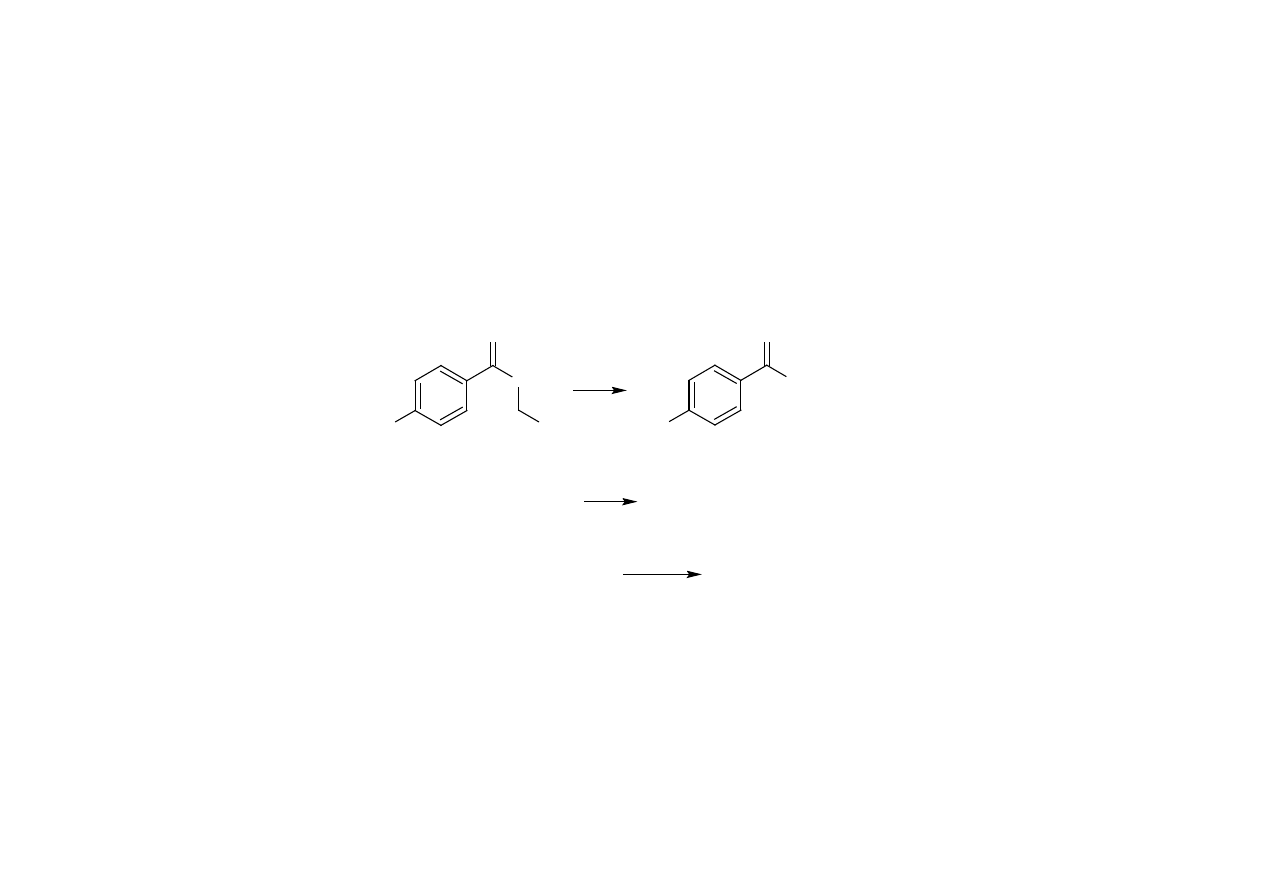
5. Inne reakcje
benzokaina
ANALIZA JAKOŚCIOWA
prokainy HCl
• reakcje na estry etylowe
N
H2
O
O
CH3
OH
-
∆
N
H2
O
H
O
+ C
2
H
5
OH
C
2
H
5
OH + 4I
2
+ 6OH
-
CHI
3
+ HCOO
-
+ 5I
-
+ 5H
2
O
reakcja jodoformowa
CH
3
COOH
+
C
2
H
5
OH
st
ęż
. H
2
SO
4
- H
2
O
CH
3
COOC
2
H
5
transestryfikacja
• uwolnienie wolnej zasady
• reakcja z alkoholem furylowym i stęż. H
2
SO
4
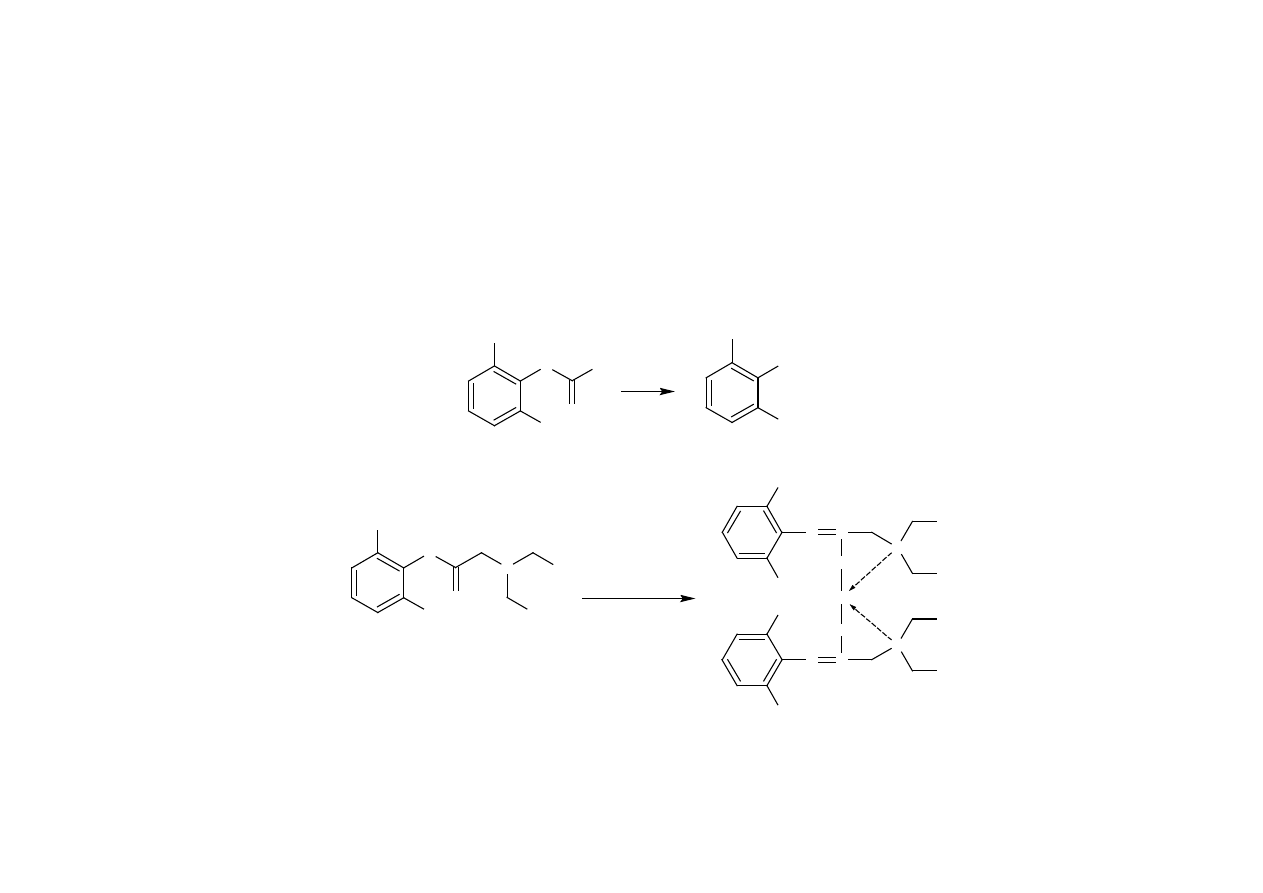
5. Inne reakcje - c.d.
lidokainy HCl
ANALIZA JAKOŚCIOWA
• reakcja po hydrolizie na grupę aminową I-rzędową aromatyczną
• reakcja z dymiącym HNO
3
i KOH/EtOH
bupiwakainy HCl
N
H
O
CH
3
CH
3
R
H
+
/ H
2
O
∆
NH
2
CH
3
CH
3
• tworzenie zielonych kompleksów z jonami Co
+2
2
Co
2+
/ OH
-
N
C
O
N
Co
CH
3
CH
3
N
C
O
N
CH
3
CH
3
CH
3
CH
3
CH
3
CH
3
N
H
O
CH
3
CH
3
N
CH
3
CH
3
5. Inne reakcje - c.d.
tetrakainy HCl
ANALIZA JAKOŚCIOWA
• reakcja na grupę aminową II-rzędową aromatyczną
N
H
O
O
N
H
9
C
4
CH
3
CH
3
NaNO
2
/ H
+
N
O
O
N
H
9
C
4
CH
3
CH
3
N
O
ANALIZA ILOŚCIOWA
1. Acydymetria
• oznaczenie w środowisku niewodnym
2. Redoksymetria
• oznaczenie bromianometryczne odwrócone
(nadmiar bromu oznaczany jodometrycznie)
Br
2
+ 2I
-
I
2
+ 2Na
2
S
2
O
3
2Br
-
+ I
2
2NaI + Na
2
S
4
O
6
prokainy HCl
tetrakainy HCl
lidokainy HCl
bupiwakainy HCl
prokainy HCl
benzokaina
1) OH
-
/
∆
2) H
+
/ 3Br
2
, -CO
2
- 3HBr
N
H
2
Br
Br
Br
N
H2
O
O
CH3
KBrO
3
+ 5KBr + 6HCl
3Br
2
+ 6KCl + 3H
2
O
H
+
/ 2Br
2
-2HBr
N
H
2
O
O
N
CH3
CH3
N
H
2
O
O
N
CH3
CH3
Br
Br

ANALIZA ILOŚCIOWA
3. Azotynometria
• oznaczenie możliwe po hydrolizie ugrupowania amidowego
4. Precypitometria
• oznaczenie argentometryczne odwrócone
(metoda Volharda oznaczania chlorków)
prokainy HCl
benzokaina
lidokainy HCl
bupiwakainy HCl
prokainy HCl
tetrakainy HCl
lidokainy HCl
bupiwakainy HCl
5. Spektrofotometria w UV
• w oparciu o elementy struktury absorbujące promieniowanie elektromagnetyczne
w zakresie nadfioletu
6. Inne

ANALIZA LEKÓW
NARKOTYCZNYCH PRZECIWBÓLOWYCH
ZWIĄZKI POCHODNE MORFINENU
ZWIĄZKI POCHODNE PIPERYDYNY
Morphini hydrochloridum FPVI
Morfiny chlorowodorek
C
17
H
20
ClNO
3
*3H
2
O
m.cz. 375.85
Ethylmorphini hydrochloridum FPVI
Etylomorfiny chlorowodorek
C
19
H
24
ClNO
3
*2H
2
O
m.cz. 385.89
* HCl, * 3H
2
O
* HCl, * 2H
2
O
* H
3
PO
4
, *
1
/
2
H
2
O
Codeini phosphas FPV
Kodeiny fosforan
C
18
H
24
NO
7
P *
1
/
2
H
2
O
m.cz. 406,37
N
O
O
H
O
H
CH
3
H
N
O
O
H
O
CH
3
H
C
H
3
N
O
O
H
O
CH
3
H
C
H
3
N
N
O
C
H
3
COOH
COOH
OH
COOH
*
Fentanyli citras FPVI
Fentanylu cytrynian
C
28
H
36
N
2
O
8
m.cz. 528,60
N
O
O
CH
3
CH
3
* HCl
Pethidini hydrochloridum FPVI
Petydyny chlorowodorek
C
15
H
22
ClNO
2
m.cz. 283,80
1. Reakcje z odczynnikami na zasady organiczne
morfiny HCl
ANALIZA JAKOŚCIOWA
petydyny HCl
etylomorfiny HCl
fentanylu cytrynian
2. Reakcje na aniony
kodeiny fosforan
• reakcja na jony chlorkowe
• reakcje na jony fosforanowe
reakcja z mieszaniną magnezową
reakcja z AgNO
3
w środowisku obojętnym
• reakcja na jony cytrynianowe
CH
2
COOH
COOH
CH
2
COOH
O
H
H
2
SO
4
CH
2
COOH
CHO
CHCOOH
CH OH
+
OH
O
H
-2H
2
O
O
O
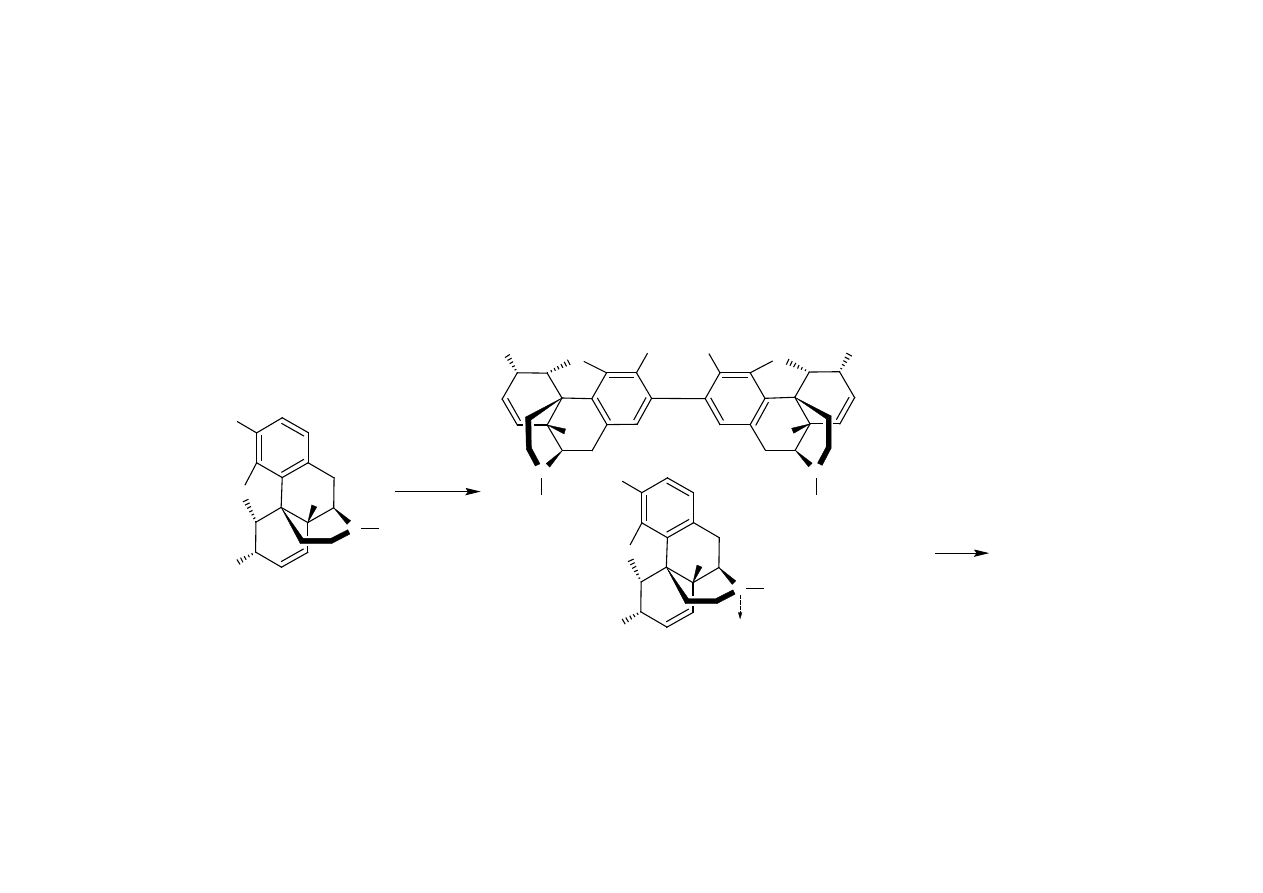
ANALIZA JAKOŚCIOWA
3. Reakcje specyficzne w obrębie grupy
• reakcja z heksocyjanożęlazianem (III) potasu i FeCl
3
morfiny HCl
• reakcja na grupę fenolową (z FeCl
3
)
Fe
3+
Fe
4
[Fe(CN)
6
]
3
O
O
H
N
CH
3
H
O
H
+ K
3
Fe(CN)
6
O
OH
N
CH
3
H
O
H
O
O
H
N
CH
3
H
OH
+
O
O
H
N
CH
3
H
O
H
O
K
4
[Fe(CN)
6
]
+

ANALIZA JAKOŚCIOWA
3. Reakcje specyficzne w obrębie grupy - c.d.
• reakcja na grupę fenolową po przeprowadzeniu w apokodeinę
kodeiny fosforan
• wykrywanie etanolu po hydrolizie alkalicznej
etylomorfiny HCl
reakcja jodoformowa
petydyny HCl
• reakcje na estry etylowe
reakcja jodoformowa
transestryfikacja

ANALIZA ILOŚCIOWA
1. Acydymetria
• oznaczenie w środowisku niewodnym
morfiny HCl
petydyny HCl
etylomorfiny HCl
fentanylu cytrynian
kodeiny fosforan
2. Precypitometria
• oznaczenie argentometryczne odwrócone
(metoda Volharda oznaczania chlorków)
morfiny HCl
petydyny HCl
etylomorfiny HCl
3. Spektrofotometria w UV
• w oparciu o elementy struktury absorbujące promieniowanie elektromagnetyczne
w zakresie nadfioletu
4. Inne
Wyszukiwarka
Podobne podstrony:
anestetyki i narkotyki materiały 2007
NARKOTYKI PREZENTACJA DODATKOWA 2006
Anestetyki i narkotyki
anestetyki i narkotyki materiały 2007
Narkotyki Prezentacja B Różańskiego
anestetyki i narkotyki materiały 2007
NARKOTYKI PREZENTACJA DODATKOWA 2006
Narkotyki prezentacja
Leki narkotyczne przeciwbólowe - receptura, PIELĘGNIARSTWO, anestezjologia i pielęgniarstwo anestezj
Prezentacja1=narkotyki walka
Siemano mały prezent z Anestezji
narkotyki www prezentacje org
prezentacja finanse ludnosci
prezentacja mikro Kubska 2
więcej podobnych podstron