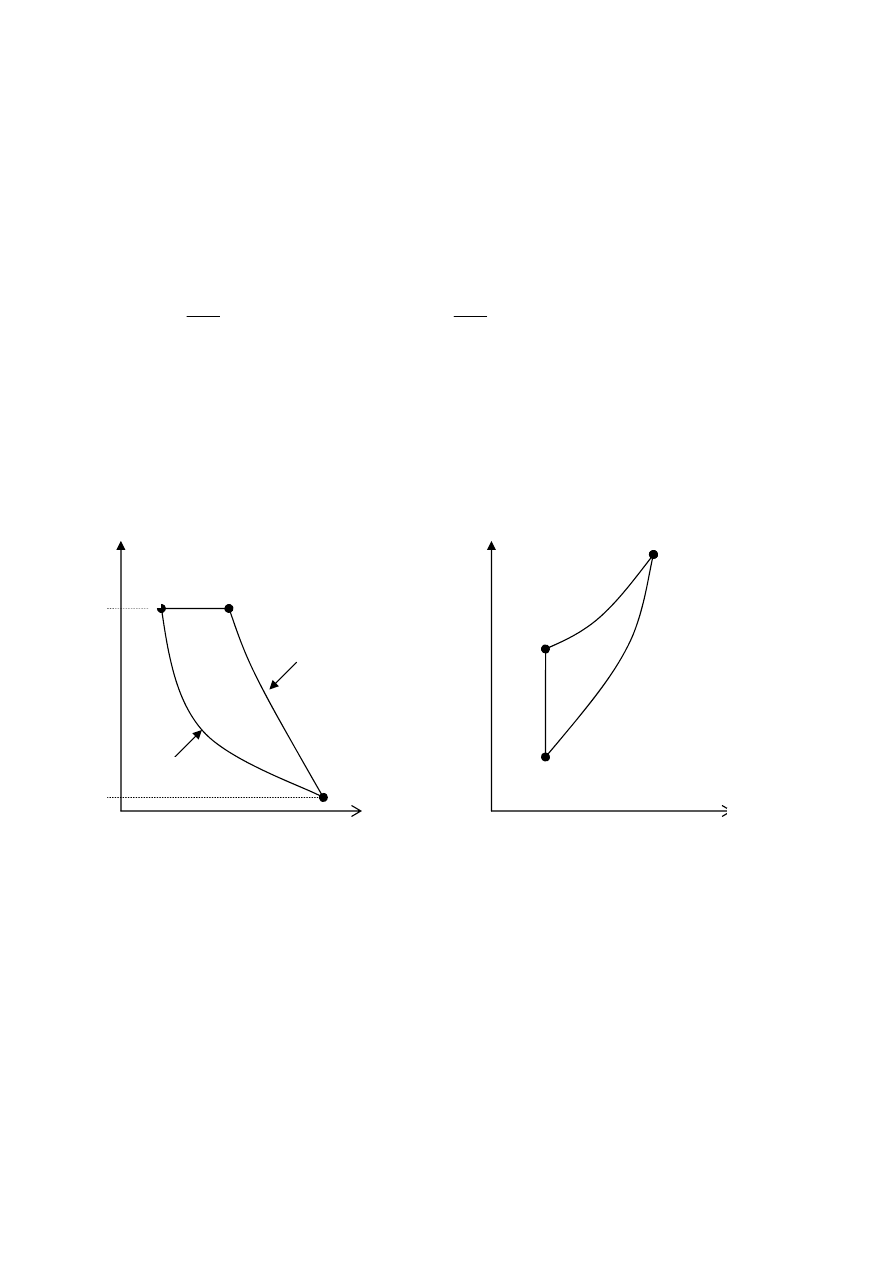
p
2
=p
3
Zadanie II 3.1
Obieg prawobieżny złożony jest z odwracalnych przemiana termodynamicznych, adiabaty
zgęszczania, izobary i politropy. Czynnikiem roboczym jest azot traktowany tak jak gaz
doskonały. Ciśnienie i temperatura na początku przemiany adiabatycznej zgęszczania azotu
jest równa p
1
= 0,9[at] i t
1
=27[
o
C] zaś na jej końcu T
2
=900[K], natomiast temperatura
początku przemiany politropowej T
3
=1900[K]. Indywidualna stała gazowa azotu
R=296,75[
kgK
J
] zaś ciepło właściwe C
p
=1043[
kgK
J
]. Obliczyć parametry stanu w punktach
charakterystycznych obiegu oraz wykładnik politropy.
Rozwiązanie
1. Wykresy prawobieżnego obiegu termodynamicznego azotu we współrzędnych p,
υ oraz T, s
1
2
1
2
3
c= const
s= const
3
p
1
υ
p
s
T

2. Tabela zestawienia danych oraz wyników obliczeń
punkt charaktery-
styczny
parametr stanu
1 2 3
p
i
[p
1
]
1
1
2
2
p
T
T
p
R
Cp
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
p
3
=p
2
T
i
[T
1
] [T
2
] [T
3
]
υ
1
1
p
RT
=
υ
1
2
2
1
2
p
R
T
T
T
R
Cp
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
υ
1
3
2
1
3
p
R
T
T
T
R
Cp
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
υ
3.Obliczam parametry stanu w punktach charakterystycznych obiegu
3.1 Obliczam masową gęstość zasobu objętości w punkcie 1
1
1
p
RT
=
υ
3.2 Obliczam gęstość zasobu objętości powietrza w punkcie 2
Z równania mamy:
const
p
k
=
υ
,
piszemy równanie na z punktu 1 i 2 i otrzymujemy zależności:
k
k
p
p
2
2
1
1
υ
υ
=
υ
RT
p
=
1
2
2
1
1
1
−
−
=
k
k
T
T
υ
υ
stąd
1
1
2
1
2
−
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
k
T
T
υ
1
1
2
1
−
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
k
T
T
υ
1
2
1
2
1
1
1
p
R
T
T
T
p
R
T
k
k
−
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
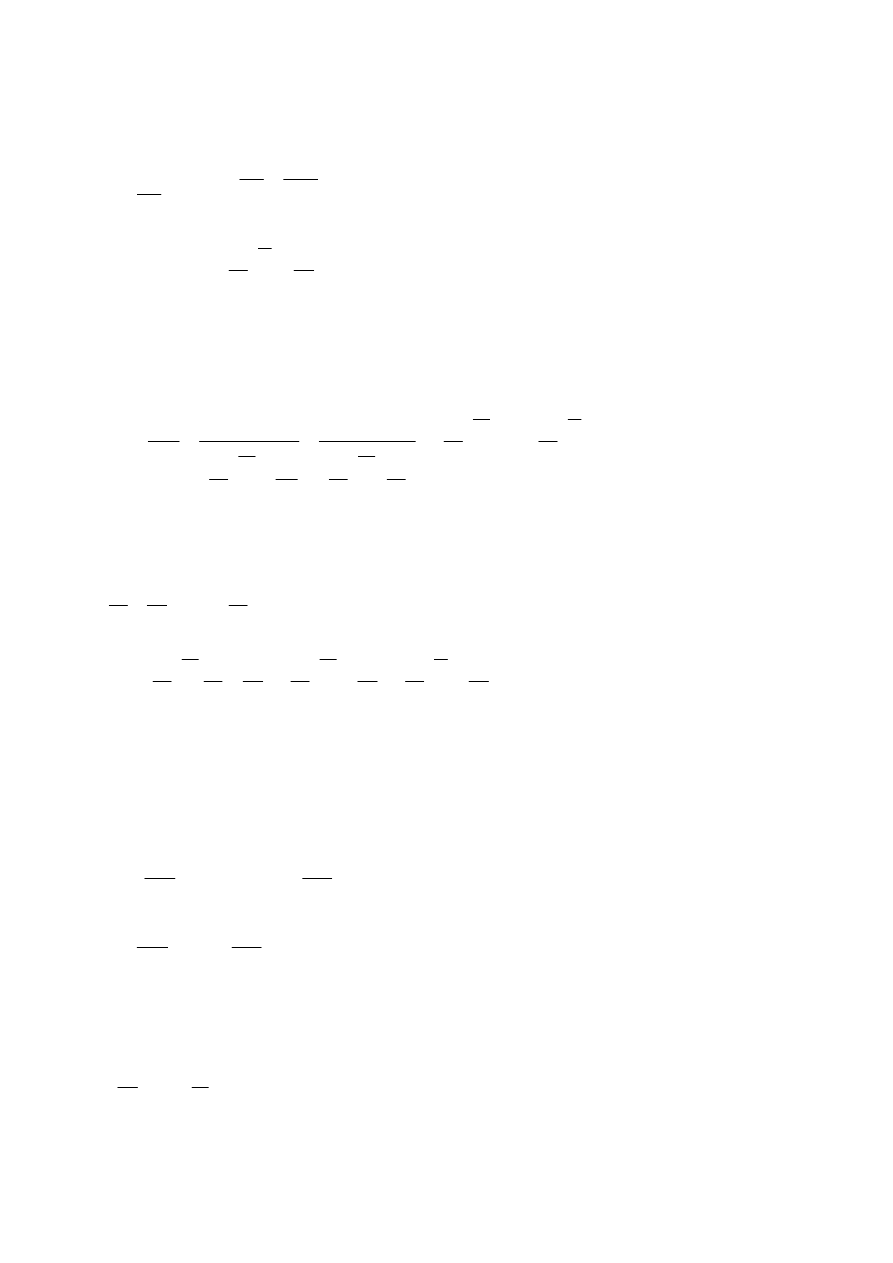
Z równania Mayer’a oraz z definicji izotropii określamy zależności
υ
υ
C
C
k
R
C
C
p
p
=
=
−
⇒
1
−
=
k
k
R
C
p
otatecznie:
1
2
2
1
p
R
T
T
T
R
Cp
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
υ
4. Obliczam ciśnienie powietrza w punkcie 2 obiegu
Z równania stanu gazu doskonałego mamy:
1
1
2
1
1
1
2
2
1
1
1
2
1
1
2
1
1
1
2
1
2
2
2
p
T
T
p
T
T
T
T
T
T
p
p
R
T
T
T
RT
RT
p
R
Cp
k
k
k
k
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
=
−
−
−
υ
5. Obliczam masową gęstość zasobu objętości powietrza w punkcie 3 obiegu. Między
punktami 2 a 3 mamy przemianę izobaryczną.
2
2
3
3
2
3
2
υ
υ
υ
υ
T
T
T
T
s
=
⇒
=
1
3
2
1
1
3
1
2
1
1
3
2
1
1
1
2
1
3
p
R
T
T
T
p
R
T
T
T
p
R
T
T
T
T
T
R
Cp
k
k
k
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
−
−
υ
6. Obliczam wykładnik politropy z równania politropy
n
n
p
p
1
1
3
3
υ
υ
=
Z równania stanu gazu doskonałego Clapeyron’a
3
3
3
p
RT
=
υ
1
1
1
p
RT
=
υ
n
n
p
RT
p
p
RT
p
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
1
1
1
3
3
3
stąd:
n
n
n
n
T
p
T
p
3
1
3
1
1
1
−
−
=
n
n
T
T
p
p
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
1
3
1
3
1
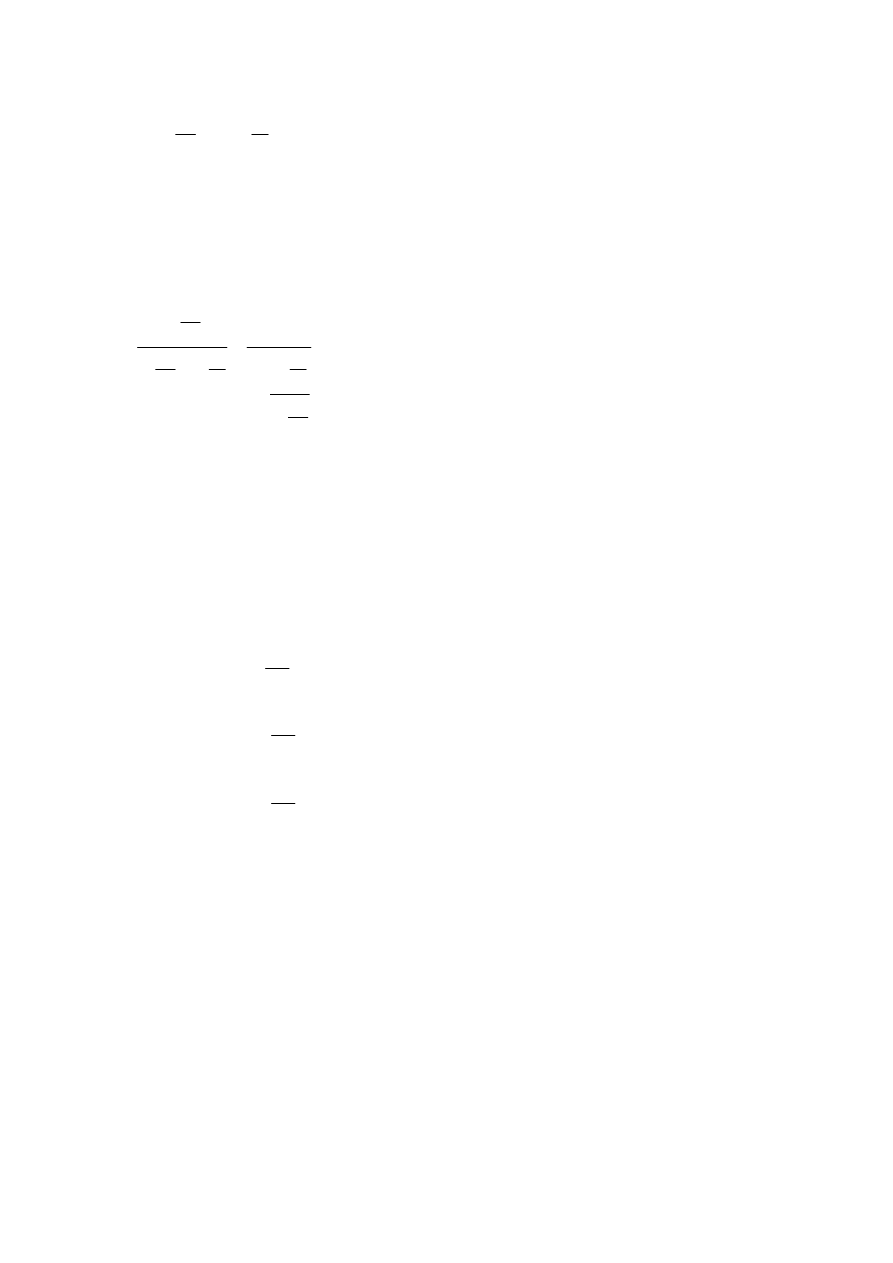
(
)
1
3
3
1
ln
ln
1
T
T
n
p
p
n
=
⎟⎟
⎠
⎞
⎜⎜
⎝
⎛
−
ostatecznie:
3
1
1
3
1
3
3
1
3
1
ln
ln
1
1
ln
ln
ln
p
p
T
T
T
T
p
p
p
p
n
+
=
+
=
6. Obliczam wartości parametrów stanu w punktach charakterystycznych obiegu
6.1 Obliczam wartości parametrów stanu w punktach charakterystycznych obiegu
p
2
= 4,188848[MPa]
p
3
=p
2
= 4,188848[MPa]
p
1
= 0,9 · 9,81 · 10
4
= 0,08829 [MPa]
7. Obliczam wartości mas gęstości zasobu azotu w punktach charakterystycznych obiegu
υ
1
= 1,00886
⎥
⎦
⎤
⎢
⎣
⎡
kg
m
3
υ
2
= 0,063764
⎥
⎦
⎤
⎢
⎣
⎡
kg
m
3
υ
3
= 0,134613
⎥
⎦
⎤
⎢
⎣
⎡
kg
m
3
8. Obliczam wartość wykładnika politropie
n = 1,91615
Wyszukiwarka
Podobne podstrony:
31 9 id 34934 Nieznany (2)
31 3 id 34927 Nieznany (2)
6 31 id 43159 Nieznany (2)
II Wyklad id 210139 Nieznany
II 83 id 209795 Nieznany
II czesc id 209842 Nieznany
biochemia II 1 plus id 86425 Nieznany (2)
3 31 id 32909 Nieznany (2)
F II wyklad 4 id 167240 Nieznany
II 32 id 209764 Nieznany
II 43 id 209770 Nieznany
D 2 calosc I,II,III id 130089 Nieznany
biochemia II 2 plus id 86427 Nieznany (2)
kolokwia, II semestr id 240233 Nieznany
II 82 id 209794 Nieznany
NIP 31 id 320174 Nieznany
F II wyklad 7 id 167243 Nieznany
PL wyklad dla II roku id 360452 Nieznany
więcej podobnych podstron