BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
1
1.
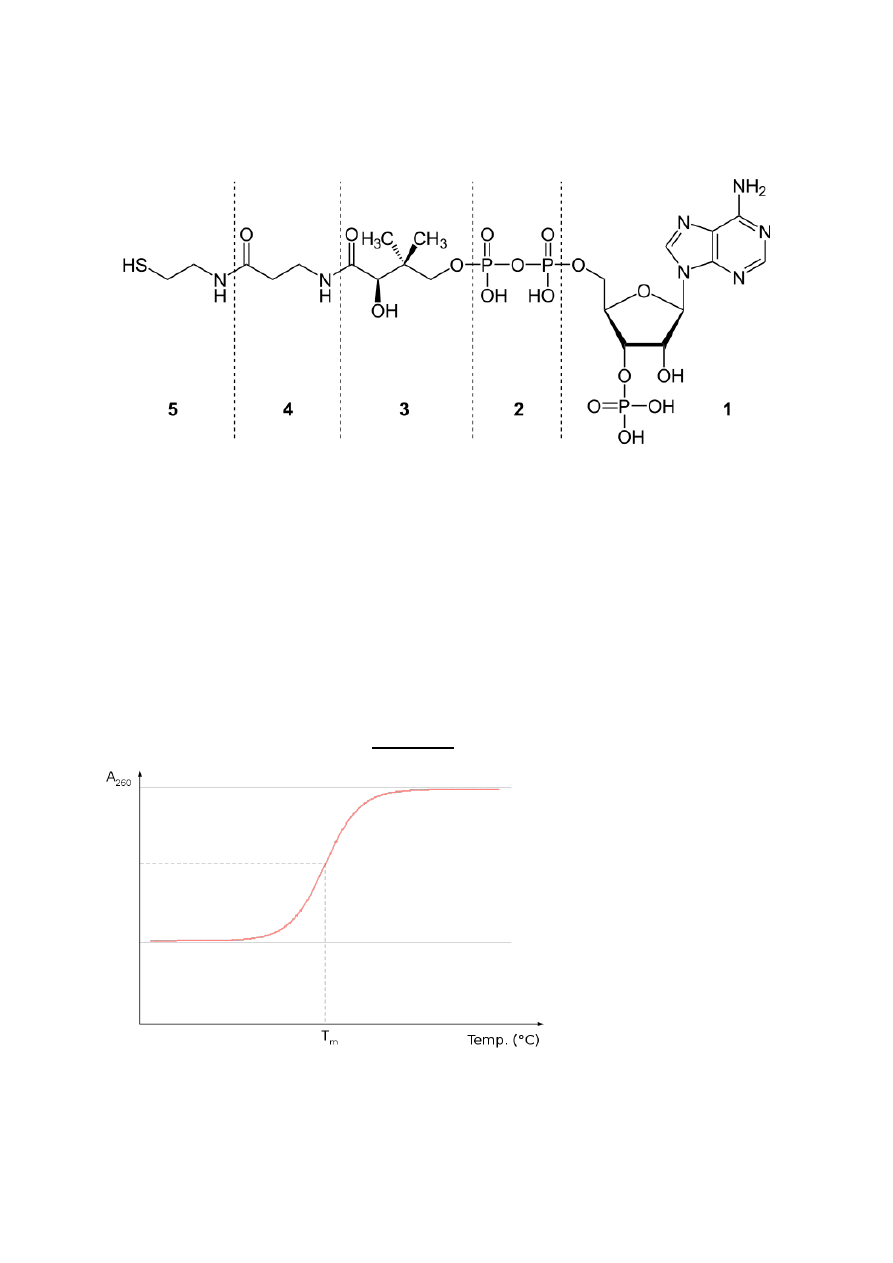
Koenzym zawierający wit. B
5
(kwas pantotenowy) -> CoA: przenośnik grup arylowych; w cyklu
kwasu cytrynowego
2.
Funkcje:
a)
ATP
– koenzym oraz nośnik energii chemicznej używanej w metabolizmie komórki. Powstaje jako
magazyn energii w procesach fotosyntezy i oddychania komórkowego. Zużywają go liczne enzymy, a
zgromadzona w nim energia służy do przeprowadzania różnorodnych procesów, jak biosyntezy,
ruchu i podziału komórki;
b)
UDP
– pochodne UDP-cukier uczestniczą w epimeryzacji cukrów i biosyntezie glikogenu,
dwucukrów (disacharydów) glukozylowych i oligosacharydów występujących w glikoproteinach i
proteoglikanach. UDP-kwas glukuronowy tworzy koniugaty wielu leków (np. aspiryny) oraz bilirubiny
w moczu.
3.
Wpływ mocznika na topnienie DNA (brak danych) + krzywe absorpcji
Wyznaczenie temperatury topnienia kwasu nukleinowego z wykorzystaniem efektu
hiperchromowego
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
2
Krzywa, przedstawiająca zależność absorbancji od temp. to „krzywa topnienia”.
Temperatura, która powoduje wzrost absorbacji równy 50% absorbancji max w czasie podgrzewania
nazywamy temp. topnienia. Max pochłaniania występuje przy 260nm.
Wyznaczenie tego pozwala nam na ocenę czystości preparatu kwasu nukleinowego – białka będące
zanieczyszczeniem mają max w 280 nm (wzrasta wartość A280/A260).
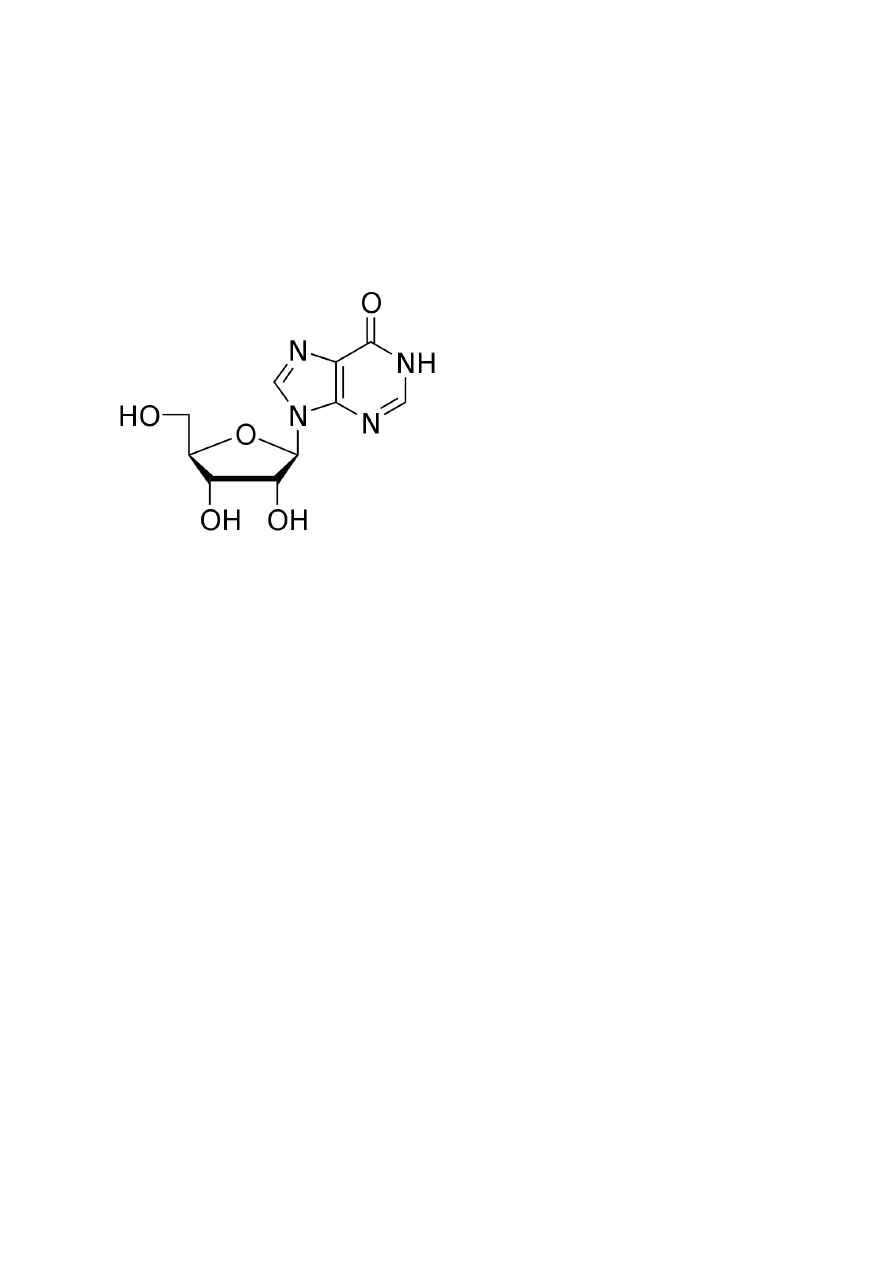
4.
Wzór inozyny
5.
Degradacja nieenzymatyczna kwasów nukleinowych może być wywoływana przez następujące
czynniki zebrane w 3 grupy:
- mechaniczne: rozcinanie, wytrząsanie, zbyt intensywne mieszanie, szybkie przemieszczanie przez
kapilary – dochodzi do tego najczęściej w czasie preparatyki;
- fizyczne: wysoka temp, promieniowanie jonizujące oraz nadfioletowe, ultradźwięki;
- chemiczne:
- hydroliza kwaśna poprzez stężone kwasy jak HClO
4
, H
2
SO
4
, trichlorooctowy (TCA).
hydrolizują one zarówno DNA jak i RNA do wolnych zasad azotowych oraz kwasu
fosforowego, deoksyrybozy lub rybozy.
- hydrolizie zasadowej ulegają tylko RNA, w efekcie czego powstają cykliczne 2’ 3’ –
nukleozydomonofosforany.
6.
Stopień depolimeryzacji kwasów można zmierzyć badając absorbancję światła ultrafioletowego
ich roztworów.
7.
Odnośnie ułamków molowych w nici wzorcowej i komplementarnej:
A łączy się z T, natomiast G z C. Nie znając żadnej wartości oczywiście nic nie wyczarujemy. Jednak
wiemy, że suma wszystkich ułamków molowych musi się równać 1.0, dlatego znając ułamek molowy
dla A, T i G na jednej nici, bądź A, G na jednej nici i T na nici komplementarnej, zgodnie z logiką,

BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
3
możemy wyliczyć ułamki molowe dla wszystkich zasad na obydwóch niciach.
Przykład 1:
Ułamek molowy na nici 1 dla A wynosi 0.24, dla T 0.26 i dla G 0.32;
Ułamek molowy dla C na nici 1 wynosi: 1.0 - (ułamek A + ułamek T + ułamek G)
1.0 - (0,24 + 0.26 + 0.32) = 0.18
Na nici 2 ułamki będą wynosiły:
A 0.26
T 0.24
G 0.18
C 0.32
Przykład 2:
Ułamek molowy na nici 1 dla A wynosi 0.28 a dla G 0.16, natomiast na nici 2 dla T ma on wartość
0.28. Jakie są wartości ułamka molowego dla wszystkich zasad na obydwóch niciach?
Jeśli na nici 2 ułamek dla T wynosi 0.28 to zgodnie z zasadą komplementarności zasad, na nici 1
ułamek ten musi wynosić 0.50 - ułamek T = 0.22. Przyjąłem wartość 0.50 ponieważ w zasadzie liczymy
jedynie stosunek A/T, który podajemy w wartości ułamka molowego. Znając ułamki molowe dla A, T i
G na nici 1 możemy wyliczyć ułamek molowy dla C na nici 1. Następnie, jak w przykładzie pierwszym,
wyliczamy ułamki molowe dla zasad na nici drugiej.
Wygląda na to, że nie da się tego wyliczyć znając jedynie ułamki molowe dwóch zasad, niezależnie od
tego, dla której nici są one podane.
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
4
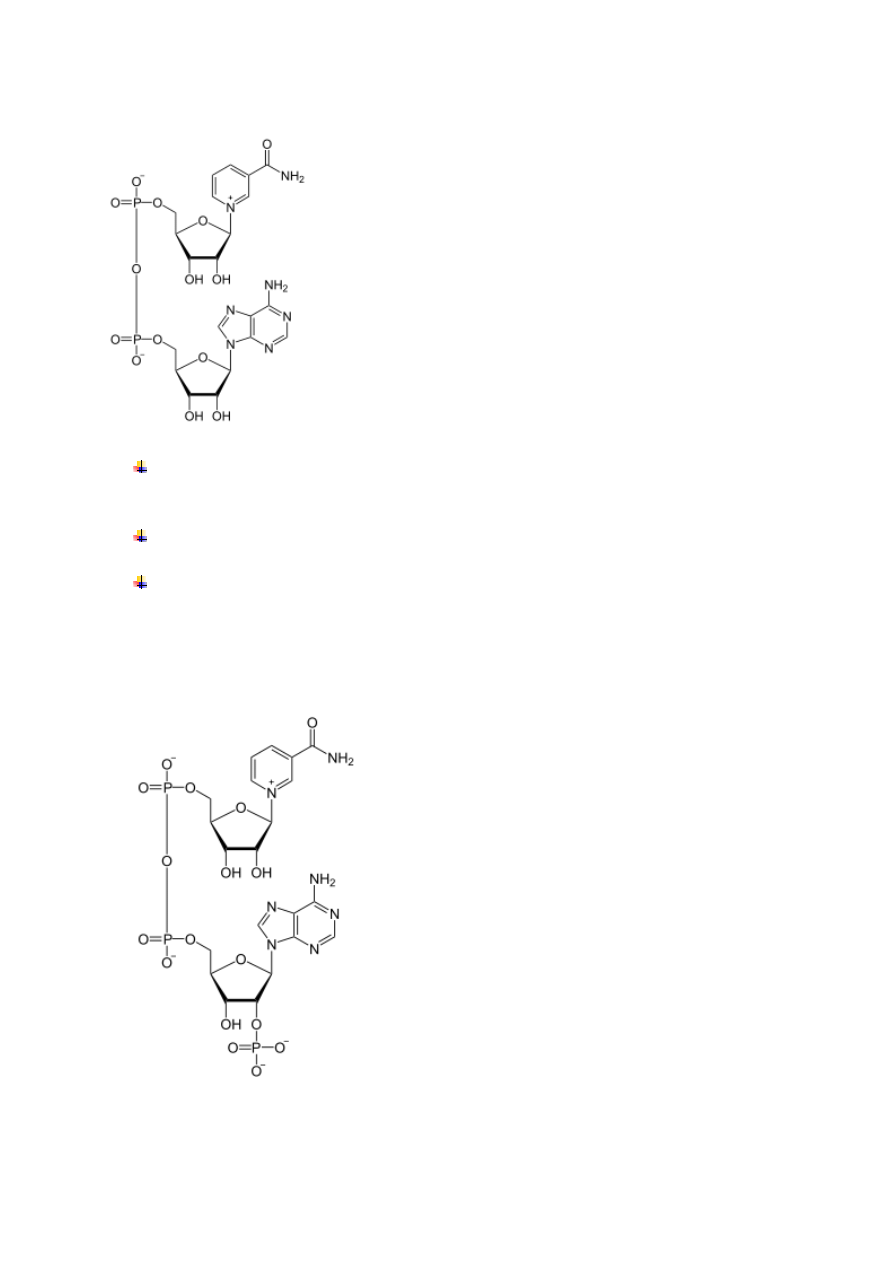
8. NAD dinukleotyd nikotynoamido-adeninowy
funkcje:
NAD zależne dehydrogenazy katalizują reakcje oksydoredukcji w oksydacyjnych szlakach
metabolizmu np.: w glikolizie, cyklu kwasu cytrynowego i mitochondrialnym łańcuchu
oddechowym ,
Różne pochodne tego związku są akceptorami elektronów i protonów w procesach utleniania
komórkowego (Wiki)
Pełni też rolę koenzymów oksydoreduktaz. Wiki
NADP
fosforan di nukleotydu nikotydynoamidowo-adeninowego
funkcje:
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
5
NADP-zależne dehydrogenazy są charakterystyczne dla syntez redukcyjnych np.:
pozamitochindrialnej syntezy kwasów tłuszczowych i syntezy steroidów,
NADP jest koenzymem dehydrogenaz cyklu pentozo fosforanowego
NADP+ jest także akceptorem protonu i elektronów w reakcjach redukcji, w ten sposób
powstaje NADPH (Wiki)
Jest on następnie zużytkowywany w różnych reakcjach redukcji, głównie w przebiegu
biosyntezy kwasów tłuszczowych i cholesterolu. (Wiki)
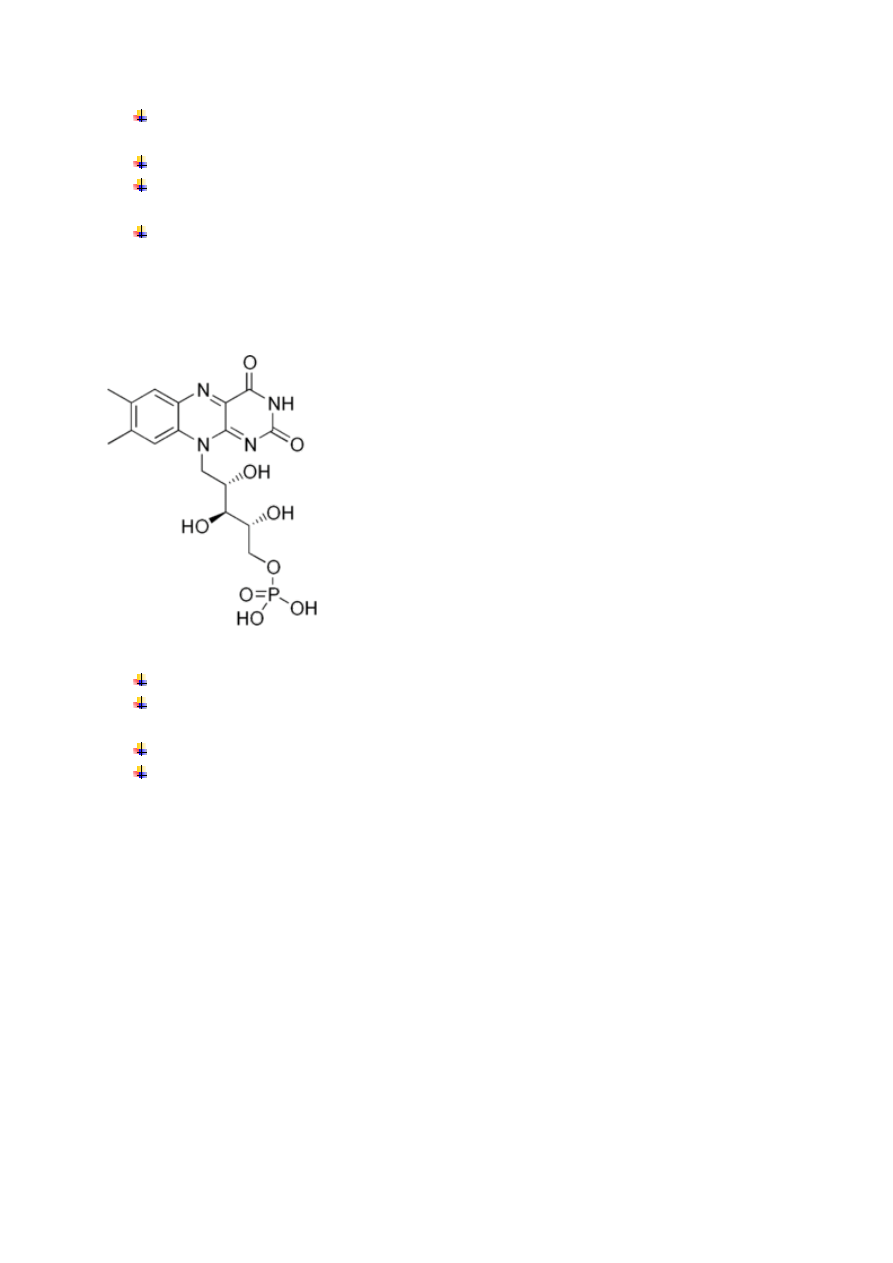
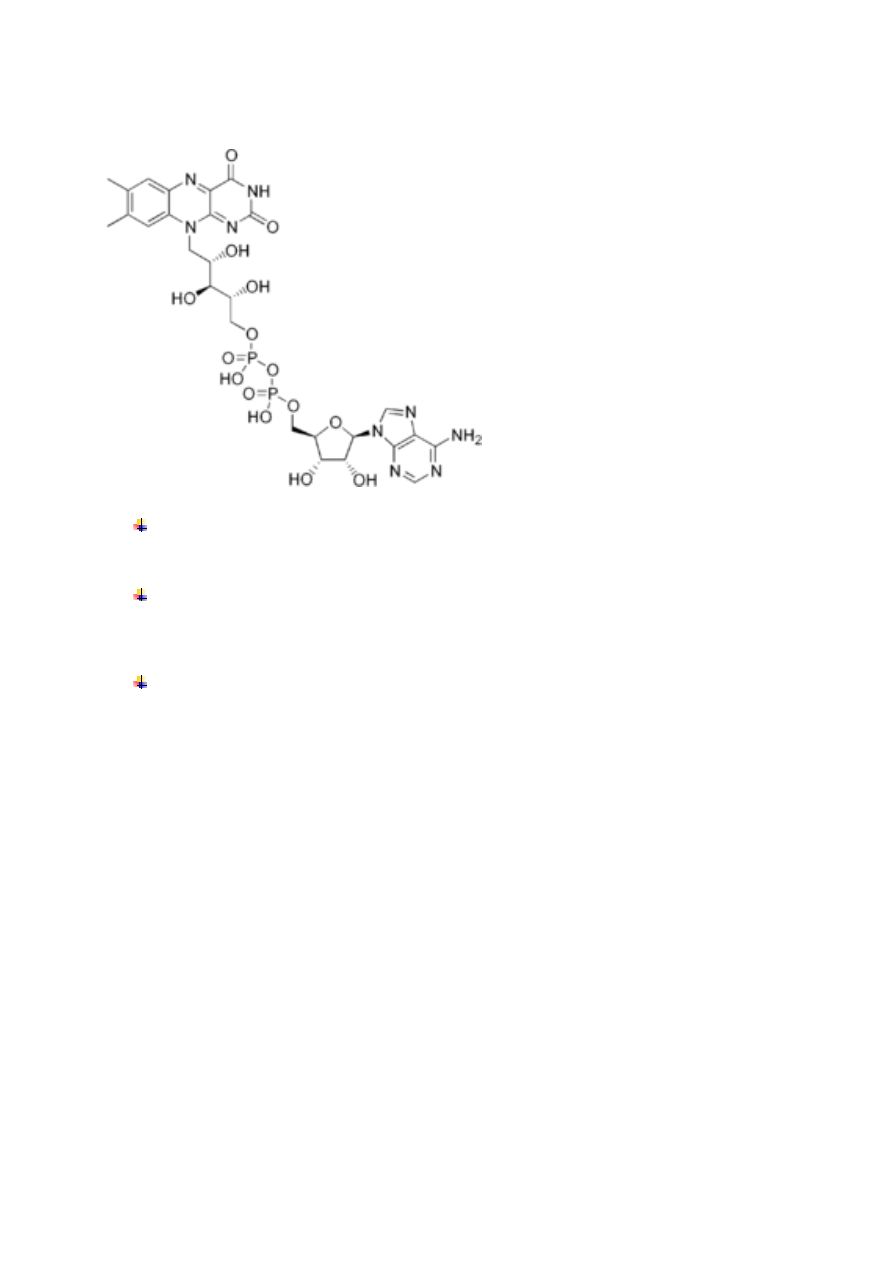
FMN mononukleotyd flawinowy
Funkce :
Zwykle mocno (nie kowalencyjnie) związane z odpowiednim apoenzymem,
Współdziałając z oksydazą L-aminokwasową katalizuje deaminację oksydacyjną L-
aminokwasów,
stanowi grupę prostetyczną niektórych oksydaz
Zarówno FMN, jak i jego sól sodowa (FMN-Na) stosowane są jako żółte barwniki spożywcze
(oznaczane odpowiednio jako E101a i E106) (wiem co jem :D )
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
6
FAD di nukleotyd flawinoadeninowy
Funkcje
koenzym oksydoreduktaz pełniący funkcję przenośnika elektronów i protonów (kationów
wodorowych). Przenosi dwa protony i dwa elektrony, w efekcie czego utleniona forma FAD
przechodzi odwracalnie w formę zredukowaną FADH2
FAD-zależny enzym: oksydaza glukozowa ma zastosowanie przy oznaczaniu stężenia glukozy
9. II rzędowa struktura DNA
II- rzędowa struktura DNA – podwójna helisa, przestrzenne ułożenie nukleotydów
10.
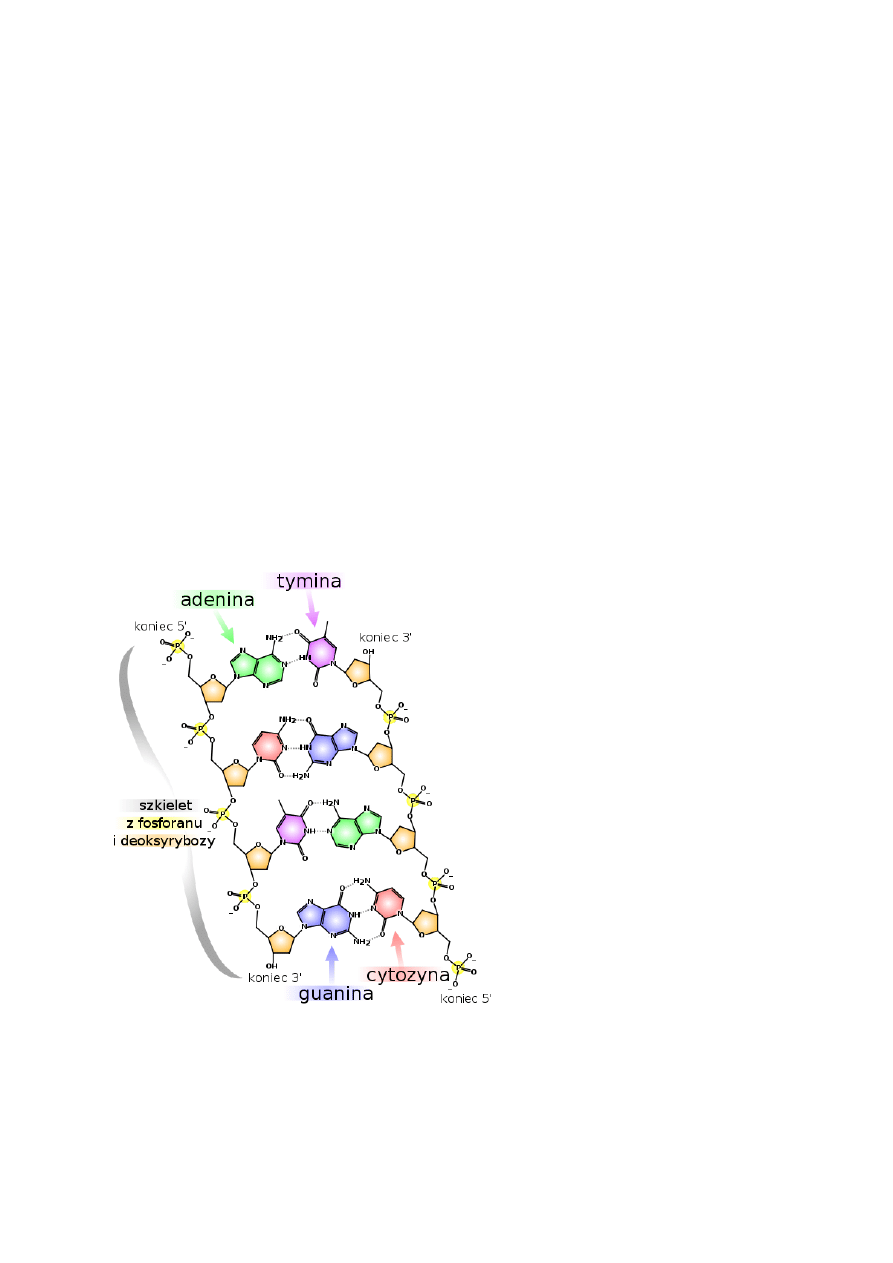
Struktura DNA
Dwuniciowa helisa
Składa się z nukleotydów: zasada azotowa (puryny – A, G; pirymidyny – C, T),
deoksyryboza, reszta kwasu fosforowego
Zasady, skierowane do wewnątrz spirali, łączą obie nici miedzy sobą wiązaniami
wodorowymi (A i T dwoma; G i C trzema), wiązanie między C i G jest ok. 50%
silniejsze, dlatego obszary z dużą ilością A-T są bardziej podatne na rozluźnienie
struktury
„na zewnątrz” spirali nukleotydy połączone wiązaniem 3’,5’- fosfodiestrowym
Podwójna helisa na powierzchni posiada dwa rowki: większy i mniejszy, które różnią
się w zależności od rodzaju struktury II-rzędowej, które pięknie opisze Olek ;P. Np.
struktura B ma rowek większy o szer. 2,2 nm, mniejszy ma 1,2 nm, a struktura Z ma
tylko 1 rowek
Opisano 6 struktur II-rzędowych (A-E i Z), z czego jedynie Z jest lewoskrętna
Struktury II-rzędowe różnią się też stopniem skręcenia (skok w strukturze B wynosi
3,4 nm).
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
7
11.
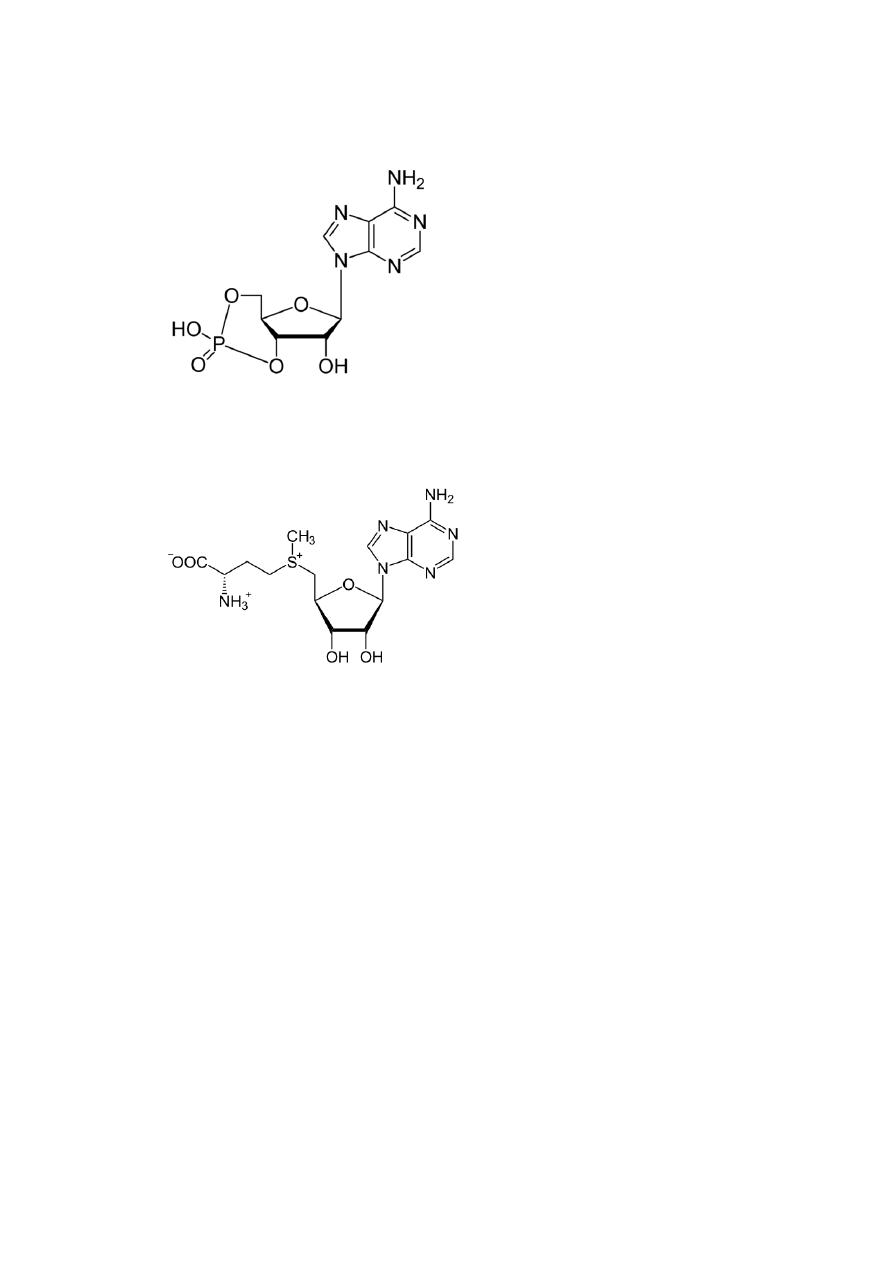
Wzory i role cAMP oraz s-adenozylometioniny
cAMP
-rola cAMP: drugorzędowy przekaźnik, bierze udział w wielu funkcjach regulatorowych w
komórce(np. regulacja cAMP-zależnych kinaz białkowych), do poprawnego funkcjonowania
wystarczy b. małe stężenie w kom. (1nmol/l).
S-Adenozynometionina
-rola: aktywna forma metioniny, dawca grup metylowych w reakcji metylacji, źródło
propyloaminy do syntezy poliamin.
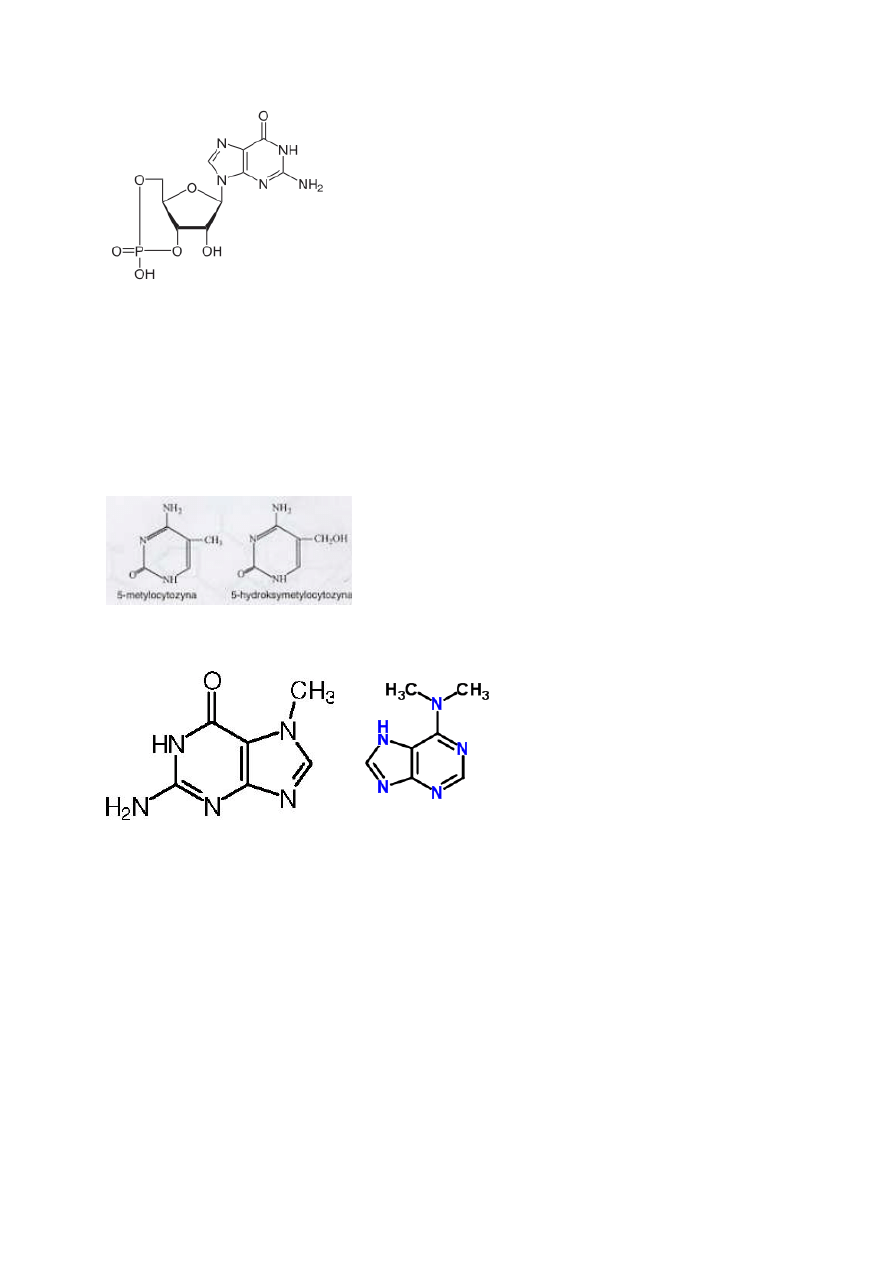
12. Cykliczny GMP
(cGMP: guanozyno-3’,5’-monofosforan) (Harper ’06 – 468)
powstaje z GTP przez cyklazę guanylową (reakcja analogiczna do r. katalizowanej przez
cyklazę adenylową; obie cyklazy regulowane przez efektory obejmujące hormony)
wewnątrzkomórkowy sygnał, wtórny przekaźnik (messenger) (np. NO ze śródbłonka [czynnik
relaksacyjny] zwiększenie stężenia cGMP [drugi przekaźnik] procesy charakterystyczne
dla rozluźnienia mięśni gładkich)
może działać antagonistycznie do cAMP
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
8
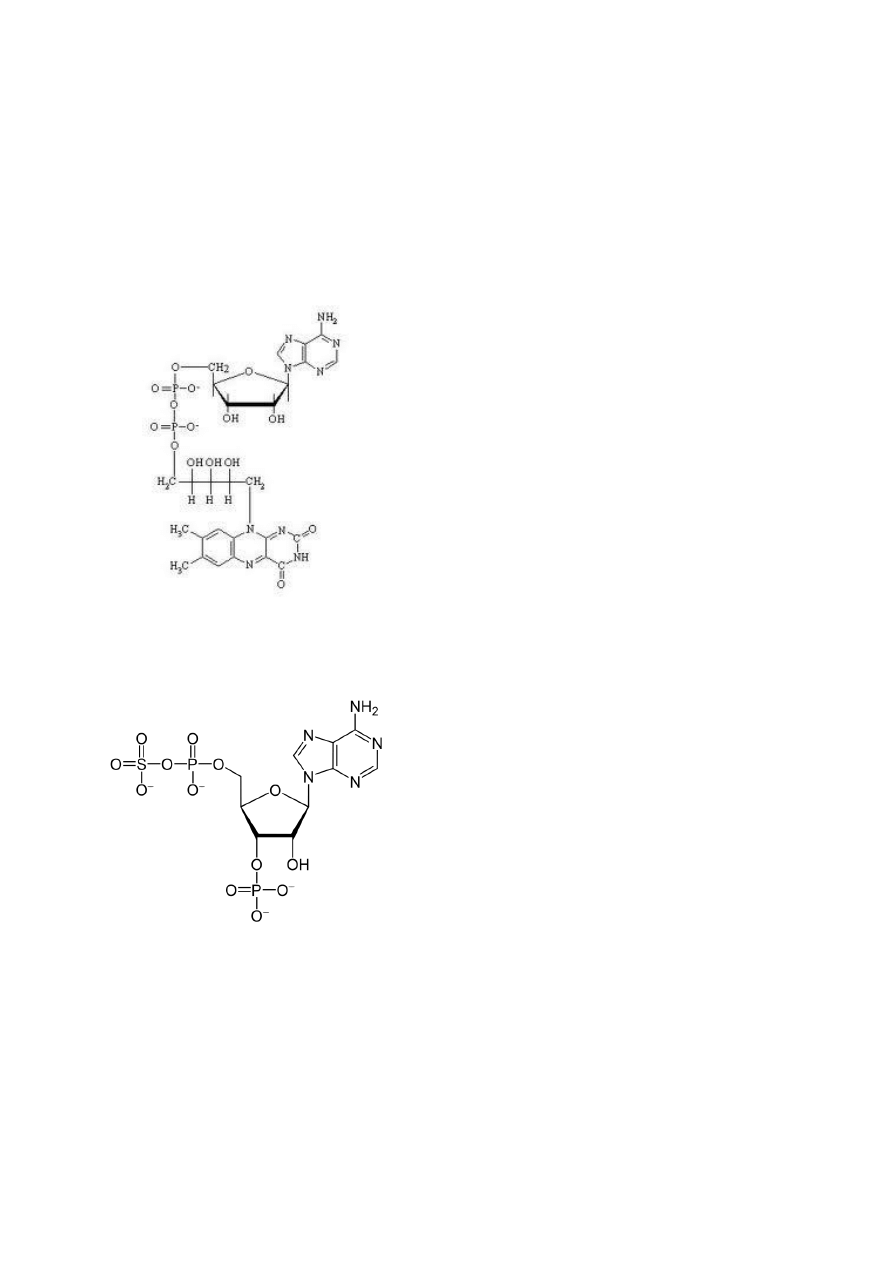
13. Rzadkie zasady
(w stosunkowo małych ilościach, oprócz głównych zasad, są w DNA i RNA
pro- i eucaryotów; szeroko rozpowszechnione w przyrodzie – mylące synonimy „podrzędne”,
„niezwykłe”)
w DNA i RNA – ważne funkcje w procesie rozpoznawania oligonukleotydów (np. odróżnienie
własnych od wirusowych i bakteryjnych)
w RNA – regulowanie długości życia cząsteczek
PIRYMIDYNY
PURYNY
N
7
-metyloguanina N
6
,N
6
-dimetyloadenina
14.
Histony – klasa, właściwości, rola
Histony – małe, zasadowe białka wchodzące w skład chromatyny, najbardziej obfite białka
chromatyny; są nieco heterogenne, składają się z wielu blisko spokrewnionych białek.
Wyróżniamy 5 klas histonów:
H1 – najbardziej zasadowy i największy z histonów, wiąże się z DNA gdy ten wchodzi i
wychodzi z rdzenia nukleosomu
H2A; H2B } bogate w lizynę
H3; H4 } bogate w argininę, ściśle konserwatywne ewolucyjnie
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
9
Ułożone kolejno histony H2A – H2B – H4 – H3 – H3 – H4 – H2B – H2A tworzą rdzeń nukleosomu.
15.
Narysuj i podaj funkcje pochodnej witaminy B2 o budowie nukleotydowej i PAPS.
Chodzi o :
Dinukleotyd flawinoadeninowy
(FAD – forma utleniona, FADH
2
– forma
zredukowana) – jest aktywną postacią ryboflawiny, powstaje w wyniku reakcji FMN z ATP,
stanowi grupę prostetyczną enzymów oksydoredukcyjnych –> flawoprotein, pełni funkcję
przenośnika elektronów i protonów.
(wzór zgodny w 100% z Harperem 1994)
PAPS (3’-fosforano-5’-fosfosiarczan adenozyny)
– donor grup siarczanowych dla
proteoglikanów.
16.
Narysować wzór nukleotydu zawierającego nikotynamid i wpisać jego pełną nazwę

BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
10
NAD+ – dinukleotyd nikotynamido-adeninowy ( -OR = -OH )
NADP+ - fosforan dinukleotydu nikotynamido-adeninowego (-OR = -H
2
PO
4
)
17.
Fragment DNA przepisać na RNA
nić DNA
kodująca
5’-…ACGT…-3’
matrycowa
3’-…TGCA…-5’
Transkrypt RNA
5’-…ACGU…-3’
Transkrypt jest komplementarny do nici matrycowej (która jest odwrotnej polarności) i ma taką samą
sekwencję (po zamianie T na U) i polarność jak nić kodująca.
18. Rodzaje RNA:
informacyjne lub matrycowe RNA (mRNA) – produkt transkrypcji DNA, matryca do translacji
rybosomów
rybosomalne RNA (rRNA) – buduje podjednostki większe i mniejsze rybosomów,
transferowe RNA (tRNA) – transportuje określone aminokwasy na rybosom w procesie
transalcji, w obrębie tRNA występuje antykodon komplementarny do kodonu mRNA, miejsce
wiązania aminokwasu, ramię rybotymidowe do wiązania z rybosomem,
heterogenne jądrowe RNA (hnRNA lub pre-mRNA) – głównie produkty transkrypcji DNA i
przetwarzania surowego transkryptu do mRNA, zawiera sekwencje kodujące – egzony oraz
niekodujące – introny,
antysensowne RNA albo interferencyjne RNA (siRNA i miRNA) – produkowane w celu
precyzyjnej regulacji ekspresji genów kodujących białka (za pomocą mechanizmu wspólnego lub
bardzo zbliżonego do systemu zwalczania wirusów RNA)
małe cytoplazmatyczne RNA (scRNA) – odpowiedzialne za rozpoznawanie sygnału w
komórce,
małe jądrowe RNA (snRNA) – pełniące funkcje enzymatyczne przy wycinaniu intronów z tran
skryptów (splicing),
małe jąderkowe RNA (snoRNA) – biorące udział w modyfikacji chemicznej pre-mRNA.
BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
11
19. Enzymy restrykcyjne
– (restryktazy, endonukleazy restrykcyjne) – enzymy bakteryjne
rozpoznające i hydrolizujące DNA w określonych miejscach. Są zaangażowane w obronę komórki
bakteryjnej przed wirusami.
Enzymy te rozpoznają określony odcinek łańcucha DNA i hydrolizują wiązania fosfodiestrowe w
obrębie tzw. sekwencji restrykcyjnych – są to krótkie (najczęściej 4-8 par zasad), palindromowe
fragmenty (sekwencja zasad w jednej nici DNA jest taka sama jak odczytywana wspak sekwencja nici
komplementarnej). Produkty hydrolizy mogą mieć zakończenia w postaci tzw. lepkich końców
(miejsce przecięcia w obrębie jednej nici DNA jest przesunięte w stosunku do miejsca cięcia w drugiej
nici) lub tępych końców (miejsce cięcia występuje w obu niciach na tym samym poziomie).
Zastosowanie w biologii molekularnej i diagnostyce np.:
Tworzenie map restrykcyjnych cząsteczek DNA,
Analiza fragmentów restrykcyjnych w celu zdiagnozowania choroby genetycznej lub
wirusowej po zastosowaniu metody hybrydyzacji,
Wprowadzanie transgenów do wektorów w celu transfekcji lub transdukcji.
20.
Wiązania A-T i C-G
1) konfiguracja przestrzenna helisy DNA (rotacja wiązania fosfodiestrowego + ułożenie zasad
purynowych względem deoksyrybozy) powodują, że A łączy się tylko z T, a C tylko z G.
2) W cząsteczce DNA liczba A = liczbie T, liczba C = liczbie G.
3) Wiązanie A z T jest podwójne (wodorowe), a C-G jest potrójne, silniejsze o 50%.
4) DNA tym bardziej odporne na denaturację, im więcej par C-G.
21. Struktura nukleosomu
1) nukleosom składa się z oktameru histonowego i z odcinka DNA (146 par zasad, 1,75 skrętu wokół
białkowego rdzenia).
2) Oktamer histonowy: (H2A-H2B) - (H3 - H4)2 - (H2A - H2B)

BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
12
3) Najważniejszy dla właściwości nukleosomu jest tetramer (H3 - H4)2 w centrum.
4) Pomiędzy nukleosomami – odcinek 30 par zasad.
5) Tworzenie nukleosomów jest wspomagane przez białko – nukleoplazminę.
6) Nukleosom chroni DNA przed działaniem nukleaz.
22. Wiązania w RNA:
- wiązania 3',5'-fosfodiestrowe między nukleotydami
- wiązania N-glikozydowe między resztami rybozylowymi i zasadami azotowymi
- wiązania wodorowe w strukturze II - rzędowej przy wewnątrzcząstkowym parowaniu zasad (3
między C i G oraz 2 między A i U)
23. Wzór DNA
- patrz pkt. 20
24. Co to jest Tm – definicja i od czego zależy
Tm – temperatura topnienia, temperatura w której połowa cząsteczek DNA uległa denaturyzacji.
(Poniżej Tm następuje renaturyzacja). Zależy od składy zasad DNA i od stężenia soli w roztworze.
GC (3 wiązania wodorowe) topią się w wyższej temperaturze niż AT (2 wiązania wodorowe)
10 krotne stężenie kationów jednowartościowych zwiększenie wartości Tm o 16,6°C
Formamid zmniejsza Tm przez destabilizację wiązań wodorowych.
25. Narysuj wykres DNA, gdy zawartość GC = 40%/70%
40% narysowane wystarczy walnąć komplementarną, a co do 70 % to analogicznie ;) P.S. Ciachnęło
tlen w ostatniej cytozynie.
26.
Denaturacja DNA
– separacja podwójnej nici DNA na dwie pojedyncze nici wskutek
zerwania więzi wodorowych pomiędzy nićmi; dwuniciowa helisa DNA jest stabilizowana przez
wiązania wodorowe między zasadami oraz solwatację – cząsteczki wody wytwarzają powłokę
dookoła cząsteczki , to właśnie te wiązania i oddziaływania trzeba przezwyciężyć, by doprowadzić do

BIOCHEMIA wejście kwasy nukleinowe – opracowanie
© gr. 3 WL I 2011-2017
13
denaturacji; dwie nici DNA ulegają wyraźnemu rozdzieleniu po inkubacji w roztworach o pH>12 i
pH<2, ze względu na jonizację zasad, przy bardzo wysokim lub niskim pH powłoka hydratacyjna
otaczająca cząsteczkę DNA ulega zaburzeniu, powodując destabilizację nakładania się par zasad,
traktowanie DNA kwasem prowadzi do depurynacji i depirymidyzacji – utraty zasad przez trawienie
wiązania glikozydowego, wiązanie fosfodiestrowe w miejscach pozbawionych zasad staje się bardziej
podatne na hydrolizę, wobec tego silne kwasy wywołują degradację DNA, ze względu na to, że
pojedyncze nici DNA są stosunkowo stabilne w środowisku alkalicznym, denaturację przeprowadza
się zazwyczaj właśnie w takich warunkach; wzrost temperatury DNA powoduje destabilizację
podwójnej helisy, ciepło zaburza zarówno wiązania wodorowe, jak i powłokę hydratacyjną,
prowadząc do zmniejszenia sił utrzymujących obie nici razem; temperaturę, w której 50% składu
próbki DNA ulega denaturacji, nazywa się temperaturą topnienia lub temperaturą mięknięcia DNA.
Renaturacja DNA
– szybkie ochłodzenie zdenaturowanej pod wpływem wysokiej temperatury
próbki DNA prowadzi do powstania nieuporządkowanej struktury, dlatego tylko powolne ochładzanie
umożliwia łączenie komplementarnych obszarów.
27. Struktury DNA:
a) jednoniciowy DNA inaczej ssDNA
b) dwuniciowy DNA w formach: A-DNA, B-DNA, C-DNA, E-DNA, H-DNA,P-DNA, Z-DNA – postaci
te odróżniają liczba par zasad, które zajmują każdy zwój, kąt między każdą par zasad,
średnica heliksu, kierunek skrętu
c) trójniciowy DNA
d) czteroniciowy DNA
B- DNA
– dominująca postać w warunkach fizjologicznych kierunek skrętu – prawy, wielkość skoku
na każdy zwój 3,4 nm, w obrębie zwoju jest 10 par zasad, średnica helisy wynosi ok. 2 nm.
28. Hydroliza enzymatyczna RNA
Rybonukleazy:
mogą występować endo i egzonukleazy.
enzymy trawienne soku trzustkowego
29. Efekt hiperchromowy
– zjawisko polegające na wzroście absorbancji DNA (lub RNA)
poddanego hydrolizie chemicznej lub enzymatycznej o 20-30% w stosunku do jego formy natywnej.
Jest to związane z tym, że w postaci natywnej uporządkowana struktura łańcuchów
polinukleotydowych i zwarte ułożenie w nich poszczególnych nukleotydów maskuje część grup
chromoforowych. Wzrost absorbancji wywołuje również ogrzewanie, które powodując denaturacje
zaburza strukturę cząsteczki.
Efekt hipochromowy
– obniżenie pochłaniania promieniowania nadfioletowego, wywołane
renaturacją cząsteczki DNA(lub RNA) poprzez obniżenie temp., co powoduje odtworzenie struktury.
Tak więc, natywne DNA/ RNA wykazuje ok. 25-35% niższa absorbancje w porównaniu z absorbancją
wszystkich składowych nukleotydów.
Wyjaśnienie: Kwasy nukleinowe maja zdolność pochłaniania światła nadfioletowego w zakresie fal
220-300nm, dzięki występującym w nich zasadom purynowym i pirymidynowym, w których są
sprzężone wiązania podwójne.
Wyszukiwarka
Podobne podstrony:
Biochemia wej cie kwasy nukleinowe opracowanie
kwasy nukleinowe opracowanie
Wersja A-TEST, Analityka semestr IV, Biochemia, tłuszcze kwasy nukleinowe
biochemia kolo III, Analityka semestr IV, Biochemia, tłuszcze kwasy nukleinowe
pkt1 kwasy nukleinowe-biochemia, Biochemia, Zagadnienia na kolokwia
pkt.4-kwasy nukleinowe- biochemia, Biochemia, Zagadnienia na kolokwia
Biochemia Wykład VII 9 01 15 r Kwasy nukleinowe, DNA, RNA
biochenia kwasy nukleinowe
pkt.5-kwasy nukleinowe-biochemia, Biochemia, Zagadnienia na kolokwia
KWASY NUKLEINOWE, Ogrodnictwo UP Lbn, Biochemia, kwasy nukl
pkt.6-kwasy nukleinowe-biochemia, Biochemia, Zagadnienia na kolokwia
(3969) kwasy nukleinowe, Prywatne, biochemia, biochemia 1, biochemia, biochemia
sciąga kwasy nukleidowe kolos 3, Zootechnika, Biochemia
Kolokwium 3 - Kwasy nukleinowe, Zootechnika, Biochemia
Kwasy nukleinowe sprawozdanie, Ochrona środowiska, Biochemia
biochem kwasy nukleinowe, BIOCHEMIA
pkt2 kwasy nukleinowe-biochemia, Biochemia, Zagadnienia na kolokwia
sprawko biochemia kwasy nukleinowe, Biochemia, BIOCHEMIA Z DC++
więcej podobnych podstron