
Określenie stopnia
zaawansowania klinicznego
raka jelita grubego
Piotr Narbutt
Klinika Chirurgii Ogólnej i Kolorektalnej UM w
Łodzi
Kierownik Kliniki: Prof. dr hab. n. med. Adam
Dziki

Rak jelita grubego
II miejsce pod względem
częstości wśród nowotworów
złośliwych u obu płci

Rak jelita grubego
Standaryzowany współczynnik zachorowalności
na 100 000 mieszkańców:
Mężczyźni:
Okrężnica 12,4
Odbytnica 9,6
Kobiety
Okrężnica 8,7
Odbytnica 5,6

Rak jelita grubego
Standaryzowany współczynnik umieralności
na 100 000 mieszkańców:
Mężczyźni:
Okrężnica 11,1
Odbytnica 4,7
Kobiety
Okrężnica 7,0
Odbytnica 2,7

Rak jelita grubego
Przeżycie 5. letnie w Polsce:
Okrężnica 30,8-32,4%
Odbytnica24-33,2%
Kraje Europy zachodniej ok. 50%

Rak jelita grubego
Ryzyko zachorowania rośnie
po 50 r. ż., a szczyt
zapadalności
to 8. dekada życia

Przyczyny raka jelita grubego
Rak sporadyczny 65 – 85%
Rak występujący rodzinnie 10-30%
Dziedziczny rak bez polipowatości HNPCC 1-
5%
FAP 0,5%
Inne zespoły polipowatości (Peutz-Jegersa,
polipowatości młodzieńczej) 0,5%

HNPCC zespół Lynch
Dziedziczenie w sposób autosomalny
dominujący
Mutacja w obrębie genów naprawy
( MLH1, MSH2, MSH6)
Zwiększone ryzyko występowania innych
nowotworów – trzonu macicy, żołądka,
jajnika, dróg moczowych, jelita cienkiego

HNPCC zespół Lynch
Kryteria Amsterdamskie
Co najmniej 3 krewnych nowotwory HNPCC
(rak j. grubego, bł. śl. trzonu macicy, j.
cienkiego, moczowodu miedniczki nerkowej)
Jedna z osób jest krewnym I st dla pozostałych
Zachorowania w dwóch kolejnych pokoleniach
Przynajmniej jedno zachorowanie przed 50 r. ż.
U chorych wykluczono FAP
Zachorowanie na raka potwierdzono badaniem
hist. pat.

HNPCC zespół Lynch
Kryteria Amsterdamskie
Co najmniej 3 krewnych nowotwory HNPCC
(rak j. grubego, bł. śl. trzonu macicy, j.
cienkiego, moczowodu miedniczki nerkowej)
Jedna z osób jest krewnym I st dla pozostałych
Zachorowania w dwóch kolejnych pokoleniach
Przynajmniej jedno zachorowanie przed 50 r. ż.
U chorych wykluczono FAP
Zachorowanie na raka potwierdzono badaniem
hist. pat.

Wytyczne Bethesda
RJG rozpoznany przed 50 r. ż.
2 zachorowania na nowotwory ze spektrum Lynch,
łącznie
z guzami synchronicznymi i metachronicznymi u tej
samej osoby niezależnie od wieku
Chorzy na RJG z krewnym I stopnia, który zachorował
na RJG lub inny ze spektrum Lynch przed 50 r.ż.
RJG rozpoznany u 2 lub więcej krewnych 1 lub 2 stopnia
z nowotworem ze spektrum Lynch niezależnie od wieku
RJG z MSI high w histopatologii guza u osoby przed 60
r. ż.

Badania zalecane u członków rodzin
z zespołem Lynch
Wiek
Zalecane badania
20-25 lat
Kolonoskopia co 12-24
miesiące
Od 30 r. ż.
Gastroskopia co 2 lata
Od 25 r. ż.
USG ginekologiczne
u kobiet co rok

FAP
zespół rodzinnej gruczolakowatej
polipowatości
Mutacja genu supresorowego APC
Autosomalny dominujący
Ryzyko rozwoju raka jelita grubego 100%
U nosicieli mutacji badania endoskopowe
od lat młodzieńczych 12-14 r. ż.
Kolektomia\ proktokolektomia odtwórcza

Określenie stopnia zaawansowania
klinicznego raka jelita grubego opiera
się na klasyfikacji TNM

Klasyfikacja TNM
T Guz pierwotny
Tx
T0
Tis
T1
T2
T3
T4
Nie można ocenić guza pierwotnego
Nie stwierdza się guza pierwotnego
Ca in situ- komórki raka widoczne w nabłonku, naciek nie
przekracza błony mięśniowej błony śluzowej (muscularis
mucosae)
Guz nacieka błonę podśluzową
Guz nacieka warstwę mięśniową właściwą
Guz nacieka przez warstwę mięśniową do warstwy
podsurowiczej lub niepokrytych otrzewną warstw
okołokrężniczych lub okołodbytniczych
Guz nacieka przez ciągłość inne narządy i/lub przerasta
otrzewną trzewną
N okoliczne węzły
chłonne
NX
N0
N1
N2
Nie można ocenić okolicznych węzłów chłonnych
Regionalne węzły chłonne bez przerzutów
Przerzuty nowotworu w 1-3 węzłach chłonnych
Przerzuty w 4 i więcej regionalnych węzłach chłonnych
M przerzuty
odległe
MX
M0
M1
Nie można ocenić występowania przerzutów odległych
Nie stwierdza się przerzutów odległych
Obecne przerzuty odległe

Zalety skali TNM
Duża powtarzalność ze względu na ścisłe
definicje cech guza, węzłów chłonnych
i przerzutów
Łączy w sobie informacje dotyczące
zaawansowania klinicznego oraz
patomorfologicznego
Precyzyjna dla lekarzy różnych specjalności
ze względu na ujednolicone mianownictwo

Stopień zaawansowania klinicznego określany
na podstawie klasyfikacji TNM
Stopień 0
Tis N0 M0
Stopień I
T1 N0 M0
T2 N0 M0
Stopień II
T3 N0 M0
T4 N0 M0
Stopień III
Każdy T N1 M0
Każdy T N2 M0
Stopień IV
Każdy T Każdy N M1

Cel określenia zaawansowania
klinicznego
Określenie rokowania dla chorego z chorobą
nowotworową
Zaplanowanie prawidłowej strategii leczenia
Uniknięcie zbyt radykalnego leczenia w
przypadku raka wczesnego
Optymalne leczenie w przypadku raka
zaawansowanego

Postępowanie w guzach odbytnicy w zależności
od głębokości naciekania guza
T0/T1 Miejscowe wycięcie
(TEM)
T2 TME\PME
T3 Pre TME: 5 x 5.5 Gy
T4 Terapia
neoadjuwantowa

Postępowanie w guzach odbytnicy
w zależności od stopnia zaawansowania
klinicznego
Stopień 0
Miejscowe wycięcie
(TEM)
Stopień I, II, III
LAR\APR
Stopień IV
operacje paliatywne
LAR\APR\kolostomia lub radykalne
– radykalne leczenie zmian
przerzutowych

Postępowanie w guzach okrężnicy i zagięcia esiczo
odbytniczego w zależności od stopnia zaawansowania
klinicznego
Stopień 0
wycięcie endoskopowe
Stopień I, II, III
resekcja przednia, resekcja
esicy, hemikolektomia prawostronna,
lewostronna
Stopień IV
operacje paliatywne zespolenie
omijające, kolostomia lub ileostomia,
resekcja paliatywna
radykalne – usunięcie zmian przerzutowych

Metody diagnostyczne wykorzystywane
w ocenie zaawansowania klinicznego
USG jamy brzusznej
CT jamy brzusznej i miednicy mniejszej
RTG/CT klatki piersiowej
USG transrektalne
Oznaczenie CEA antygenu
karcynoembrionalnego
PET pozytronowa tomografia emisyjna
MRI cewką endorektalną

USG jamy brzusznej
Pozwala na wykrycie zmian przerzutowych
w wątrobie przestrzeni zaotrzewnowej,
powiększonych węzłów chłonnych krezki
i okolicy guza
Czułość badania dla zmian przerzutowych
w wątrobie 85-87%

USG jamy brzusznej
USG jamy brzusznej nie odgrywa roli
w ocenie zawansowania miejscowego
guza
Ma jedynie wartość diagnostyczną
– uwidocznienie zmiany

CT jamy brzusznej
Wykrywanie zmian podobnie jak w USG
Czułość dla zmian w wątrobie 89%
Połączenie badania USG i CT jamy brzusznej
podnosi czułość do 96% w przypadku zmian
przerzutowych w wątrobie
Wskazane szczególnie u chorych z wysokim
poziomem CEA (>20ng/ml), u których nie
stwierdzono zmian ogniskowych w badaniu
USG

CT jamy brzusznej
Wykazuje wysoką czułość w ocenie
naciekania guza na sąsiadujące tkanki
- guzy T4

CEA-
antygen karcynoembrionalny
Nie jest badaniem określającym stopień
zawansowania według kryteriów TNM
Ale
Istnieje korelacja między stężeniem CEA
w surowicy a stopniem zaawansowania choroby
Test Abbotta CEA> 20ng/ml duże
prawdopodobieństwo przerzutów do wątroby
Czułość badania 50-60%
Swoistość 80-90%
Jest przydatnym badaniem w monitorowaniu
pooperacyjnym

USG transrektalne
Jest obecnie uznaną metodą
diagnostyczną w ocenie miejscowego
zawansowania guzów odbytnicy oraz
regionalnych węzłów chłonnych
Charakteryzuje się wysoką czułością
i swoistością potwierdzoną wieloma
badaniami

Dokładność USG transrektalnego
w ocenie głębokości naciekania guza
odbytnicy
Autor
Rok
Czułość
Swoistość
Akasu
1990
97%
93%
Jochem
1990
92%
76%
Sailer
1997
81%
98%
Kim
2000
83%
96%
Santoro
2001
82%
93%

Dokładność USG transrektalnego
w ocenie głębokości naciekania guza
odbytnicy
USG transrektalne jest szczególnie
przydatne w ocenie guzów o niskim
stopniu zaawansowania - T1, T2 i w
przypadku tych guzów wykazuje większą
swoistość od CT
i MRI
Kim NK i wsp. Comparative study of transrectal ultrasonography,
pelvic computerized tomography and magnetic resonance imaging
in preoperative staging of rectal cancer. Dis Colon Rectum
1999;42:770-5
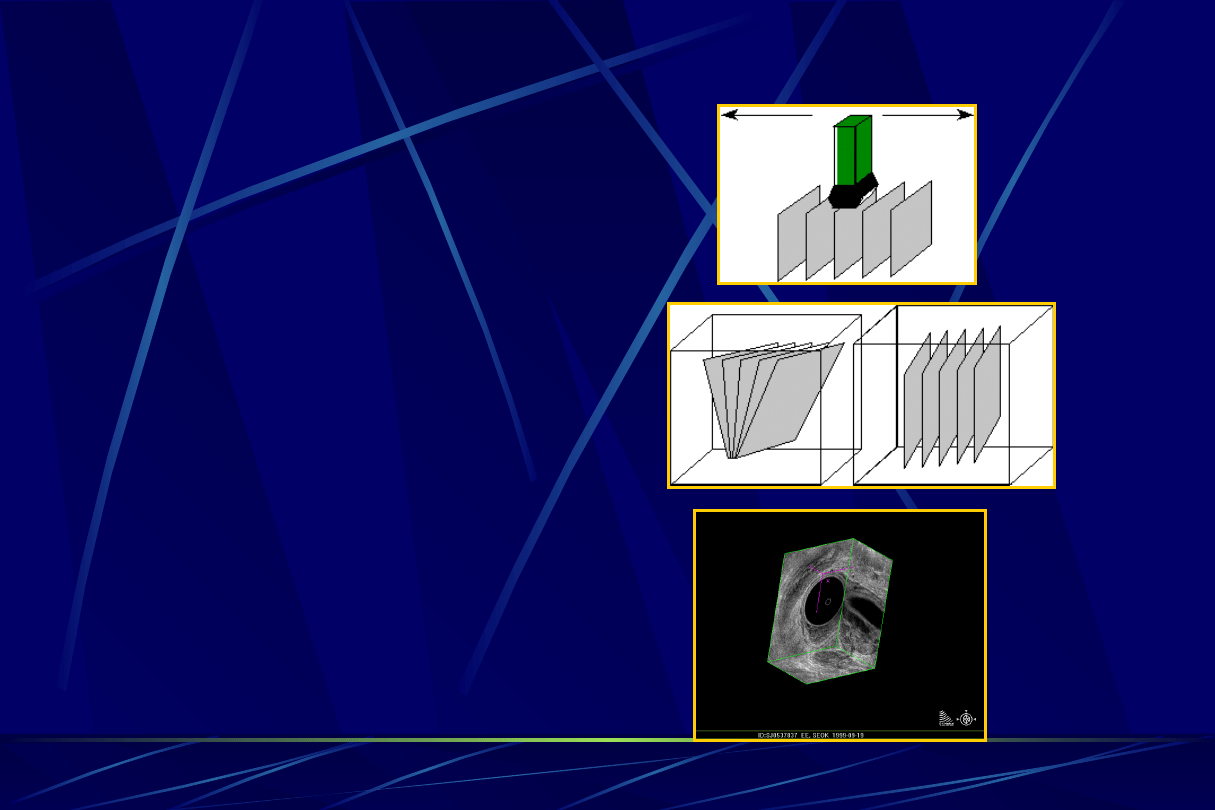
Obrazowanie 3D
Skanowanie
Przesuwająca się sonda
wykonuje szereg
równoległych skanów 2-D
Rekonstrukcja
W czasie rzeczywistym
obrazy 2-D przetwarzane
są na 3-D Jednocześnie
korekcja zniekształceń
geomertycznych
Wizualizacja
Zbudowany obraz w
postaci bryły dający się
dowolnie obrabiać

Zalety obrazowania 3D
Możliwość oceny guza i sąsiednich
struktur
w różnych płaszczyznach
Możliwość dokładnej oceny zmiany jej
wielkości i lokalizacji
Znaczne ułatwienie oceny dla badającego
Komputerowa akwizycja i archiwizacja
pozwala na wielokrotną analizę zmiany

Porównanie USG 2D z 3D
N=33
3D EUS
2D EUS
T1
91%
85%
T2
85%
76%
N
85%
67%
Kim JC, Cho YK, Kim SY
,
Park SK, Lee MG. Comparative study of three-dimensional and conventional
endorectal ultrasonography used in rectal cancer staging. Surg Endosc. 2002 Sep;16(9):1280-5

Porównanie USG 2D z 3D
Nie wykazano przewagi 3D EUS nad 2D
EUS w ocenie guzów ani węzłów
chłonnych
Podkreślana jest natomiast dużo większą
łatwość oceny
Wykazana przewaga 3D EUS
w diagnozowaniu przetok
okołodbytniczych

Ocena regionalnych węzłów chłonnych
Dokładnoćś USG transrektalnego w
ocenie zajęcia regionalnych węzłów
chłonnych
73%-83%
Cechy zajęcia mieszana echostruktura
ogniska hypo i hyperechogeniczne
Hypoechogeniczność węzła
charakterystyczna dla zmian zapalnych

Ograniczenia USG transrektalnego
Dokładność badania zależna od doświadczenia
badającego – krzywa uczenia
Nie nadaje się do oceny guzów znacznie
zwężających światło odbytnicy i położonych
wysoko
Mało przydatne w bardzo niskich guzach – brak
obrazowania dźwigaczy odbytu
Nie obrazuje powięzi mezorektum
overstaging

Overstaging
Ze względu na często występujący odczyn
zapalny w okolicy guza (wcześniejsza biopsja)
może imitować to naciekanie głębszych
struktur niż są w rzeczywistości
Dotyczy w szczególności guzów T2
Guz w pobliżu zastawki Hustona lub zagięcia
odbytniczo odbytowego
Brak doświadczenia badającego
Częstość 10 -18%

MRI cewką doodbytniczą
Czułość i swoistość porównywalna z EUS 3D
Ze względu na wysokie koszty badania
używane obecnie tylko do badań klinicznych
Udowodniona przewaga w ocenie aparatu
zwieraczowego
PET – pozytronowa tomografia
emisyjna

PET – pozytronowa tomografia
emisyjna
Jest badaniem wykorzystującym
znajomość procesów metabolicznych
zachodzących
w tkance guza
F
18
deoksyglukoza –metabolit
wykorzystywany w diagnostyce zmian
nowotworowych

PET – pozytronowa tomografia
emisyjna
Nie jest przydatny w oznaczeniu
miejscowego zaawansowania guza i
regionalnych węzłów chłonnych ze względu
na zbyt niską rozdzielczość badania
Czułość badania w ocenie regionalnych
węzłów chłonnych
29%
Abdel-Nabi H, Doerr RJ, Lamonica DM, Cronin VR, Galantowicz PJ, Carbone GM, Spaulding MB.
Staging of primary colorectal carcinomas with fluorine-18 fluorodeoxyglucose whole-body PET:
correlation with histopathologic and CT findings. Radiology. 1998 Mar;206(3):755-60.

PET – pozytronowa tomografia
emisyjna
PET w wykrywaniu przerzutów
odległych charakteryzuje się bardzo
wysoką czułością
i specyficznością, która dla
zmian >
1cm
wynosi prawie
100%
Imdahl A, Reinhardt MJ, Nitzsche EU, Mix M, Dingeldey A, Einert A, Baier P, Farthmann EH.
Impact of 18F-FDG-positron emission tomography for decision making in colorectal cancer
recurrences. Langenbecks Arch Surg. 2000 Mar;385(2):129-34.

PET – pozytronowa tomografia
emisyjna
Pomimo tak dużej czułości i swoistości
nie może być jedynym badaniem
stosowanym w diagnostyce zmian
przerzutowych wątroby
u chorych planowanych do zabiegów
resekcyjnych bądź ablacyjnych
wykonywanych z intencją wyleczenia

PET – pozytronowa tomografia
emisyjna
W takim przypadku konieczne
połączenie z badaniem obrazowym –
CT, które określi wielkość zmiany, jej
położenie w stosunku do struktur
anatomicznych – dużych naczyń
i dróg żółciowych

PET – pozytronowa tomografia
emisyjna
Rozszerzenie diagnostyki o PET u chorych
planowanych do resekcji wątroby z powodu
przerzutów raka grubego zmniejsza liczbę
przeprowadzanych zabiegów o 10%15% w wyniku
innych zmian przerzutowych nierozpoznanych w CT
Huebner RH, Park KC, Shepherd JE, Schwimmer J, Czernin J, Phelps ME, Gambhir SS.
A meta-analysis of the literature for whole-body FDG PET
detection of recurrent colorectal cancer.J Nucl Med. 2000 Jul;41(7):1177-89
.

Podsumowanie
Dostępne obecnie środki diagnostyczne dają
duże możliwości prawidłowego określenia
stopnia zaawansowania klinicznego raka jelita
grubego
Pozwala to na zaplanowanie optymalnej
strategii leczenia
Rozsądne posługiwanie się nawet drogimi
metodami wpływa na poprawę wyników
leczenia nie zwiększając ogólnych kosztów
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
Wyszukiwarka
Podobne podstrony:
Badania przesiewowe w celu wykrycia raka jelita grubego
Histoklinika raka jelita grubego
03 0000 004 02 Leczenie raka jelita grubego irinotekanem
03 0000 005 02 Leczenie raka jelita grubego kapecytabina
Leczenie systemwe raka jelita grubego
Rola ekspresji receptorów hormonów płciowych, prostaglandyn i czynników angiogenezy w patogenezie ra
Molekularne podstawy czynników ryzyka raka jelita grubego
Rola mikroflory jelitowej i bakterii probiotycznych w profilaktyce i rozwoju raka jelita grubego
ONE ZABIJAJĄ RAKA JELITA GRUBEGO
Inhibitory aromatazy w leczeniu uzupełniającym raka piersi
prelekcja Choroby jelita grubego
Choroby zapalne jelita grubego
więcej podobnych podstron