
Gazy
Gazy

W XIX wieku sformułowano
prawa opisujące własności
gazów na podstawie szeregu
wyników eksperymentalnych.
Są to :
Prawo Boyle’a-Mariotte’a
Prawo Gay-Lussaca
Prawo Charlesa
Hipoteza Avogadro
Prawo Daltona
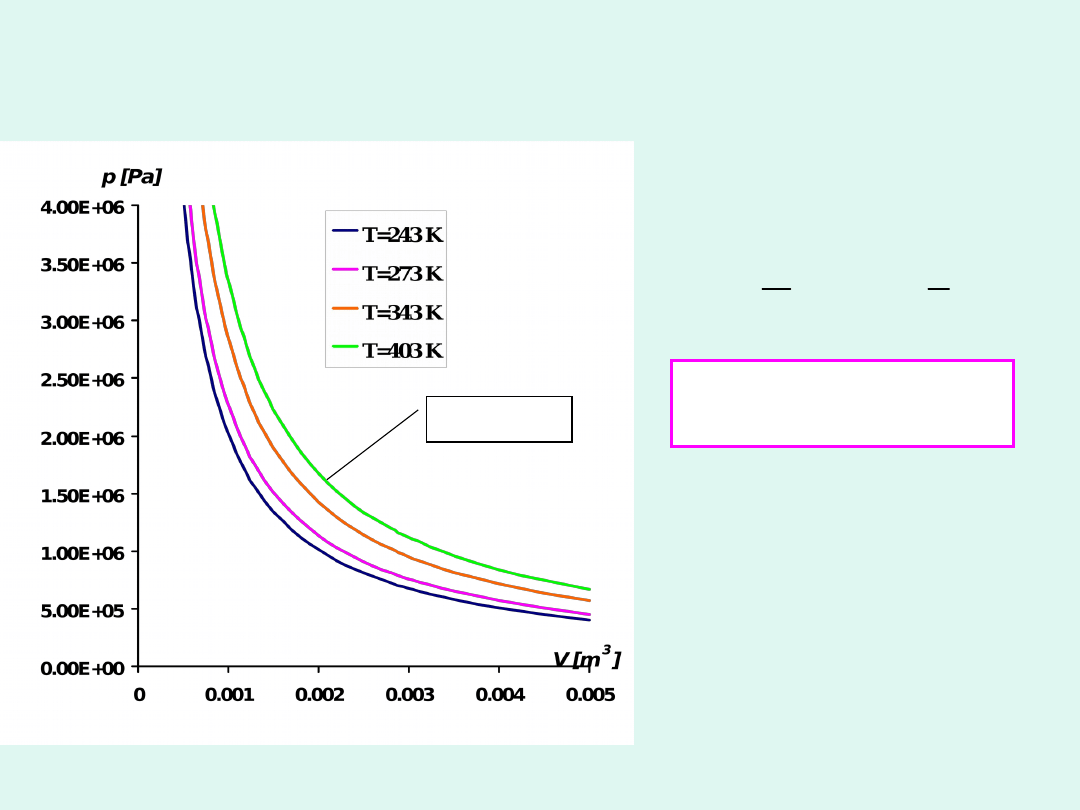
Prawo Boyle’a-Mariotte’a
p
1
V
lub
V
1
p
const
T
i
const
m
lub
const
n
const
pV
Dla pewnej stałej
ilości gazu w stałej
temperaturze
ciśnienie jest
odwrotnie
proporcjonalne do
objętości czyli iloczyn
ciśnienia i objętości
jest stały.
izoterm
a
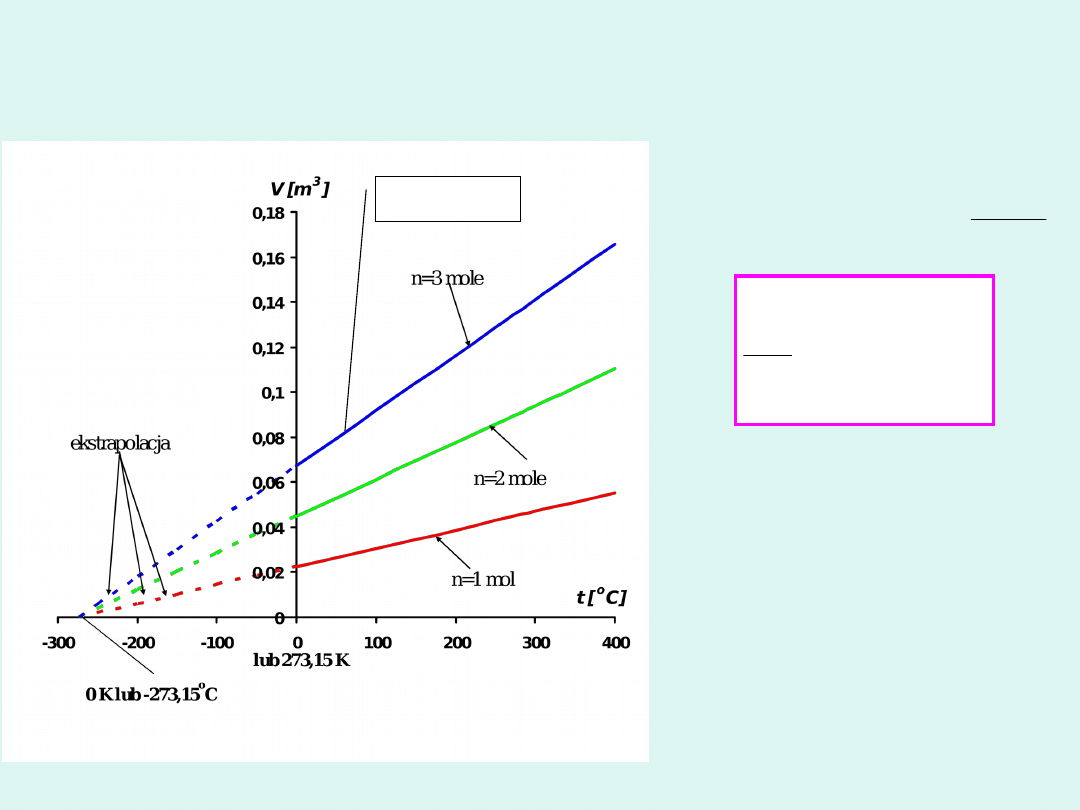
Prawo Gay-Lussaca
273,15
1
o
t
1
V
V
const
p
i
const
m
lub
const
n
const
T
V
Dla pewnej stałej
ilości gazu pod
stałym ciśnieniem
objętość jest wprost
proporcjonalna do
temperatury.
izobara
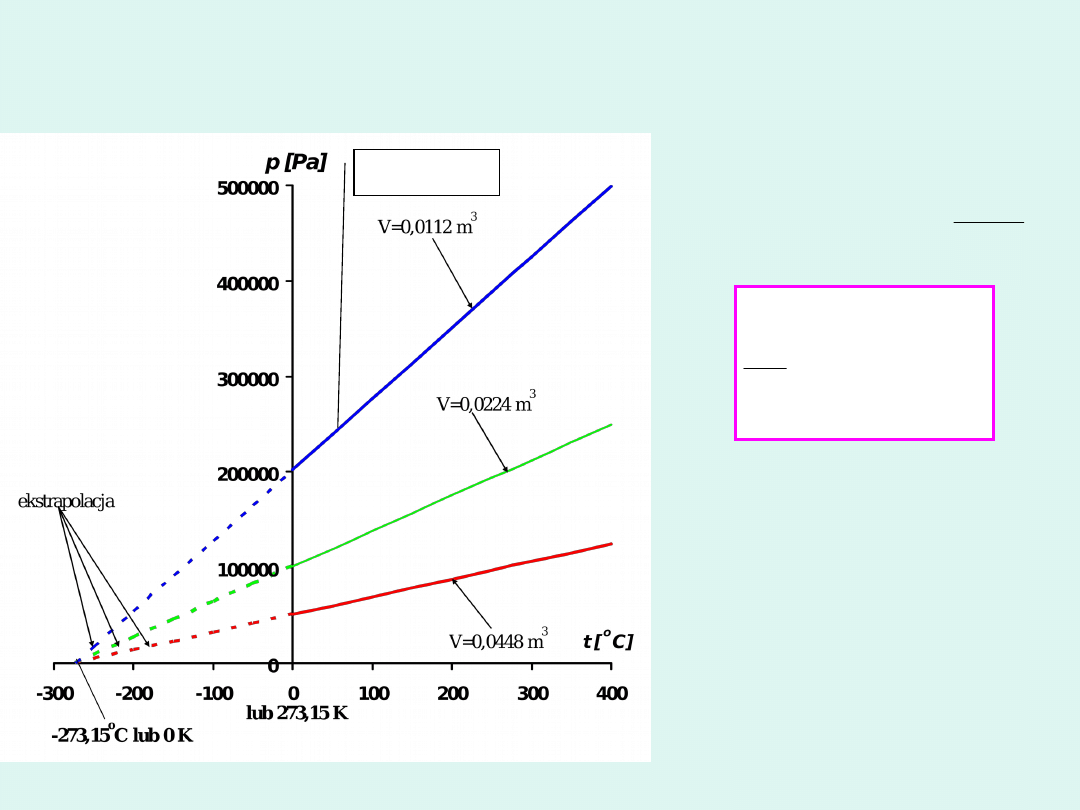
Prawo Charlesa
273,15
1
o
t
1
p
p
const
V
i
const
m
lub
const
n
const
T
p
izochor
a
Dla pewnej stałej
ilości gazu
znajdującej się w
stałej objętości
ciśnienie jest wprost
proporcjonalne do
temperatury.

Hipoteza Avogadro
Jeśli mamy różne gazy w tej
samej objętości i temperaturze
i pod tym samym ciśnieniem, to
zawierają one te same ilości
cząsteczek.
1 mol gazu zawiera liczbę
cząsteczek wyrażającą się
liczbą Avogadro.
1
23
A
mol
10
022
6
N
,

Równanie stanu gazu
doskonałego (Clapeyrona)
nRT
pV
p
– ciśnienie [Pa]
V
– objetość [m
3
]
n
– liczba moli [mol]
T
- temperatura w skali
bezwzględnej [K]
R
– stała gazowa
K
mol
J
314
8
R
,
15
273
C
t
K
T
,

Warunki normalne
t
o
= 0°C (T = 273,15 K)
p
o
= 1,013·10
5
Pa
Objętość 1 mola gazu w tych
warunkach
V
o
= 22,4·10
-3
m
3
/mol
K
mol
J
314
8
K
15
273
mol
m
10
22,4
Pa
10
013
1
T
V
p
R
3
3
-
5
o
o
o
,
,
,

Gaz, który spełnia
równanie Clapeyrona
nazywamy doskonałym.
Wszystkie gazy, z jakimi mamy do czynienia
są,
gazami
rzeczywistymi
i
wykazują
odchylenia od równania stanu doskonałego
(nie spełniają go).
Własności gazów rzeczywistych stają się
zbliżone do własności gazu doskonałego, gdy
ich ciśnienie dąży do zera.
Inaczej mówiąc im ciśnienie gazu niższe tym
lepiej spełnia on równanie Clapeyrona.

Prawo Daltona
i
i
i
i
i
i
i
x
n
n
P
p
n
n
V
nRT
P
V
RT
n
p
p
P
Prawo to dotyczy mieszanin
gazów.
Ciśnienie całkowite mieszaniny gazów jest sumą
ciśnień cząstkowych poszczególnych składników.
Ciśnienie cząstkowe danego składnika gazowego, to
ciśnienie jakie wywierałby, gdyby sam znajdował się
w danych warunkach.
Wniosek z prawa
Daltona
P
x
p
i
i
Teoria kinetyczno-
molekularna gazów –
model gazu doskonałego
Wymiary cząsteczek są znikomo
małe w porównaniu z
odległościami pomiędzy nimi.
Można traktować je jako punkty
materialne.
Cząsteczki są w ciągłym,
chaotycznym ruchu.
Cząsteczki nie oddziaływują na
siebie na odległość, jedynie
dochodzi do doskonale
elastycznych zderzeń.
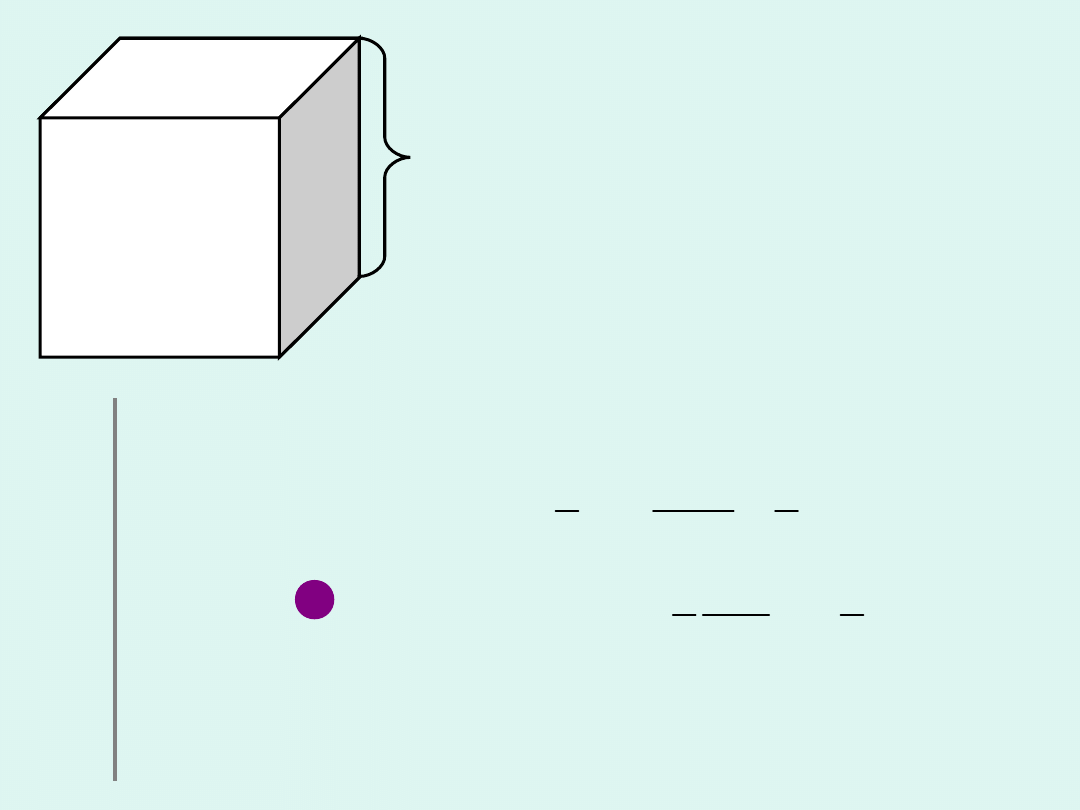
l
N
A
W sześcianie o boku
l
zamknięty jest
1 mol (N
A
)
cząsteczek, każda o masie
m
poruszająca się ze
średnią szybkością
v
.
Cząsteczki zderzając się ze
ścianami naczynia
przekazują im pęd,
wywierając na nie ciśnienie.
2
A
A kin
kin
B
A
2
mv
2
pV
N
N E
RT
3
2
3
3 R
3
E
T
k T
2N
2
=
=
=
=
=
Stała Boltzmanna
k
B
=
R/N
A
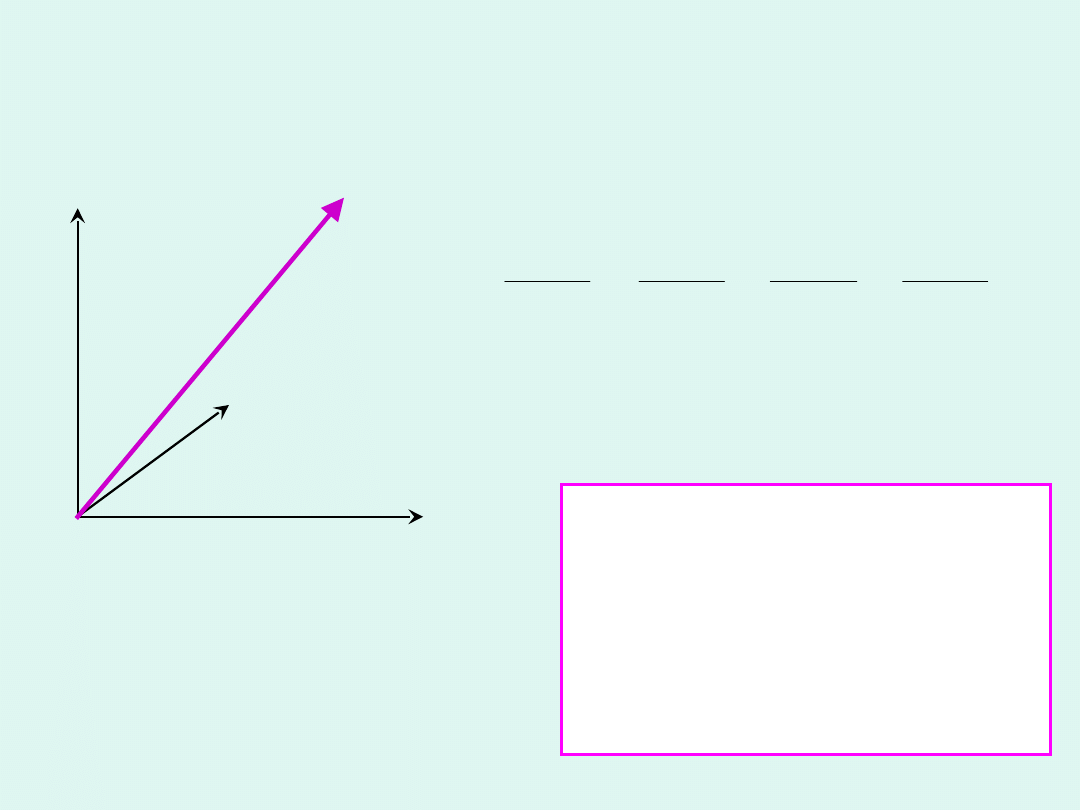
x,
v
x
z,
v
z
y,
v
y
v
Zasada ekwipartycji (równego
podziału) energii
z
,
kin
y
,
kin
x
,
kin
kin
2
z
2
y
2
x
2
z
y
x
E
E
E
E
2
mv
2
mv
2
mv
2
mv
v
v
v
v
Na każdy stopień
swobody ruchu
cząsteczki przypada
energia wynosząca
½k
B
T
.

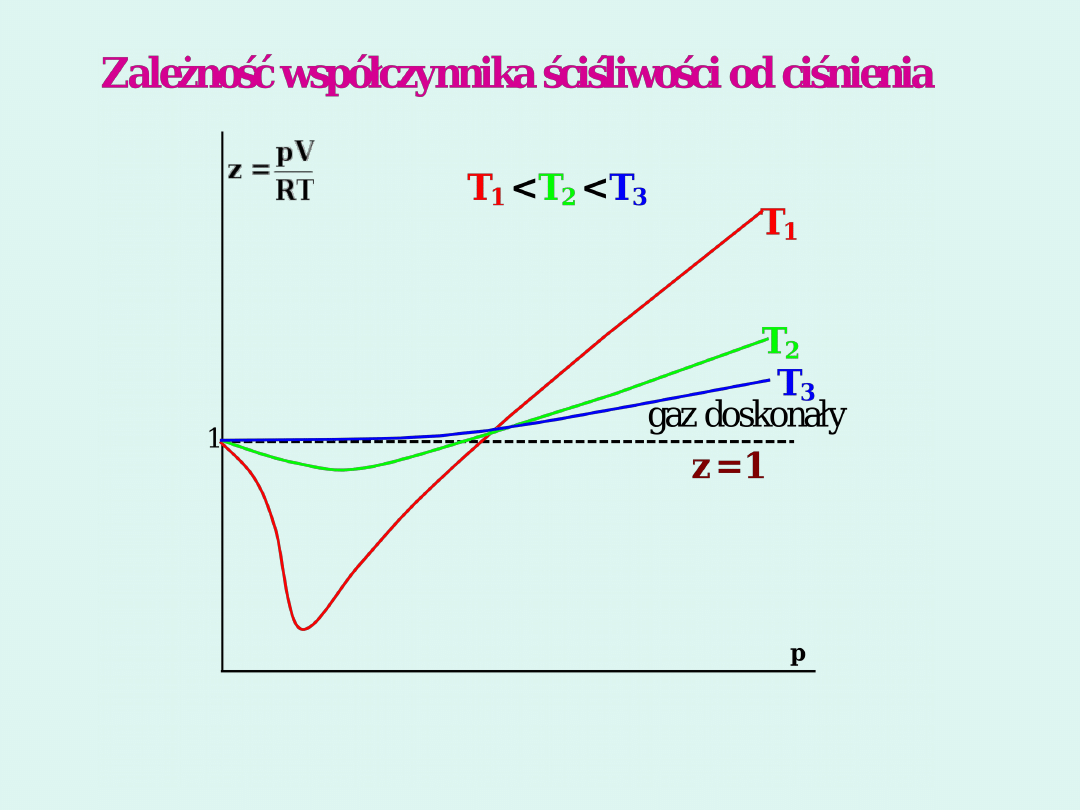
Gazy rzeczywiste
Wszystkie gazy są gazami rzeczywistymi. Nie
spełniają równania Clapeyrona.
nRT
z
pV
z
– współczynnik ściśliwości
Zależy od temperatury i ciśnienia. Dla gazu
doskonałego z = 1; dla gazu rzeczywistego
dąży do 1, gdy ciśnienie dąży do zera.

Gazy rzeczywiste
Do gazu rzeczywistego nie można zastosować modelu
opisującego gaz doskonały.
Cząsteczki gazu rzeczywistego posiadają pewną
objętość, której nie można zaniedbać.
Cząsteczki gazu rzeczywistego oddziaływają ze sobą
na odległość.
Oddziaływania międzycząsteczkowe mają charakter
odpychający i przyciągający. Gdy odległość pomiędzy
cząsteczkami jest niewielka i energia termiczna
cząsteczek jest też stosunkowo mała, zderzenia
pomiędzy nimi nie są elastyczne. Przeważają
oddziaływania przyciągające i cząsteczki „sklejają się”
z sobą, a gaz się skrapla.
Równanie
opisujące
gaz
rzeczywisty
musi
uwzględniać
objętość
własną
cząsteczek
i
oddziaływania
międzycząsteczkowe
(przyciąganie
cząsteczek).

Równanie van der Waalsa
RT
b
V
V
a
p
2
dla 1 mola
gazu
dla
n
moli
gazu
nRT
nb
V
V
an
p
2
2
a,b
– stałe charakterystyczne dla danego gazu,
niezależne od temperatury
a
– stała związana z oddziaływaniami
międzycząsteczkowymi (przyciąganiem)
b
- stała związana z objętością własną
cząsteczek
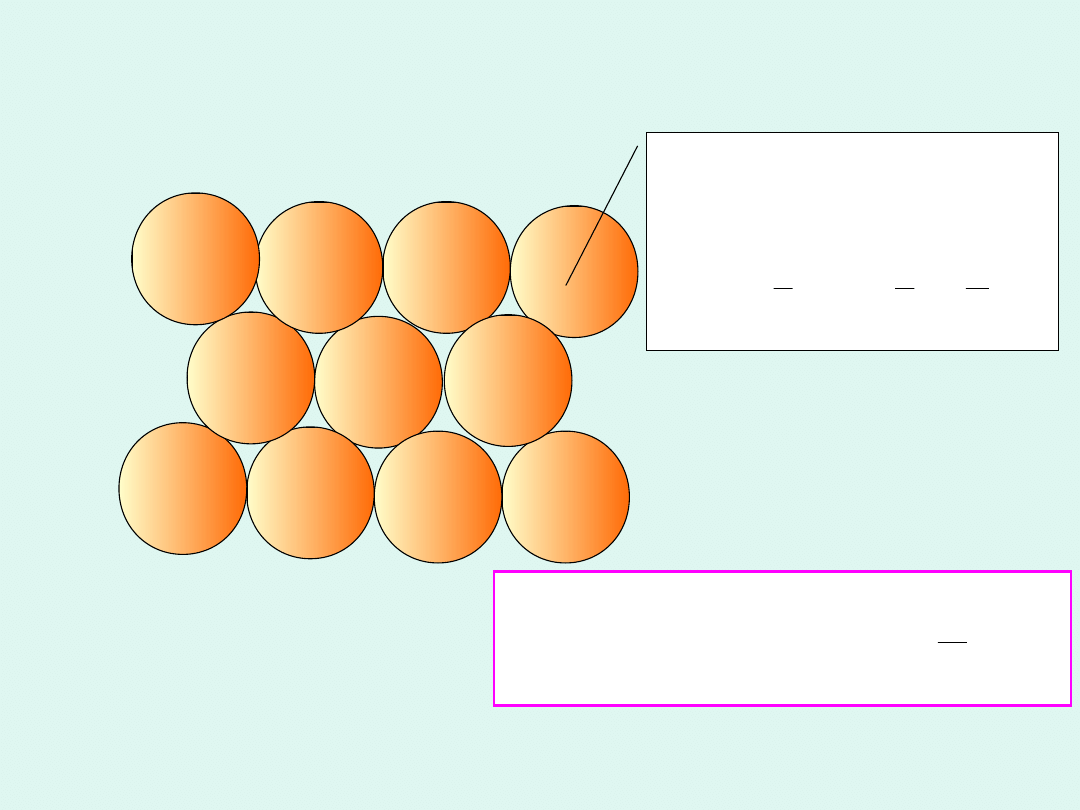
Pojedyncza
cząsteczka ma
objętość :
3
3
cz
2
3
4
r
3
4
V
1 mol cząsteczek
może zająć
najgęściej
upakowany,
objętość :
3
A
cz
A
r
3
4
N
4
V
N
4
b
Interpretacja stałej van der
Waalsa b
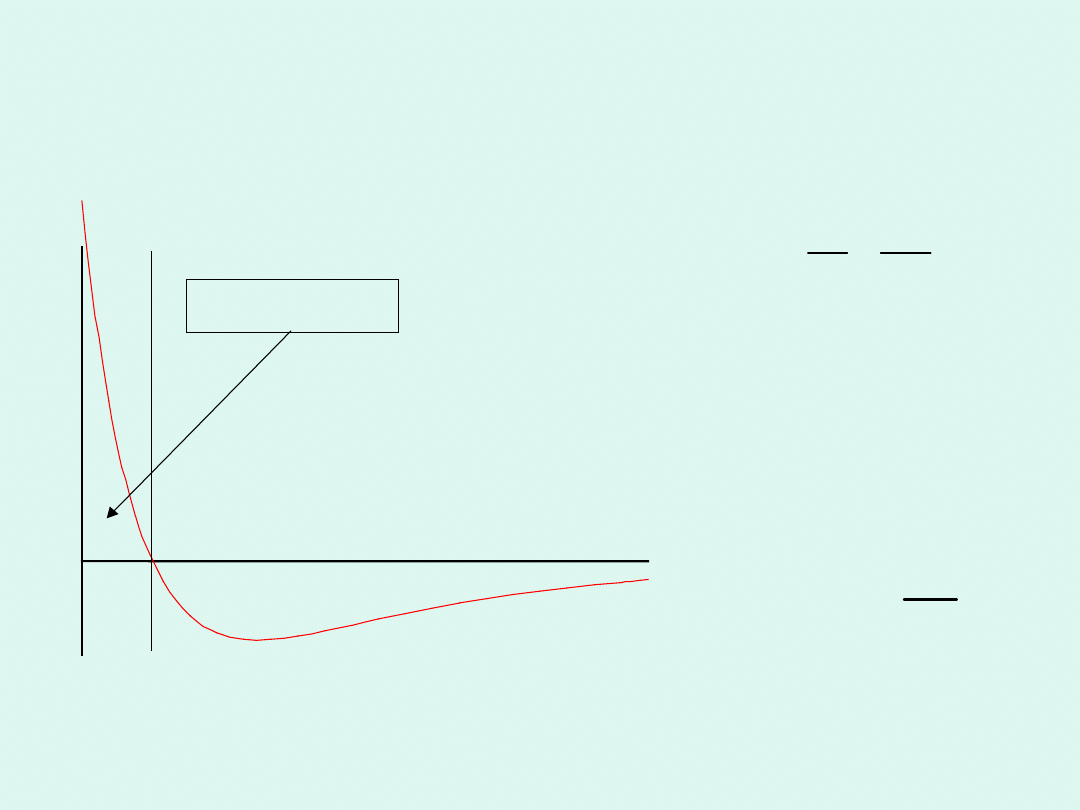
Oddziaływania pomiędzy
rzeczywistymi cząsteczkami
6
12
A
B
E
x
x
=-
+
odległość pomiędzy
cząsteczkami
E
przewaga
przyciągania
przewaga
odpychania
0
Siły odpychające są
istotne tylko dla
bardzo małych
odległości
pomiędzy
cząsteczkami,
wobec tego :
6
A
E
x
�-

Punkt krytyczny
jest to taki stan
substancji, określony przez parametry :
ciśnienie krytyczne, temperatura
krytyczna i objętość krytyczna, w którym
zanika różnica pomiędzy cieczą a parą.
Gazu nigdy nie można skroplić w
temperaturze wyższej od temperatury
krytycznej.
Powyżej temperatury krytycznej mamy do
czynienia z płynem (fazą) nadkrytyczną.
Nadkrytyczny CO
2
jest wykorzystywany do
ekstrakcji nadkrytycznej olejków
naturalnych, barwników i wielu innych
substancji z surowców naturalnych.
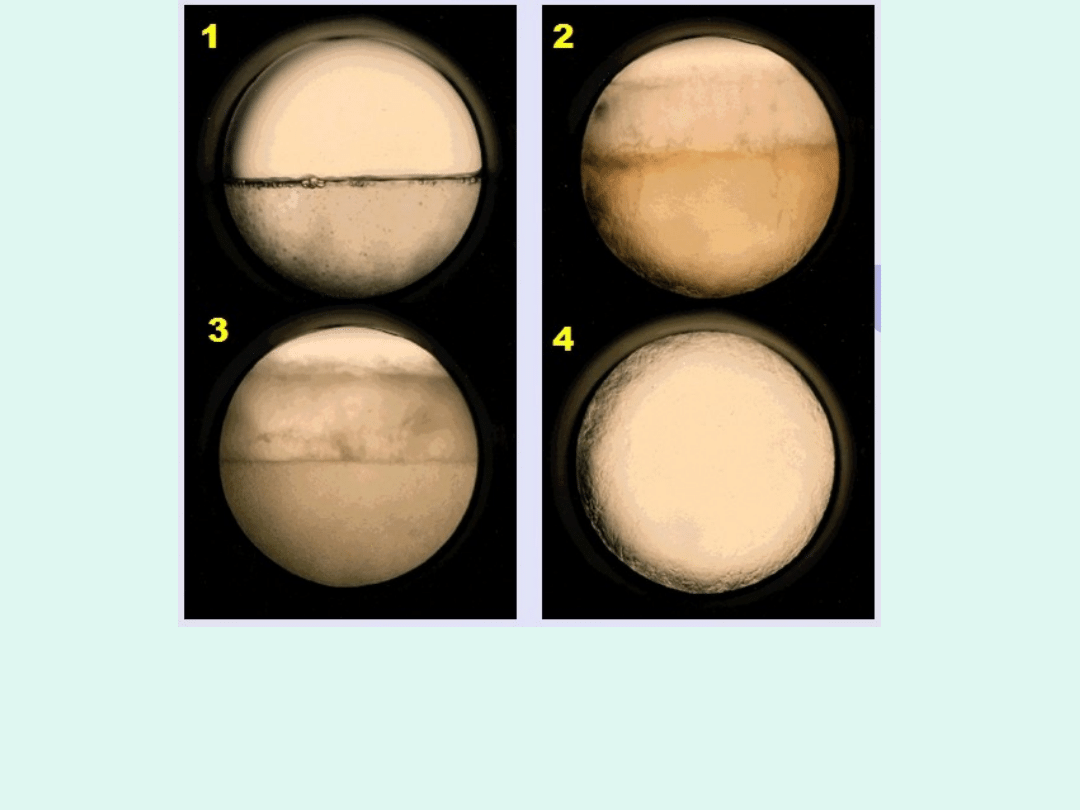
Znikanie różnicy pomiędzy gazem a
cieczą na przykładzie CO
2
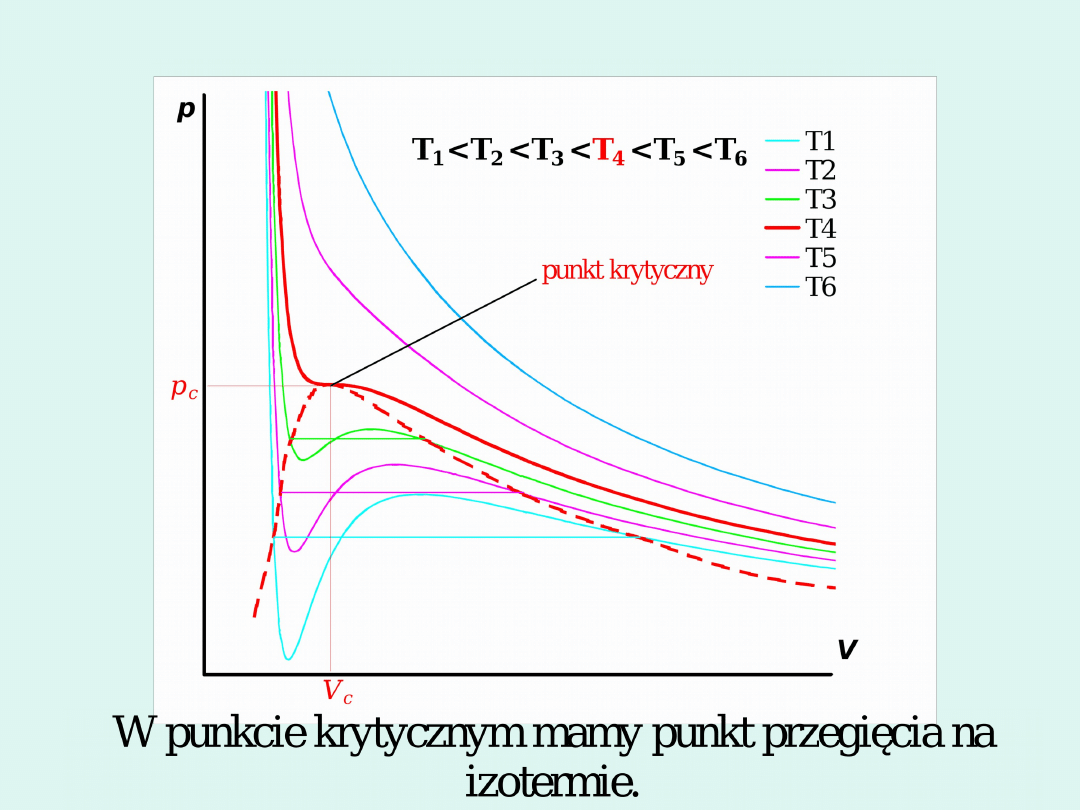
Izotermy van der Waalsa
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
Wyszukiwarka
Podobne podstrony:
10 Wykład Ch F wielkości koligatywneid 11188 ppt
20091205 Wyklad Zarzadzanie Przedsiebiorstwem 2id 26884 ppt
10 Wykład Ch F wielkości koligatywne 2id 11189 ppt
Wykład 2id 1466 ppt
2008 wyklad psychologia w postepowaniu karnym 2id 26564 ppt
2= Wykład wprowadzający Podstawowe pojęcia genet Prof Grzeszczak cz 2id 20087 ppt
002 Prawo transportowe wykład nr 2id 2226 ppt
2 UW HD Wykład 2id 20888 ppt
1 Wykład Ch F wstępid 10087 ppt
Wykład 2id 1466 ppt
więcej podobnych podstron