
1
Antybiotykoterapia
Romuald Krajewski

2
Antybiotyki
•
Są stosowane od około 60 lat
•
W latach 40. penicylina była „cudownym
lekiem”, skutecznym w prawie wszystkich
infekcjach
•
Oporność bakterii na antybiotyki może stać
się powodem powrotu schorzeń infekcyjnych
na czołowe miejsce wśród przyczyn zgonów
•
Antybiotyki są powszechnie stosowane w
rolnictwie

3
Sytuacja w Polsce
•
Wydatki na antybiotyki stanowią średnio 16%
(10-40%) wydatków na leki w szpitalach
•
W szpitalach zużywa się 10% wszystkich
antybiotyków (90% - POZ)
•
Liczba badań bakteriologicznych w szpitalach w
Polsce jest bardzo niska – 12/łóżko/rok, 4-5 razy
mniej niż w UE
•
Antybiotyki są stosowane bez badań
mikrobiologicznych („empirycznie”) – ocenia się,
że około 40% jest podawanych niepotrzbnie

4
Największe zagrożenia
•
W środowisku pozaszpitalnym – oporne na
penicylinę paciorkowce i oporne na leki
prątki gruźlicy
•
W środowisku szpitalnym:
−MRSA (gronkowiec złocisty oporny na metycylinę)
−VRE (enterokoki oporne na wankomycynę)
−Wzrastająca oporność pałeczek Gram- na
chinolony i cefelosporyny 3 generacji
−Pojawiają się gronkowce oporne na wankomycynę

5
Antybiotyki
•
Antybiotyki działają na drobnoustroje
hamując syntezę ściany komórkowej,
aktywując enzymy niszczące ścianę
komórkową, zwiększając
przepuszczalność ściany, zaburzając
syntezę białek, zaburzając
metabolizm kwasów nukleinowych.

6
Antybiotyki
•
Powinny być podawane zgodnie z posiewem
•
Posiew zawsze należy wykonać przed
rozpoczęciem leczenia
•
Wrażliwość drobnoustroju na antybiotyk w
laboratorium na ogół dobrze oddaje wrażliwość
w organizmie pacjenta
•
Dzieli się na antybiotyki niszczące bakterie oraz
na hamujące wzrost bakterii
•
W większości infekcji zahamowanie wzrostu jest
wystarczające do wyleczenia

7
Podział
•
Antybiotyki beta-laktamowe (penicyliny,
cefalosporyny, imipenem)
•
Aminoglikozydy (streptomycyna, gentamycyna,
amikacyna)
•
Makrolidy (erytromycyna, linkomycyna)
•
Tetracykliny (doxycyklina, tetracyklina)
•
Chinolony ( ...floksacyna)
•
Polipeptydy (bacytracyna, kolistyna)
•
Sulfonamidy (biseptol, sulfadiazyna)
•
Inne (wankomycyna, rifampicyna, nitrofurantoina)

8
Stosowanie
•
Musi uwzględniać farmakokinetykę i
farmakodynamikę leku
•
Poziom antybiotyku we krwi musi
osiągnąć przynajmniej minimalne
stężenie hamujące wzrost bakterii (MIC)
•
Penicyliny powinny być podawane często
•
Aminoglikozydy – duże dawki
•
Fluorochinolony – krótko – szybko
narasta oporność

9
Mechanizmy oporności
•
Podawanie leków przeciwbakteryjnych szybko
selekcjonuje szczepy oporne, ponieważ
„przemiana pokoleń” bakterii jest bardzo szybka
•
Mutacje w genach bakterii są bardzo częste i
niektóre z nich mogą prowadzić do oporności
jeżeli obecny jest czynnik selekcjonujący
•
Bakterie mogą przekazywać geny oporności
poprzez plazmidy lub przez wirusy (bakteriofagi)
•
Funkcjonowanie licznych mechanizmów
umożliwia wytworzenie oporności na każdy lek

10
Mechanizmy oporności
•
Najczęstszy problem – beta-laktamazy
(penicylinazy), czyli enzymy rozkładające
antybiotyki beta-laktamowe, również
półsyntetyczne
•
Dodatek kwasu klawulanowego służy
blokowaniu beta-laktamaz, co umożliwia
skuteczne działanie antybiotyku
•
Bakterie rozwijają różne rodzaje laktamaz i
kwas klawulanowy jest coraz częściej
nieskuteczny (przykład - MRSA)

11
Mechanizmy oporności
•
Staphylococcus aureus – 90% szczepów produkuje
beta-laktamazy
•
Szczepy VISA i VRSA – oporność na glikopeptydy
•
Cefalosporyny selekcjonują oporne enterokoki
•
Bakterie G- używają mechanizmów zmiany
przepuszczalności błon komórkowych, aktywnego
wypłukiwania antybiotyku, beta-laktamazy
•
ESBL – laktamazy o rozszerzonym spektrum
działania, dają oporność na wszystkie cefalosporyny

12
Oporność drobnoustrojów w
dużym szpitalu
•
G+ 47%
−Staphylococcus aureus – 14%
−w tym MRSA – 12%
•
G- 53%
−Escherichia coli – 21%
−w tym ESBL – 3%
13
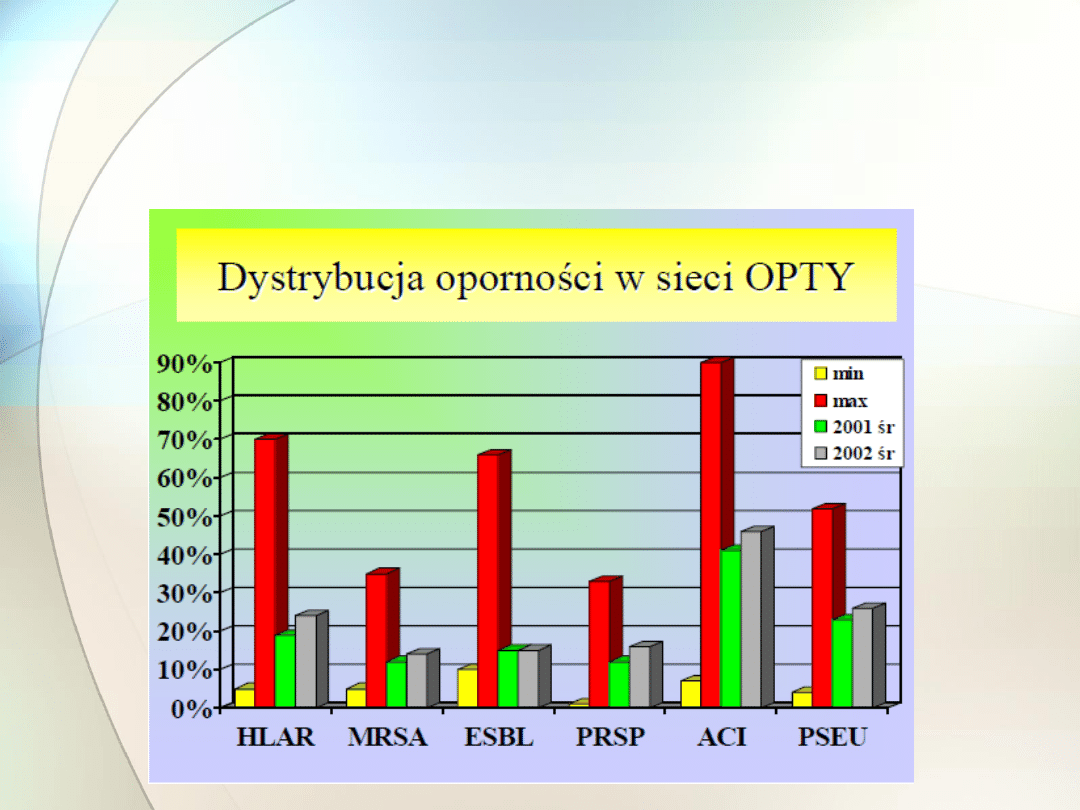
Oporność drobnoustrojów w
Polsce

14
Przyczyny
•
Niewłaściwe stosowanie
antybiotyków
−niepotrzebnie
−za długo
−nieskutecznie
•
Selekcja szczepów opornych (w
normalnych warunkach rozwój
bakterii jest hamowany przez inne)

15
Przyczyny
•
Dodawane do pasz antybiotyki, należące do grup
terapeutycznych stosowanych w medycynie, zwiększają
prawdopodobieństwo rozpowszechniania oporności wśród
patogenów człowieka (oporność na glikopeptydy - szczepy VRE
jako efekt jednoczesnego nadużywania wankomycyny w
lecznictwie i awoparcyny jako dodatku do pasz).
•
Decyzją Komisji Europejskiej wprowadzono w 1998 roku zakaz
stosowania na terenie Unii Europejskiej dostępnych wcześniej
paszowych dodatków antybiotykowych, takich jak: tylosyna,
spiramycyna, bacytracyna i wirginamycyna.
•
Komisja, oprócz zakazu stosowania antybiotyków jako dodatków
paszowych w celach optymalizacji warunków hodowli, zaleca
również racjonalizację ich stosowania w celach terapeutycznych
w weterynarii.

16
Nowe antybiotyki
•
Poszukiwanie nowych antybiotyków jest
coraz trudniejsze
•
Koszty opracowania nowego antybiotyku są
bardzo duże
•
Liczba nowych antybiotyków
wprowadzanych do leczenia bardzo szybko
maleje
•
Producenci nie są zainteresowani
prowadzeniem kosztownych badań

17
Postępowanie
•
Użycie antybiotyków powinno być ograniczone
do minimum
•
Antybiotyk podaje się wtedy, gdy pacjent ma
objawy zakażenia i wiadomo, że ten antybiotyk
jest skuteczny
•
Antybiotyki stosowane w profilaktyce (np. przed
zabiegami) nie mogą być w tym samym oddziale
stosowane do leczenia
•
„Przedłużona profilaktyka” jest niecelowa u
większości pacjentów

18
Postępowanie
•
Częste wykonywanie posiewów
wstępnych aby zidentyfikować
nosicieli szczepów opornych
•
Ścisła izolacja nosicieli szczepów
opornych i pacjentów zakażonych
szczepem opornym

19
Postępowanie
•
Zachowywanie i przekazywanie
informacji o nosicielstwie/zakażeniu
szczepem opornym
•
Rejestr pacjentów z zakażeniami
bakteriami opornymi na antybiotyki
•
Izolacja nosicieli od momentu
przyjęcia do szpitala

20
Profilaktyka antybiotykowa
•
Jest skutecznym sposobem zapobiegania
zakażeniom rany operacyjnej
•
Większość zabiegów w polu czystym nie
wymaga profilaktyki antybiotykowej
•
Wskazana w chirurgii:
−przewodu pokarmowego i dróg oddechowych
−ośrodkowego układu nerwowego
−związanej z implantowaniem protez i innych
urządzeń

21
Profilaktyka - zasady
•
Antybiotyk stosowany profilaktycznie nie
powinien być stosowany do leczenia
•
Antybiotyk powinien być dobrany do znanych
czynników ryzyka zakażeń
•
Antybiotyk powinien mieć maksymalne stężenie
we krwi w momencie ekspozycji na bakterie
(czyli powinien być podany około 1 godziny
wcześniej)
•
Najczęściej stosuje się jedną dawkę, w
niektórych zabiegach (implanty, długi zabieg)
antybiotyk podaje się przez 24-72 godziny

22
Profilaktyka
•
Chorzy z obniżoną odpornością –
chemioterapia (neutropenia),
immunosupresja
−antybiotyki, zwłaszcza chinolony, zmniejszają
ryzyko zgonu zakażenia o około 50%
−profilaktyka zakażeń grzybiczych
−profilaktyka zakażeń wirusowych
•
Radioterapia
−przy nasilonych odczynach skórnych i ze strony
błon śluzowych

23
Postępowanie
•
W myśl decyzji Komisji Europejskiej i rekomendacji
Światowej Organizacji Zdrowia, wszystkie kraje są
zobowiązane do utworzenia międzysektorowych
programów pod nadzorem Ministrów Zdrowia, których
celem jest permanentne monitorowanie, bieżąca ocena
oraz aktywne modelowanie zużycia antybiotyków we
wszystkich gałęziach gospodarki i ochrony zdrowia.
•
W Polsce, realizacja tego postulatu rozpoczęta została w
2004 roku w związku z powołaniem Narodowego
Programu Ochrony Antybiotyków w Polsce,
koordynowanego przez Zespół Badań Mikrobiologicznych
w Narodowym Instytucie Zdrowia Publicznego w
Warszawie.

24
Postępowanie
•
Konsumpcja antybiotyków w Polsce wzrasta i jest jedną z
najwyższych w Europie, a jednocześnie wzrasta liczba raportów
dotyczących nieskuteczności antybiotyków w leczeniu różnych
zakażeń.
•
W ostatnich latach alarmująco wzrasta lekooporność
drobnoustrojów odpowiedzialnych za groźne zakażenia, co
powoduje poważne zagrożenie dla społeczeństwa, wzrost
śmiertelności, szczególnie w skrajnych grupach wiekowych
(noworodki, osoby w podeszłym wieku) oraz pacjentów
wymagających intensywnej terapii w szpitalach.
•
Nieskuteczność terapii antybiotykowej powoduje, że obecnie
koszty antybiotyków stanowią często ponad 30% budżetu
przeznaczanego na zakup wszystkich leków w szpitalach, a w
niektórych oddziałach, jak np. OIOM, hematologia, przekraczają
nawet 50%.

25
Postępowanie – cele
programu
1. Uzyskanie danych reprezentatywnych dla kraju oraz
zwiększenie świadomości społecznej wszystkich osób
stosujących i zlecających antybiotyki,
2. Wdrożenie skoordynowanej polityki antybiotykowej w
różnych działach gospodarki
3. Wprowadzenie do systemu prawnego zmian i nowych
aktów prawnych zapobiegających nadużywaniu
antybiotyków i mających na celu racjonalizację
diagnostyki i terapii zakażeń oraz redukcji zagrożenia dla
zdrowia społeczeństwa,
4. Harmonizacja nadzoru nad stosowaniem antybiotyków w
Polsce z rekomendacjami i dyrektywami Unii
Europejskiej.

26
Postępowanie
•
Monitorowanie antybiotykooporności oraz
kontrola i nadzór nad konsumpcją antybiotyków.
•
Profilaktyka i kontrola chorób zakaźnych i
zakażeń, racjonalizacja stosowania i konsumpcji
antybiotyków
•
Wspieranie badań w kierunku poszukiwania
nowych leków, środków, a także metod terapii i
profilaktyki zakażeń i chorób zakaźnych o
etiologii bakteryjnej
•
Współpraca międzynarodowa

27
Podsumowanie
•
Każde zastosowanie antybiotyku powinno
wynikać ze ściśle określonych wskazań
•
Częste wykonywanie posiewów umożliwia
wczesne rozpoznanie szczepów opornych
•
Należy prowadzić własny rejestr nosicieli
szczepów opornych
•
Mając do czynienia z nosicielem należy
zachować szczególne środki ostrożności

28
Podsumowanie
•
Profilaktyka antybiotykowa jest
niecelowa/niepotrzebna w większości czystych i
krótkotrwałych zabiegów chirurgicznych
•
Niecelowe jest stosowanie antybiotyku
profilaktycznie dłużej niż 24-72 godziny (nie daje
dodatkowej ochrony, selekcjonuje szczepy oporne)
•
Wybór antybiotyku do profilaktyki musi być
dokonany we współpracy z laboratorium
mikrobiologicznym i tego antybiotyku nie wolno
stosować do leczenia zakażeń
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
Wyszukiwarka
Podobne podstrony:
17 DNSid 17180 ppt
17 grudniaid 17235 ppt
17 prezentacjaid 17335 ppt
17 2id 17094 ppt
(12) Makrolidy, Linkozamidy, Aminoglikozydy, Tetracykliny, Chloramfenikol, Antybiotyki, inne(1) ppt
1 Wprowadzenie do psychologii pracy (17)id 8734 ppt
17 Kontrakty werbalne ppt
17 NIEDOKRWISTOŚĆid 17151 ppt
Antybiotyki aminoglikozydowe ppt
17 turystykaid 17359 ppt
17 DNSid 17180 ppt
17 grudn
więcej podobnych podstron