
Magnetyczne własności
materii

Podział substancji ze względu na własności
magnetyczne:
• diamagnetyki
• paramagnetyki
•
ferromagnetyki
•
antyferromagnety
ki
• ferrimagnetyki
•
asperomagnetyki
• i inne …
słabe
własności
magnetyczne
Magnetyki
silne
własności
magnetyczne
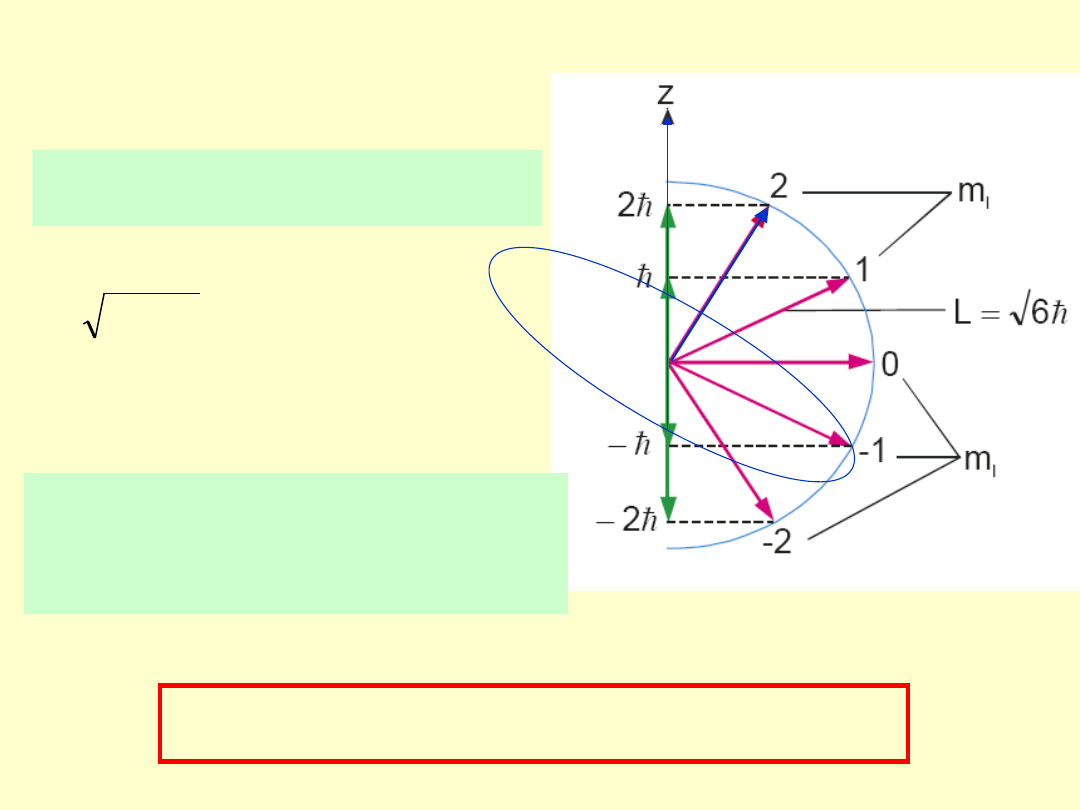
l =2 (stan
d)
Moment pędu i moment magnetyczny elektronu
Orbitalny moment pędu i jego rzut
na oś z są skwantowane.
1
n
,
0,1,2,
,
L
l
)
l(l 1
l
,
3,
2,
1,
0,
m
,
m
L
l
l
z
Wektor momentu pędu jest skwantowany w
przestrzeni
Skwantowany jest więc również kąt,
jaki tworzy wektor momentu pędu z
osią z; kąt ten nigdy nie jest dokładnie
równy zero.
m
l
=2
L
2m
e
n
2m
e
l
Ponadto:
Orbitalny moment magnetyczny jest proporcjonalny do orbitalnego
momentu pędu, a współczynnik proporcjonalności wynosi –e/(2m). Znak
minus wynika z faktu, że elektron ma ujemny ładunek elektryczny.
Moment magnetyczny μ
l
podlega takiemu samemu kwantowaniu, jak
moment pędu.
l
l
l
l
l
l
l
B
z
l
B
l
....
,
2
,
1
,
0
,
)
1
(
)
1
(
m
m
2m
e
L
2m
e
Chmura elektronowa w atomie wytwarza tzw. orbitalny moment
magnetyczny.
n
B
l
2m
n
e
πr
mr
2π
en
IS
mr
2π
en
r
2π
ev
v
r
2π
e
T
e
I
2
2
2
μ
B
– najmniejsza wartość
orbitalnego momentu
magnetycznego, nazywana
magnetonem Bohra
Am
10
·
9.27
2m
e
24
-
B
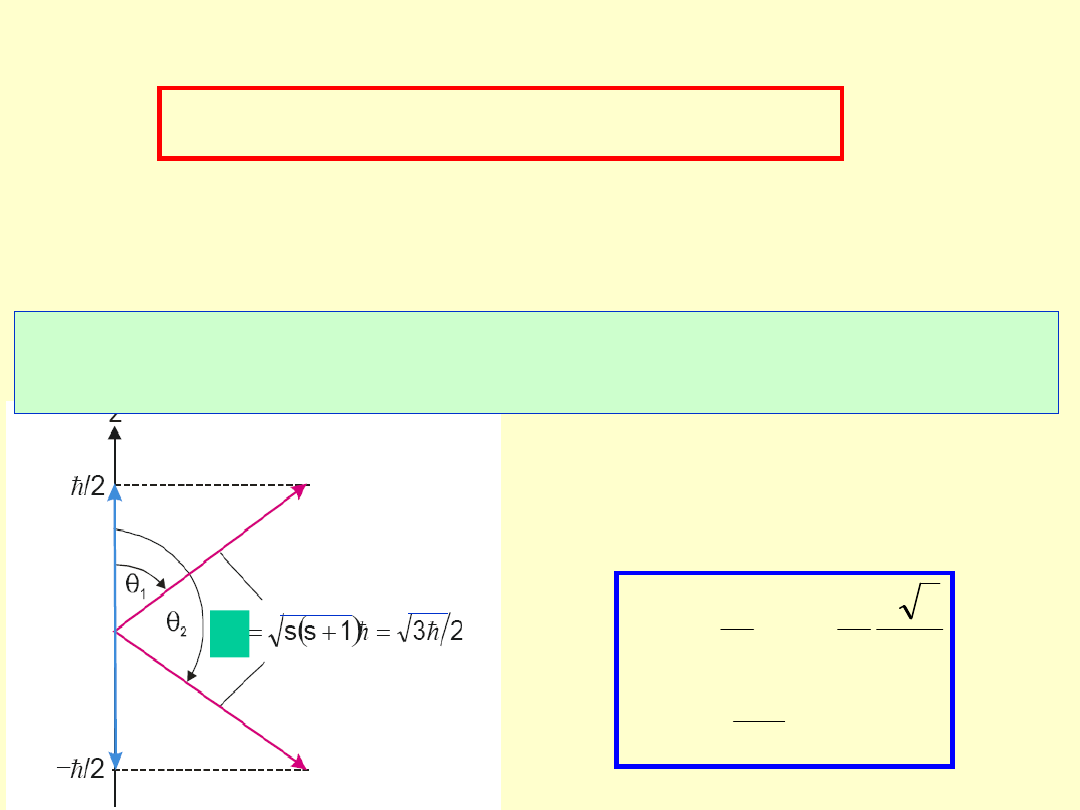
S
Ze spinowym momentem pędu S
związany jest spinowy moment
magnetyczny μ
s
, przy czym wsp. prop.
jest dwa razy większy, niż przy
momentach orbitalnych:
W zewnętrznym polu magnetycznym elektron ma dodatkową energię:
B
m
B
cos
B
B
B
l
z
l
l
l
E
Znika wówczas degeneracja poziomów energetycznych ze względu na
magnetyczną liczbę kwantową. Poziom o liczbie kwantowej
l
rozszczepi się
na 2
l
+1 podpoziomów, różniących się liczbą m
l
.
Zjawisko rozszczepienia linii widmowych atomu w polu magnetycznym nosi
nazwę
zjawiska Zeemana
. Potwierdza ono skwantowanie momentu
magnetycznego elektronów.
B
z
s
s
m
e
m
e
S
m
e
2
2
3
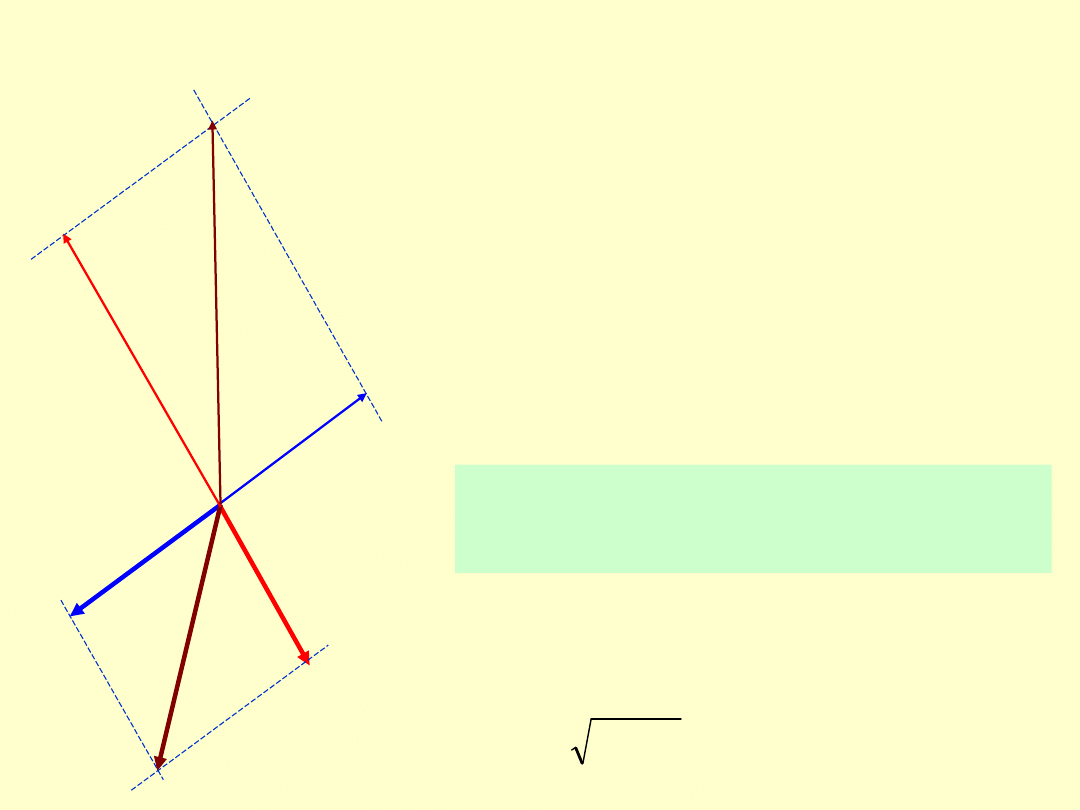
Wypadkowy moment pędu i wypadkowy moment
magnetyczny
S
L
J
s
l
J
l
s
j
L
S
J
Wypadkowy moment pędu jest sumą
momentów oraz , a wypadkowy
moment magnetyczny – sumą
momentów magnetycznych oraz
S
L
l
s
Wypadkowy moment magnetyczny
ma na ogół inny kierunek, niż
wypadkowy moment pędu
Całkowity moment pędu J jest
skwantowany i odpowiada mu liczba
kwantowa j.
s
j
lub
s
j
,
1)
j(j
J
l
l

W atomach wieloelektronowych momenty orbitalne i spinowe
poszczególnych elektronów sumują się (wektorowo), dając
wypadkowy moment magnetyczny atomu p
m
.
Wartość tego momentu decyduje o własnościach
magnetycznych materiału.
Gdy
p
m
≠ 0 ----- materiał jest
paramagnetykiem
lub
ferromagnetykiem
, …..(lub innym z grupy magnetyków)
Gdy
p
m
= 0 ----- materiał jest
diamagnetykiem
.
Przyłożenie do jakiegoś materiału zewnętrznego pola
magnetycznego o indukcji B powoduje wystąpienie wypadkowego
momentu magnetycznego substancji – mówimy, że jest ona
namagnesowana. Miarą namagnesowania jest wielkość M zwana
magnetyzacją (lub namagnesowaniem)
.
m
A
m
Am
[M]
V
p
obj.
jedn.
dip.
mom.
magn.
M
3
2
k
mk
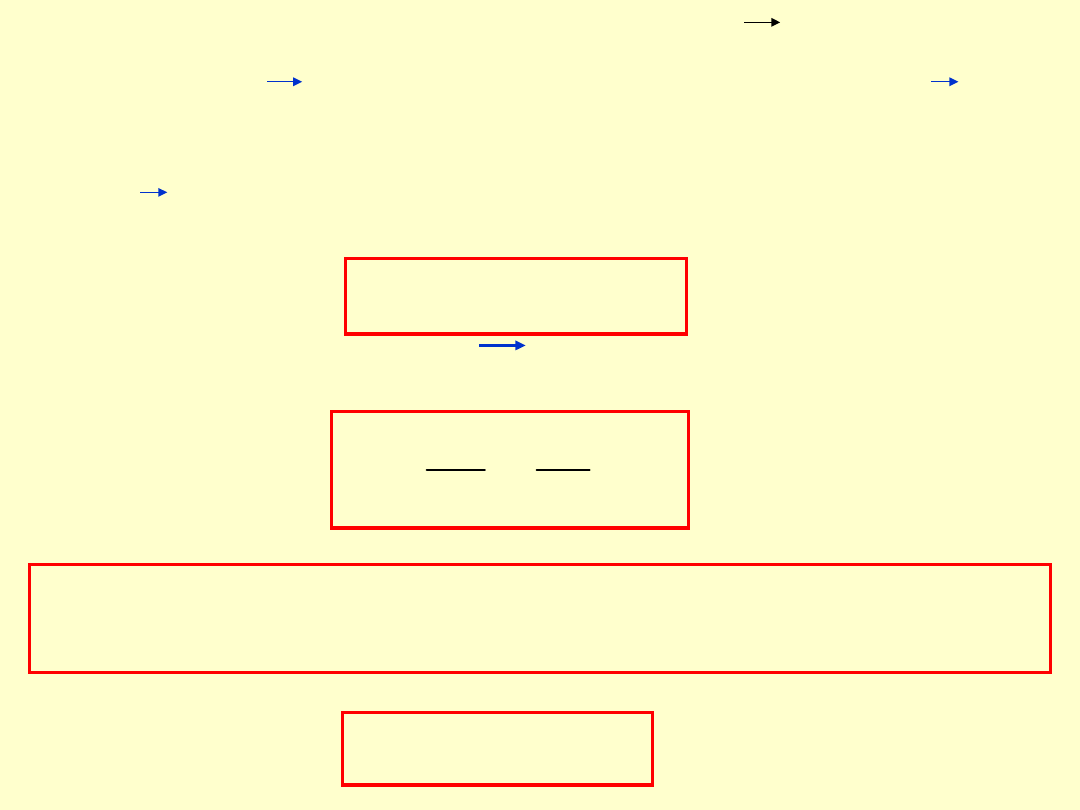
M
μ
B
μ
B
H
0
0
0
Jednostką natężenia pola magnetycznego jest [A/m].
Za pomocą tej wielkości możemy wygodnie zapisać wyrażenie na
indukcję magnetyczną wewnątrz substancji:
Wektor natężenia pola magnetycznego H.
Pole magnetyczne B wewnątrz materiału jest sumą pola
zewnętrznego B
0
oraz dodatkowego pola wytworzonego przez
uporządkowane dipole magnetyczne. Można pokazać, że to
dodatkowe pole jest proporcjonalne do magnetyzacji i równe μ
0
M.
Zatem mamy:
M
μ
B
B
0
0
Natężeniem pola magnetycznego H nazywamy wielkość:
)
M
H
(
μ
B
0
0
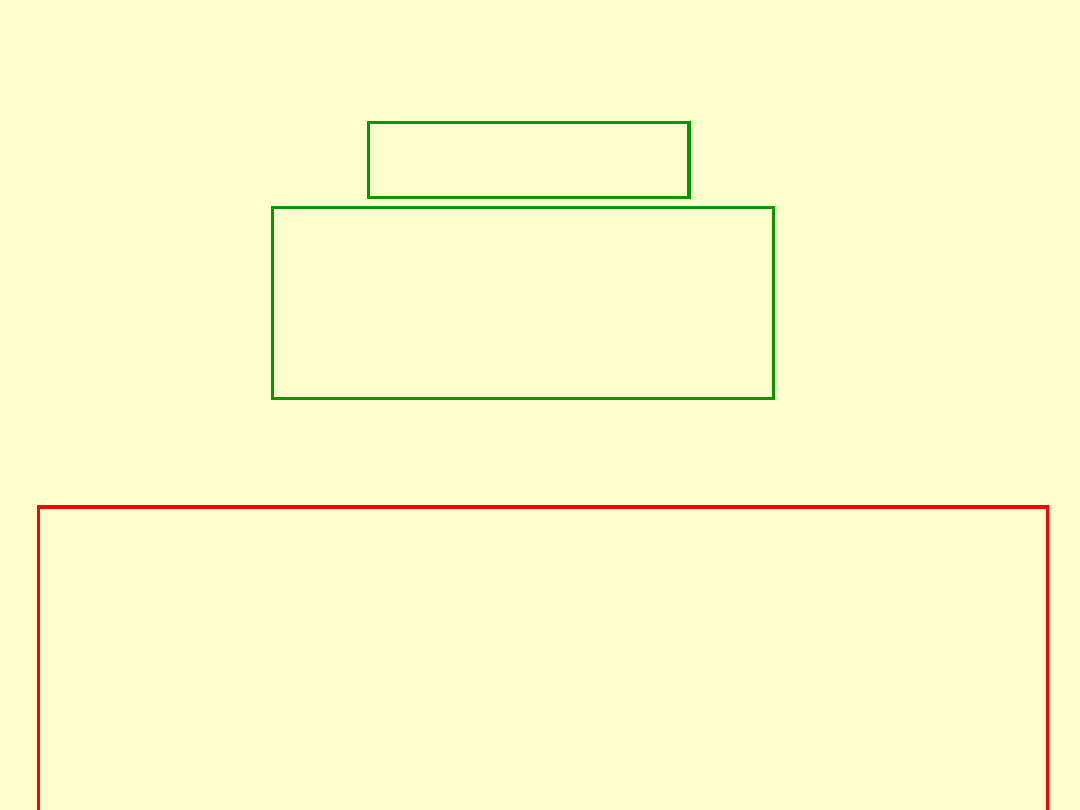
Do opisu zdolności magnesowania substancji używamy tzw.
względnej przenikalności magnetycznej (jest to wielkość
bezwymiarowa).
0
0
0
0
B
χ
M
μ
,
H
χ
M
H
1)
(μ
M
)
M
H
(
μ
H
μ
μ
Bezwymiarowa wielkość
= ( - 1)
nazywana jest podatnością
magnetyczną
H
μ
μ
B
μ
B
o
0
Ze względu na właściwości magnetyczne materiały dzielimy na
ogół na trzy grupy:
diamagnetyki
χ - 10
-6
1
<1
paramagnetyki χ 10
-9
– 10
-3
1
>1
ferromagnetyki χ 10
4
– 10
5
=10
4
– 10
5
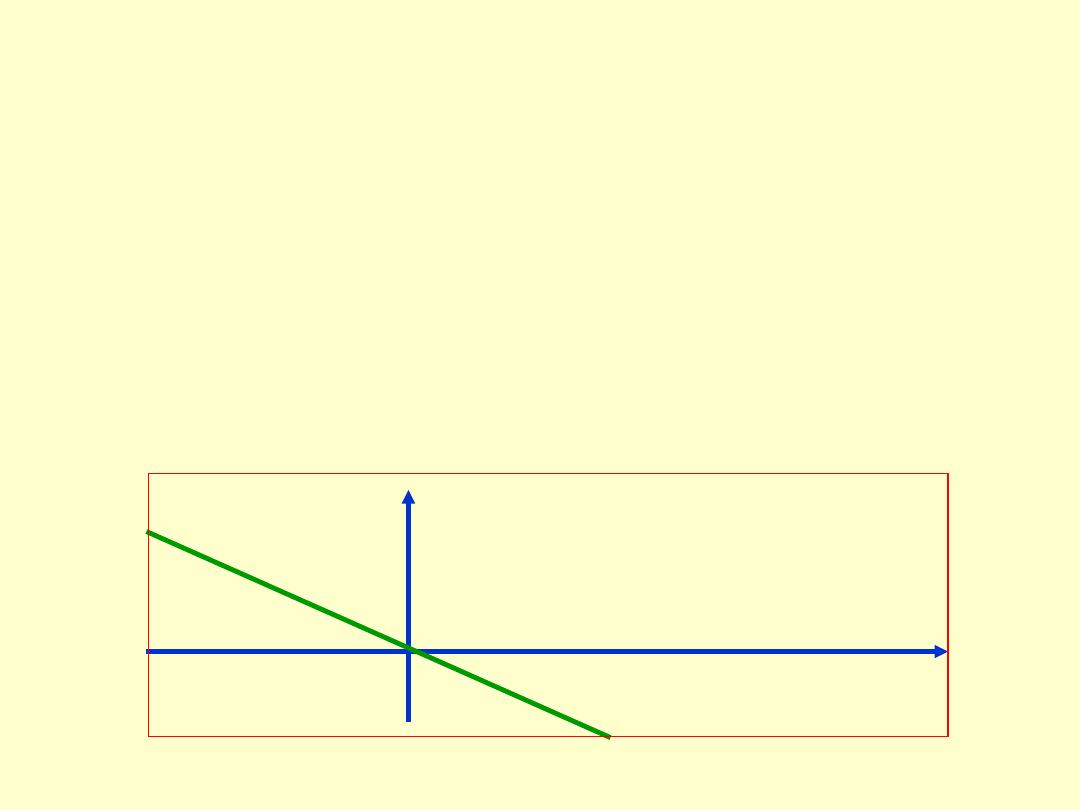
W
diamagnetykach
magnetyczne momenty orbitalne i spinowe
elektronów w atomie kompensują się. Atom nie ma więc
własnego momentu magnetycznego.
Do diamagnetyków mogą należeć te pierwiastki, które mają
parzystą liczbę elektronów w atomie. Podatność magnetyczna
jest dla diamagnetyków ujemna i niezależna od temperatury
Typowymi diamagnetykami są: gazy szlachetne, cynk, złoto, rtęć,
bizmut, gal, nadprzewodniki, fosfor, grafit, woda….
W niejednorodnym polu magnetycznym diamagnetyki są
wypychane z obszaru silnego pola
M
H

A small (~6mm) piece of pyrolytic graphite levitating
over a permanent neodymium magnet array (5mm
cubes on a piece of steel). Note that the poles of the
magnets are aligned vertically and alternate (two with
north facing up, and two with south facing up,
diagonally)
English Wikipedia
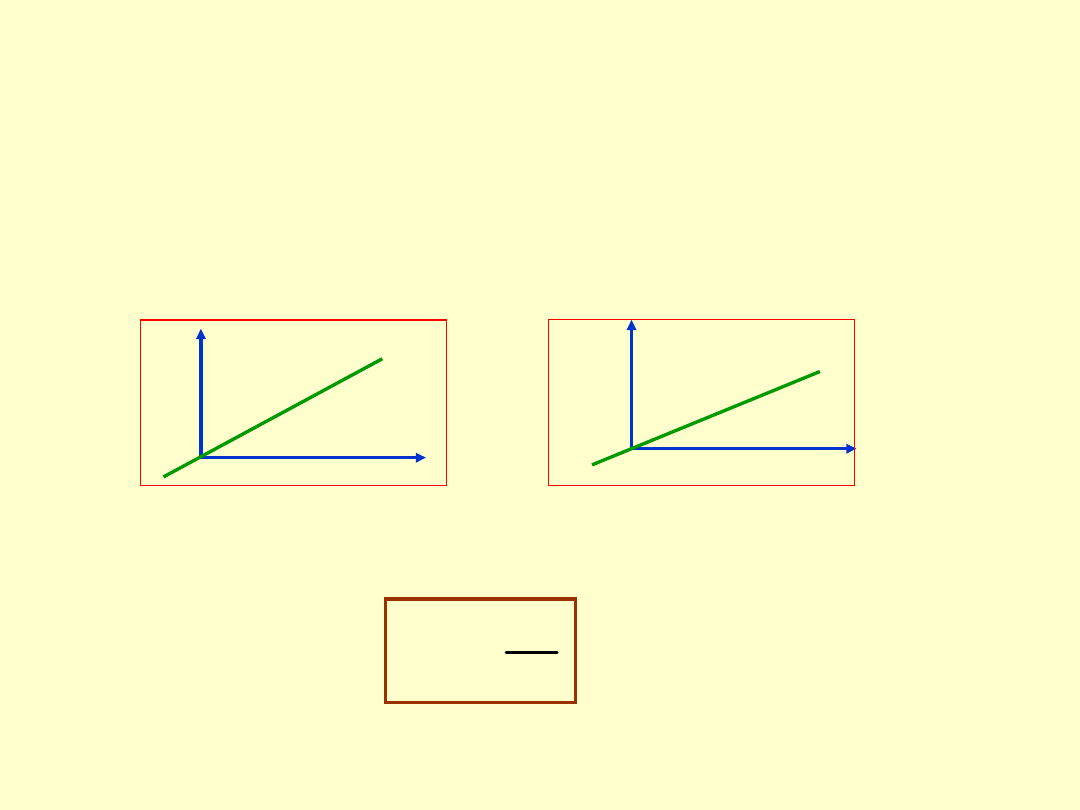
B
H
M
H
W
paramagnetykach
magnetyczny moment dipolowy atomu jest
różny od zera. W normalnych warunkach momenty magnetyczne
poszczególnych atomów są ustawione chaotycznie w różnych
kierunkach, tak że magnetyzacja materiału jest równa zero. W
polu magnetycznym zachodzi „porządkowanie”, czyli tzw.
polaryzacja atomowych momentów magetycznych, co w efekcie
obserwujemy jako magnesowanie materiału. Po usunięciu pola
materiał natychmniast się rozmagnesowuje.
Do paramagnetyków należą np: wodór, sód, lit, potas, aluminium,
itd
T
1
~
χ
Podatność magnetyczna dla paramagnetyków zmienia się z
temperaturą zgodnie z prawem Curie:
W niejednorodnym polu magnetycznym zarówno
paramagnetyki, jak i ferromagnetyki są wciągane w obszar
silnego pola.
Ferromagnetyzm znika powyżej temperatury Curie.
Temperatury Curie wynoszą przykładowo: dla Gd - 20
0
C, dla Ni - 358
0
C,
dla Fe -770
0
C, dla Co - 1131
0
C.
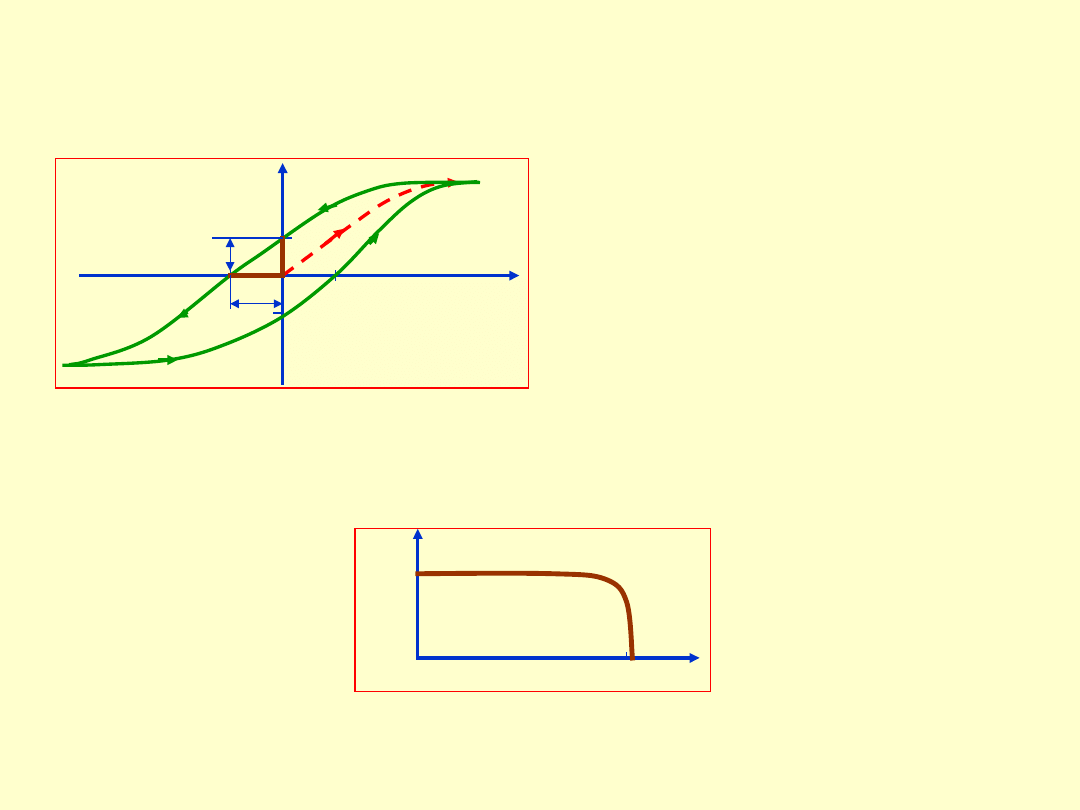
B(M)
H
B
R
H
K
Krzywą histerezy charakteryzują dwie wielkości, remanencja B
R
(lub inaczej pozostałość magnetyczna), oraz koercja H
K
.
B
T
T
C
W
ferromagnetykach
atomowe
momenty
magnetyczne
oddziałują ze sobą tak silnie, że występuje ich wzajemne
uporządkowanie
nawet
bez
pola
magnetycznego.
Ferromagnetyk może być więc namagnesowany poza polem
magnetycznym.
Ferromagnetykami
są:
żelazo,
kobalt,
nikiel,
gadolin
oraz
wiele
ich
stopów
i
związków
chemicznych.
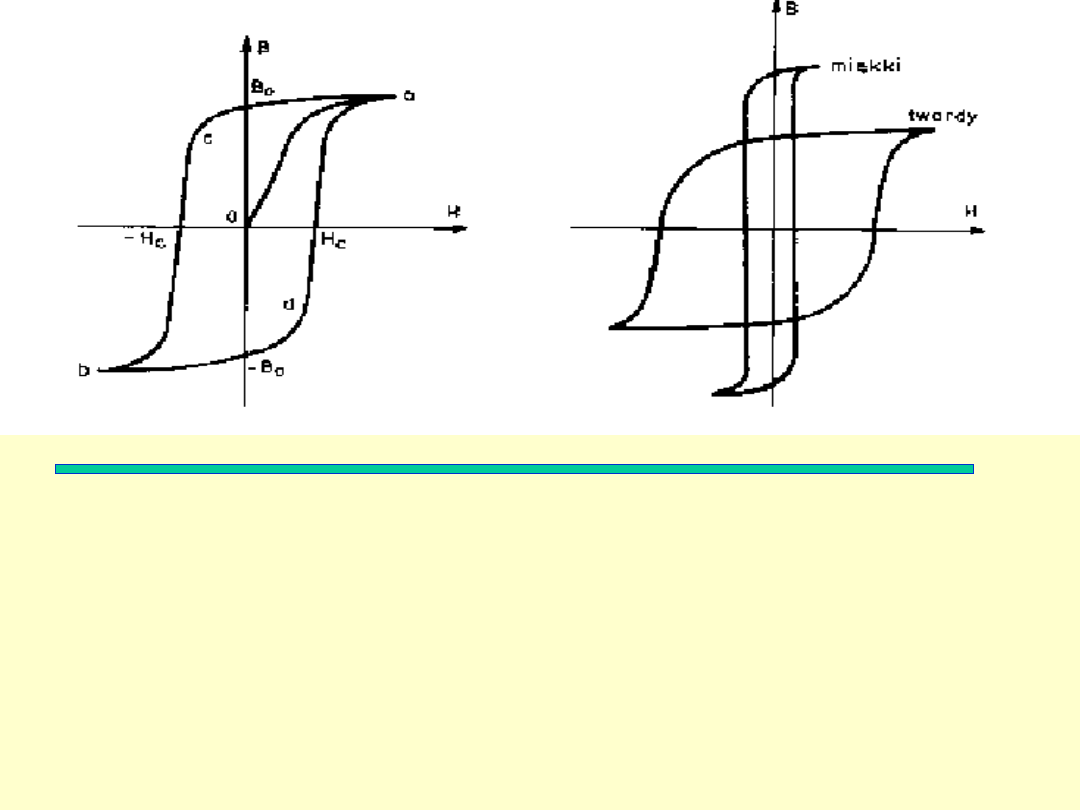
Rysunki:
Po lewej:
typowy przebieg pętli histerezy.
Po prawej:
kształt krzywej histerezy w przypadku materiałów
miękkich magnetycznie (1-100 A/m-czyste żelazo, stopy Fe-Si, Fe-
Ni, magnetyki amorficzne i nanokrystaliczne) i twardych
magnetycznie (1000 – 10000 A/m np. niektóre stale, stopy,
magnesy wytwarzane z proszków).
Kształt pętli histerezy silnie zależy od struktury materiału, a nie
tylko od składu chemicznego.

Jakie oddziaływanie powoduje tak silne sprzężenie
atomowych momentów magnetycznych?
Nie jest to „zwykłe” oddziaływanie magnesów, tzw.
magnetyczne oddziaływanie dipolowe (jest zbyt słabe)
lecz tzw. oddziaływanie wymiany (lub in.
oddziaływanie wymienne). Jest ono związane z
oddziaływaniem elektrostatycznym i ma naturę
kwantową, gdyż wynika z symetrii funkcji falowych
elektronów należących do różnych atomów.
Efektywny hamiltonian pary atomów można zapisać w
postaci:
2
1
S
S
2J
H
ˆ
ˆ
ˆ
gdzie J jest tzw. całką wymiany (hamiltonian
Heisenberga).
Jeśli J > 0, to energia jest najmniejsza przy
równoległym ustawieniu spinów
(ferromagnetyzm),
jeśli J < 0, to energia jest najmniejsza przy
antyrównoległym ustawieniu spinów
(antyferromagnetyzm)

Domeny w materiale ferromagnetycznym: a) substancja nie
namagnesowana,
b) w niezbyt silnym polu magnetycznym nastąpiło przesunięcie
granic domen,
c) stan nasycenia. W przypadkach b) i c) występuje niezerowa
magnetyzacja, w stanie nasycenia magnetyzacja jest maksymalna.
M=0
M≠0
H
a)
b)
c)

Powstawanie domen jest wynikiem współistniejących,
konkurencyjnych procesów, z których najważniejsze,
to:
• oddziaływanie wymienne
• makroskopowe oddziaływanie magnetyczne
dipolowe
• anizotropia magnetokrystaliczna.
Wzrost temperatury powoduje zwiększanie się energii
drgań termicznych, co wpływa na „rozporządkowanie”
układu momentów magnetycznych
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
Wyszukiwarka
Podobne podstrony:
ETYKA I OCHRONA WLASNOSCI INTELEKTUALNEJ (wykłady-część), INNE, Materiały Edukacyjne, Etyka i Ochron
Ochrona własności intelektualnej - wykład 2013, PB-materiały, semestr VI, ochrona własności intelekt
Notatki wykładowe, WEEIA Informatyka, Semestr 1, Prawo inżynierskie i ochrona własności intelektualn
Materialoznawstwo Wyklad3 WlasnosciEnergetyczne
Materialoznawstwo Wyklad3 WlasnosciEnergetyczne
Wyklad 7 Wlasnosci elektryczne metali
pdf wykład 02 budowa materii, podstawowe prawa chemiczne 2014
BHP - wykład III - biomechanika, materiauy
Informatyka - wykład II, Inne materiały
Wykład 1 cd2, Elektrotechnika-materiały do szkoły, Gospodarka Sowiński
własności mechaniczne materiałow 1
MC W Wyklad 08 Tlenkowe Materialy Konstrukcyjne
miernictwo wyklad 09, INNE MATERIAŁY
miernictwo wyklad 05, INNE MATERIAŁY
Wykład 3 cd, Elektrotechnika-materiały do szkoły, Gospodarka Sowiński
5.Ochrona własności intelektualnej, Materiały prawo
Partie i Systemy Partyjne Wyklady[1], Politologia UMCS - materiały, III Semestr zimowy, Partie polit
wyklady 1-5, umb rok 3, materiały, mikroby, mikro, MIKROBY I KOLO
więcej podobnych podstron