
Farmakodynamika
leków
przeciwnowotworow
ych

Chemioterapia
Hormonoterapia
Immunoterapia

5-FU
•Zespół
erytrodyzestezji
dłoniowo -
podeszwowej

Kapecytabina
• Mechanizm działania
– Pozbawiony cytotoksyczności
karbaminian fluoropirymidyny
– W reakcji enzymatycznej przekształcana
do 5-FU
– Enzym odpowiedzialny za ostateczną
konwersjędo 5-FU to fosforylaza
tymidynowa (ThyPase) jest obecna w
tkankach guza; także występuje w
tkankach prawidłowych w niższym
stężeniu

Kapecytabina
•Xeloda

Kapecytabina (Xeloda) -
wskazania
• Pooperacyjne leczenie
uzupełniające raka okrężnicy
• Leczenie chorych na raka jelita
grubego i odbytnicy z przerzutami
• Leczenie I rzutu chorych na
zaawansowanego raka żołądka
w skojarzeniu z pochodnymi
Pt

Kapecytabina (Xeloda) -
wskazania
• W skojarzeniu z
docetakselem w leczeniu
pacjentek z miejscowo
zaawansowanym rakiem
piersi lub rakiem piersi z
przerzutami po
niepowodzeniu leczenia
antracyklinami

Kapecytabina (Xeloda) -
wskazania
• W monoterapii u pacjentek z
miejscowo zaawansowanym lub
rozsianym rakiem piersi po
niepowodzeniu leczenia
taksanami i antracyklinami lub
u pacjentek, u których dalsze
leczenie antracyklinamim jest
przeciwwskazane

Kapecytabina – działania
niepożądane (monoterapia
)
• Zakażenia – zakażenia wirusem
opryszczki
• Zaburzenia hematologiczne –
neutropenia, niedokrwistość
• Zaburzenia odżywiania – jadłowstręt
• Kardiotoksyczność
• Zaburzenia układu nerwowego –
bóle, zawroty głowy, parestezje ,
zaburzenia smaku

Kapecytabina – działania
niepożądane
• Zaburzenia układu oddechowego –
duszność, kaszel
• Zaburzenia żołądkowo-jelitowe –
nudności, wymioty, biegunka,
zapalenie jamy ustnej
• Zaburzenia czynności nerek –
wodonercze, krwiomocz
• Zaburzenia ogólne – zmęczenie,
astenia

Kapecytabina – działania
niepożądane
• Zaburzenia skory bardzo często:
zespół
erytrodyzestezji
dłoniowo –
podeszwowej
;
często: wysypka, łysienie,
rumień. suchość skóry, świąd

Zespół dłoniowo –
podeszwowy
(określany też jako
skórna reakcja rąk i
stóp, erytrodyzestezja
dłoniowo –
podeszwowa lub
wywołany
chemioterapią rumień
kończynowy)

Zespół dłoniowo –
podeszwowy stopień 1
• Definiowany jako drętwienie ,
zaburzenia czucia/przeczulica,
mrowienie, bezbolesny obrzęk
lub rumień rak i stóp i/lub
dyskomfort bez wpływu na
normalną aktywność pacjenta

Zespół dłoniowo –
podeszwowy stopń 2
• Bezbolesny rumień oraz obrzęk
rak
i stóp- i/lub dyskomfort
zaburzający codzienną
aktywność pacjenta

Zespół dłoniowo –
podeszwowy stopień 3
• Wilgotne łuszczenie,
owrzodzenia, pęcherze i duży ból
rak i stop i/lub ciężki dyskomfort
uniemożliwiający pracę lub
wykonywanie codziennych
życiowych czynności

Zespół dłoniowo -
podeszwowy
• W 2 lub 3 stopniu podawanie
kapecytabiny powinno być
przerwane do czasu jego
ustąpienia lub złagodzenia do
stopnia 1

Zespół dłoniowo -
podeszwowy
•W przypadku stopnia 3
następne dawki leku
powinny być obniżone

Zespół dłoniowo -
podeszwowy
• W przypadku leczenia kapecytabiną
w skojarzeniu z cisplatyną nie zaleca
się stosowania witaminy B6
(pirydoksyna) w celu leczenia
objawowego lub wtórnej profilaktyki
zespołu dłoniowo – podeszwowego
ze względu na doniesienia
sugerujące , że taka terapia może
zmniejszać skuteczność cisplatyny

Gemcytabina – mechanizm
działania
• Antymetabolit pirymidyny
• Przekształcana
wewnątrzkomórkowo do
aktywnych nukleotydów dFdCDP
– difosforanu
difluorodeoksycytydyny i dFdCTP
– trifosforanu
difluorodeoksycytydyny

Gemcytabina - mechanizm
działania
• dFdCDP hamuje aktywność
reduktazy nukleotydowej, która
jest katalizatorem reakcji
prowadzących do powstawania
trifosforanów
deoksynukleotydów dCTP
wykorzystywanych w syntezie
DNA

Gemcytabina – mechanizm
działania
• Trifosforan
difluorodeoksycytydyny (dFdCTP)
konkuruje z dCTP
o wbudowywanie do nici DNA
(tzw. samowzmocnienie)
• Zmniejszenie stężenia
wewnątrzkomórkowego dCTP
nasila wbudowywanie dFdCTP do
nici DNA

Gemcytabina – mechanizm
działania
• Polimeraza episoln DNA nie jest
zdolna do usunięcia gemcytabiny i
naprawy wydłużającej się nici DNA
• Po wbudowaniu nukleotydów
gemcytabiny do DNA, do nici DNA
dodawany jest tylko jeden
dodatkowy nukleotyd, po czym
dalsza synteza DNA zostaje
zahamowana
• Inicjacja procesu apoptozy

Gemcytabina - wskazania
• Rak pęcherza moczowego miejscowo
zaawansowany lub z przerzutami
(kojarzenie z cisplatyną)
• Gruczolakorak trzustki miejscowo
zaawansowany lub z przerzutami
• NDRP (niedrobnokomórkowy rak
płuc)
w monoterapii lub w skojarzeniu
z cisplatyną

Gemcytabina -
wskazania
• W skojarzeniu z karboplatyną –
leczenie nabłonkowego raka jajnika
w stadium miejscowo
zaawansowanym lub z przerzutami
(terapia wskazana po niepowodzeniu
chemioterapii I rzutu opartej na
związkach Pt i co najmniej
6-miesięcznym okresie bez
nawrotów)

Gemcytabina -
wskazania
• W skojarzeniu z paklitakselem –
miejscowy nawrót raka piersi,
który nie kwalifikuje się do
leczenia operacyjnego lub z
przerzutami, po niepowodzeniu
chemioterapii antracyklinami lub
w przypadku przeciwwskazań do
ich stosowania

Gemcytabina działania
niepożądane
• Zaburzenia krwi – leukopenia,
trombocytopenia, niedokrwistość
• Zaburzenia układu oddechowego
– duszność, kaszel
• Zaburzenia żołądkowo-jelitowe –
wymioty, nudności, biegunka lub
zaparcie

Gemcytabina działania
niepożądane
• Zaburzenia wątroby – zwiększenie
aktywności enzymów wątrobowych
(AspAT, ALAT) i fosfatazy zasadowej
• Zaburzenia skórne: wysypka
alergiczna, łysienie
• Zaburzenia nerkowe – krwiomocz,
białkomocz
• Zaburzenia ogólne – objawy
grypopodobne

Taksany
•Paklitaksel
•Docetaksel
•Kabazytaksel

Kabazytaksel – mechanizm
działania
•Stabilizacja mikrotubul co
powoduje zahamowanie
mitotycznych i
interfazowych podziałów
komórki

Kabazytaksel (Jevtana)
wskazania
• W piołączeniu z prednizonem
lub prednizolonem – leczenie
pacjentów z hormonoopornym
rakiem gruczołu krokowego
z przerzutami, leczonych
wcześniej schematem
chemioterapii zawierającym
docetaksel

Kabazytaksel – działania
niepożądane
• Reakcje nadwrażliwości
• Neutropenia najczęstsze działanie
niepożądane po kabazytelu;
niezbędne jest wykonywanie
badań pełnej morfologii krwi co
tydzień podczas I cyklu leczenia
oraz przed każdym kolejnym
cyklem, tak aby w razie
konieczności można było
dostosować dawkę

Kabazytaksel – działania
niepożądane
• Nudności, wymioty, biegunka i
odwodnienie
• Neuropatia obwodowa (obwodowa
neuropatia czuciowa – parestezje,
dystezje; obwodowa neuropatia
ruchowa)
• Niewydolność nerek
• Ryzyko zaburzeń rytmu serca
(tachkardia i migotanie
przedsionków)

Alkaloidy barwinka
różowatego (Vinca rosea)
Winkrystyna
Winblastyna
Winorelbina
Winflumina

Alkaloidy barwinka
różowatego mechanizm
działania
• Hamowanie podziału komórki w
stadium metafazy
• Wiążą się z tubuliną będącą
składnikiem mikrotubul tworzących
wrzeciono podziałowe
• Następuje zniekształcenie wrzeciona
co prowadzi do zakłócenia
rozmieszczenia chromosomów w
płaszczyźnie równikowej – chromosomy
grupują się w cytoplazmie chaotycznie,
co prowadzi do śmierci komórki

Winorelbina wskazania
•Niedrobnokomórkowy rak
płuc
•Zaawansowany rak piersi

Winorelbina działania
niepożadane
• Leukopenia i trombocytopenia
• Zaburzenia żołądkowo – jelitowe
(nudności, wymioty, biegunka
lub zaparcie)
• Wstrzyknięcie poza żyłę może
spowodować martwicę tkanek

Winflunina - wskazania
•Leczenie zaawansowanego
raka
przejściowokomórkowego
dróg moczowych po
niepowodzeniu
wcześniejszej terapii
pochodnymi Pt

Winflunina
działania niepożądane
• Zaburzenia krwi – neutropenia,
leukopenia, trombocytopenia,
niedokrwistość
• Zaburzenia odżywiania –
anoreksja
• Zaburzenia układu nerwowego
obwodowa neuropatia czuciowa
• Zaburzenia serca - tachykardia

Winflunina
działania niepożadane
• Zaburzenia żołądkowo-jelitowe –
nudności, wymioty, zaparcia, ból
brzucha, zapalenie błony śluzowej
jamy ustnej
• Zaburzenia skórne – łysienie
• Zaburzenia mięśniowe – ból mięśni
• Zaburzenia ogólne – astenia,
zmęczenie

PM
Rytuksymab
Trastuzuma
b

Trastuzumab
• Rekombinowane, humanizowane
PM IgG
1
• Łączy się wybiórczo z receptorem
ludzkiego naskórkowego
czynnika wzrostu typu 2
(receptor HER2)

Trastuzumab
mechanizm działania
• Wiąże się z dużym
powinowactwem i
specyficznością z IV subdomeną
związaną z błoną w regionie
zewnątrzkomórkowej domeny
receptora HER2 (hamowanie
aktywności receptora HER2)

Trastuzumab
mechanizm działania
• Silny mediator cytotoksyczności
komórkowej zależnej od przeciwciała
(ADCC); in vitro wykazano, że
cytotoksyczność typu ADCC
stymulowana trastuzumabem jest
preferencyjnie wywierana na
komórki guza wykazujące
nadekspresję HER2 w porównaniu
z komórkami guza bez nadekspresji
HER2

Trastuzamab
(Herceptin)
• Powinien być stosowany
wyłącznie u pacjentów z
przerzutowym lub wczesnym
rakiem piersi, u których
stwierdzono w komórkach guza
nadekspresję receptora HER2 lub
amplifikację genu HER2

Trastuzumab
• Powinien być stosowany
wyłącznie u pacjentów z
rakiem żołądka
z przerzutami, u których
stwierdzono w komórkach
guza nadekspresję HER2,
określaną jako IHC2+

Trastuzumab
wskazania
• Rak piersi z przerzutami (MBC –
metastatic breast cancer
)
– W monoterapii do leczenia tych pacjentów,
którzy otrzymywali dotychczas co najmniej
dwa schematy monoterapii (uprzednio
stosowane schematy muszą zawierać
antracykliny i taksany, o ile nie było
przeciwwskazań do tego typu leczenia; u
pacjentów z dodatnim wynikiem badania na
obecność receptorów hormonalnych, u
których nie powiodła się hormonoterapia, o ile
nie było przeciwwskazań do jej zastosowania)

Trastuzamab
wskazania
•MBC
– W skojarzeniu z paklitakselem do
leczenia tych pacjentów, którzy nie
otrzymywali dotychczas
chemioterapii z powodu choroby
nowotworowej z przerzutami i dla
których antracyklina jest
przeciwwskazana

Trastuzuma
wskazania
•MBC
– W skojarzeniu z docetakselem do
leczenia tych pacjentów, którzy nie
otrzymywali dotychczas
chemioterapii z powodu choroby
nowotworowej z przerzutami

Trastuzumab
wskazania
•MBC
– W skojarzeniu z inhibitorami
aromatazy do leczenia pacjentek po
menopauzie
z dodatnim wynikiem badania na
obecność receptorów hormonalnych,
u których doszło do rozwoju choroby
nowotworowej z przerzutami, a nie
poddanych wcześniej leczeniu
trastuzumabem

Trastuzumab
wskazania
• Wczesne stadium raka piersi (EBC
– early breast cancer)
– Pooperacyjnie i po chemioterapii
adiuwantowej i neoadiuwantowej
– Po chemioterapii adiuwantowej
z doksorubicyną i CPA, w skojarzeniu
z paklitakselem lub docetakselem
– W skojarzeniu z chemioterapią
adiuwantową z użyciem docetakselu
i karboplatyny

Trastuzumab
wskazania
•EBC
– W skojarzeniu z neoadiuwantową
chemioterapią i następnie w terapii
adiuwantowej opartej o
trastuzumab
w miejscowo zaawansowanym (w
tym zapalnym) raku piersi lub w
przypadku guza>2 cm średnicy

Trastuzumab
wskazania
• Rak żołądka z przerzutami (MGC
–
metastatic gastric cancer)
– W skojarzeniu z kapecytabiną lub 5-
FU i cisplatyną jest wskazany w
leczeniu pacjentów z HER2(+)
gruczolakorakiem żołądka z
przerzutami lub połączenia
żołądkowo-przełykowego, których
nie poddawano wcześniej terapii z
powodu choroby rozsianej

MBC podawanie
trastuzumabu
• Schemat trzytygodniowy
• Schemat tygodniowy
• Stosowanie w skojarzeniu
z paklitakselem lub
docetakselem
• W skojarzeniu z inhibitorami
aromatazy

EBC podawania
trastuzumabu
• Schemat trzytygodniowy
–
zalecana początkowa dawka
nasycająca wynosi 8mg/kg m.c.;
zalecana dawka podtrzymująca
powtarzana w
trzytygodniowych odstępach
wynosi 6mg/kg m.c., zaczynając
trzy tygodnie po dawce
nasycającej

EBC podawanie
trastuzumabu
• Schemat tygodniowy
–
początkowa dawka nasycająca
wynosi 4mg/kg m.c.,
a następnie 2mg/kg m.c. co
tydzień, w skojarzeniu z
paklitakselem, po chemioterapii
z użyciem doksorubicyny
i CPA

MGC – podawanie
trastuzumabu
• Schemat tygodniowy- zalecana
dawka nasycająca 8mg/kg m.c.;
zalecana dawka podtrzymująca
6mg/kg m.c. powtarzana w
trzytygodniowych odstępach
zaczynając trzy tygodnie po
dawce nasycającej

Trastuzumab
kardiotoksyczność
• Obserwowano niewydolność mięśnia
sercowego (wg klasyfikacji NYHA –
klasa II – IV) u pacjentów
otrzymujących trastuzumab –
Herceptin w monoterapii, w
skojarzeniu z
paklitakselem lub docetakselem
szczególnie po chemioterapii
zawierającej antracykliny
(doksorubicynę lub epirubicynę)

Trastuzumab
kardiotoksyczność
• t0.5 = 4 – 5 tygodni, może być
obecny w krążeniu około 20 -25
tygodni od zakończenia podawania
• Powinno się unikać stosowania
terapii opartej na antracyklinach w
okresie do 25 tygodni po
zakończeniu leczenia
trastuzumabem (antracykliny też
kardiotoksyczne)

Trastuzumab
kardiotoksyczność
• W przypadku konieczności
zastosowania antracyklin –
wymagane uważne
monitorowanie czynności serca
• Nie powinno się stosować
trastuzumau z antracyklinami
jednocześnie

Trastuzumab reakcje
związane z wlewem
• Objawy grypopodobne (dreszcze,
gorączka)
• Objawy zwykle występują
podczas pierwszego wlewu i w
czasie pierwszych kilku godzin
od jego rozpoczęcia

Trastuzumab zaburzenia
związane z układem
oddechowym
• Nacieki w płucach
• Ostry zespół zaburzeń
oddechowych
• Zapalenie płuc
• Wysięk w opłucnej
• Zaburzenia oddechowe
• Ostry obrzęk płuc
• Niewydolność oddechowa

Rytuksymab
(MabThera)
• Wiąże się swoiście z antygenem
CD20, który jest nieglikozylowaną
fosfioproteiną występującą na
limfocytach pre-B i na dojrzałych
limfocytach B
• Antygen CD20 występuje na
>95% przypadków wszystkich
chłoniaków nieziarniczych (NHL) z
komórek B

Rytuksymab
• Domena Fab cząsteczki
rytuksymabu wiąże się z
antygenem CD20 na limfocytach
B i poprzez domenę Fc
uruchamia mechanizmy układu
odpornościowego prowadzące do
lizy komórek B.

Rytuksymab
• Mechanizmy lizy komórek to:
– CDC
(cytotoksyczność zależna
od układu dopełniacza)
– ADCC
(cytotoksyczność
komórkowa zależna od
przeciwciał

Rytuksymab
•Indukuje apoptozy

Rituximab – zastosowanie
Jest stosowany w agresywnych, nawracających i
uporczywych NHL w kombinacji ze standardowymi
chemioterapeutykami (cyklofosfamid, doxorubicyna,
vinkrystyna i prednison).
Stosowanie tych kombinacji znacznie wydłużyło
okres remisji w porównaniu do pacjentów leczonych
samymi cytostatykami.
Stosowany w białaczkach limfatycznych w kombinacji
z innymi PM lub molekularymi czynnikami
cytotoksycznymi;
próby łączenia z terapia genową i modyfikatorami
odpowiedzi biologicznej.

Rituksymab – działania
niepożądane
• Zespół uwalniania cytokin
(manifestuje się dusznością,
skurczem oskrzeli, gorączką,
dreszczami i obrzękiem
naczynioruchowym
• Zespół rozpadu guza

Rituksymab – działania
niepożądane
• Zespół rozpadu guza – to
zagrażający życiu zespół
zaburzeń metabolicznych
wynikających z szybkiego
rozpadu komórek
nowotworowych

Zespół rozpadu guza
• Nagły rozpad komórek
nowotworowych powoduje
uwalnianie dużych ilości K
+
,
puryn pochodzących z kwasów
nukleinowych (metabolizowanych
w wątrobie do kwasu
moczowego) i
fosforanów

Zespół rozpadu guza
• Skutkiem jest kwasica
metaboliczna, hiperkalemia,
hiperurykemia
i hiperfosfatemia
• Fosforany wiążą we krwi jony Ca
2+
,
co prowadzi do hipokalcemii

Modulatory przekazu
sygnałów
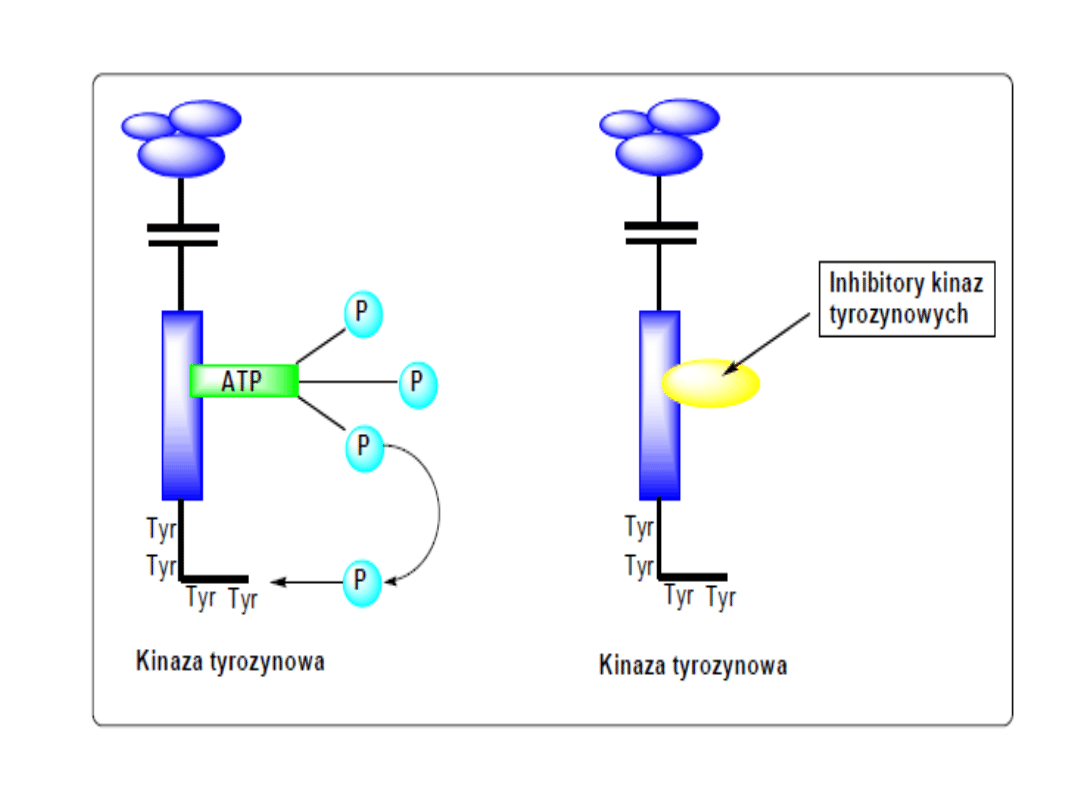

Pazopanib (Votrient)
• Tabletki powlekane
• Tabletka zawiera 200 mg
chlorowodorku pazopanibu

Pazopanib mechanizm
działania
• Inhibitor kinazy tyrozynowej
receptorów naczyniowo-
śródbłonkowego czynnika wzrostu
(VEGFR) -1, -2, -3
• TKI receptora płykowopochodnego
czynnika wzrostu PDGFR-α, -β
• TKI receptora czynnika komórek
macierzystych c-KIT

Pazotynib wskazania
• Leczenie pierwszego rzutu
dorosłych pacjentów z
zaawansowanym rakiem
nerkowokomórkowym (RCC) oraz
leczenie pacjentów u których
wcześniej stosowano cytokiny z
powodu zaawansowanego raka
nerkowokomórkowego (RCC)

Pazopanib
wskazania
• Leczenie dorosłych pacjentów
z zaawansowanymi podtypami
mięsaka tkanek miękkich (STS),
którzy wcześniej otrzymywali
chemię w leczeniu choroby rozsianej
lub u których nastąpiła progresja
choroby w ciągu 12 miesięcy od
leczenia neoadiuwantowego i
adiuwantowego

Pazotynib działania niepożądane
zidentyfikowane w badaniach klinicznych u
pacjentów z RCC i STS
• Przemijające napady niedokrwienne
• Udar niedokrwienny mózgu
• Niedokrwienie mięśnia sercowego
• Zawał serca i mózgu
• Zaburzenia czynności serca
• Perforacje i przetoki w przewodzie
pokarmowym
• (< 1% pacjentów)

Pazotynib działania niepożądane
zidentyfikowane w badaniach
klinicznych u pacjentów z RCC i STS
• Wydłużenie odstępu QT
• Krwotoki z płuc i z przewodu
pokarmowego
• Krwotoki do mózgu
• (< 1% pacjentów)

Działania niepożądane
pazotynibu zidentyfikowane w
badaniach klinicznych u
pacjentów z RCC i STS –
występowały u < 1% leczonych
pacjentów

Pazotynib najczęstsze działania niepożądane
(występowały u co najmniej 10% pacjentów
z RCC i STS)
•
Biegunka, nudności, wymioty
•
Zmiana koloru włosów
•
Hipopigmentacja skóry
•
Złuszczająca wysypka
•
Nadciśnienie tętnicze
•
Ból głowy
•
Uczucie zmęczenia
•
Jadłowstręt
•
Zaburzenia smaku
•
Zapalenie błony śluzowej jamy ustnej
•
Zmniejszenie masy ciała
•
Zwiększenie aktywności aminotransferazy
alaninowej i asparaginianowej
•

Imatinib (Glivec)
• Kapsułki twarde
• Kapsułka zawiera 50 mg
metanosulfonianu imatynibu

Imatinib mechanizm
działania
• Kompetyczyjny inhibitor kinaz
tyrozynowych
• TKI ABL (produkt genu BCR-ABL)
• TKI receptora c-KIT dla czynnika
wzrostu komórek macierzystych
(SCF – Stem Cell Factor)
• TKI receptora dla
płytowopochodnego czynnika
wzrostu (PDGF – Platelet – derived
Growth Factor)

Imatinib wskazania
• Leczenie dorosłych oraz dzieci
i młodzieży z nowo rozpoznaną
przewlekłą białaczką szpikową
(Chronic Myeloid Leukaemia CLL)
z chromosomem
Philadelphia (ber-abl, Ph+),
którzy nie kwalifikują się do
zabiegu transplantacji szpiku jako
leczenia pierwszego rzutu

Imatinib wskazania
• Leczenie dorosłych pacjentów
oraz dzieci i młodzieży z
CMLPh+ w fazie przewlekłej gdy
leczenie interferonem α jest
nieskuteczne lub w fazie
akceleracji choroby lub w
przebiegu przełomu
blastycznego

Imatinib wskazania
• Leczenie dorosłych pacjentów z
nowo rozpoznana ostra białaczką
limfoblastyczną z chromosomem
Philadelphia (Ph+ ALL) w
skojarzeniu z
chemioterapią
• Leczenie dorosłych pacjentów
z nawracającą lub oporną na
leczenie Ph+ALL w monoterapii

Imatinib wskazania
• Leczenie dorosłych pacjentów
z zespołami
mielodysplastycznymi/mieloprolifera
-cyjnymi
(myelodysplastic/myeloproliferate –
MDS/MPD) związanymi z rearanżacją
genu receptorareceptora
płytkopochodnego czynnika wzrostu
PDGFR (platelet derived growth
factor receptor PDGFR)

Imatinib
wskazania
• Leczenie dorosłych pacjentów
z zaawansowanym
zespołem hipereozynofilowym
(Hypereosinophilic syndrom –
HES) i/lub przewlekłą biłaczką
eozynofilową (Chronic
Eosinophilic Leukemia – CEL)
z rearanżacją FIP1L1 -
PDGFRα

Imatinib (Glivec)
dodatkowe wskazania
• Leczenie dorosłych pacjentów ze
złośliwymi nieoperacyjnymi i/lub
z przerzutami Kit (CD117)
dodatnimi nowotworami
podścieliskowymi przewodu
pokarmowego (Gastrointestinal
Stromal Tumor – GITS)

Imatinib dodatkowe
wskazania
• Leczenie adiuwantowe dorosłych
pacjentów z istotnym ryzykiem
nawrotu po zabiegu usunięcia Kit
(CD117) dodatnich nowotworów
podścieliskowych przewodu
pokarmowego (GITS). Pacjenci z
małym lub bardzo małym ryzykiem
nawrotu nie powinni otrzymywać
leczenia adiuwantowego

Imatinib wskazania
• Leczenie dorosłych z
nieoperacyjnymi guzowatymi
włókniakomięsakami skóry
(dermatofibrosarcoma
protuberans – DFSP) oraz
dorosłych pacjentów z
nawracającymi i/lub z przerzutami
DFSP, którzy nie kwalifikują się do
zabiegu chirurgicznego

Środki ostrożności dotyczące
stosowania imatinibu
(Glivec)
Możliwe wystąpienie
zespołu rozpadu guza
(tumor lysis syndrom
TLS).
Przed rozpoczęciem
leczenia zaleca się
leczenie zmniejszające
podwyższone stężenie
kwasu moczowego

Imatinib działania
niepożądane
• Zaburzenia krwi – neutropenia,
trombocytopenia, niedokrwistość
• Zaburzenia układu nerwowego –
ból głowy
• Zaburzenia żołądkowo-jelitowe –
nudności, wymioty, biegunka,
niestrawność, ból brzucha

Imatinib działania
niepożądane
• Zaburzenia skóry – obrzęk
okołonaczyniowy, zapalenie skóry,
wypryski, wysypka
• Zaburzenia mięśniwo-szkieletowe –
skurcze mięśni, bóle mięśniowo-
szkieletowe, w tym bole mięśni, bóle
stawów, bóle kości
• Zatrzymanie płynów, uczucie
zmęczenia
• Zwiększenie masy ciala

Gefitinib (Iressa)
• Tabletki powlekane
• 250 mg gefitinibu w tabletce

Gefitinib mechanizm
działania
• Wysoce selektywny, odwracalny
TKI, domeny związanej z
naskórkowym czynnikiem
wzrostu (EGFR – Epidermal
Growth Factor Receptor)

Gefitinib wskazania
• Leczenie dorosłych pacjentów
z
niedrobnokomórkowym rakiem
płuc (NDRP), miejscowo
zaawansowanym lub z
przerzutami, z uaktywnioną
mutacją EGFR-TK

Gefitinib działania
niepożądane
• Zaburzenia odżywiania – anoreksja
• Zaburzenia żołądkowo-jelitowe –
biegunka
• Zaburzenia wątroby – zwiększenie
aktywności aminotransferazy
alaninowej
• Zaburzenia skórne – reakcje skórne,
wysypka krostkowa na podłożu
rumienia; bardzo rzadko – martwica
toksyczno-rozpływna naskórka

Gefitinib działania
niepożadane
•Rzadko (1% chorych) –
śródmiąższowa choroba
płuc (ILD – Interstinal
Lang Disease)

Erlotinib (Tarceva)
• Tabletki powlekane
• Tabletka zawiera 25 mg
chlorowodorku erlotinibu

Erlotinib mechanizm
działania
•TKI HER1/EGFR

Erlotinib (Tarceva)
wskazania
• Niedrobnokomórkowy rak płuca
(NDRP) – leczenie pierwszego
rzutu pacjentów z NDRP miejscowo
zaawansowanym lub
z przerzutami, z
aktywnymi mutacjami EGFR
• Rak trzustki w skojarzeniu
z gemcytabiną
(pacjenci z przerzutami)

Erlotinib (Tarceva) działania
niepożądane
• Wysypka
• Biegunka
• Jadłowstręt
• Zmęczenie
• Zaburzenia oddychania
• Kaszel
• Nudności, wymioty
• Podatność na infekcje
• Swędzenie skory
• Odnotowano przypadki erytrodyzestezji

Lapatinib (Tyverb)
•Tabletki 250 mg

Lapatinib mechanizm
działania
•TKI EGFR/ErbB1
•HER2/ErbB2

Lapatinib
wskazania
• W połączeniu z kapecytabiną
leczenie zaawansowanego raka
piersi i raka piersi z przerzutami
u pacjentek, u
których wcześniej stosowano
antracykliny, taksany lub
trastuzumab

Lapatinib działania niepożądane w
leczeniu skojarzonym z kapecytabiną
• Biegunki, nudności, wymioty
• Zmęczenie
• Wynaczynienia na dłoniach
i stopach

Sunitinib (Sutent)
• Kapsułki twarde
• Kapsułka zawiera jabłczan
sunitinibu 12.5 mg

Sunitinib mechanizm
działania
• Inhibitor receptorów
śródbłonkowego czynnika
wzrostu (VEGFR-1, -2, -3)
• Inhibitor receptorów czynnika
wzrostu pochodzenia płytkowego
PDGFR-α, -β
• Inhibitor receptorów czynnika
komórek pnia (KIT)

Sunitinib mechanizm
działania
• Inhibitor receptorów czynnika
stymulującego powstawanie
kolonii CSF-1R
• Inhibitor glejopochodnego
czynnika neurotroficznego

Sunitinib wskazania
• Nowotwory podścieliskowe
przewodu pokarmowego (GIST –
Gastrointestinal Stromal Tumor)
• Nowotwory nieoperacyjne i/lub
z przerzutami u
dorosłych po niepowodzeniu
leczenia imatinibem ze względu
na oporność lub nietolerancję

Sunitinib wskazania
• Rak nerki zaawansowany i/lub z
przerzutami (MRCC, Metastatic
Renal Cell Carcinoma)
• Nowotwory neuroendokrynne
trzustki (pNET – Pancreatic
Neuroendocrine Tumors)
• Wysoko zróżnicowane nowotwory
pNET nieoperacyjne lub z
przerzutami

Sunitinib działania
niepożądane
• Niewydolność mięśnia sercowego
• Krwawienia
• Nadciśnienie
• Zaburzenia oddychania
• Biegunka, wymioty, zaparcia

Sorafenib
• Tabletki powlekane
• Tabletka zawiera 200 mg
tozylanu sorafenibu

Sorafenib
•CRAF, BRAF
•C-KIT
•VEGFR-2, -3

Sorafenib -
wskazania
•Zaawansowany rak
nerki

Sorafenib działania
niepożadane
• Limfopenia
• Hipofosfatemia
• Zaburzenia żołądkowo-jelitowe –
biegunki, nudności, wymioty
• Zaburzenia skóry –
erytrodyzestezja dłoniowo-
podeszwowa
• Zaburzenia ogólne - osłabienie

Wemurafenib (Zelboraf
)
• Tabletki powlekane
• Tabletka zawiera 240 mg
wemurafenibu (koprecypitat
wemurafenibu i
octano-bursztynian
hypromelozy)

Wemurafenib mechanizm
działania
• Drobnocząsteczkowy inhibitor kinazy
serynowo-treoninowej BRAF
• Mutacje genu BRAF dotyczące
kodonu 600 powodują konstytutywną
aktywację białek BRAF, co może
prowadzić do proliferacji komórki,
przy nieobecności czynników
niezbędnych w
prawidłowych warunkach

Wemurafenib
wskazania
• Monoterapia dorosłych chorych
na nieresekcyjnego lub z
przerzutami czerniaka
wykazującego mutację
BRAF V600

Wemurafenib działania
niepożądane (>30%)
• Bóle stawów
• Zmęczenie
• Wysypka
• Nadwrażliwość na światło
• Łysienie
• Świąd
• Bardzo często obserwowano przypadki
raka kolczystokomórkowego skóry;
najczęściej stosowanym leczeniem
było miejscowe wycięcie zmiany
• Zespół ręka-stopa
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
- Slide 97
- Slide 98
- Slide 99
- Slide 100
- Slide 101
- Slide 102
- Slide 103
- Slide 104
- Slide 105
- Slide 106
- Slide 107
- Slide 108
- Slide 109
- Slide 110
- Slide 111
- Slide 112
- Slide 113
- Slide 114
- Slide 115
- Slide 116
- Slide 117
- Slide 118
- Slide 119
- Slide 120
Wyszukiwarka
Podobne podstrony:
Leczenie wrzodziejacego zapalenia jelit, wyklad 2013
Socjologia Ogólna wykłady (2013), dr A Roter
Podatki w Działalności Gospodarczej wykłady 2013 03 16
Pedagogika ogolna wyklady 2013 Nieznany
Ekonometria II wykład 5 2013
Gleboznawstwo.GiK.Pytania.Wykłady 2013 MOJE, geodezja i kartografia PW
NOTATKI WYKLAD2 2013 03 09
patomorfa wykłady 2013 2014 1
Mikroekonomia wykład 8 9 2013
NOTATKI WYKLADI 2013 03 09
PPPiPU wykłady (2013 14)
Podatki w Działalności Gospodarczej wykłady 2013 04 06
materialy dla studentow wyklad 2
MS PiUP Wyklad 2013 01 17
Energoelektronika wykłady2 2013
Sekurytyzacja-Sroczyńska-Baron - Wykłady 2013, UE KATOWICE, Sekurytyzacja aktywów
Wykład 1 + program wykładów PROGRAM WYKŁADÓW 2013
więcej podobnych podstron