
Co to jest NMR
Spektroskopia NMR -
Spektroskopia
Magnetycznego Rezonansu Jądrowego
(ang. Nuclear Magnetic Resonance)
Potocznie w języku polskim: rezonans
magnetyczny.
Jedna z najczęściej stosowanych obecnie
technik spektroskopowych w chemii i
medycynie.

Historia NMR
Teoretycy przewidzieli zjawisko NMR już dość wcześnie, bo tuż po I
Wojnie Światowej. Ze względu jednak na kłopoty techniczne
doświadczalnego potwierdzenia tych przewidywań dokonano dopiero
tuż po II Wojnie Światowej. Uczyniły to w 1945 r. równocześnie dwie
grupy uczonych: z Uniwersytetu Stanfort i z Uniwersytetu Harvard.
Rezonansem początkowo zajmowali się głównie fizycy, jednak z
momentem odkrycia przesunięcia chemicznego - rok 1950 -
stał on się domeną chemików.
W roku 1953 amerykańska firma
VARIAN
wyprodukowała pierwsze
komercyjne urządzenie służące do wykonywania widm tzw.
rezonansu magnetycznego o wysokiej zdolności rozdzielczej zwane
spektrometrem NMR. Rok 1966 to data przełomowa dla NMR -
profesor
Ernst
ulepsza metodę detekcji sygnału NMR wykorzystując
matematyczną operację zwaną transformacją Fouriera (dostał za to
Nagrodę Nobla w 1991 r.).

Nobel 1952 (Fizyka)
"for their development of new methods for
nuclear magnetic precision measurements and
discoveries in connection therewith"
Felix Bloch
Stanford University
Edward Mills Purcell
Harvard University
Charakter metody
• NMR to metoda:
– spektroskopowa
h
1
E
1
E
2
h
2
absorpcj
a
źródło
promieniowania
obserwacja
Spektroskopia NMR polega na wzbudzaniu spinów
jądrowych znajdujących się w zewnętrznym polu
magnetycznym poprzez wiązkę fal elektromagnetycznych,
a następnie rejestrację promieniowania
elektromagnetycznego powstającego na skutek zjawisk
relaksacji, gdzie przez relaksację rozumiemy powrót układu
spinów jądrowych do stanu równowagi termodynamicznej.
NMR jest zatem jedną ze spektroskopii absorpcyjnych.

Warunkiem obserwacji
oddziaływania
materii
z
promieniowaniem
elektromagnetycznym
jest
absorpcja energii

Aby nastąpiła absorpcja energii
...
• Konieczne jest zróżnicowanie stanów energetycznych
(tj. cząsteczki muszą mieć możliwość przebywania w
stanach o niższej i wyższej energii)
• Konieczne jest istnienie cząsteczek w stanie zdolnym
przyjąć energię (tj. niewzbudzonych)
• Kwant promieniowania elektromagnetycznego
niosącego tę energię musi być taki sam jak różnica
energii pomiędzy stanem przed i po wzbudzeniu

Przejście pomiędzy jakimi
poziomami energetycznymi
cząsteczki można uzyskać
napromieniowując ją
promieniowaniem o
częstości
fal radiowych
?
Nie ma takich poziomów

Jądro atomowe posiada spin
spin
• spin może przyjmować różne wartości dla różnych jąder (dla jądra danego
nuklidu jest zawsze taki sam)
• ze spinem związana jest
jądrowa kwantowa liczba spinowa I
, która przyjmuje
wartości całkowite lub połówkowe t.j. 0, 1, 2, … lub 1/2, 3/2, 5/2, …
• ze spinem związany jest
moment magnetyczny μ
• wielkość momentu magnetycznego jest kwantowana (przyjmuje tylko
niektóre, dyskretnie zadane wartości)
magnetyczną liczbą spinową m
I
= I, I-1,
I-2,…, -I
• jądrowy moment magnetyczny oddziałuje z zewnętrznym polem
magnetycznym
• energia tego oddziaływania jest proporcjonalna do wielkości momentu
magnetycznego
• w polu magnetycznym następuje zróżnicowanie energii stanów jądra
(zniesienie degeneracji) ze względu na m
I
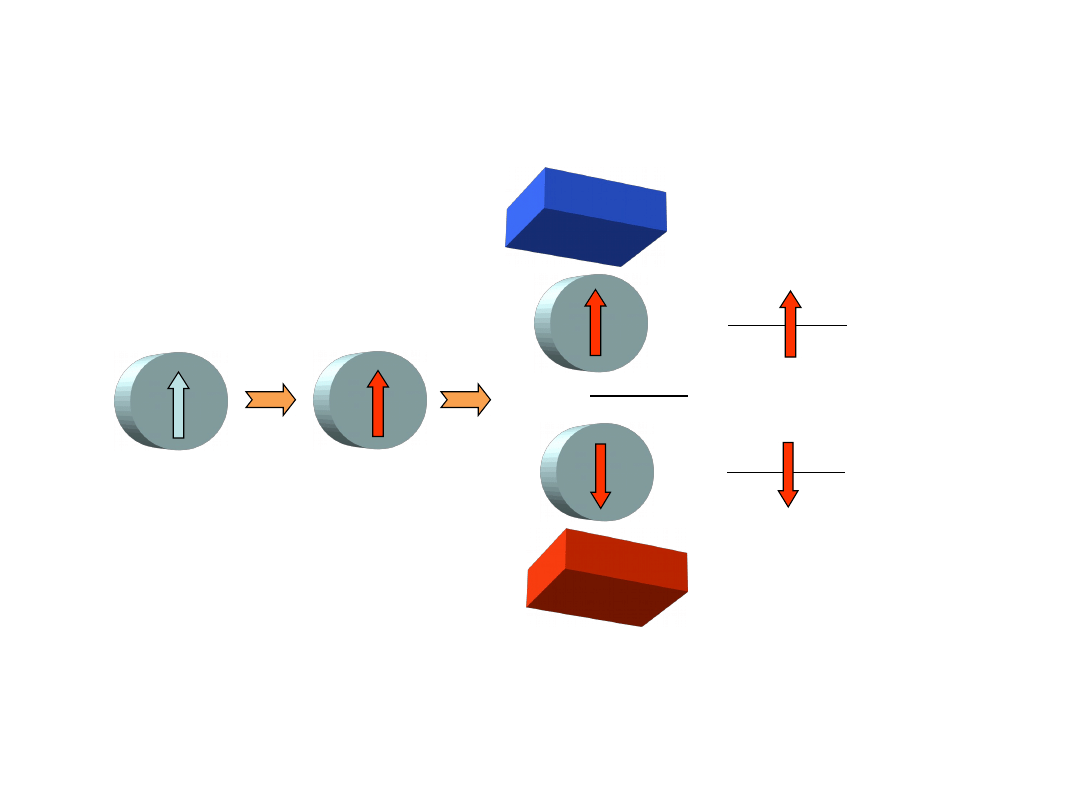
Jądro atomowe posiada spin
spin
SPIN
I
ħ
MOMENT
MAGNETYCZNY
ħ
I
S
N
ħ
I
B
-
ħ
I
B
ZRÓŻNICOWANIE
ENERGII
POLE
MAGNETYCZNE
O INDUKCJI B
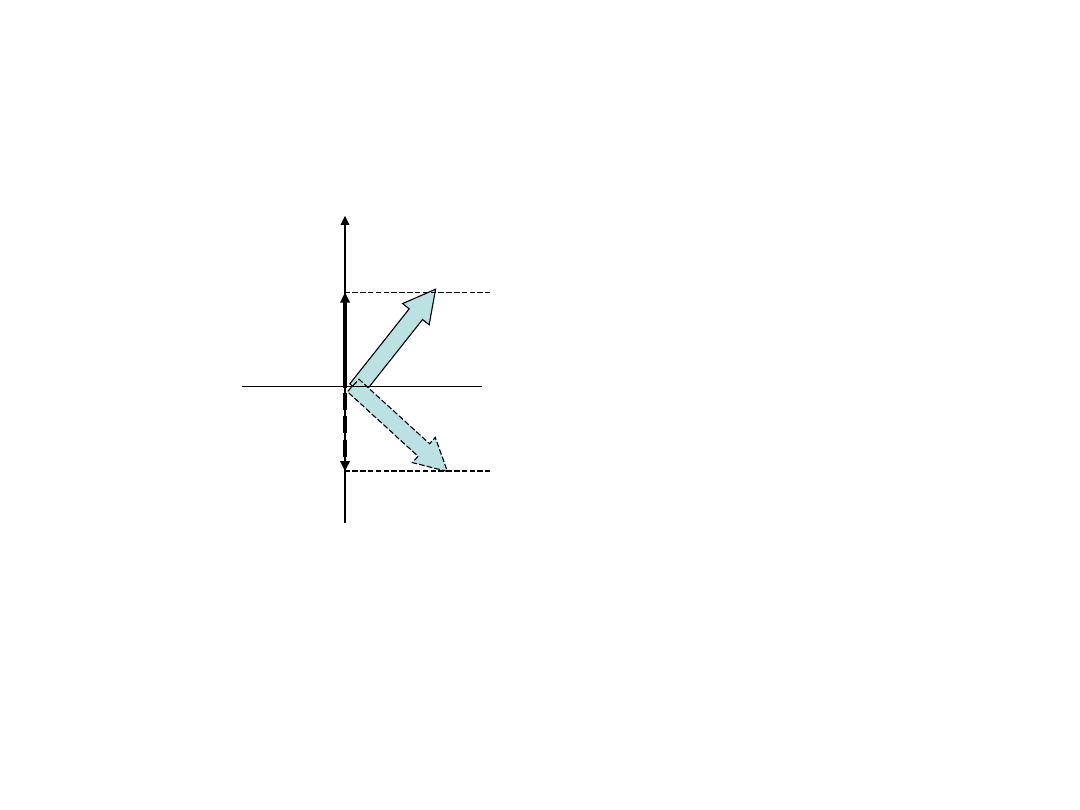
JĄDRO ATOMOWE W POLU
MAGNETYCZNYM
μ
B
o
μ
z
m
I
= -
½
m
I
= ½
E = - μ
z
B
0
E = μ
z
B
0
Degeneracja stanów spinowych jądra
została zniesiona przez pole
magnetyczne.
Różnica energii
E = 2 μ
z
B
0
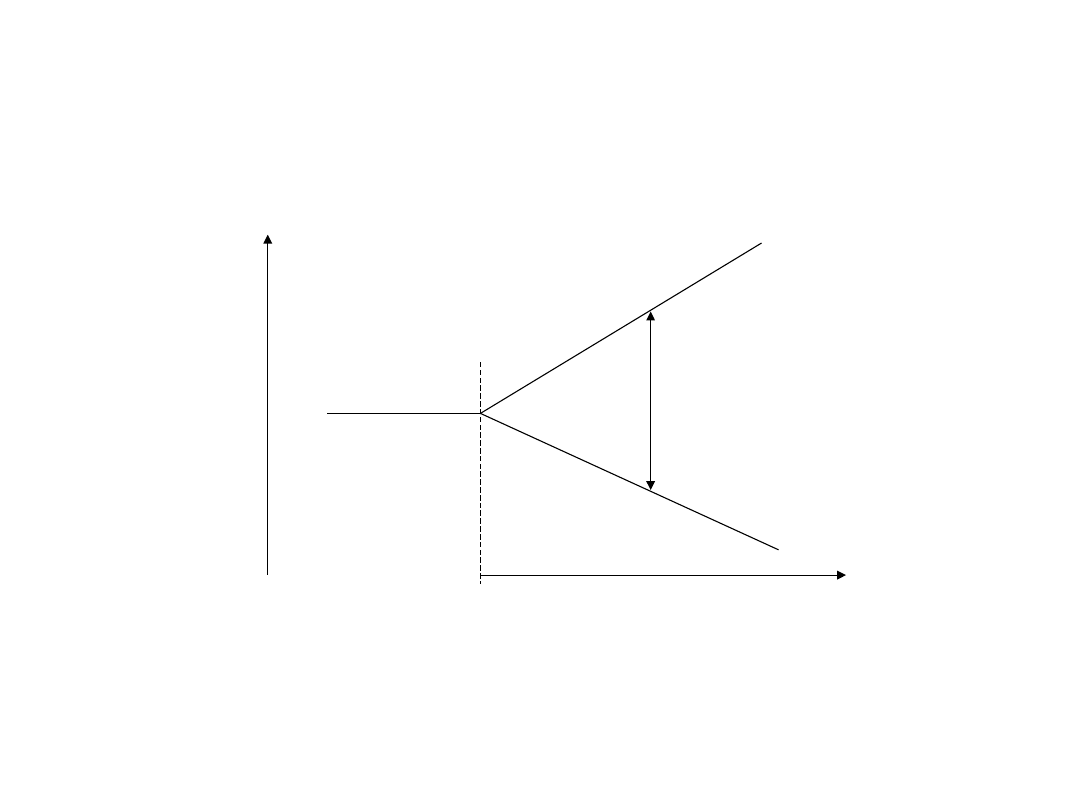
JĄDRO ATOMOWE W POLU
MAGNETYCZNYM
E
B
0
= 0
B
0
> 0
E
m
I
= -
½
m
I
= ½
(degeneracja)
(zniesienie
degeneracji)

Rezonans
• Absorpcja energii niesionej przez promieniowanie
elektromagnetyczne może zaistnieć dzięki energetycznemu
zróżnicowaniu jądrowych stanów spinowych wywołanemu
przez zewnętrzne pole magnetyczne.
• Promieniowanie elektromagnetyczne o częstości niesie
energię kwantu h.
• Aby nastąpiła absorpcja musi być spełniony warunek E =
h
• W przypadku jądra atomowego w polu magnetycznym B
0
:
h
0
= 2μ
z
B
0
=
ħB
0
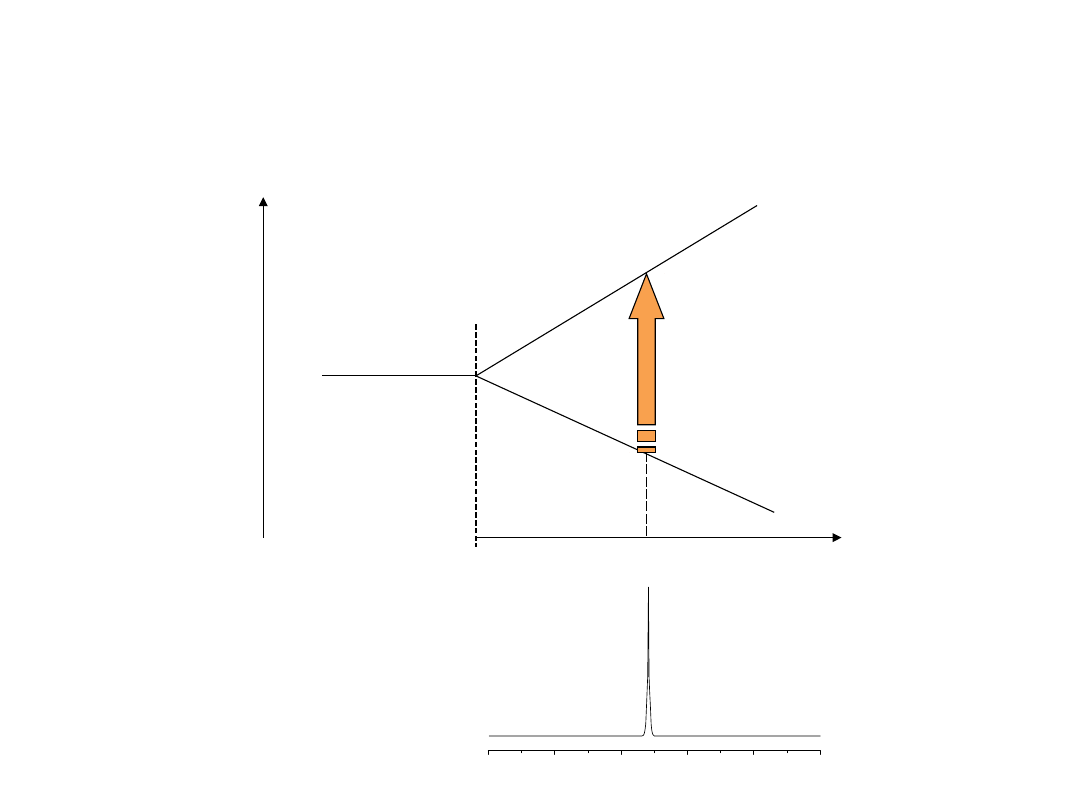
Warunek rezonansu
E
B
0
m
I
= -
½
m
I
= ½
E =
ħB
0
=
h
0
h
0
0
1
2
3
4
5
B

Niektóre jądra w polu magnetycznym ustawiają się zarówno
równolegle do linii pola (co nas nie dziwi - bo tak właśnie zachowuje się
igła magnetyczna w kompasie) jak i antyrównolegle. Oba ustawienia
różnią się tylko nieznacznie energią i dlatego tylko niewiele więcej
jąder jest ustawionych równolegle, niż antyrównolegle do linii pola
magnetycznego.
Stosunek ilości jąder ustawionych równolegle do ustawionych
antyrownolegle do linii pola zależy od rodzaju jądra (bardzo), natężenia
pola magnetycznego (tez bardzo) i od temperatury (niewiele).
W temperaturze 25
o
C i w polu o indukcji jednej tesli (1T) na każde 20
000 000 jąder wodoru ustawionych równolegle do linii pola przypadają
19 999 932 jąder ustawionych antyrownolegle.
To wyjaśnia dlaczego doświadczalnego potwierdzenia zjawiska
rezonansu dokonano dopiero w 25 lat po jego teoretycznym odkryciu -
po prostu potrzeba do tego aparatury o niewyobrażalnej wręcz
czułości.
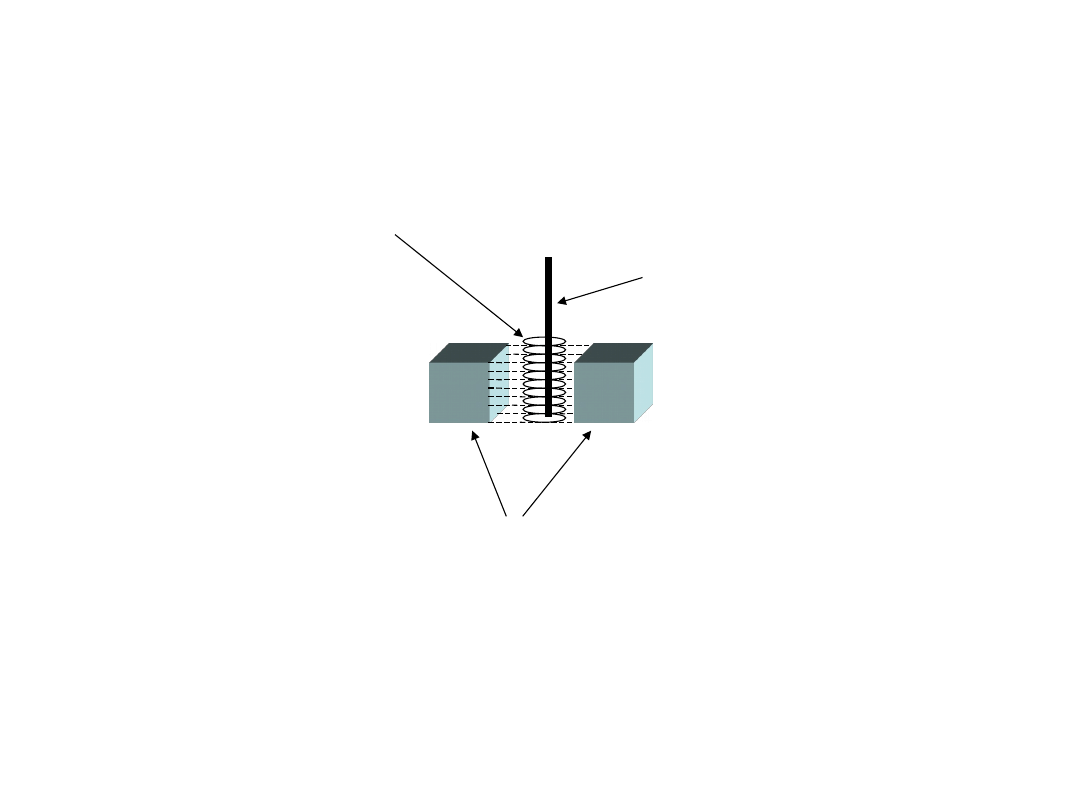
Schemat ideowy spektrometru
NMR
N
S
probówka
pomiarowa
układ cewek nadawczo-
odbiorczych
magnes
B
o
0
Choć do warunku rezonansu można dochodzić zarówno przez zmianę
częstości dla próbki w stałym polu magnetycznym jak i przez zmianę pola
przy stałej częstości, to we współczesnych spektrometrach stosowany jest
praktycznie tylko pierwszy z tych sposobów.

Do 1966r. spektrometry NMR rejestrowały widma tzw. metodą
metodą
fali ciągłej
fali ciągłej
. W stabilnym polu magnetycznym generowanym
przez dwa magnesy sztabkowe umieszczano próbkę.
Następnie generowano promieniowanie elektromagnetyczne o
liniowo zmieniającej się częstotliwości i obserwowano kiedy
zajdzie absorpcja.
Metoda ta miała jednak wiele wad.
Po pierwsze, średni czas rejestracji podstawowego widma
protonowego (jest to najprostszy do obserwacji i najczęściej
stosowany rezonans) wynosił nawet pół godziny lub dłużej. Po
drugie metody tej nie dało się zastosować do innych jąder
dających słabszy sygnał, bądź o mniejszym
rozpowszechnieniu w przyrodzie.
Pierwszym krokiem do zwiększenia czułości metody było
generowanie silniejszego pola magnetycznego - zastosowano
elektromagnesy. Zwiększenie pola powoduje, że różnica liczby
spinów ustawionych równolegle do pola i antyrównolegle
zwiększa się (jest to praktycznie zależność liniowa), a wiec
liczba jąder dających sygnał również zwiększa się. Metoda ta
jednak była mało skuteczna. Mocy magnesów nie dało się
zwiększyć aż tak znacznie, aby była możliwa obserwacja jąder
mało czułych izotopów. Węgiel 13C tak potrzebny chemikom
organikom był ciągle poza zasięgiem NMR-u.
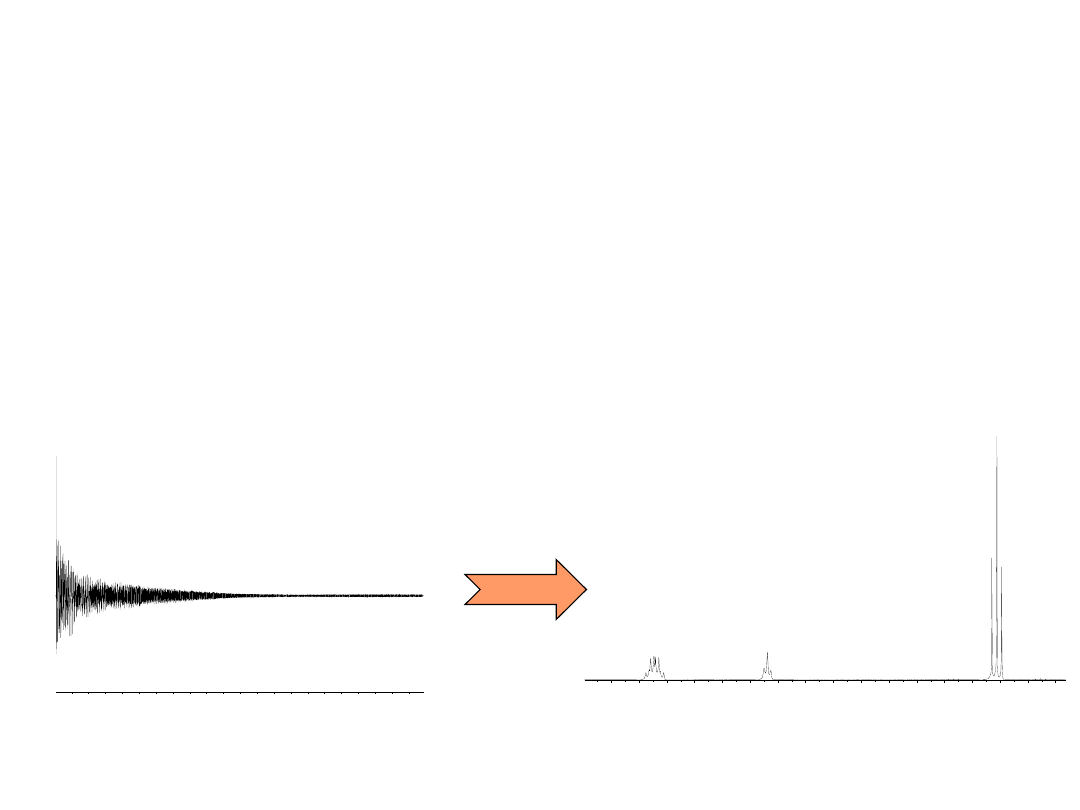
Prawdziwy przełom spowodowało odkrycie profesora Ernsta w
1966r. Wpadł on na pomysł tzw. impulsowej metody rejestracji
widm. Polega ona na tym, że próbkę umieszczoną w
jednorodnym polu magnetycznym naświetlamy na raz całym
zakresem częstotliwości, a potem w ciągu kilku sekund
zbieramy widmo. Widmo takie nie jest niestety dla nas
zrozumiale w postaci "surowej". Zebrane informacje musimy
poddać pewnym matematycznym przekształceniom (zwanym
transformacja Fouriera) aby otrzymać widmo takie jak przy
rejestracji metodą fali ciągłej.
(sec)
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
(ppm)
0.8
1.0
1.2
1.4
1.6
1.8
2.0
2.2
2.4
2.6
2.8
3.0
3.2
3.4
3.6
3.8
4.0

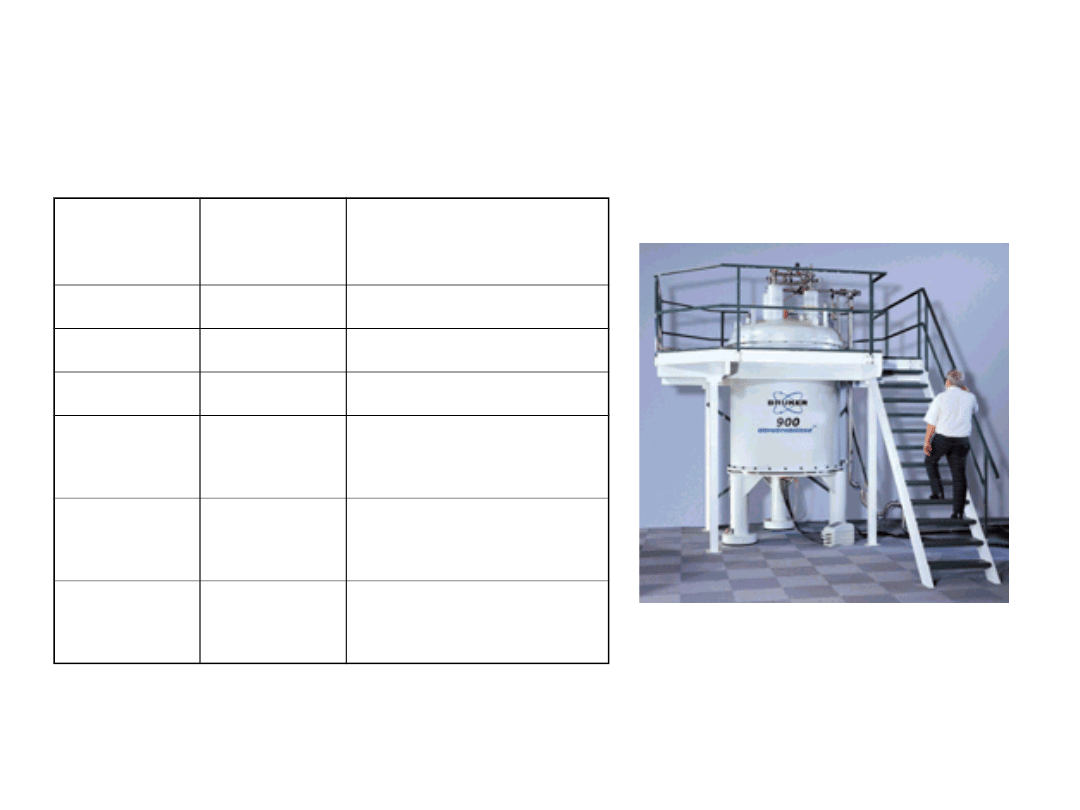
Kolejnym krokiem w NMR było wynalezienie magnesów
nadprzewodzących, pozwalających generować pola
magnetyczne nawet dziesięciokrotnie silniejsze niż pola
pochodzące z elektromagnesów. Sam w sobie taki magnes jest
cudem techniki. Solenoid z kilku kilometrów drutu miedzianego z
wtopionymi nadprzewodzącymi żyłkami zanurzony w ciekłym
helu (temp. wrzenia -269
o
C) zamknięty w płaszczu próżniowym
otoczonym ciekłym azotem i następnym płaszczem próżniowym
generuje w całej objętości próbki prawie idealnie jednorodne
pole o natężeniu ponad 20T. Magnes taki wygląda jak beczka o
wysokości 2m, średnicy około 120cm i wadze dochodzącej do
600kg.
Drugim co do ważności elementem konstrukcyjnym tego
urządzenia jest tzw. sonda. Jest to element umieszczany w
środku magnesu i służący do generowania fali
elektromagnetycznej oraz do "zbierania" sygnału.
Stosowane magnesy
B
o
[T]
o
(H)
[MHz]
typ
1.4
60
elektromagnes
2.3
100
elektromagnes
7
300
nadprzewodzący
11
500
nadprzewodzący
14
600
nadprzewodzący
21
900
nadprzewodzący

Warunek stosowalności metody
• Aby nastąpiło zróżnicowanie energetyczne
stanów spinowych musi być tych stanów
więcej niż jeden.
• Zróżnicowanie stanów jest możliwe tylko
dla spinu jądrowego różnego od zera, czyli
dla jąder atomowych tylko tych nuklidów,
dla których spinowa liczba kwantowa
I > 0
Jądra atomowe o niezerowym spinie
nazywa się
jądrami magnetycznymi.

Skład jądra atomowego a spin
jądrowy
• Dla parzystych Z i A
I
= 0
• Dla nieparzystej Z i parzystej A
I
jest liczbą
całkowitą
• Dla nieparzystych Z i A oraz parzystej Z i
nieparzystej A
I
jest całkowitą wielokrotnością ½
E
A
Z

Nuklid
Naturalna
zawartość [%]
Spin I
[ħ]
Częstość
rezonansowa
o
[MHz]
przy indukcji 2.35 T
Względna
czułość
Elektryczny moment
kwadrupolowy [e 10
-
26
cm
2
]
1
H
99.98
1/2
100
1.00
-
2
H
0.016
1
15.35
0.01
0.277
10
B
18.82
3
9.305
0.02
11.1
11
B
81.17
3/2
31.17
0.165
3.55
13
C
1.108
1/2
25.19
0.016
-
14
N
99.63
1
7.22
0.001
2.0
15
N
0.37
1/2
10.13
0.001
-
17
O
0.037
5/2
13.56
0.03
–0.4
19
F
100
1/2
94.08
0.83
-
27
Al
100
5/2
26.06
0.21
14.9
29
Si
4.67
1/2
19.86
0.08
-
31
P
100
1/2
40.48
0.07
-
33
S
0.74
3/2
7.67
0.0023
–6.4
35
Cl
75.5
3/2
9.80
0.0047
–8.0
37
Cl
24.5
3/2
8.15
0.0027
–6.2
117
Sn
7.62
1/2
35.62
0.045
-
119
Sn
8.68
1/2
37.27
0.052
-
195
Pt
33.7
1/2
21.50
0.01
-
199
Hg
16.9
1/2
17.88
0.0057
-
203
Tl
29.5
1/2
57.14
0.19
-
205
Tl
70.5
1/2
57.71
0.19
-
207
Pb
21.11
1/2
20.90
0.01
-

Charakter metody
• NMR to metoda:
– Spektroskopowa
– Rezonansowa
– Analityczna
Z warunku rezonansu można wywieść, że jądra
atomowe
różnych
nuklidów o niezerowym spinie
będą absorbować kwant energii promieniowania o
danej częstości
0
przy
różnej
wartości indukcji
magnetycznej
B
0
oraz jądra atomowe
różnych
nuklidów o niezerowym spinie przy danej wartości
indukcji magnetycznej
B
0
będą absorbować kwanty
energii promieniowania o
różnej
częstości
0
(tzw.
częstości podstawowej jądra
).
E =
ħB
0
=
h
0
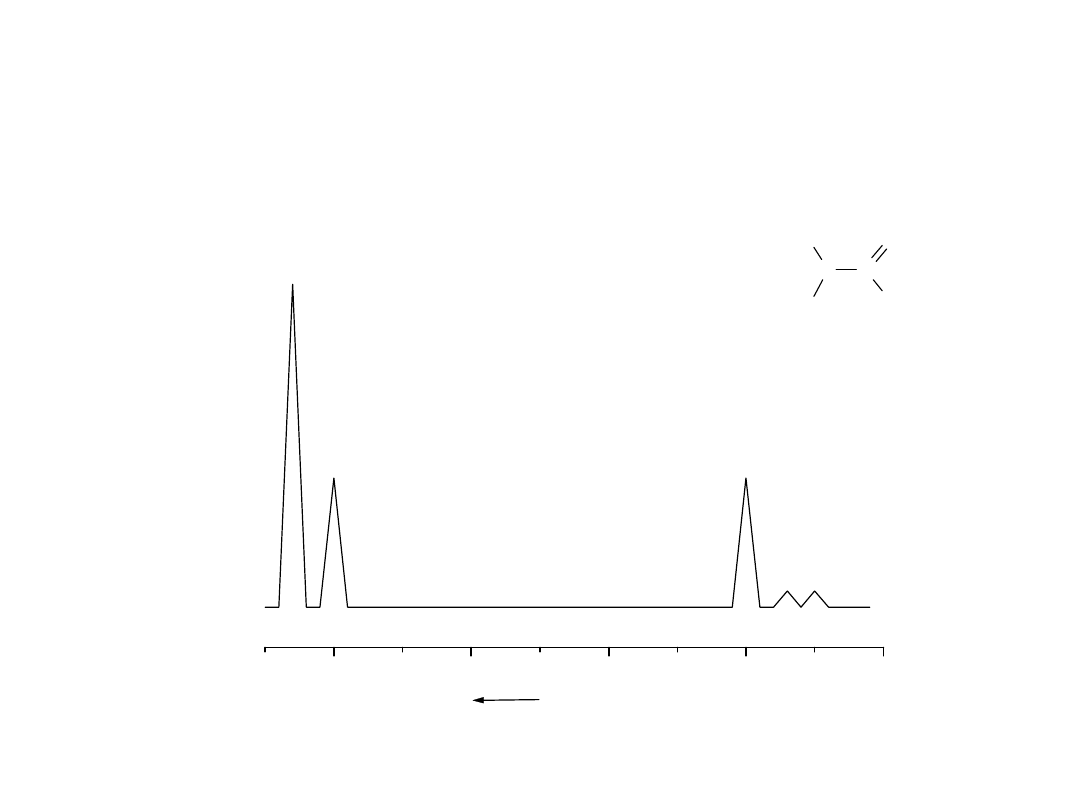
(Bardzo) Hipotetyczne widmo
multijądrowe
40
30
20
10
0
B
o
= 1 T
15
N
17
O
13
C
19
F
1
H
[MHz]
N C
O
CF
3
H
3
C
H
3
C

Spektroskopia NMR wysokiej
rozdzielczości
• Eksperymenty NMR wykonuje się dla danego typu jądra
(np.
1
H,
13
C,
31
P)
• Warunek rezonansu jest dla danego typu jądra spełniony
przy częstościach w pobliżu
0
,
a nie dokładnie przy tej
wartości
• Dla jądra danego typu rezonans może następować przy
różnych częstościach
zależnie od związku, w którym się
to jądro znajduje
• W danym związku chemicznym częstości rezonansowe
jąder tego samego typu mogą być różne (jądra mogą być
magnetycznie nierównoważne
)

Źródło zróżnicowania częstości
rezonansowych jąder danego
typu
• Jądro atomowe umieszczone w związku
chemicznym jest fragmentem złożonego
układu innych jąder i
chmur elektronowych
,
które znajdują się pomiędzy danym jądrem i
zewnętrznym polem magnetycznym.
• Zewnętrzne pole magnetyczne B
0
indukuje w
chmurze elektronowej prąd kołowy, z którym
związane jest pole magnetyczne skierowane
przeciwnie
do B
0
. Lokalne natężenie pola
magnetycznego wokół jądra jest zatem
zmniejszone o wartość proporcjonalną do B
0
.
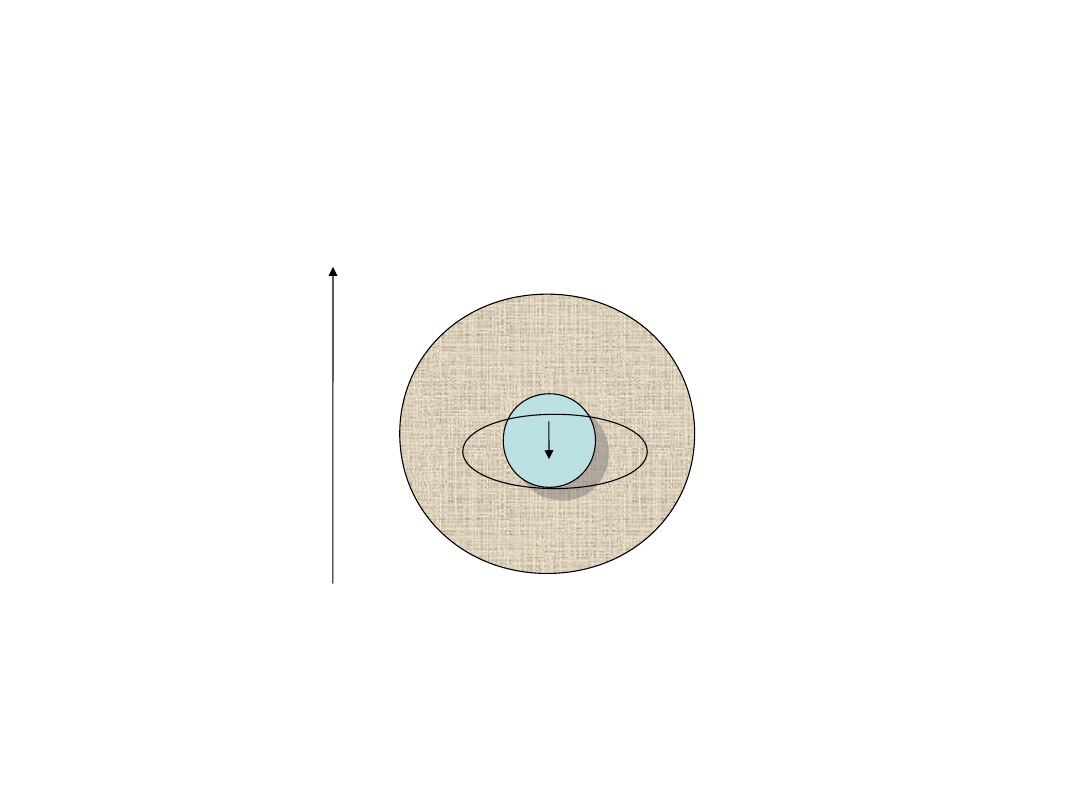
Elektrony wokół jądra
modyfikują pole magnetyczne
B
0
B
0
B
lok
= B
0
(1 - )
- stała ekranowania (przesłaniania)

Warunek rezonansu
• W wyniku przesłaniania jądra do spełnienia
warunku rezonansu konieczne jest albo większe
natężenie pola (przy danej częstości) albo mniejsza
częstotliwość (przy danym polu) niż by to wynikało
z warunku rezonansu obliczonego dla B
o
i
o
danego
jądra.
• Modyfikacja pola magnetycznego w punkcie jądra
zależy od wielkości
gęstości elektronowej
w
otoczeniu jądra czyli w danym atomie cząsteczki.
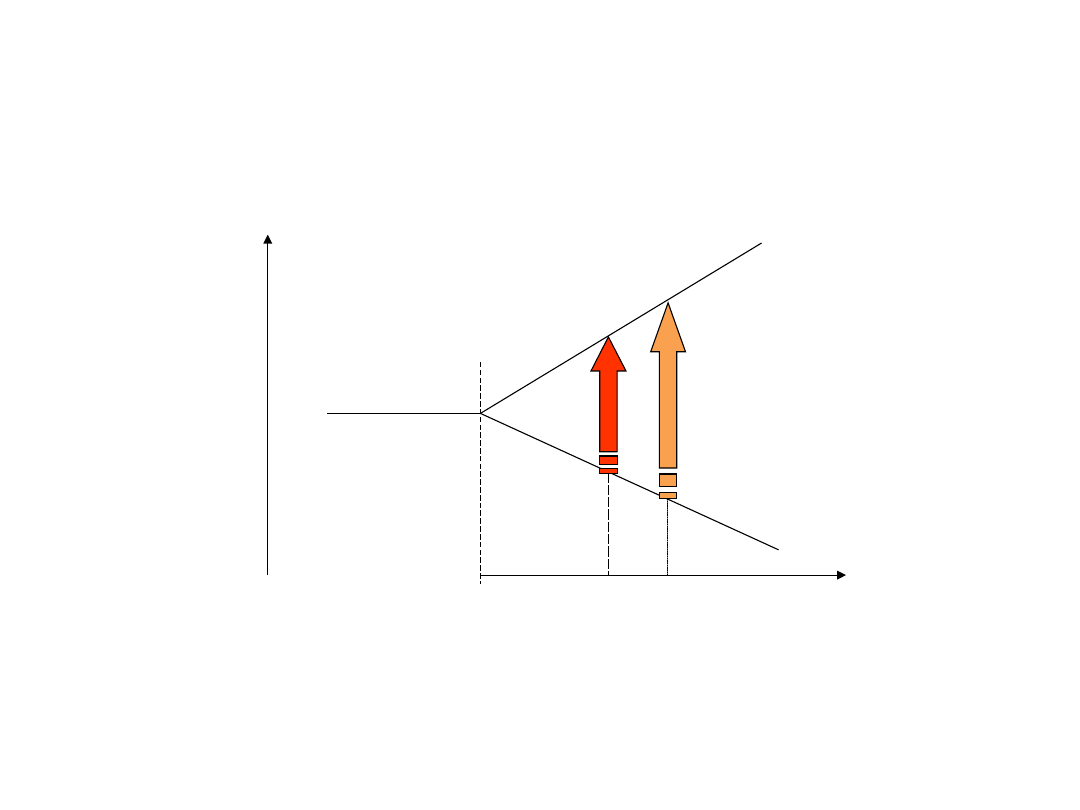
Warunek rezonansu
- przesunięcie chemiczne -
E
B
lok
B
0
m
I
= -
½
m
I
= ½
E
1
=
ħB
0
= h
0
E
2
=
ħB
lok
= h
h
0
h

Przesunięcie chemiczne
• Różnica pomiędzy częstością
rezonansową jądra w konkretnym
otoczeniu a częstością podstawową
o
dla jądra tego typu nazywa się
przesunięciem chemicznym.
• Zakres przesunięć chemicznych dla
jąder danego typu jest rzędu 0.1-10 kHz

Widmo NMR
•Wykres zależności intensywności absorpcji od
częstości rezonansowej nazywa się widmem
NMR.
•Dla substancji zawierającej różne jądra
magnetyczne można otrzymać różne widma
NMR zależnie od rodzaju pobudzanego jądra,
czyli zastosowanej częstości podstawowej
o
przy danym natężeniu pola magnetycznego B
0
np.:
B
0
= 7 T
o
= 300 MHz dla
1
H
i 75 MHz dla
13
C
B
0
= 11 T
o
= 500 MHz dla
1
H
i 126 MHz dla
13
C
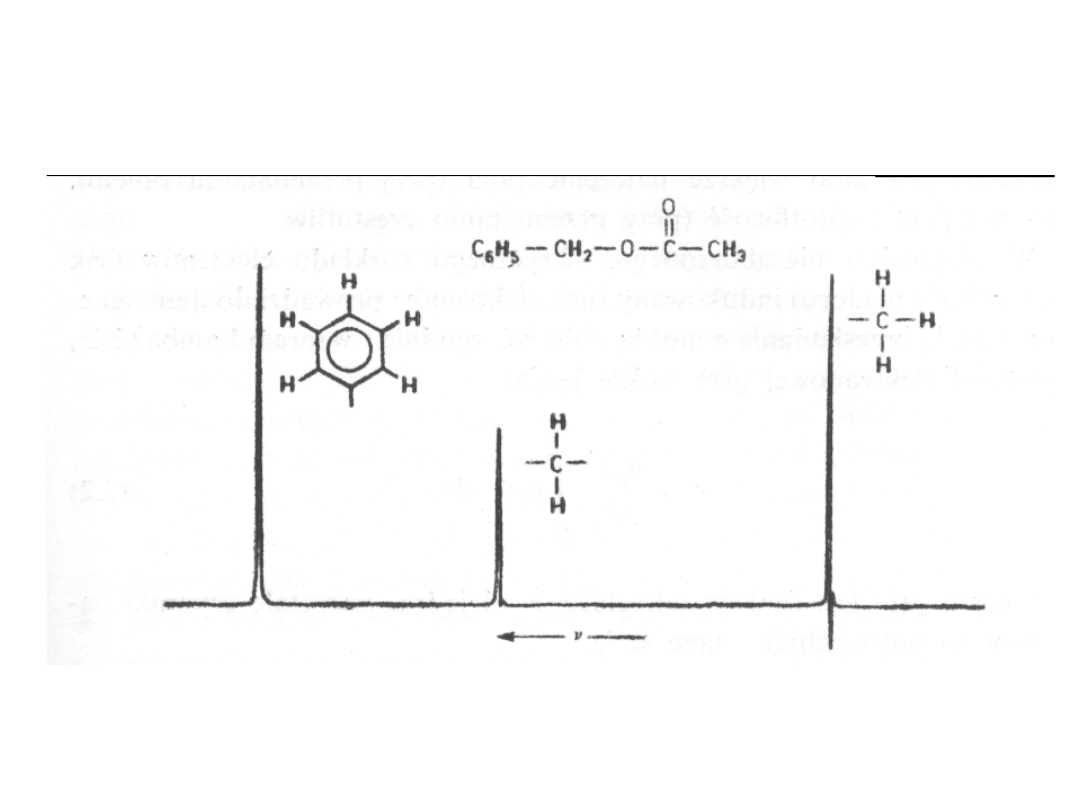
Typowe widmo
1
H NMR
116 Hz
193 Hz
965 Hz
300 Hz
500 Hz
2500 Hz
433 Hz
721 Hz
3605 Hz
1.4 T
1.4 T
2.3 T
2.3 T
11.1 T
11.1 T
B
B
0
0

Przesunięcie chemiczne
Ze względu na różne wartości stosowanej indukcji
magnetycznej B w różnych spektrometrach oraz
trudności w precyzyjnym wyznaczaniu częstości
rezonansowych skala przesunięć chemicznych
określana jest według częstości rezonansowej wzorca i
normalizowana do wartości bezwymiarowej
:
„Jednostką” tak zdefiniowanej skali przesunięć jest
ppm
(części na milion –
p
arts
p
er
m
illion)
0
wz
ν
ν
ν
δ
10
Hz
Hz
6
-
8
2
10
10
δ]
[
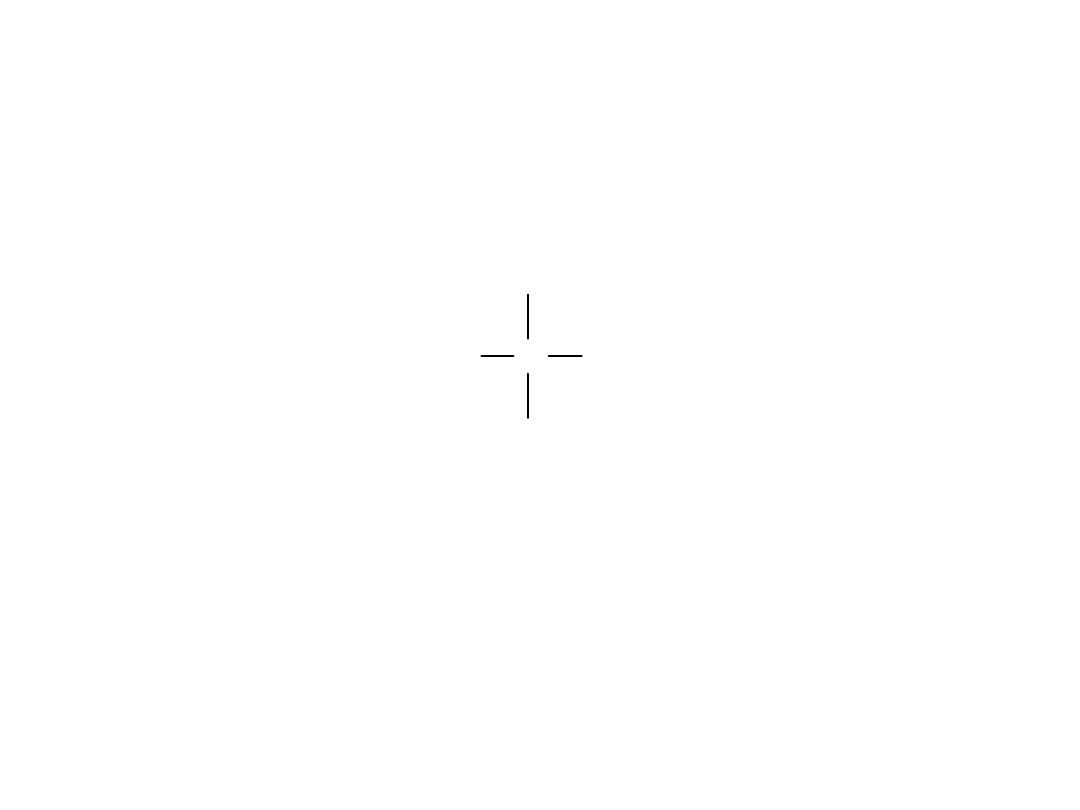
Wzorzec przesunięcia
chemicznego dla
1
H i
13
C
CH
3
Si
CH
3
CH
3
H
3
C
Tetrametylosilan
TMS
≡ 0
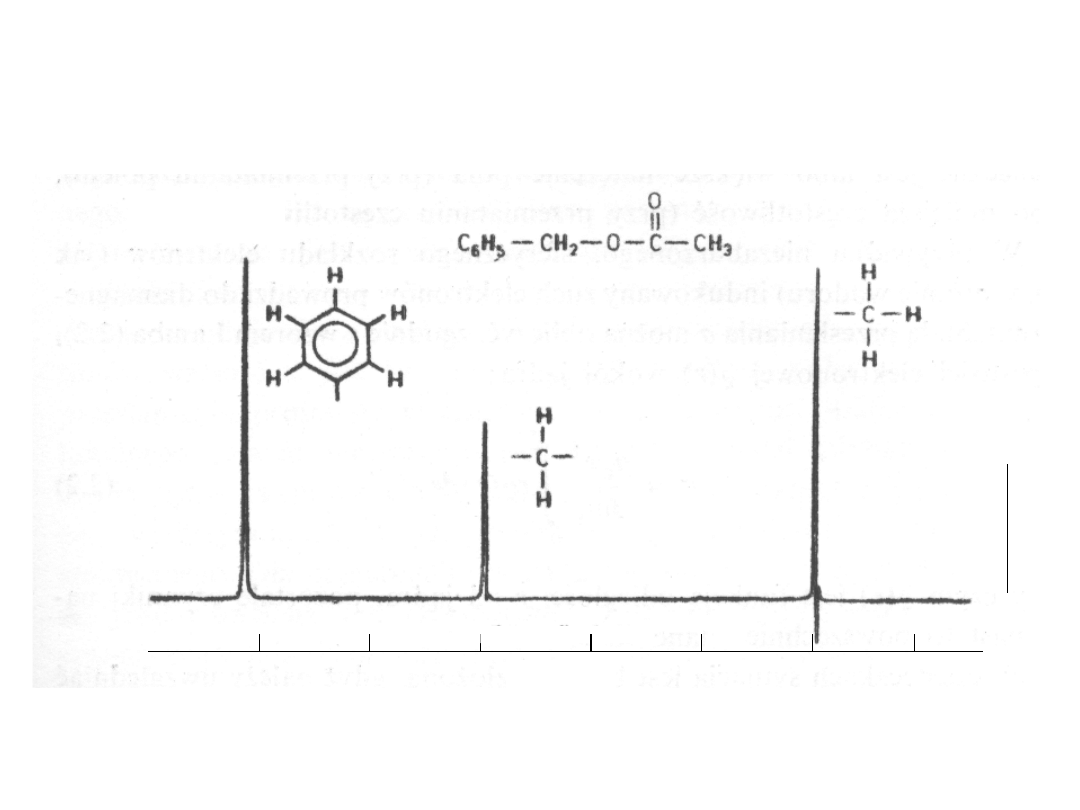
Typowe widmo
1
H NMR
7 6 5 4 3 2
1
Si(CH
3
)
4
(TMS)
= 0
Wartości przesunięć chemicznych
dla danego związku
nie zależą
od
natężenia zastosowanego pola magnetycznego B
0

Przesunięcie chemiczne
• Wartość przesunięcia chemicznego
jest bardzo
silnie zdeterminowana przez otoczenie i
jednoznacznie określa pozycję jądra w związku.
• Wartość przesunięcia chemicznego jądra w danym
otoczeniu chemicznym zawiera się w granicach
charakterystycznych dla tego otoczenia.
• Jądra atomowe danego typu, należące do danej
grupy chemicznej (np. węglowodorowej,
karbonylowej, hydroksylowej, karboksylowej),
rezonują w typowych dla tych grup zakresach
przesunięć chemicznych, więc ich przesunięcia
chemiczne
w różnych związkach będą podobne i
mogą stanowić kryterium analityczne.
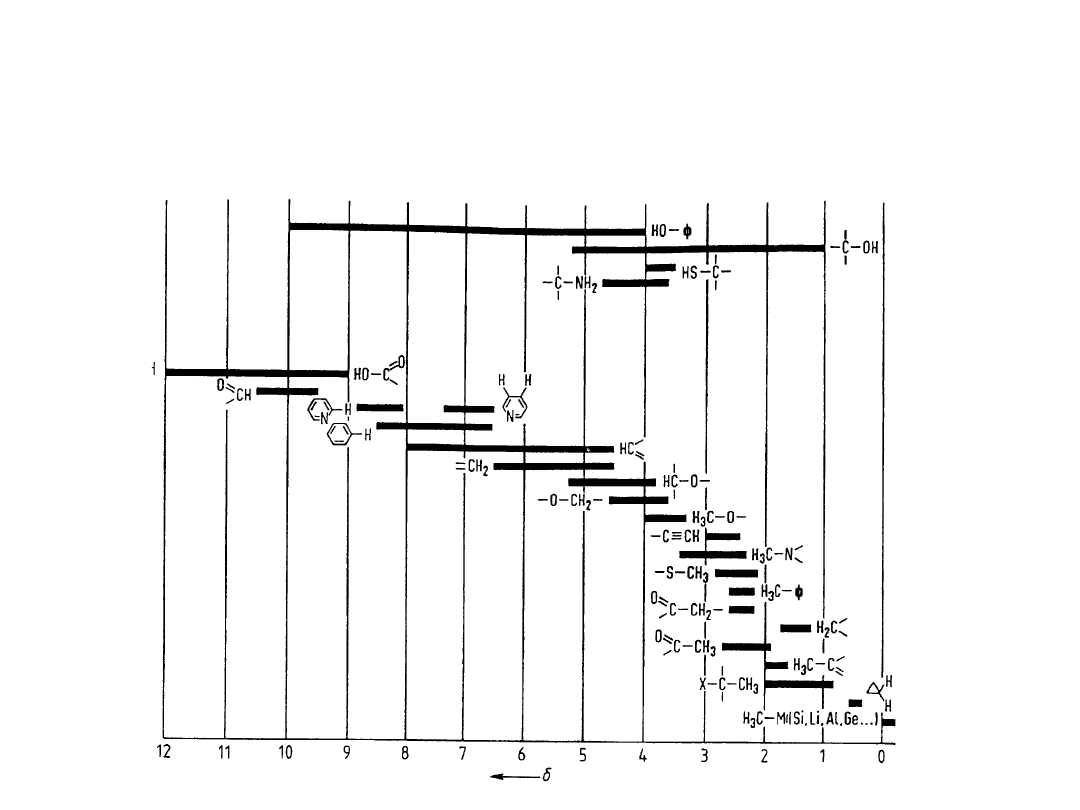
Zakresy przesunięć
chemicznych
1
H dla różnych
grup organicznych
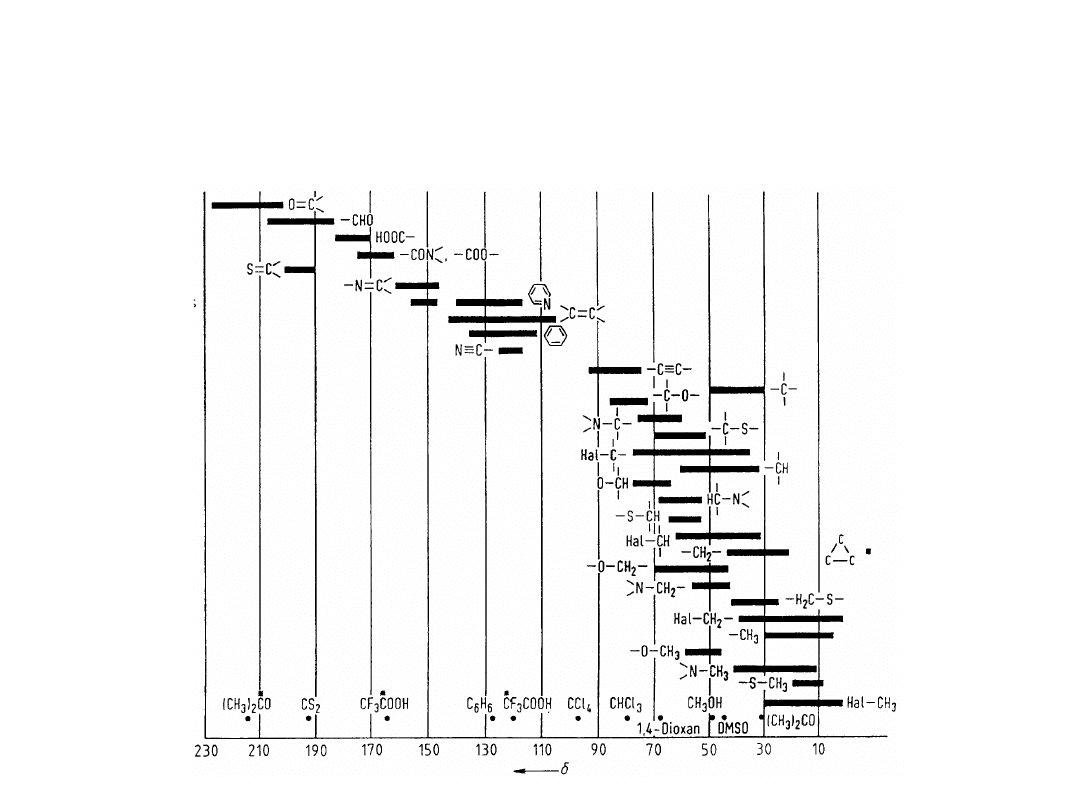
Zakresy przesunięć
chemicznych
13
C dla różnych
grup organicznych
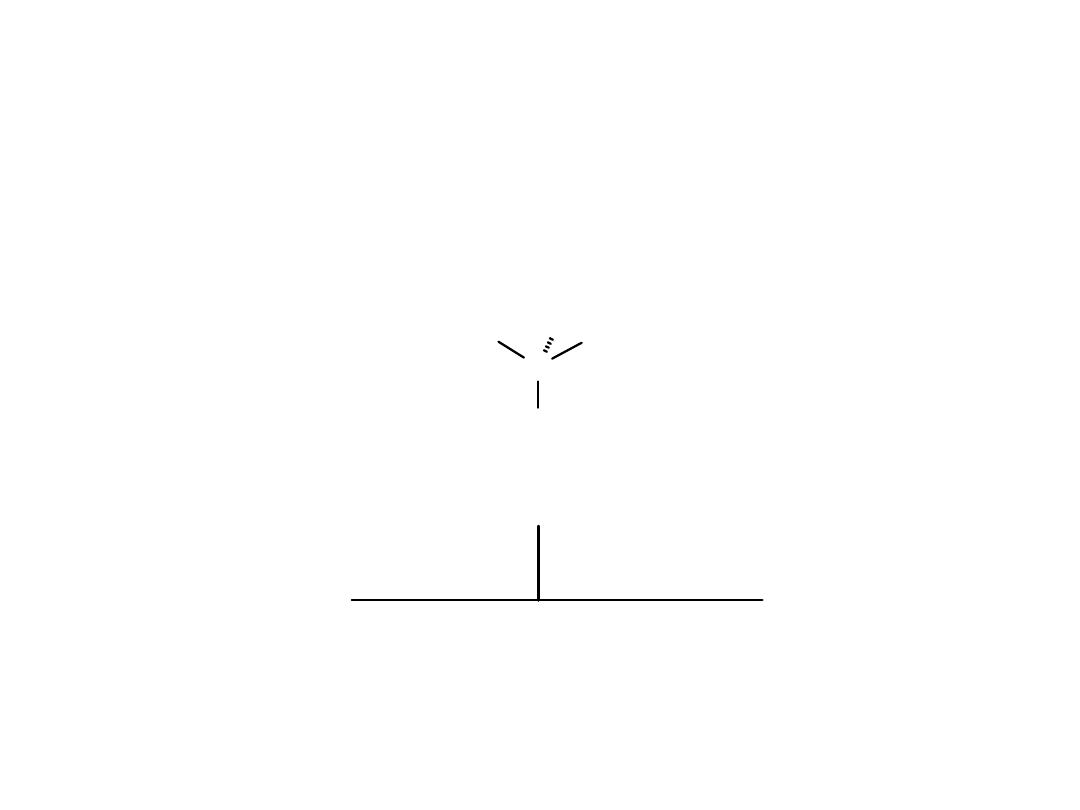
Przesunięcie chemiczne
protony w grupie metylowej CH
3
są zawsze równocenne
C
H
H
H
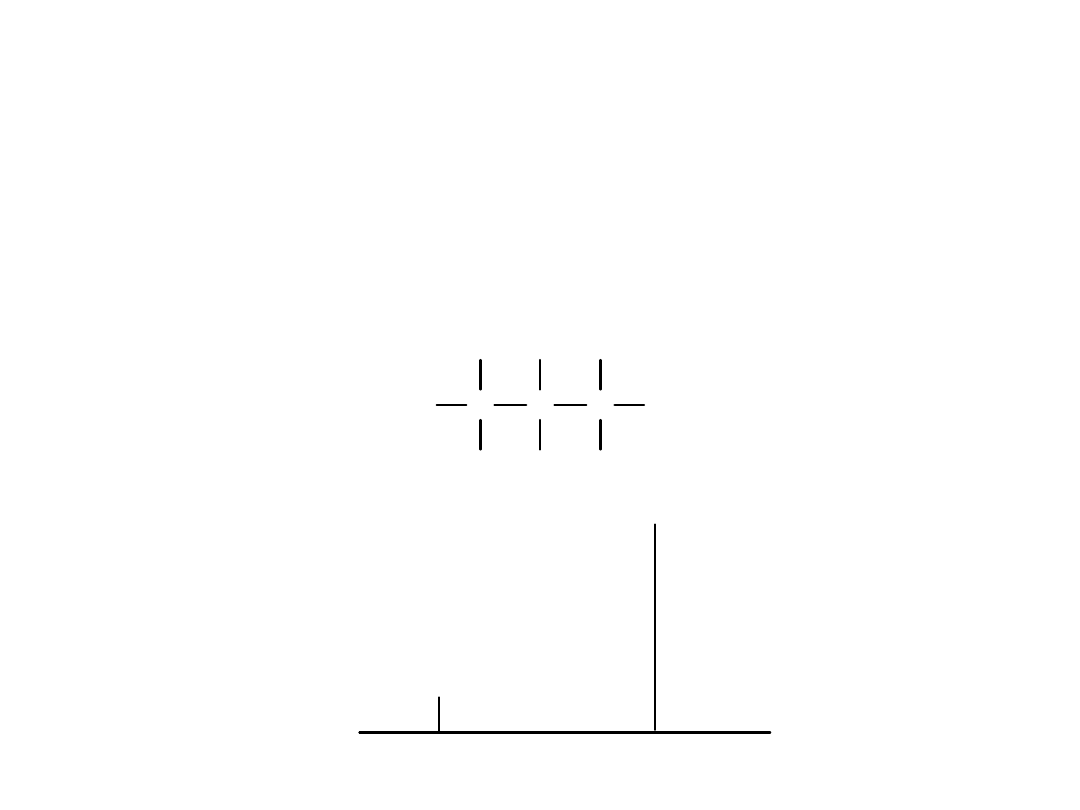
Przesunięcie chemiczne
protony i węgle w różnych grupach CH
3
połączonych z tym samym
atomem są równocenne ...
C C C
Cl
H
H
H
H
H
H
H
CH
3
CHCl

Przesunięcie chemiczne
protony i węgle w różnych grupach CH
3
połączonych z tym samym
atomem są równocenne, o ile są związane elementem symetrii
C C
Cl
H
CH
3
CH
3
CH
3
(trans)
CH
3
(cis)
Zahamowana
rotacja
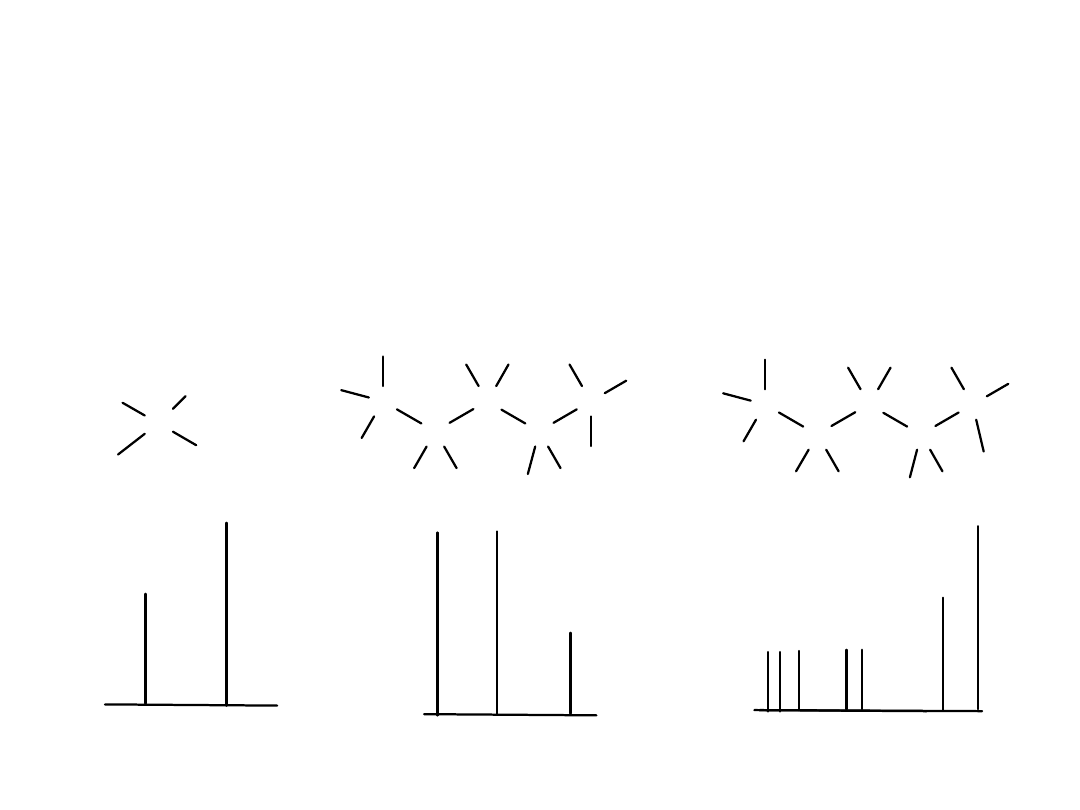
Przesunięcie chemiczne
protony grupy metylenowej -CH
2
- są równocenne, o ile nie
sąsiadują z centrum asymetrii (centrum chiralnym) …
Cl
C
CH
3
H
H
CClH
2
CH
3
CH
2
równocenne
1,5
2,4
3
C
C
C
C
C
Cl
Cl
H
H
H
H
H H H H
H H
1
2
3
4
5
C
C
C
C
C
Cl
H
H
H
H
H
H Cl H H
H H
1
2
3
4
5
1a,b 2 3a,b
4
5
CH
2
nierównocenne
2-C – węgiel
asymetryczny
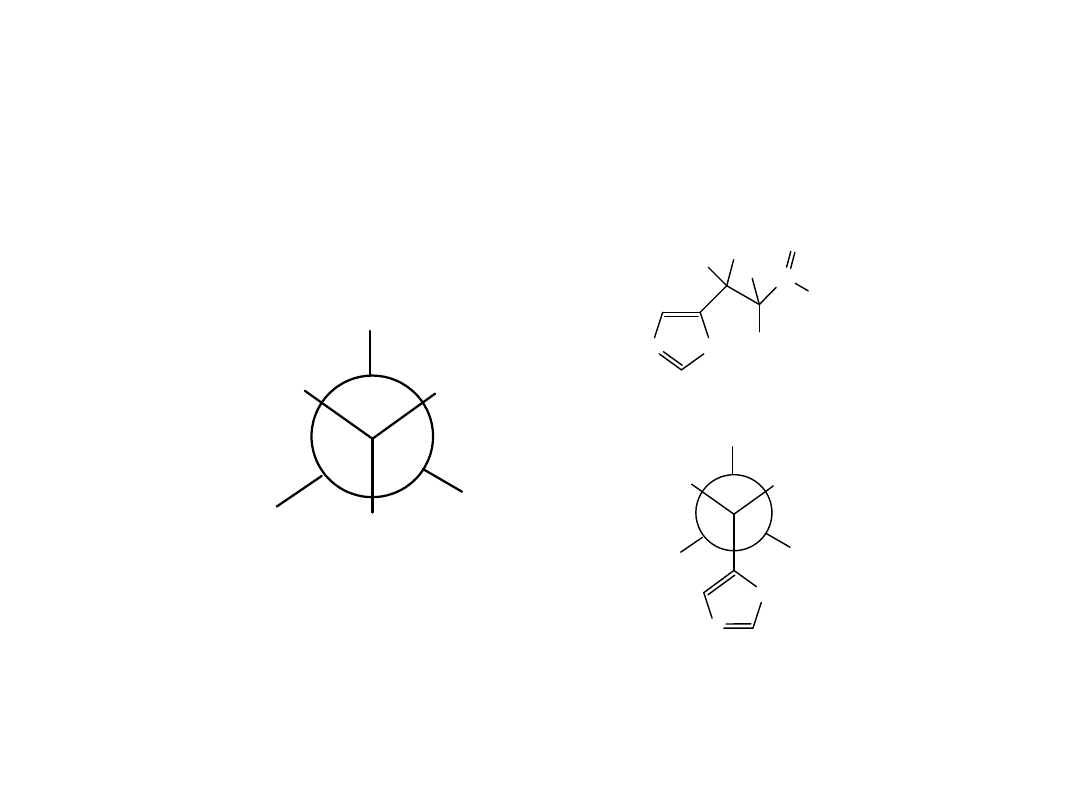
Przesunięcie chemiczne
protony grupy metylenowej -CH
2
- są równocenne, o ile nie
sąsiadują z centrum asymetrii (centrum chiralnym) …
R
1
R
3
R
2
H
a
H
b
X
Protony H
a
i H
b
są
diastereotopowe
, t.j. nie ma elementu
symetrii, który by je łączył; są nierównocenne (magnetycznie
nierównoważne) i wykazują różne przesunięcia chemiczne
C
O
OH
NH
2
H
H H
N
NH
H
a
H
b
N
NH
COOH
NH
2
H

Przesunięcie chemiczne
• Liczba zróżnicowanych sygnałów
rezonansowych (pochodzących od grup
nierównocennych jąder) w widmie NMR
pozwala określić symetrię cząsteczki.
• Analiza liczby sygnałów w widmie NMR
pozwala rozróżnić izomery.
• Widma NMR enancjomerów są identyczne.

Intensywność sygnału
• Intensywność integralna
linii
rezonansowych (pole powierzchni pod
krzywą) jest wprost proporcjonalna do
liczby rezonujących jąder o danym
przesunięciu chemicznym.
• Względna intensywność integralna linii
widmowych pozwala określić liczbę jąder
równoważnych w grupach funkcyjnych
cząsteczki.
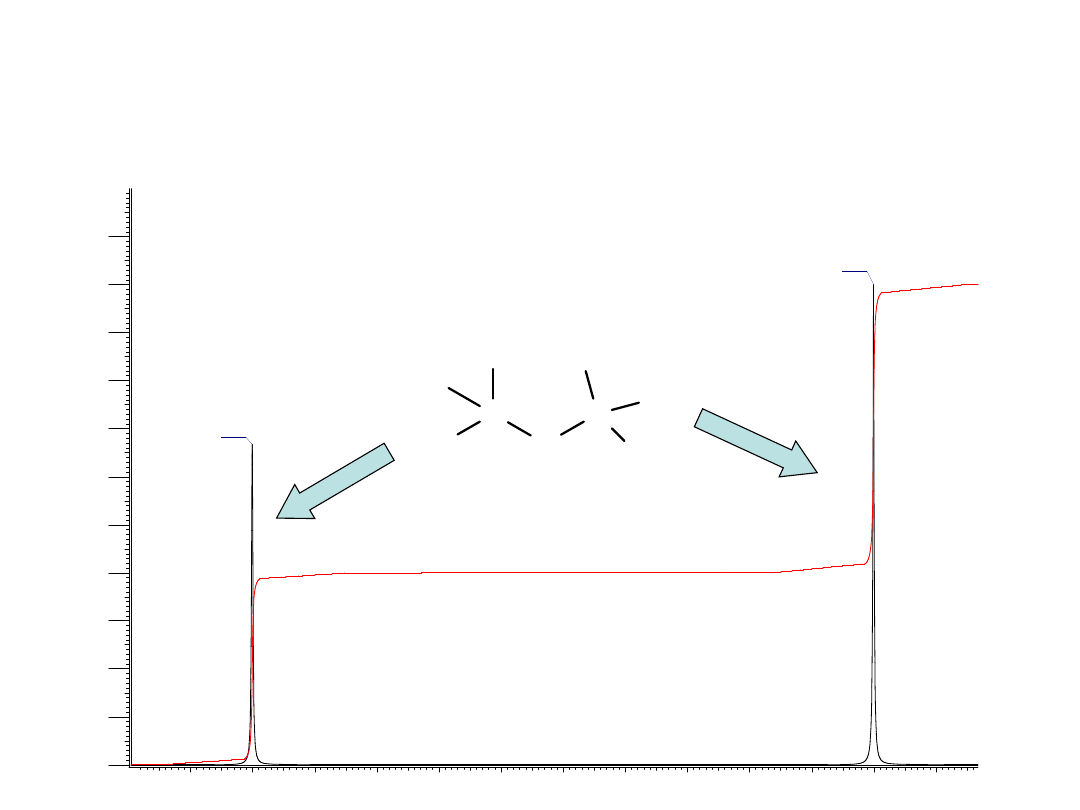
Intensywność sygnału
4.10
4.00
3.90
3.80
3.70
3.60
3.50
3.40
3.30
3.20
3.10
3.00
2.90
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
5.0
5.5
1.91
1.27
C
O
C
H
H
H
H
H
Cl
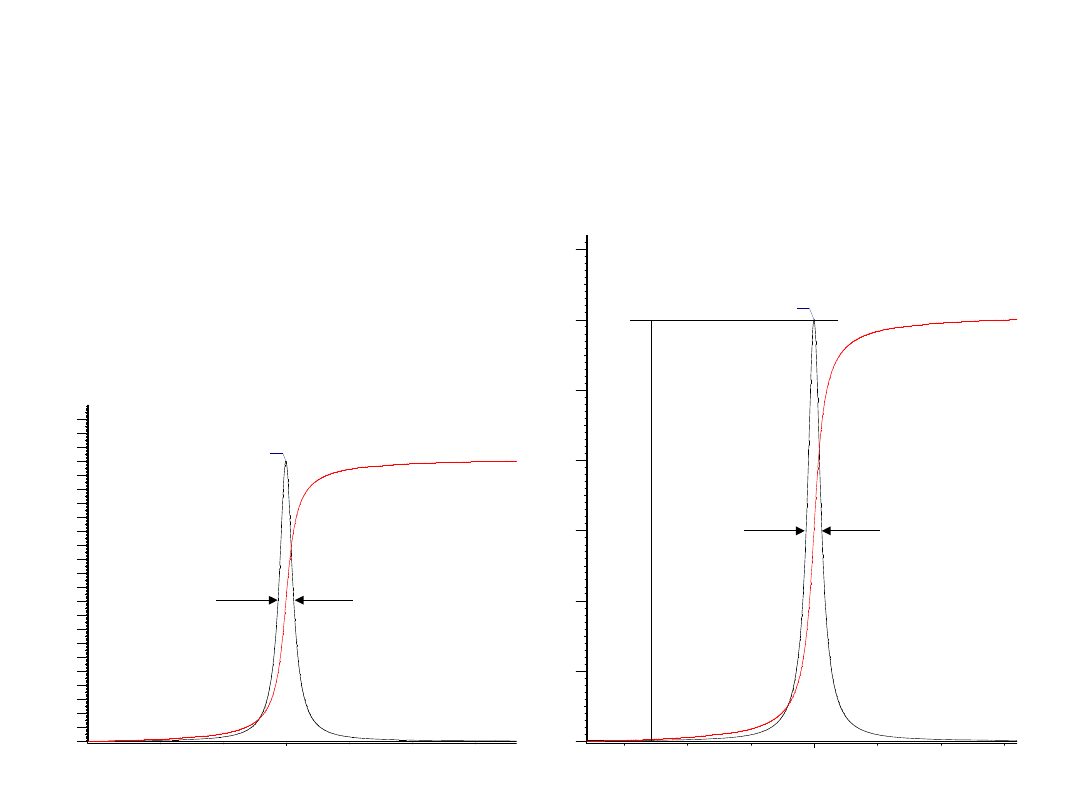
Intensywność sygnału
4.00
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
1.30
1.40
1.50
1.60
1.70
1.80
1.90
2.00
2.10
2.20
2.30
2.40
1.27
3.00
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
1.91
CH
2
CH
3
h
max
h
½
Γ
½
Γ
½
S ~ h
max
x
Γ
½
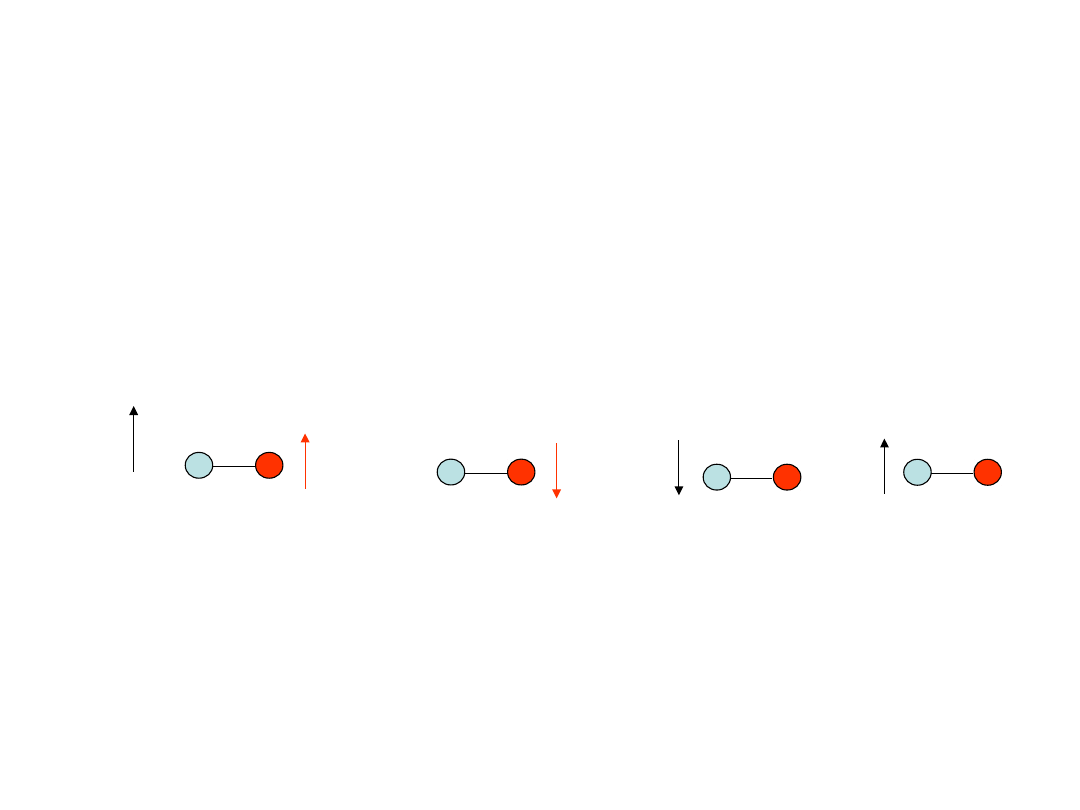
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
• W polu magnetycznym stan energetyczny
magnetycznego jądra A zależy od stanu
energetycznego sąsiedniego magnetycznego
jądra X i na odwrót.
• Indukcja magnetyczna w punkcie jądra A
zależy od tego, czy jądro X ma spin skierowany
zgodnie, czy przeciwnie do kierunku B
o
A
X
A
X
A
X
A
X
B
o

Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
• Załóżmy, że jądro A mające I = ½ oddziałuje z jądrem X I = ½
• Dla jądra A nastąpi modyfikacja stanu podstawowego i
wzbudzonego. Oba te stany ulegną rozszczepieniu na dwa
poziomy, tak że w sumie będą cztery poziomy zamiast dwóch.
• Wielkość rozszczepienia poziomów energetycznych na skutek
oddziaływania międzyjądrowego E
SS
jest proporcjonalna do
wielkości
stałej sprzężenia J
i magnetycznych spinowych liczb
kwantowych oddziałujących jąder:
E
SS
= Jm
1
m
2
h,
np. dla I = ½: E
SS
= ¼Jh

Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
• Na skutek bliskości innych jąder
magnetycznych w cząsteczce związku
chemicznego energia jądrowego stanu
spinowego zostaje zmodyfikowana.
• Jądra magnetyczne w atomach połączonych
wiązaniami chemicznymi wzajemnie
rozszczepiają swoje spinowe poziomy
energetyczne.
• Rozszczepieniu ulega zarówno poziom stanu
podstawowego jak i poziom stanu wzbudzonego.
• Wielkość rozszczepienia
nie zależy
od natężenia
pola magnetycznego.
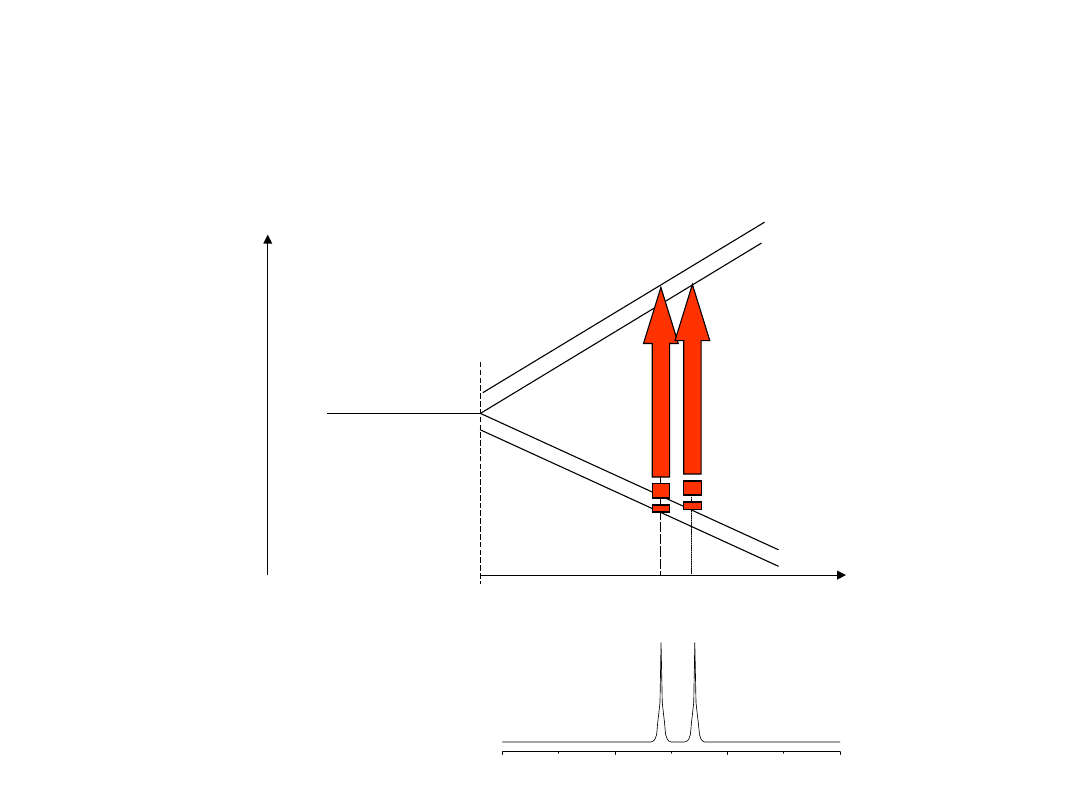
Warunek rezonansu
- sprzężenie spin-spin -
E
B
1
B
2
ħB
1
=
h
ħB
2
=
h
h
2 jądra o spinie
½
1
2
3
4
B
m
I
= ½ ,
-½
m
I
= ½ ,
½
m
I
= -½ , ½
m
I
= -½ , -½
Reguła wyboru:
Dozwolone są przejścia
między stanami, dla których |
m
T
| = 1
i
I
i
m
m
)
(
T
m
T
0
1
0
-1
AX
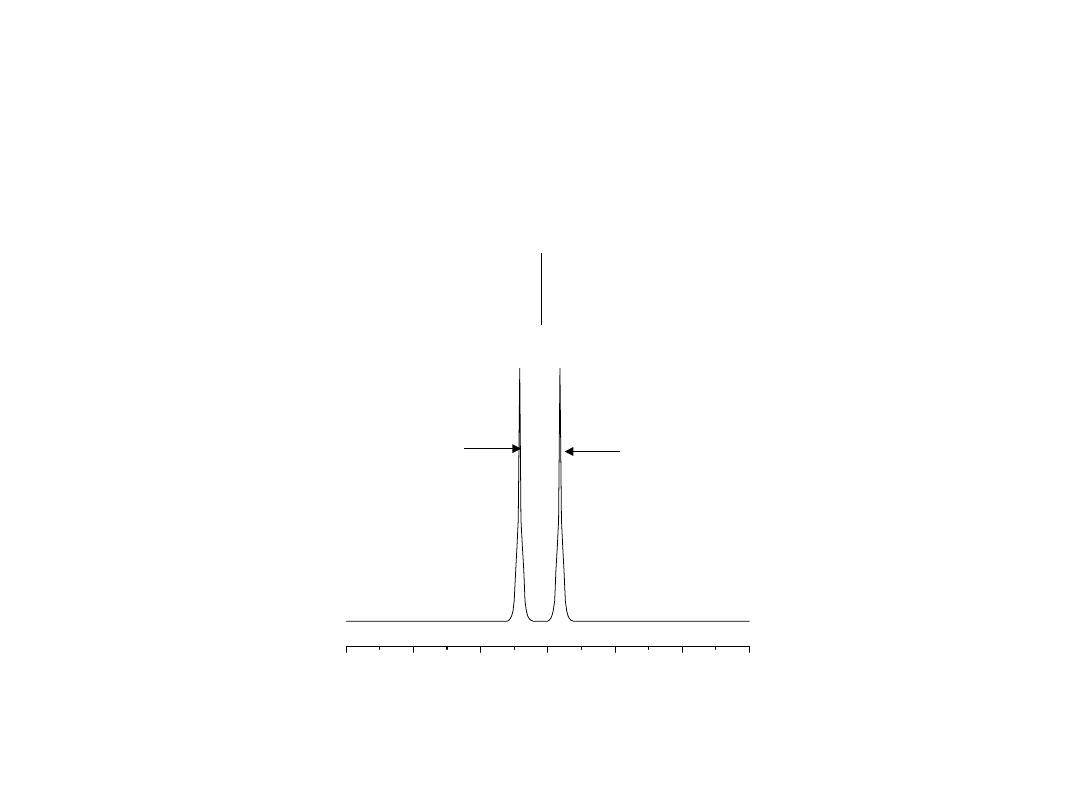
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
4.0
3.5
3.0
2.5
2.0
1.5
1.0
[Hz]
1
2
J
AX
A
A
=
1
– ½ J
AX
A
=
2
+ ½ J
AX
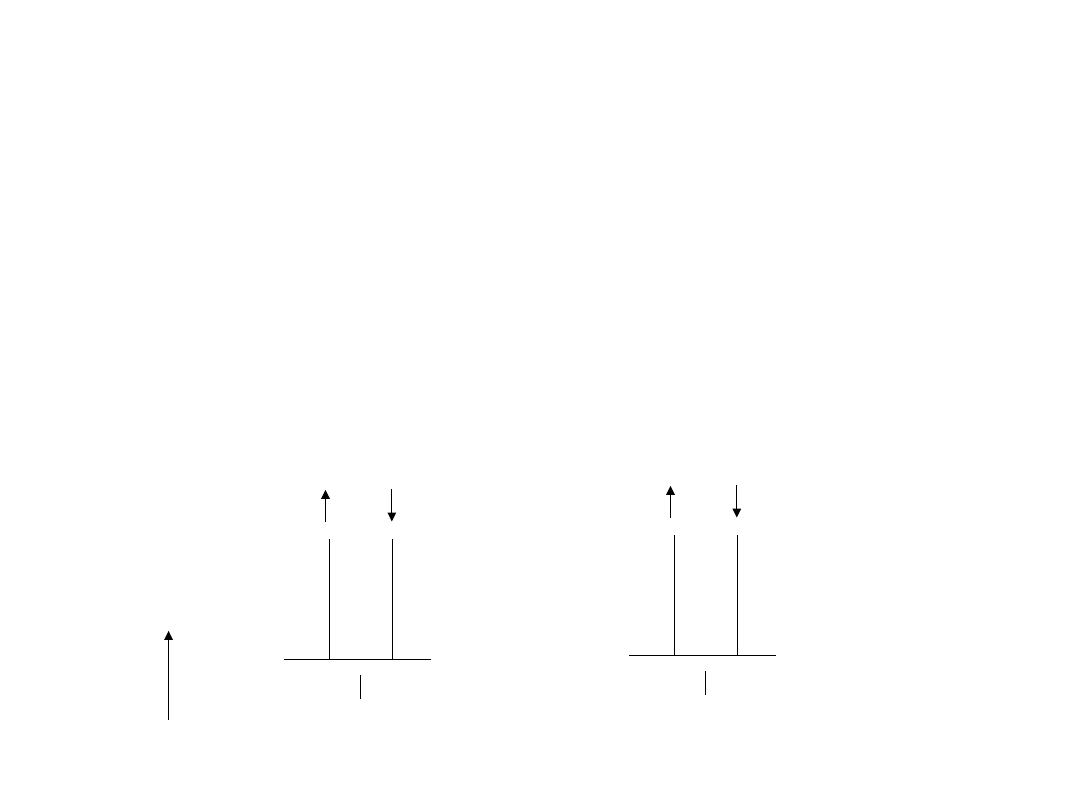
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
Układy spinowe
AX np. CH
A
-CH
X
Proton H
A
oddziałuje z protonem H
X
. Spiny jąder H
A
i H
X
mogą
przyjmować różne orientacje względem pola:
J
AX
X
1 : 1
orientacj
e spinów
X
orientacj
e spinów
A
J
AX
A
1 : 1
B
o
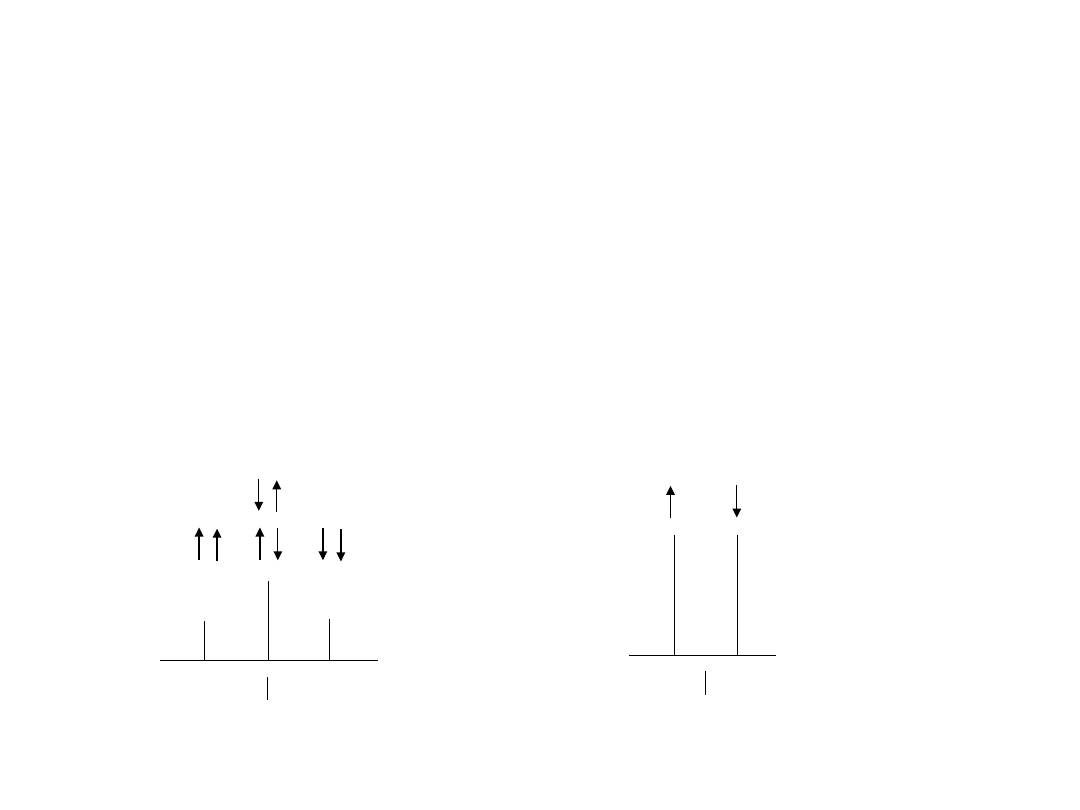
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
Układy spinowe
AX
2
np. CH
A
-
CH
2
X
Proton H
A
oddziałuje z dwoma równocennymi protonami H
X
. Spiny
jąder H
X
mogą przyjmować różne orientacje względem pola i
względem siebie:
J
AX
J
AX
J
AX
A
X
1 : 2 :
1
1 : 1
orientacj
e spinów
X
orientacj
e spinów
A
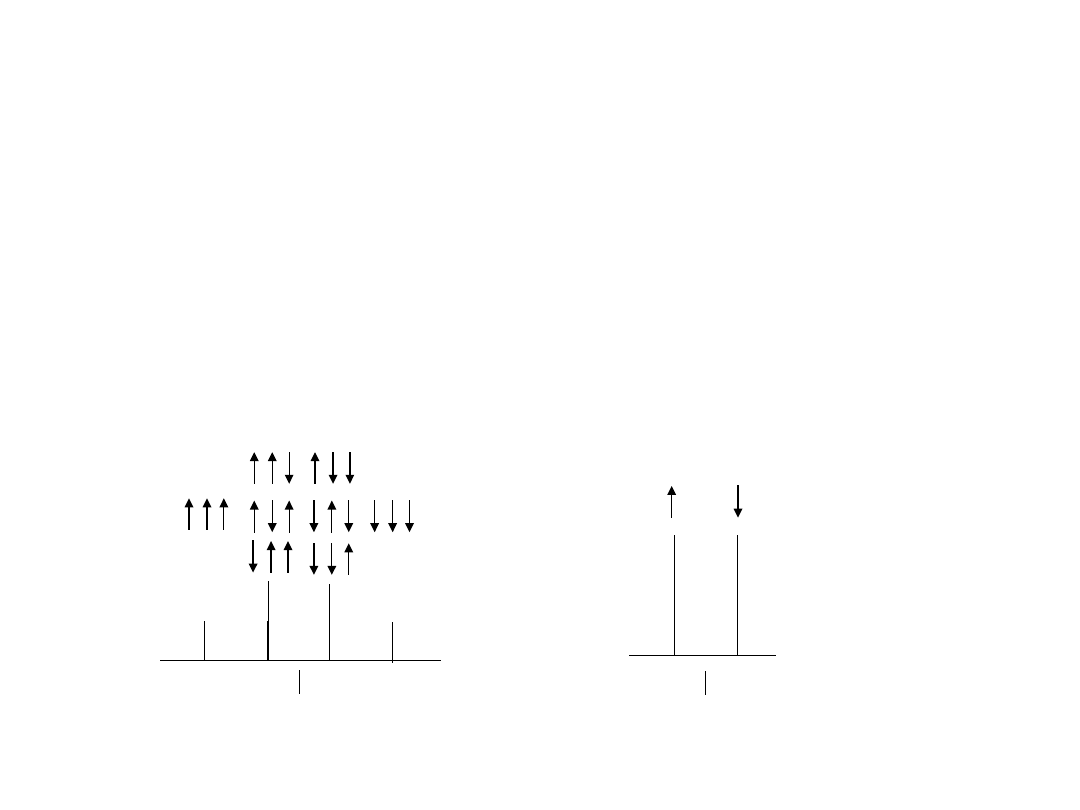
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
Układy spinowe
AX
3
np. CH
A
-
CH
3
X
Proton H
A
oddziałuje z trzema równocennymi protonami H
X
. Spiny jąder
H
X
mogą przyjmować różne orientacje względem pola i względem
siebie:
J
AX
J
AX
J
AX
A
X
1 : 1
J
AX
orientacj
e spinów
X
orientacj
e spinów
A
1 : 3 : 3 :
1
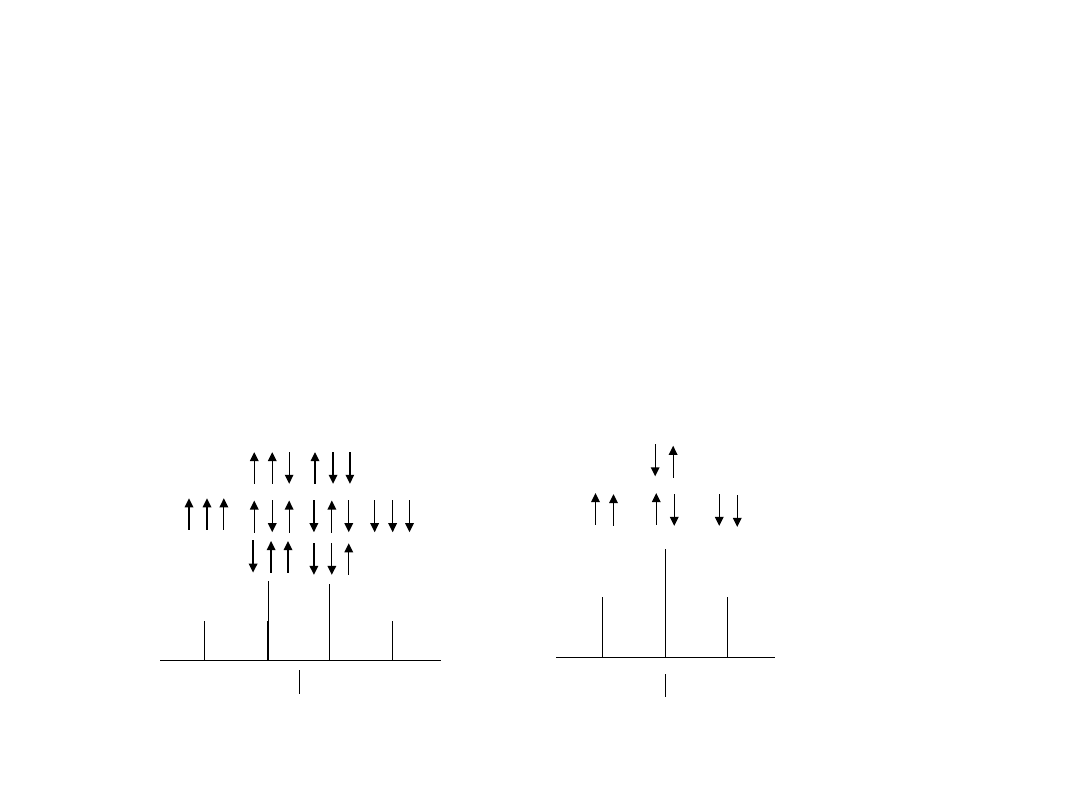
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
Układy spinowe
A
2
X
3
np. CH
2
A
-CH
3
X
Protony H
A
oddziałują z trzema równocennymi protonami H
X
. Jądra H
X
oddziałują z dwoma równocennymi jądrami H
A
. Spiny obu grup jąder
mogą przyjmować różne orientacje względem pola i względem siebie
w obrębie grupy:
J
AX
J
AX
A
1 : 3 : 3 :
1
J
AX
orientacj
e spinów
X
orientacj
e spinów
A
J
AX
J
AX
X
1 : 2 :
1
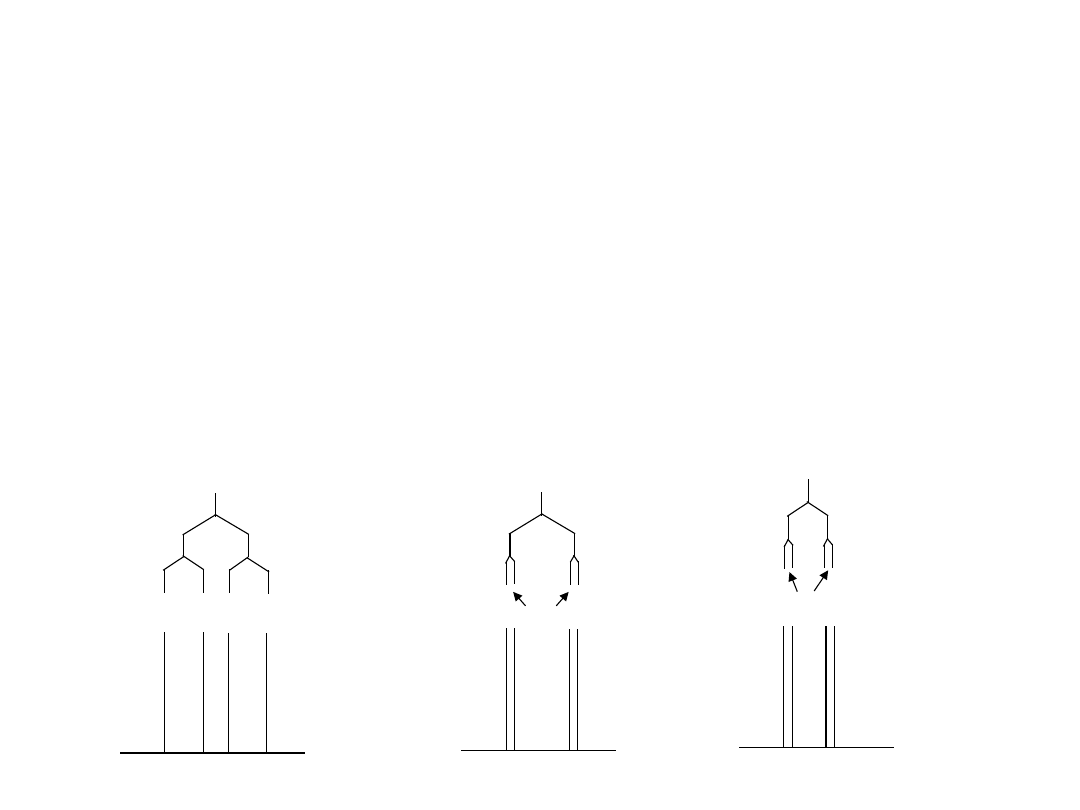
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
Układy spinowe
AMX np.
-CH
A
=CH
M
H
X
W trójspinowym układzie AMX trzy nierównocenne jądra sprzęgają się
niezależnie każde z każdym. Dla każdej pary sprzęgających się jąder
wielkość stałej sprzężenia J może być inna.
M
J
AX
A
X
J
AX
J
AM
J
AM
J
MX
J
AX
J
MX

Sprzężenie spin-spin.
Warunki występowania
rozszczepienia
• Aby na widmie NMR ujawniła się struktura subtelna
spowodowana oddziaływaniem między dwoma jądrami,
konieczne jest by były one
magnetycznie nierównoważne
(różniły się przesunięciem chemicznym ).
• W układzie spinowym A
n
obserwuje się singlet (sygnał bez
struktury subtelnej).
• Aby na widmie NMR ujawniła się struktura subtelna
spowodowana oddziaływaniem między dwoma jądrami,
konieczne jest by wielkość stałej sprzężenia między tymi
jądrami J była większa niż szerokość linii rezonansowej .
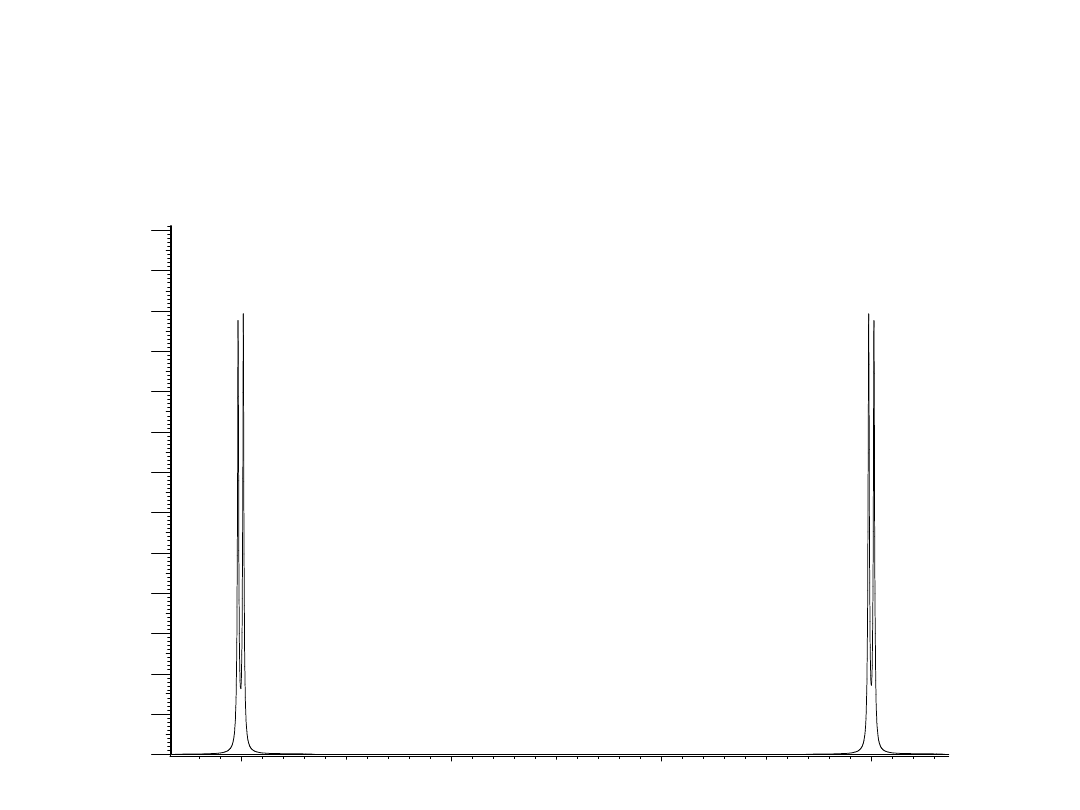
Sprzężenie spin-spin.
Warunki występowania
rozszczepienia
1.30
1.20
1.10
1.00
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
1.30
I = ½ , J = 1 Hz, = 0.3
Hz
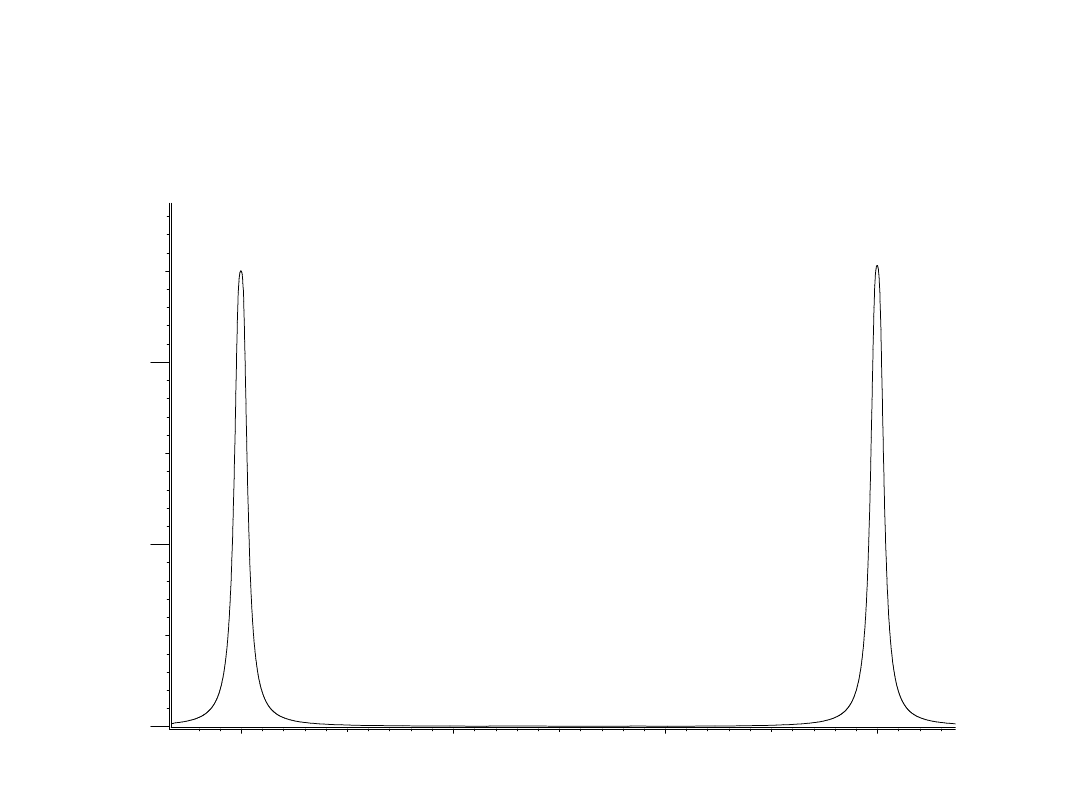
Sprzężenie spin-spin.
Warunki występowania
rozszczepienia
1.30
1.20
1.10
1.00
0.00
0.10
0.20
I = ½ , J = 1 Hz, = 2 Hz

Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
• Dla sprzężeń proton-proton (
1
H -
1
H)
zakres wielkości stałych sprzężeń J
wynosi 0.1-20 Hz.
• W tzw. widmach protonowych (
1
H
NMR) uwidaczniają się zazwyczaj
sprzężenia dla jąder wodoru
„odległych” od siebie w cząsteczce o
co najwyżej 3 wiązania.
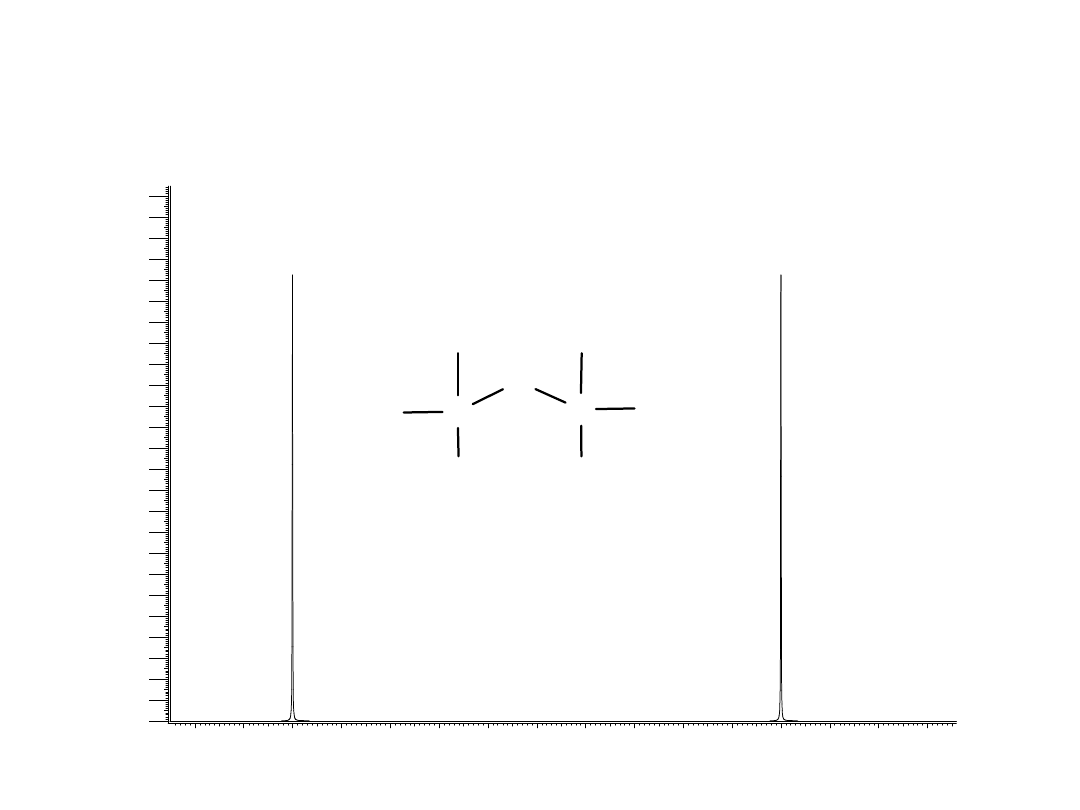
Dwa jądra nie oddziałujące
I = ½, J = 0 Hz
3.20
3.10
3.00
2.90
2.80
2.70
2.60
2.50
2.40
2.30
2.20
2.10
2.00
1.90
1.80
1.70
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
1.30
1.40
1.50
1.60
1.70
1.80
1.90
2.00
2.10
2.20
2.30
2.40
2.50
Cl C
CCl
3
H
O
C
CCl
3
CCl
3
H
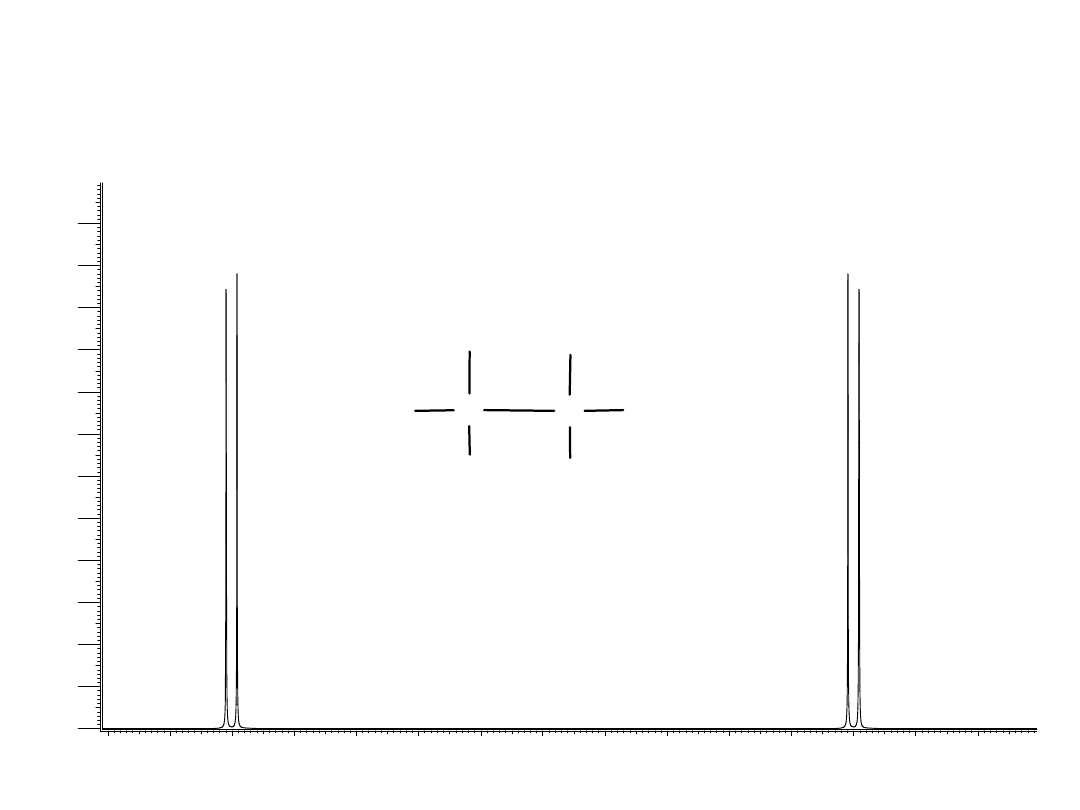
Dwa jądra oddziałujące
I = ½, J = 7 Hz
3.20
3.10
3.00
2.90
2.80
2.70
2.60
2.50
2.40
2.30
2.20
2.10
2.00
1.90
1.80
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
Cl C
CCl
3
H
H
CCl
3
CCl
3
C

Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
• Siła sprzężenia spin-spin wyrażona wielkością
stałej sprzężenia J nie zależy od zewnętrznego
pola magnetycznego. Zatem bez względu na
wielkość indukcji magnetycznej B
o
J będzie
miało tę samą wartość dla danego układu
sprzęgających się jąder.
• Wartość J odczytywana z widma NMR jako
odległość pomiędzy kolejnymi składowymi
multipletu
musi
być podawana jako różnica
częstości
tych składowych w hercach.
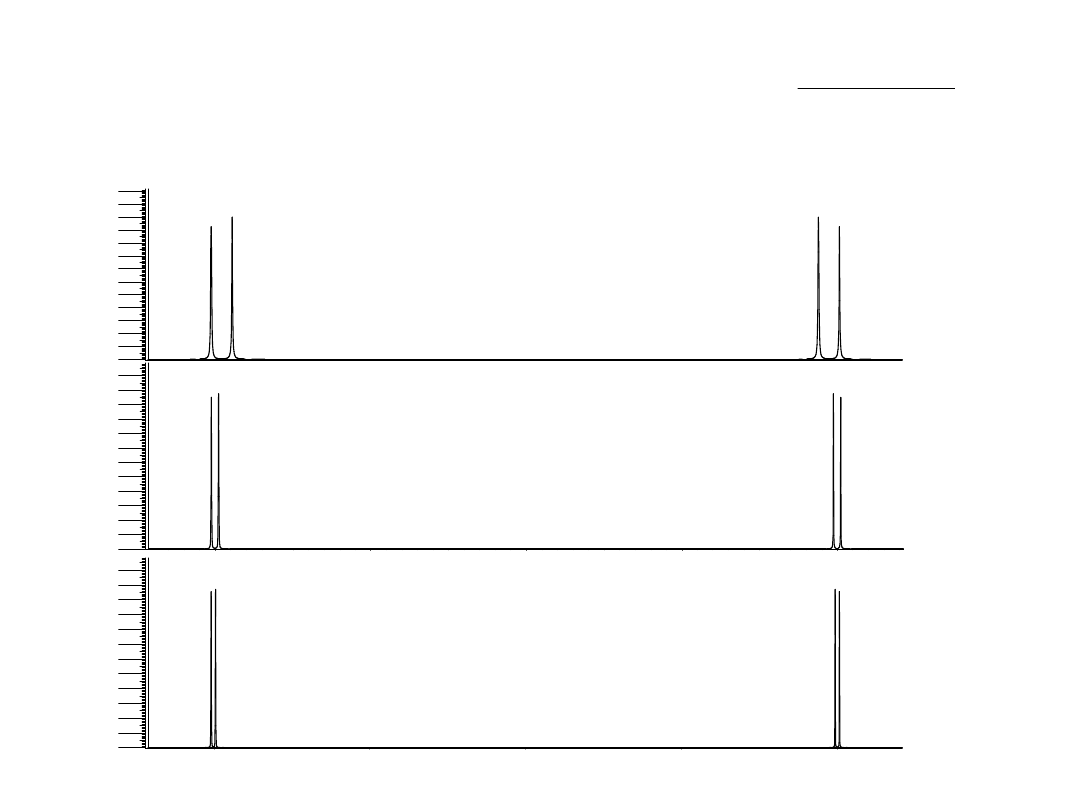
Dwa jądra
oddziałujące
I = ½, J = 7 Hz
3 .0
2 .5
2.0
1 .5
1.0
0 .0 0
0 .1 0
0 .2 0
0 .3 0
0 .4 0
0 .5 0
0 .6 0
0 .7 0
0 .8 0
0 .9 0
1 .0 0
1 .1 0
1 .2 0
1 .3 0
3.0
2.5
2 .0
1. 5
1 .0
0.0 0
0.1 0
0.2 0
0.3 0
0.4 0
0.5 0
0.6 0
0.7 0
0.8 0
0.9 0
1.0 0
1.1 0
1.2 0
3. 0
2.5
2.0
1 .5
1. 0
0 .0 0
0 .1 0
0 .2 0
0 .3 0
0 .4 0
0 .5 0
0 .6 0
0 .7 0
0 .8 0
0 .9 0
1 .0 0
1 .1 0
1 .2 0
[ppm]
100 MHz
300 MHz
500 MHz
o
wz
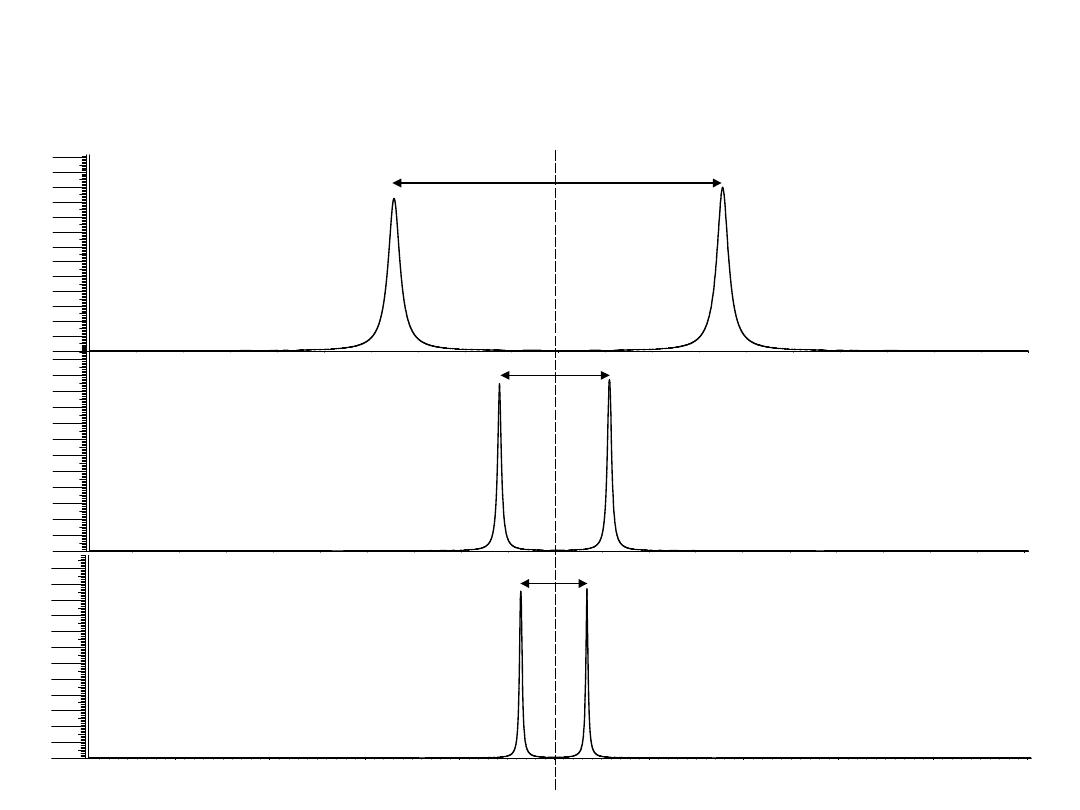
Dwa jądra oddziałujące
I = ½, J = 7 Hz
1540
1530
1520
1510
1500
1490
1480
1470
1460
1450
0. 00
0. 10
0. 20
0. 30
0. 40
0. 50
0. 60
0. 70
0. 80
0. 90
1. 00
1. 10
1. 20
3. 00
2.90
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
3.00
2. 90
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
1.30
100 MHz
300 MHz
500 MHz
o
[ppm]
7 Hz
7 Hz
7 Hz

Sprzężenie spin-spin.
Multipletowość
•
Liczba składowych struktury subtelnej
M
(
multipletowość
) linii
rezonansowej przy danym przesunięciu chemicznym
1
zależy od:
a)
kwantowej liczby spinowej
I
jądra, z którym sprzęga się jądro o
przesunięciu
1
b)
liczby
N
równoważnych magnetycznie jąder, z którymi sprzęga się
jądro o przesunięciu
1
M = 2NI + 1
•
Dla I = ½ M = N + 1 (np. dla
1
H,
19
F,
13
C,
31
P)
•
Częstość rezonansowa (przesunięcie chemiczne) sygnału
wykazującego strukturę subtelną wyznaczona jest przez centrum
multipletu, tj. centralną składową multipletu przy nieparzystej
liczbie składowych lub punkt leżący w środku pomiędzy najbardziej
wewnętrznymi składowymi multipletu przy parzystej liczbie
składowych.

Multipletowość
• Grupa etylowa –CH
2
–CH
3
Każdy z protonów grupy –CH
2
– sprzęga
się z trzema protonami grupy metylowej,
N = 3
Dla
1
H I = ½
M = 2NI+1 = 2 x 3 x ½ + 1= 4
Sygnał grupy metylenowej ulegnie
rozszczepieniu na cztery składowe
(będzie kwartetem)

Multipletowość
• Grupa etylowa –CH
2
–CH
3
Każdy z protonów grupy –CH
3
sprzęga się
z dwoma protonami grupy metylenowej,
N = 2
Dla
1
H I = ½
M = 2NI+1 = 2 x 2 x ½ + 1= 3
Sygnał grupy metylowej ulegnie
rozszczepieniu na trzy składowe (będzie
trypletem)
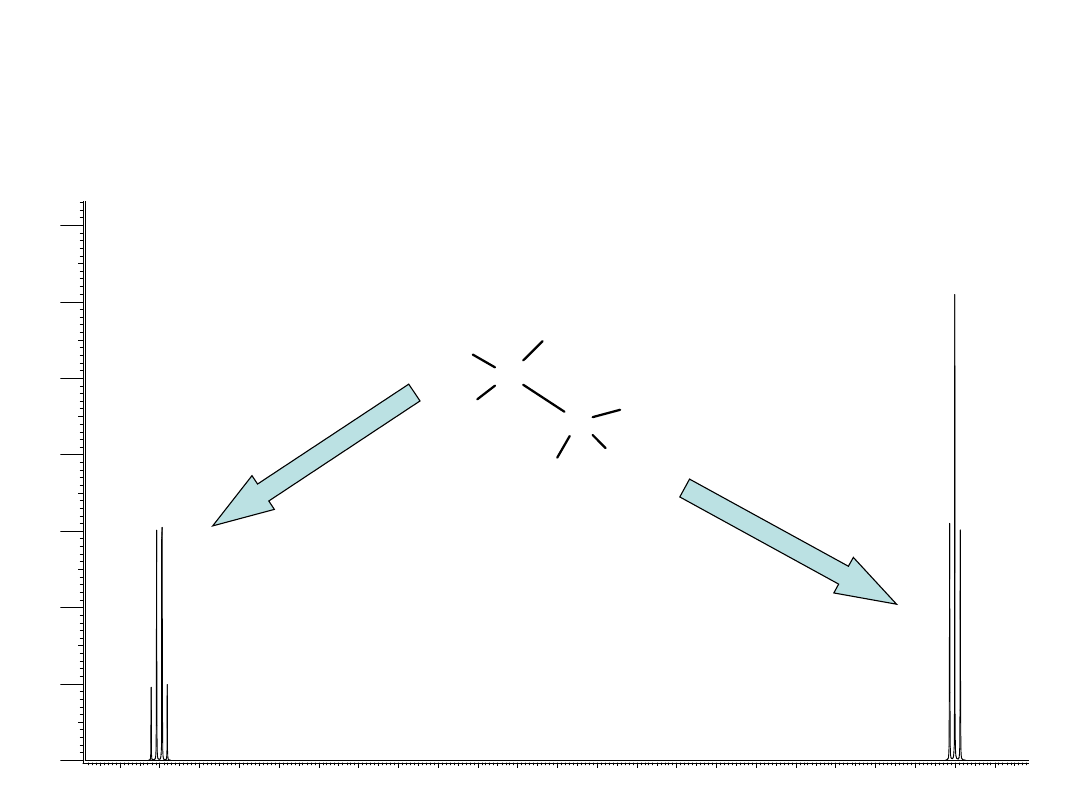
Oddziaływanie międzyjądrowe.
Sprzężenie spin-spin
3.10
3.00
2.90
2.80
2.70
2.60
2.50
2.40
2.30
2.20
2.10
2.00
1.90
1.80
1.70
1.60
1.50
1.40
1.30
1.20
1.10
1.00
0.90
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
H
C
C
H
I
H
H
H
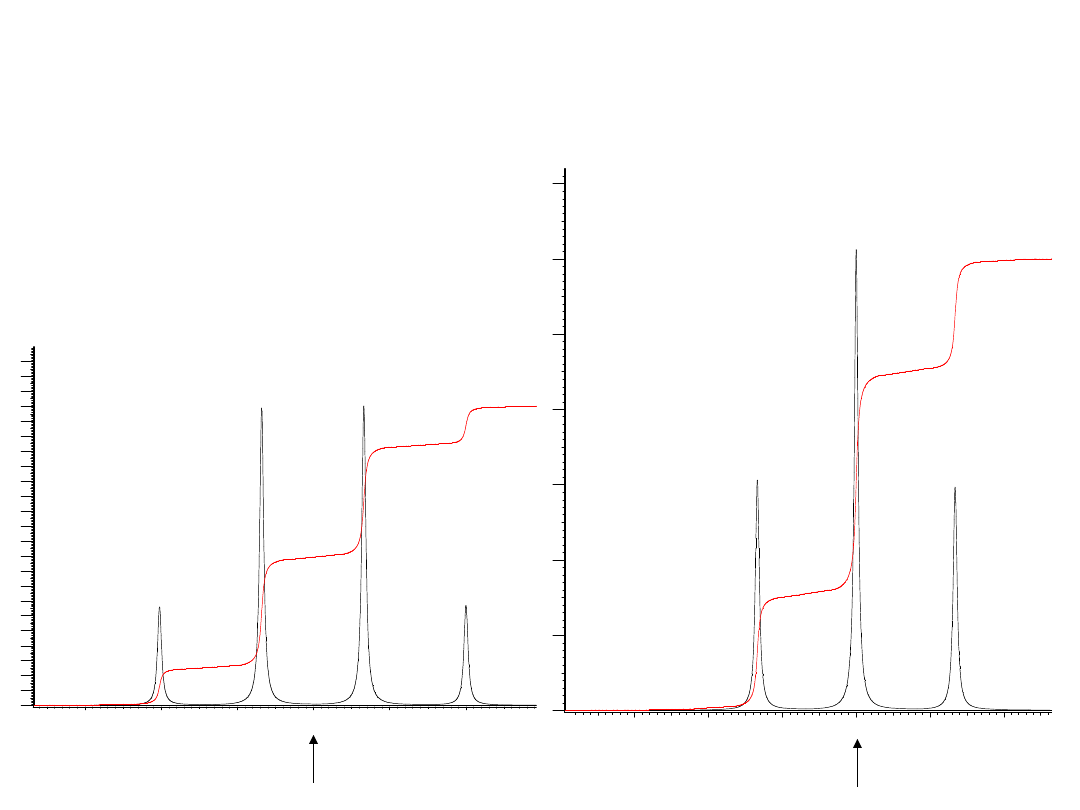
Względna intensywność składowych
multipletów grupy etylowej
1515
1510
1505
1500
1495
1490
0.00
0.10
0.20
0.30
0.40
0.50
0.60
0.70
0.80
0.90
1.00
1.10
1.20
1.30
1.40
1.50
1.60
1.70
1.80
1.90
2.00
2.10
2.20
2.30
2.40
515
510
505
500
495
490
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
CH
2
CH
3
1
3
3
1
1
1
2
W obu multipletach odległości (w
hercach) pomiędzy kolejnymi
składowymi są identyczne i wynoszą
J.
(CH
2
)
(CH
3
)

Multipletowość
• Grupa izopropylowa CH
3
–CH–CH
3
Każdy z protonów grup –CH
3
sprzęga się
z 1 protonem,
N = 1
Dla
1
H I = ½
M = 2NI+1 = 2 x 1 x ½ + 1= 2
Sygnał grup metylowych ulegnie
rozszczepieniu na dwie składowe (będzie
dubletem)

Multipletowość
• Grupa izopropylowa CH
3
–CH–CH
3
Proton grupy –CH– sprzęga się z 6
protonami,
N = 6
Dla
1
H I = ½
M = 2NI+1 = 2 x 6 x ½ + 1= 7
Sygnał grupy –CH– ulegnie rozszczepieniu
na siedem składowych (będzie septetem)
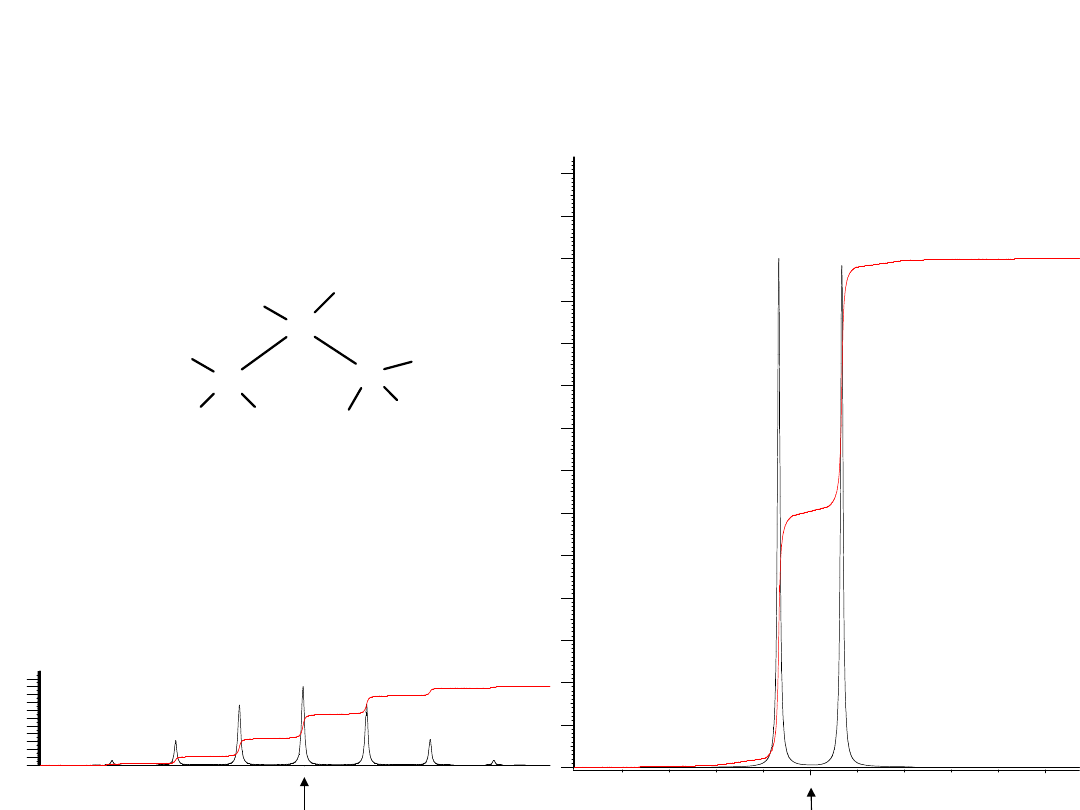
Względna intensywność składowych
multipletów grupy izopropylowej
3. 0 0
0 . 00
0 . 10
0 . 20
0 . 30
0 . 40
0 . 50
0 . 60
0 . 70
0 . 80
0 . 90
1 . 00
1 . 10
1 . 20
1.00
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
5.0
5.5
6.0
6.5
7.0
1
1
1
6
6
15
15
20
1
CH
2 x CH
3
C
C
C
H
I
H
H
H
H
H
H
(CH)
(CH
3
)

Względna intensywność składowych
multipletów dla sprzężenia z jądrami o
I = ½
• Przy sprzężeniu z N jądrami o wartości spinowej liczby kwantowej
I = ½ względne intensywności składowych multipletu mają się do
siebie jak współczynniki rozwinięcia dwumianu (a + b)
N
.
N
0
1
1
1
1
2
1
2
1
3
1
3
3
1
4
1
4
6
4
1
5
1
5
10 10 5
1
6
1
6 15 20 15
6
1
Trójkąt Pascala

Zastosowanie spektroskopii
NMR w analizie jakościowej.
Podsumowanie
1) Liczba linii rezonansowych –
symetria
cząsteczki.
2) Analiza przesunięć chemicznych –
grupy
funkcyjne.
3) Względna intensywność linii –
skład
związku chemicznego.
4) Analiza sprzężeń spin-spin –
sekwencja
grup funkcyjnych.

Zastosowanie NMR w medycynie
w szeroko pojętej tomografii komputerowej wykorzystującej źródło
pola magnetycznego (rezonans magnetyczny) w diagnostyce
mózgu, klatki piersiowej
mammografii
układów naczyniowych
ośrodkowego układu nerwowego
jamy brzusznej
przestrzeni zaotrzewnowej
miednicy

Zakres badań diagnostycznych
wykorzystujących spektroskopię NMR
diagnostyka metodą MR-I, pozwalająca na tworzenie dokładnych
obrazów narządów i okolic ciała w przekrojach w dowolnej
płaszczyźnie (w szczególności struktury wewnątrzczaszkowe i
wewnątrzkręgowe). Wysoką jakość uzyskiwanych w badaniu obrazów
zapewnia wykorzystanie magnesu nadprzewodnikowego o natężeniu
2T oraz specjalistycznych cewek narządowych (np. kolanowa,
głowowa, sutkowa). Badania rekomendowane są szczególnie do
oceny centralnego układu nerwowego i układu kostno-mięśniowo-
stawowego. Nieinwazyjność metody pozwala na bezpieczne
wykrywanie chorób oraz monitorowanie leczenia w przypadkach
zmian nowotworowych, zapalnych, urazowych i zwyrodnieniowych
Przewaga NMR nad zdjęciami rentgenowskimi jest dwojaka.
Po pierwsze ani pole magnetyczne, ani fale radiowe (bo przeważnie
takich używa się w rezonansie) nie są tak szkodliwe jak promienie X, a
po drugie NMR daje możliwość wykonania dowolnego przekroju, a nie
tylko rzutu na klisze jak w przypadku tradycyjnego prześwietlenia.
Stosując NMR możemy także praktycznie bez ograniczeń powiększać
sobie dowolny interesujący nas fragment obserwowanego
przedmiotu. Zarówno wiec lekarzom jak i biologom NMR daje do ręki
potężne narzędzie badawcze.
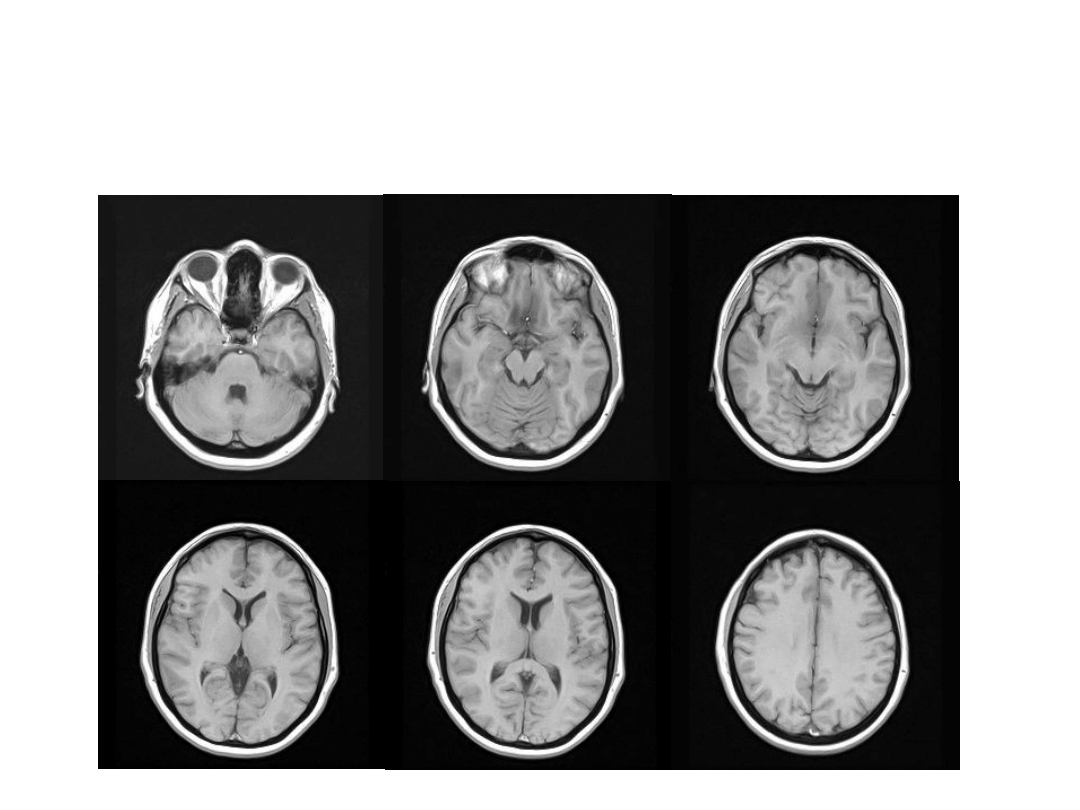
MRI – obrazowanie magnetycznym rezonansem
jądrowym
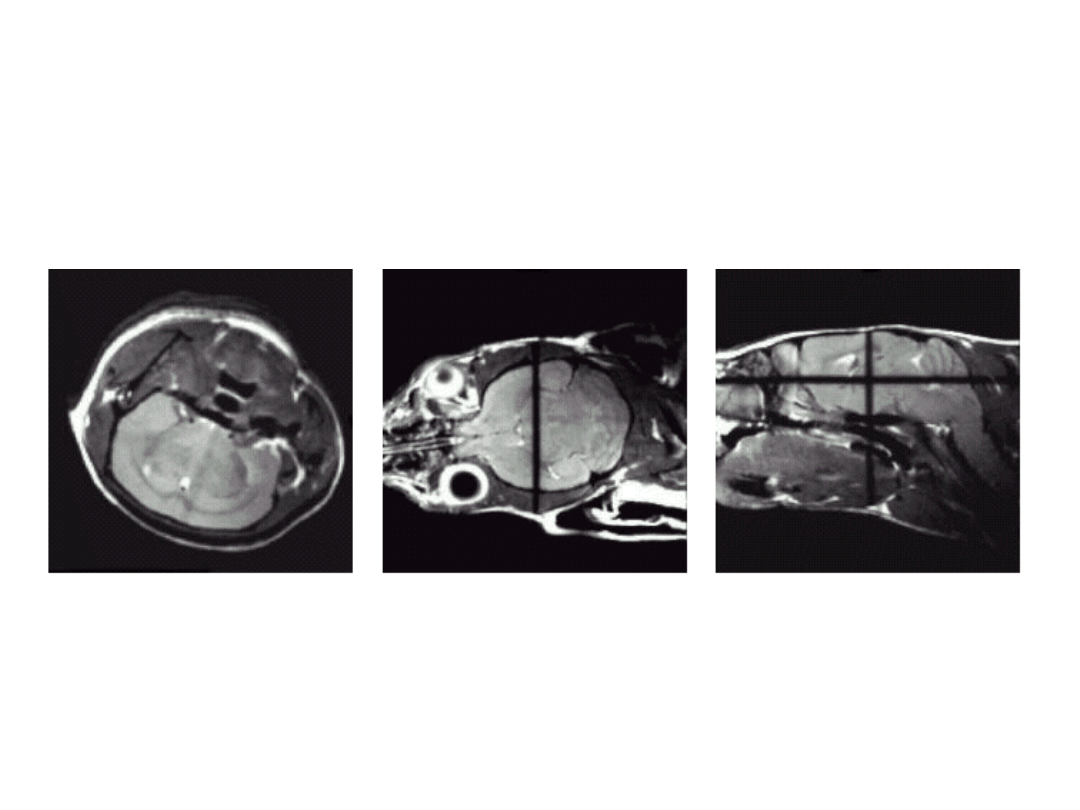
Mózg myszy, model działający
Obrazowanie rezonansem
magnetycznym in vivo

Paul C. Lauterbur
Department of Chemistry
University of Illinois
Sir Peter Mansfield
School of Physics and
Astronomy
University of Nottingham
Nobel 2003 (Medycyna i fizjologia)
za pionierskie badania nad MRI

EPR
Electron Paramagnetic Resonance

The science of electron paramagnetic
resonance (EPR) spectroscopy is very similar
to the more familiar NMR. Both deal with the
interaction of electromagnetic radiation with
magnetic moments; in case of EPR, the
magnetic moments arise from electron rather
than nuclei.
Each electron possesses an intristic
magnetic-dipole moment that arises from its
spin. In most systems electrons occur in pairs
such that the net moment is zero. Hence only
species that contains one or more unpaired
electrons possess the net spin moment
necessary for interaction with an
electromagnetic field.
EPR technique
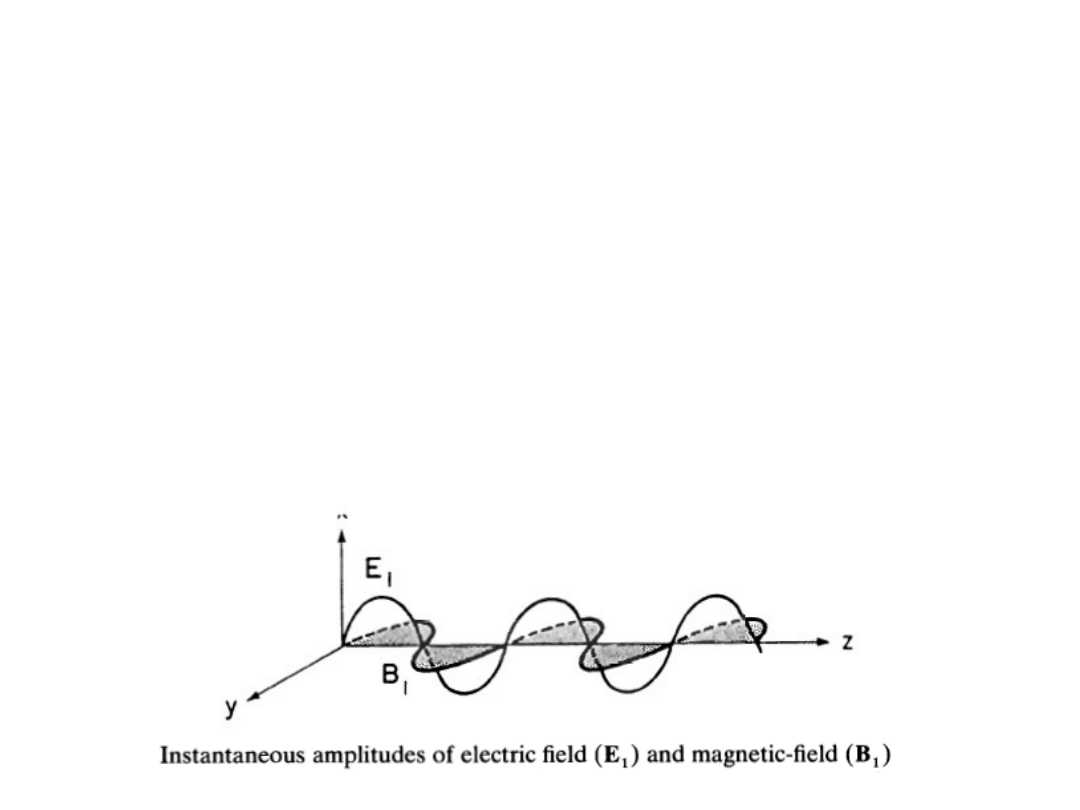
Electromagnetic radiation may be regarded
classically as coupled electric (E) and magnetic (B)
fields perpendicular to the direction of propagation
, both oscilating at some frequency ().
The energy of any given photon is given by
the quantity h, where h is the famous Planck
constant
For EPR, the commonly used frequency
range is 10
9
-10
11
s
-1
(1-100 GHz)
Electromagnetic resonance
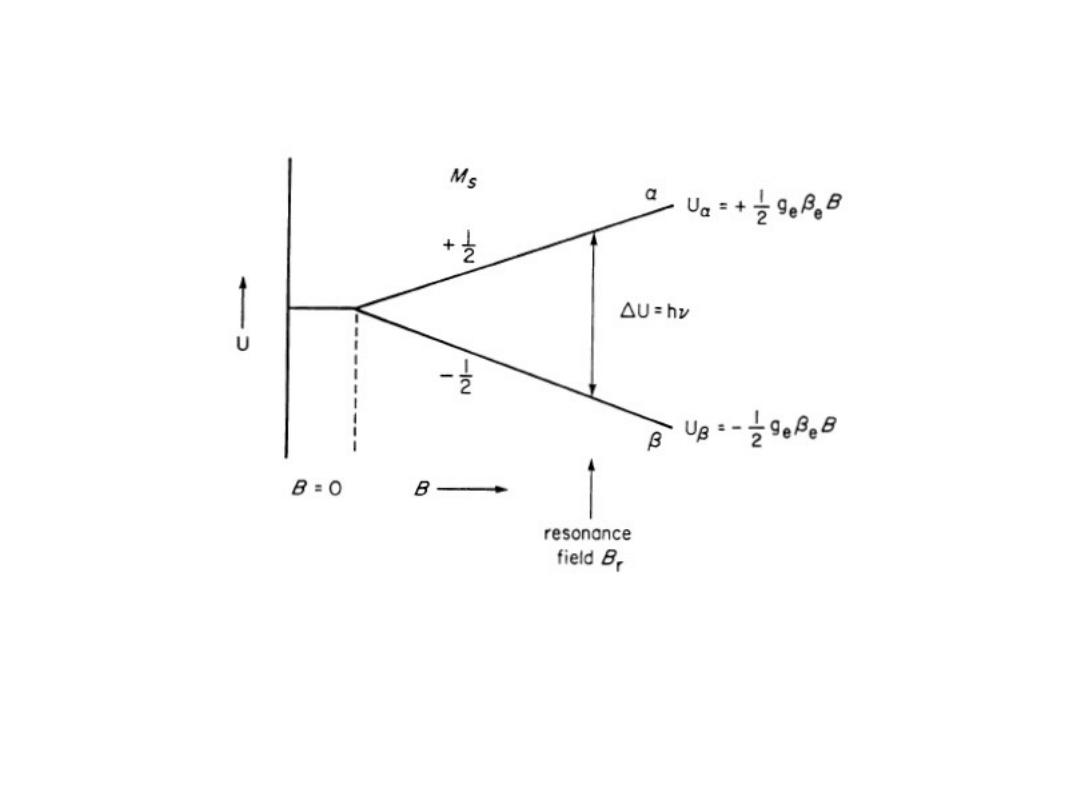
Energy-level scheme for the simplest system
(free electron) as a function of applied magnetic
field B. U
and U
represents the energies of the Ms
= +1/2 and –1/2.
Resonance condition
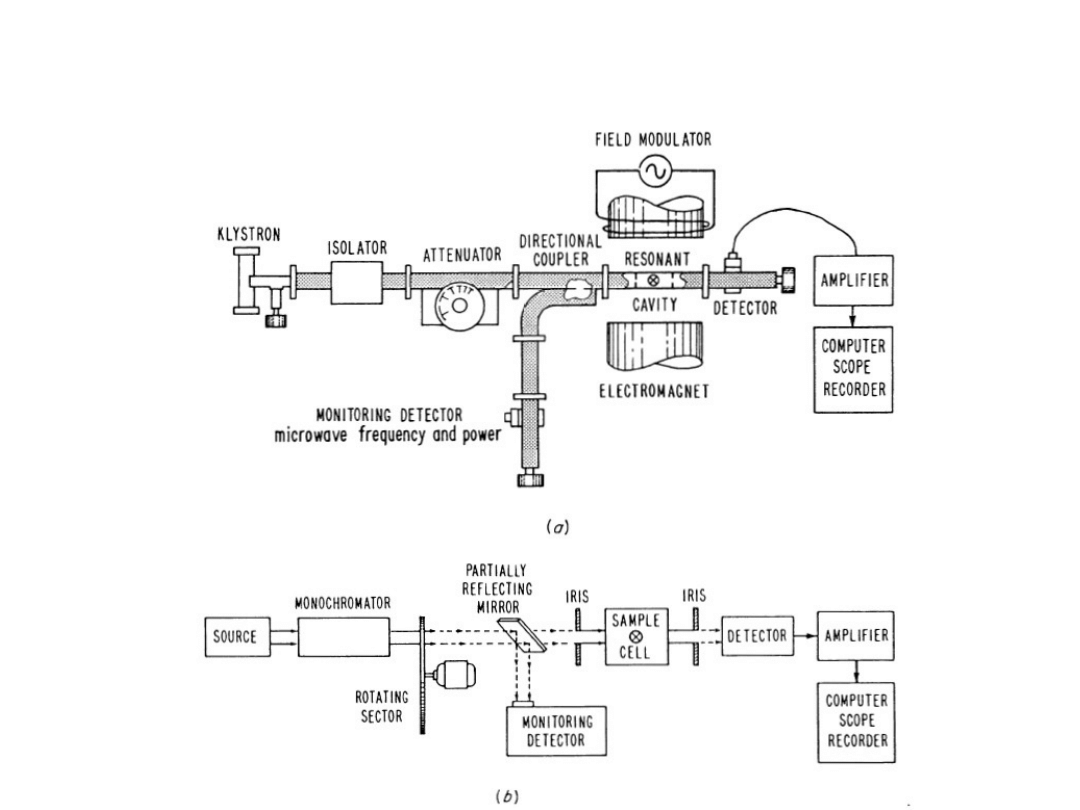
EPR spectrometer scheme

Source – usually a klystron, a vacuum tube wuth
low noise characteristics. The field is genetared by
oscillations within its own cavity. For commonly
used X-band specrometers the frequency is about
9,5 GHz (wavelenght of ~32 mm).
Resonator – most commonly used is resonant
cavity. The one wishes to operate in resonant
mode that maximalizes B in the location of the
sample – at resonance, the energy density in
resonator may be thousands of times that in the
waveguide. As alternative recently developed
loop-gap resonator may be used for energy
dissipative samples. Transmision cavities, with
separate input and output irises are rarelly used.
In practice, a reflection cavity, in which single iris
fulfills both functions, is commonly used.
EPR spectrometer

Magnetic field - for NMR and EPR the static
magnetic field is necessary and must be very stable
and uniform over sample volume, as in other case
observed spectral line is broadened. Simple
electromagnet of well defined characteristic is
used.
Detector – numerous types of solid-state diodes are
sensitive to micowave energy. Absorption of
photons by the sample is indicated by change in the
detector current. A direct detection of the
absorption signal is avoided due to noise. Signal-to-
noise ratio is improved by signal modulation at
preselected frequency. Typically, the resulting
signal is rectified and resembles the first derivative
of an absorption line.
EPR spectrometer
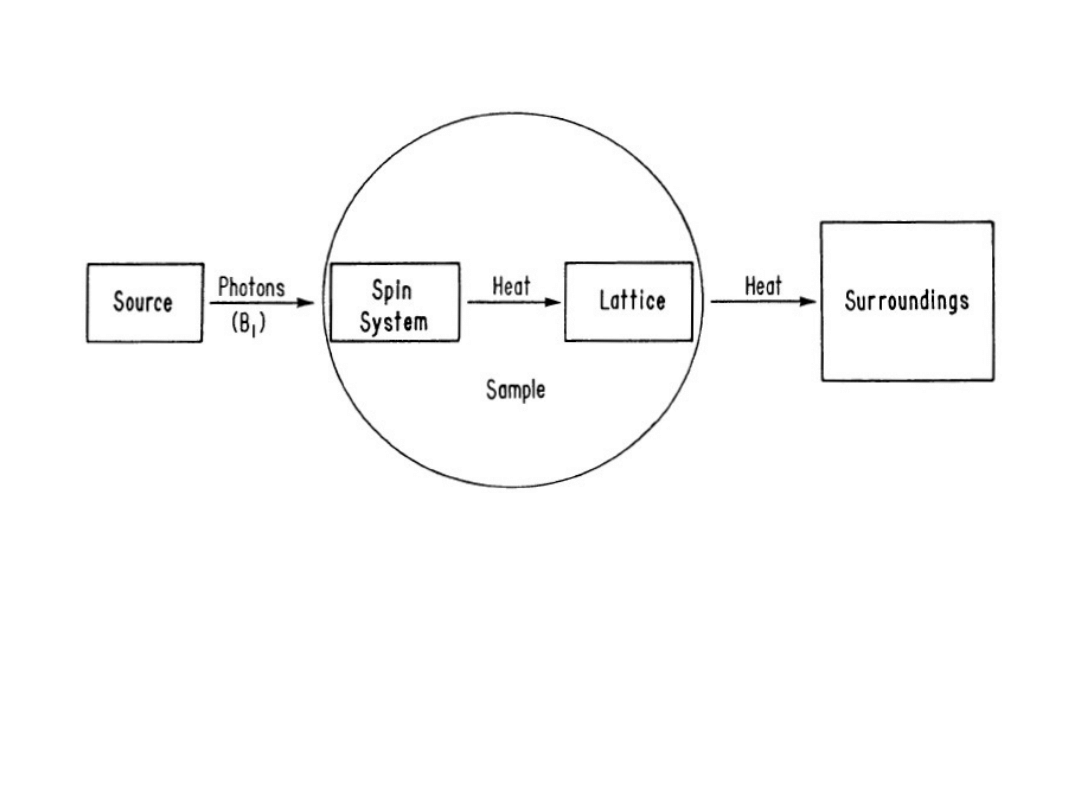
Energy flow in magnetic-resonance
experiment
Other possible way is to transfer energy to
another paramagnetic species, such as oxygen on
metal ion from transition group. This has
implications in power-saturation experiments
(described later)

- free radicals in the solid, liquid and gasseous
phases
- transition ions
- various point defects (localised inperfections) in
solids, as a F center – electron trapped in crystals
and glasses
- systems with conducting electrons, e.g.
semiconductors
- REDOX centers in biological systems
EPR in science and technology
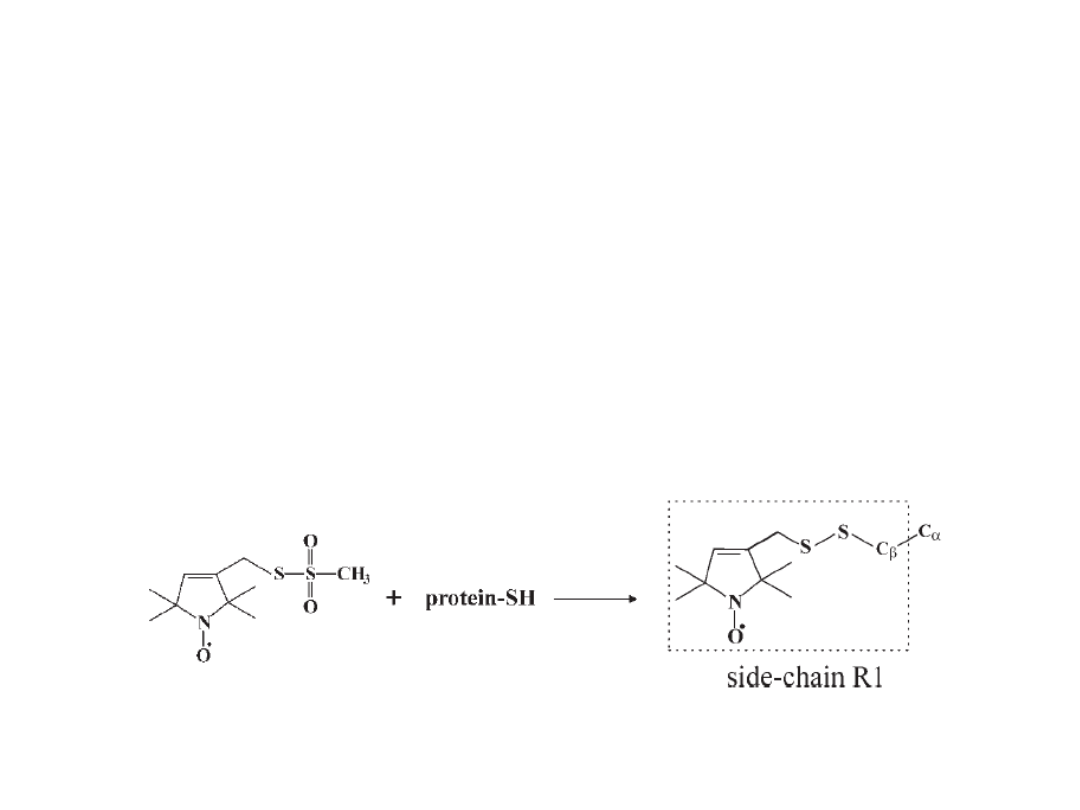
EPR and proteins
As proteins usually do not have unpaired
electrons it is necessary to introduce label to get
resonance signal. Commonly used one is MTSL [(1-
oxyl-2,2,5,5-tetramethylpyrroline-3-methyl)-
methanethiosulfonate]. MTSL react with –SH group
of cystein. The procedure is called site-directed spin
labeling (SDSL) and usually requires only one cystein
residue to be avaible for reaction.

SDSL – tool for monitoring the
structure and dynamics
From the EPR spectrum of R1, one can obtain
parameters as:
- solvent accessibility () – from the collision
frequency of the nitroxide with paramagnetic
reagents such as O2 and NiEDDA (Ni(II)
ethylenediaminediacetic acid) in solution — collision
of R1 with these reagents results in a decrease in the
spin-lattice relaxation time of the spin label
- mobility (Ms) of the R1 side chain
- the distance between R1 and another
paramagnetic center in the protein, which can be
either a second nitroxide or a metal ion
The mobility and distances are deduced from the EPR
spectral lineshape.

Advantages and disadvantages of SDSL
with EPR
+ use relatively small amounds of protein
+ sample can be prepared in conditions as close to
natural as preparation methods allow
+ spectra is simple and relatively easy to analyse
+ virtually the best approach to investigate large
membrane proteins
- need to introduce label, usually relatively small,
but still can alter protein structure/function
- not very usefull for proteins with much native
cystein residues
- getting global information about protein structure
usually means very much work
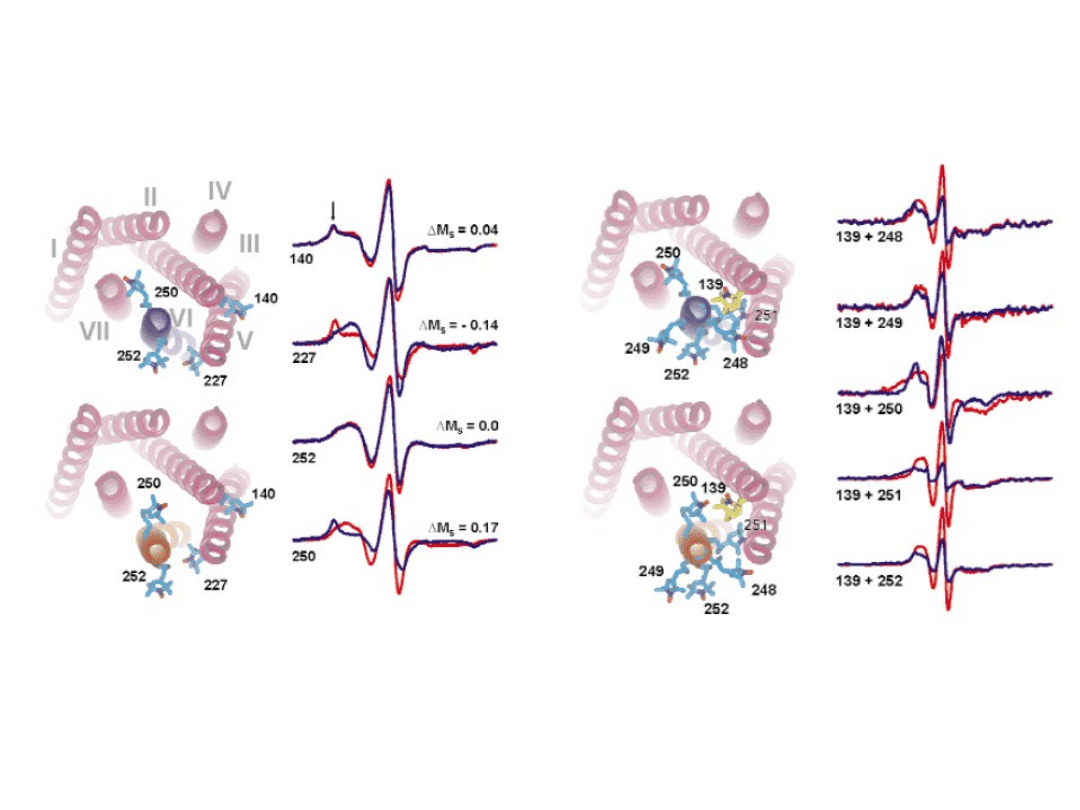
Example on rhodopsin
Mobility change in the
resting (blue helix)34
and activated (red
helix) states
Distance
measurement
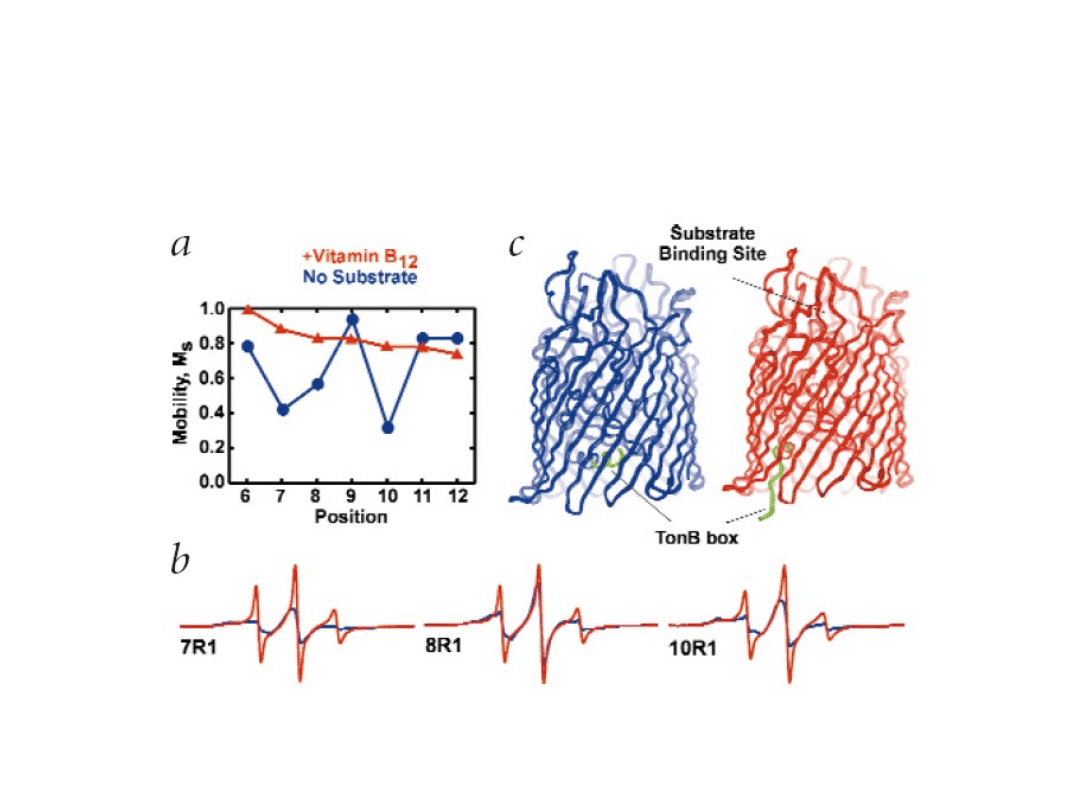
Ton-box in BtuB unfolds in response to substrate
binding becoming avaible for TonB
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62
- Slide 63
- Slide 64
- Slide 65
- Slide 66
- Slide 67
- Slide 68
- Slide 69
- Slide 70
- Slide 71
- Slide 72
- Slide 73
- Slide 74
- Slide 75
- Slide 76
- Slide 77
- Slide 78
- Slide 79
- Slide 80
- Slide 81
- Slide 82
- Slide 83
- Slide 84
- Slide 85
- Slide 86
- Slide 87
- Slide 88
- Slide 89
- Slide 90
- Slide 91
- Slide 92
- Slide 93
- Slide 94
- Slide 95
- Slide 96
Wyszukiwarka
Podobne podstrony:
Pierwsza pomoc prezentacja trener
Pierwsza Pomoc prezentacja
Patofizjologia L(1) - toksykologia leków, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne, Semes
Pomoc społeczna, służby społeczne, praca socjalna program prezentacji 2014 15
Osie, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne, Semestr II, Anatomia Prezentacje i prace
teksty do prezentacji, Pierwsza Pomoc
Pierwsza pomoc przedmedyczna PREZENTACJA MONIKI 1
Kwalifikowana I pomoc medyczna, Zabiegi medyczne - prezentacje i algorytmy
ANATOMIA DRÓG ODDECHOWYCH, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne, Semestr II, Anatomia
wers A z odpowiedziami test patofizjologia, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne,
Układ oddechowy w nurkowaniu, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne, Semestr II, Anato
Trzustka tekst, - PIERWSZA POMOC - ZDROWIE, - Ratownictwo Medyczne, Semestr II, Anatomia Prezentacj
więcej podobnych podstron