
Biokataliza – potencjalne
zastosowania w przemyśle
chemicznym
Stuart M. Thomas, Robert DiCosimo and Vasantha
Nagarajan
Trends in Biotechnology June 2002
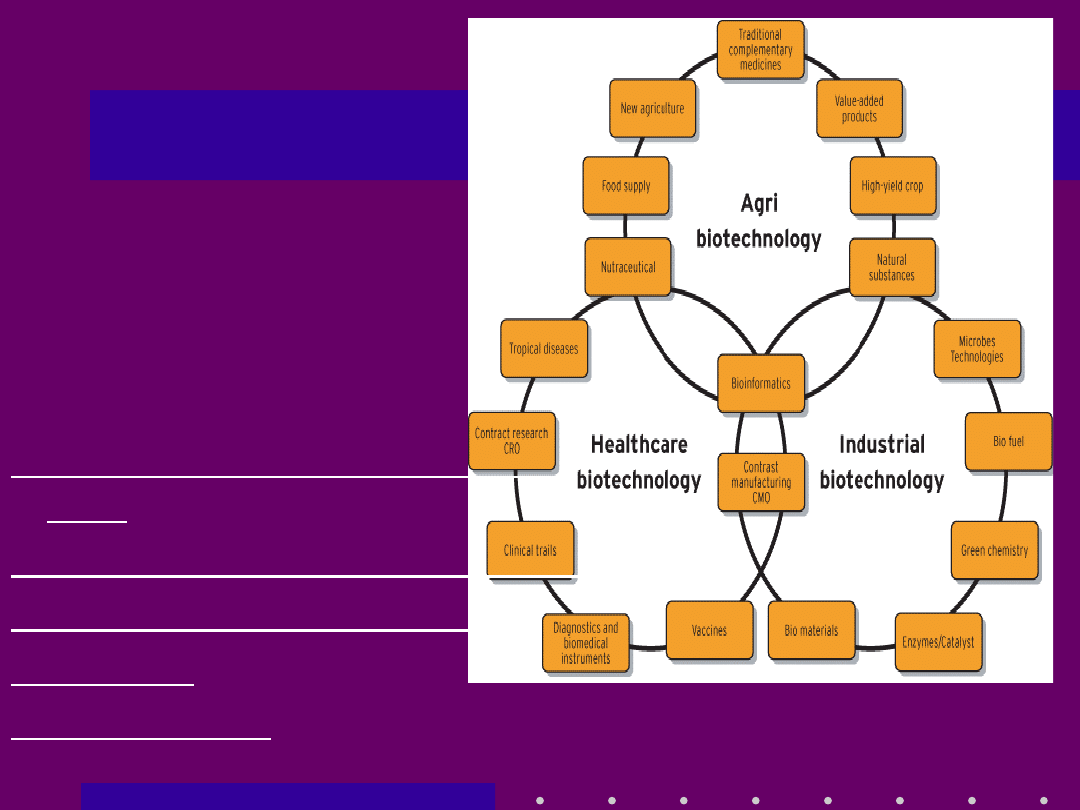
Biotechnol
ogia
• czerwona
• zielona
• biała ( przemysłowa )
Celem białej biotechnologii
jest
ukierunkowanie przemysłu na
zmianę sposobu syntezy
związków
( biokataliza )

Biotransformacja i
biokatalizatory
Biokatalizatory
są to substancje
biologiczne, które inicjują lub
zwiększają szybkość reakcji
chemicznych w żywych
organizmach, koniecznych do
przeżycia bądź reprodukcji.
Biotransformacja
jest to proces
chemiczny zachodzący przy udziale
wolnych enzymów lub zawierających
je tkanek oraz komórek
mikroorganizmów, roślin, zwierząt.

Wady i zalety biokatalizy w
porównaniu do katalizy
konwencjonalnej
•specyficzność
substratowa,
•chemoselektywność,
•regioselektywność,
•enancjoselektywność
•proces biokatalizy
prowadzony jest w
temperaturze i
ciśnieniu zbliżonych do
warunków otoczenia
Zalety
Wady
•wysokie koszty
biokatalizy
( recykling kofaktorów )
•małe objętości
otrzymanego produktu
• powstawanie tylko
jednej formy
enancjomerycznej

• mniejsza ilość
produktów ubocznych
•możliwość
wykorzystania wolnych
lub immobilizowanych
enzymów czy też całych
komórek
•zmniejszenie kosztów
poprzez użycie tanich
źródeł węgla w
pożywkach do wzrostu
mikrobiologicznego
• enzymy łatwo ulegają
inhibicji poprzez
zaostrzenie warunków
reakcji
• enzymy przejawiają
największą aktywność
katalityczną w wodzie
• wiele enzymów
wymaga kofaktorów
Wady
Zalety

Przemysł
chemiczny:
•
uznawany jest za przemysł kluczowy – chemiczne
produkty mają ogromny wpływ na codzienne życie
•
w samych tylko Stanach Zjednoczonych przemysł
chemiczny zarobił w ubiegłym roku 419 milionów
dolarów
•
a na całym świecie zysk z przemysłu chemicznego
przekracza 1,5 tryliona dolarów
•
wytwarzanie produktów chemicznych obecnie
wykorzystuje 7% produkcji energetycznej USA
•
w ciągu ostatnich dekad zwiększyło się wykorzystywanie
biokatalizy w konwersji produktów chemicznych ( np.
przemysł farmaceutyczny – kwas 6 – aminopenicylanowy,
przemysł spożywczy syrop glukozowy i fruktozowy )
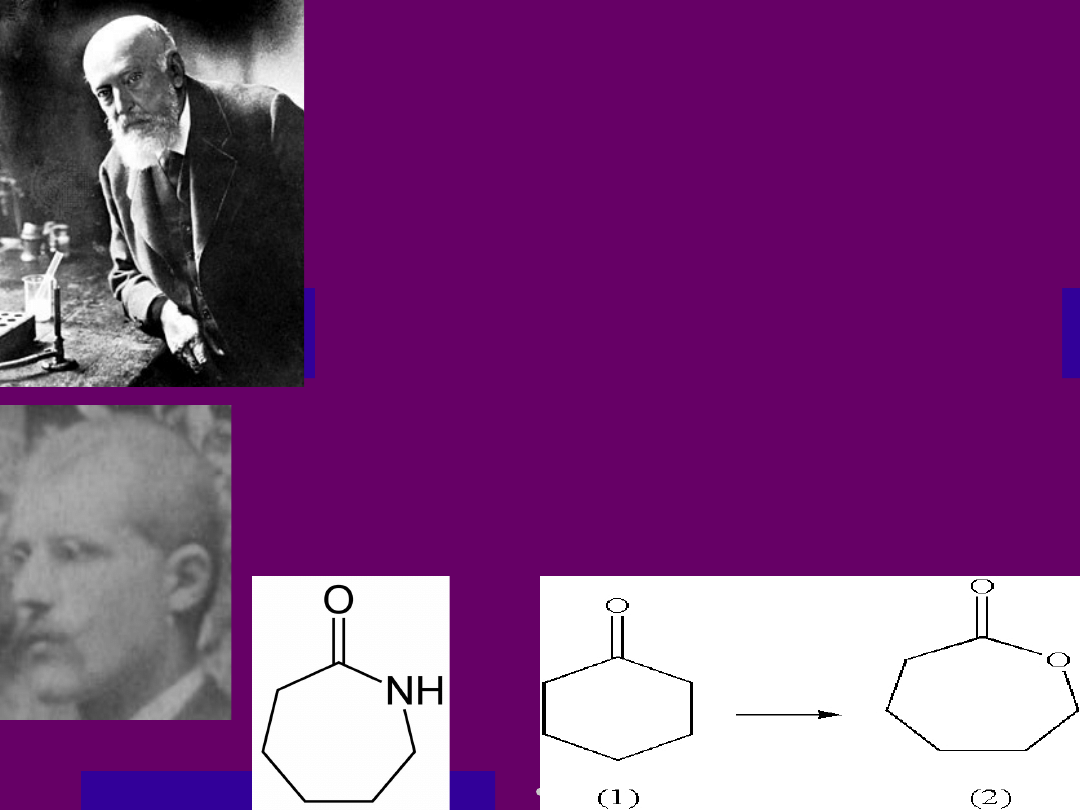
Biokonwersja
cykloketonów
Reakcja Baeyera – Villigera
• Jest to reakcja chemiczna polegająca na
utlenieniu cyklicznych ketonów do
cyklicznych estrów czyli laktonów
• W przypadku komercyjnej reakcji
chemicznej wykorzystywane są nadkwasy
• Najczęściej produkowanym laktonem jest
kaprolakton, którego światową produkcję
szacuje się na około milion funtów rocznie
( do produkcji wykorzystuje się kwas
nadoctowy ). Kaprolakton wykorzystywany
jest następnie do produkcji kaprolaktamu
•W systemach biologicznych cykliczne
ketony metabolizowane są w serii reakcji
redoks
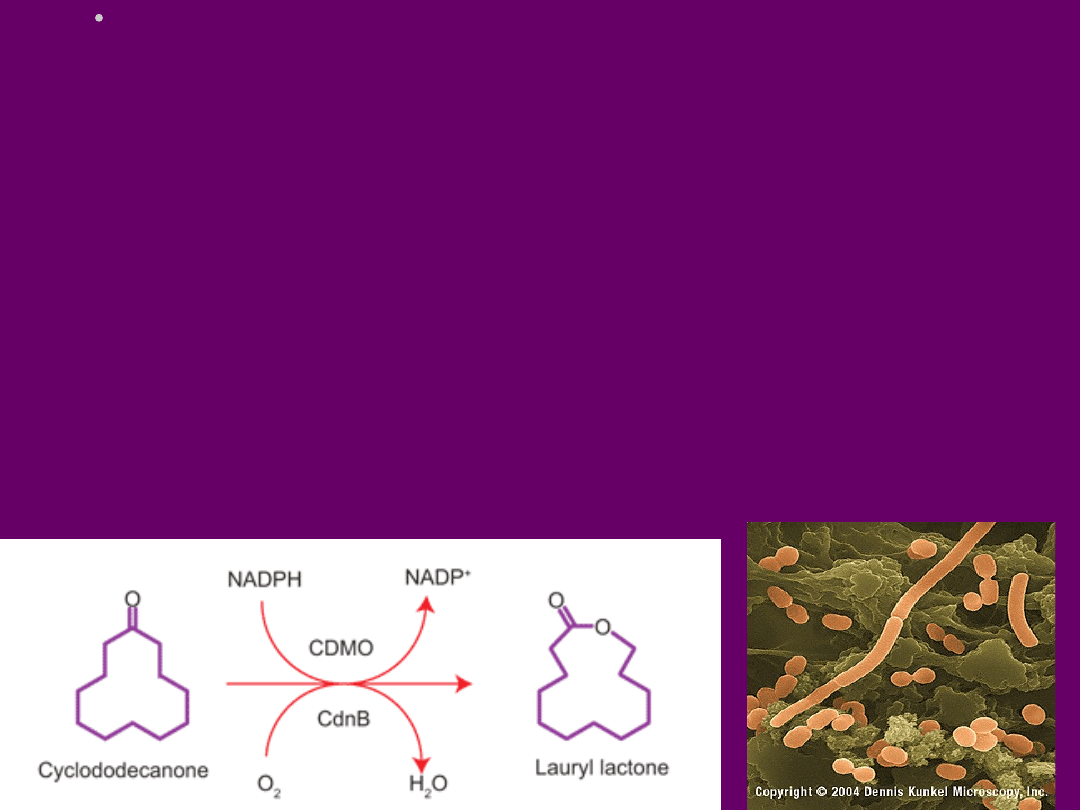
• Najczęściej stosowanym enzymem w biokatalizie tych związków jest
monooksygenaza Baeyera-Villigera
• Znajomość przebiegu cyklu metabolicznego cykloketonów pozwoli
na ukierunkowanie syntezy w stronę użytecznych i pożądanych
produktów
• Ostatnio poznano szlak oksydacji cyklodekanonu przez dwa gatunki
Rhodococcus – utlenianie to jest analogiczne jak w przypadku
cykloheksanonu. Odkrycie to pozwoli na produkcję - przykładowo
laktonu laurowego czy kwasu 12 – hydroksydodekanowego- związki
ten nie są dostępne na drodze konwencjonalnej syntezy chemicznej
• Biokataliza na skalę przemysłową prowadzona jest z użyciem
mikroorganizmów w szczególności zrekombinowanego
Acinetobacter
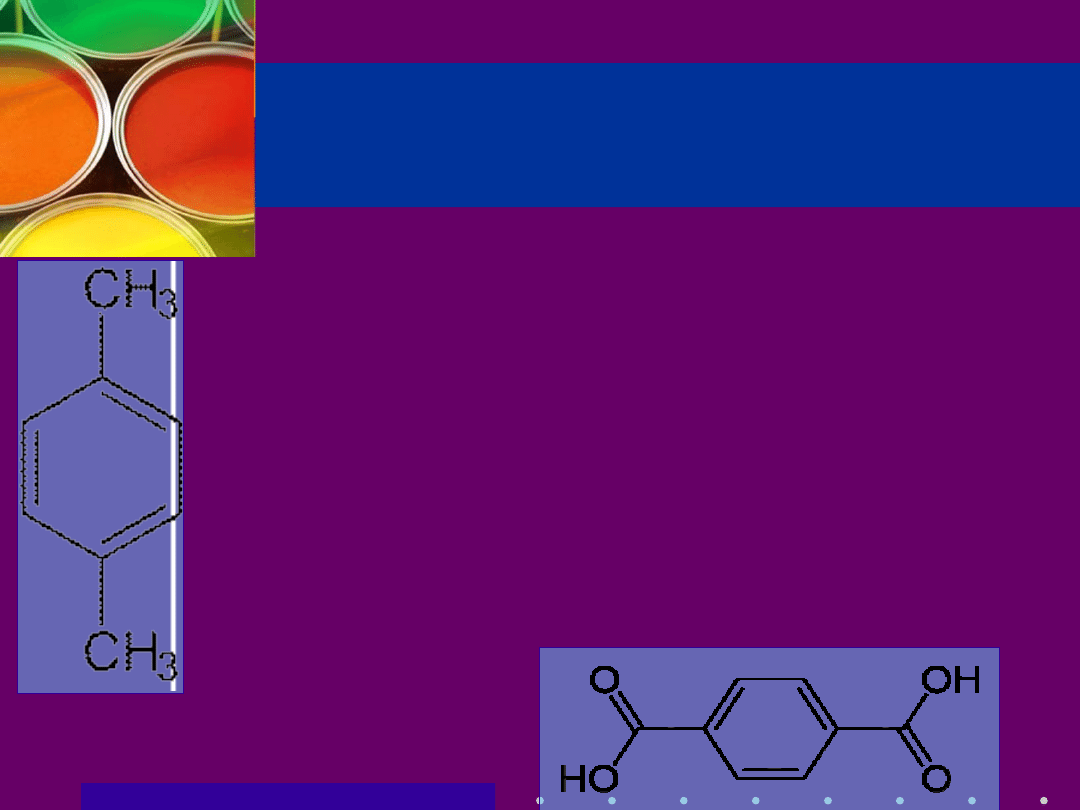
Biotransformacja
węglowodorów
aromatycznych
• Chemiczna oksydacja węglowodorów aromatycznych
ma głównie zastosowanie w produkcji składników
włókien, farb, klejów czy zmiękczaczy
• Zastosowanie biokatalizy zwiększa efektywność
energetyczną procesu, ułatwia oczyszczanie
końcowego produktu otrzymanego z wysoką
specyficznością i selektywnością
• Przykładowo wykorzystanie enzymów specyficznych
w kierunku meta -, orto -, para-ksylenu z którego
powstaję kwas tereftalowy, ułatwi proces
oczyszczania mieszanin poprzez selektywną
hydroksylację - punkty wrzenia składników
mieszaniny będą na tyle różne, że możliwe będzie
zastosowanie standardowej destylacji

Nitryle
• nitryle pochodzenia naturalnego są
syntetyzowane przez rośliny, grzyby i bakterie
• służą nie tylko jako magazyn azotu, ale także
jako czynnik chroniący przed atakiem
drapieżników
• istnieje kilka ścieżek biochemicznej degradacji
nitryli tj. utlenianie i hydroliza
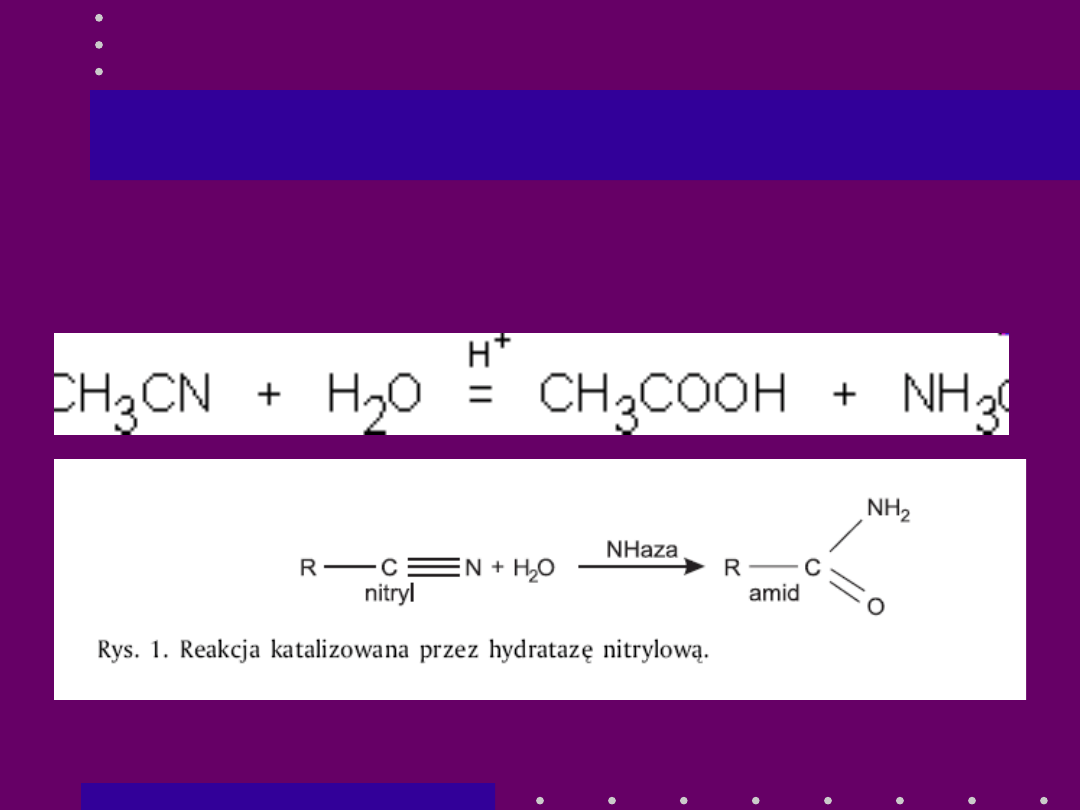
Biokonwersja nitryli
• Enzymatyczna hydroliza nitryli przebiega z udziałem enzymów -
hydratazy nitrylowej i nitrylazy
• Hydrataza katalizuje przekształcenie nitryli do odpowiednich
karboksyamidów (RCONH
2
), podczas gdy nitrylaza
przekształca nitryle w kwasy karboksylowe i amoniak
• Przykładem hydrolizy nitryli jest konwersja akrylonitrylu do
akrylamidu
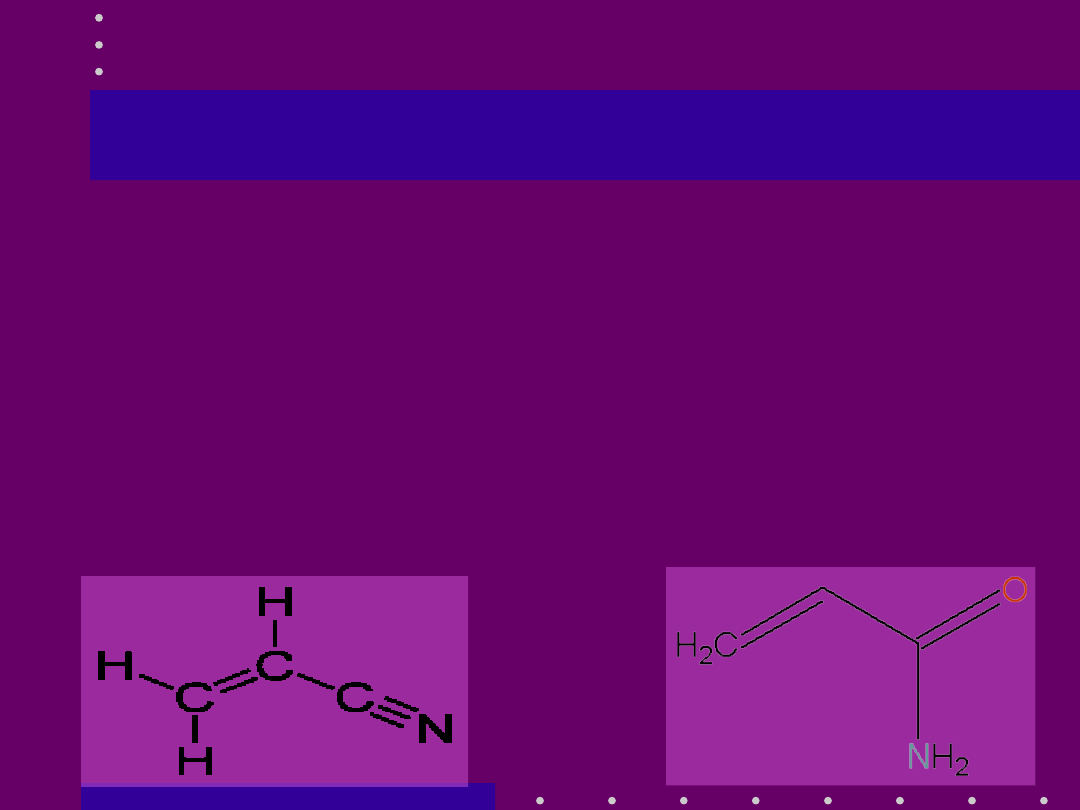
Enzymatyczna hydroliza
akrylonitrylu
• Firma Mitsubishi Rayon Co produkuje rocznie ok. 20
000 ton akrylamidu z akrylonitrylu wykorzystując
rekombinowane szczepy Rhodococcus rhodochnis J1. Z
1 grama suchej masy komórek produkowane jest
> 7000 g akrylamidu
• tradycyjnie akrylamid otrzymywany jest z
wykorzystaniem katalizatorów miedziowych; w
konwencjonalnej metodzie pojawia się problem izolacji
czystego produktu, konieczność eliminacji metali
ciężkich, wysokie straty wody i wysokie koszty
utrzymywanie wysokiej temperatury i ciśnienia podczas
trwania całego procesu
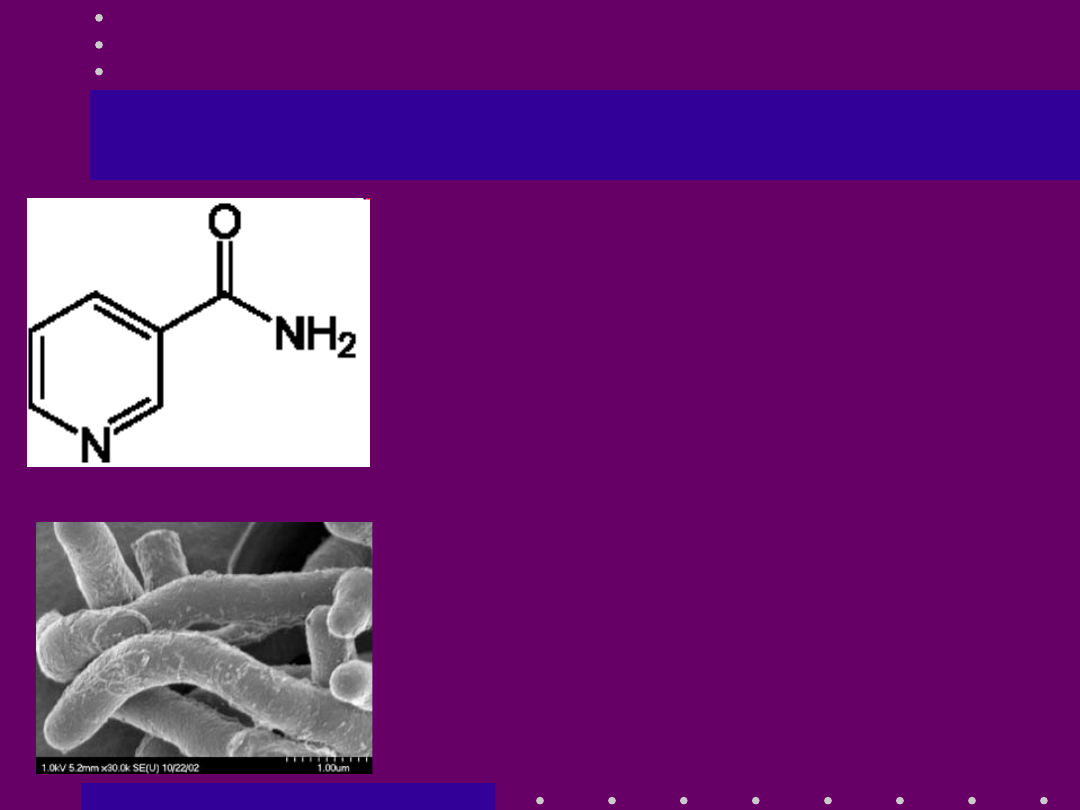
Otrzymywanie niacyny
• Firma Lonza Guangzhou Fine
Chemicals produkuje rocznie ok.
3400 ton niacyny
• wykorzystuje się immobilizowane
komórki Rhodococcus rhodachrous
• najpierw 2-metylo-1,5-diaminopentan
jest przekształcany do 3-
metylopirydyny, która jest następnie
amonifikowana a rezultatem procesu
jest 3-cyjanopirydyna ostatecznie
hydrolizowana do niacyny
• reakcja ta przebiega ze 100%
konwersją związku oraz powstaje
jedynie ok. 4% produktów ubocznych

Enzymatyczna produkcja 5-
cyjanowaleramidu
(5-CVAM)
•
tradycyjne otrzymywanie 5-CVAM
przebiega z zastosowaniem
katalizatorów w postaci dwutlenku
manganu, jednak proces ten jest
mało wydajny (już przy 25%
konwersji pojawia się produkt
uboczny adipoamid)
•
biotransformacja 5-CVAM
zachodzi z wykorzystaniem
szczepów Pseudomonas
chlororaphis B23. Hydratacja
adiponitrylu (ADN) w ilości 218 kg
daje 13,6 ton produktu, reakcja
przebiega z wydajnością 97%
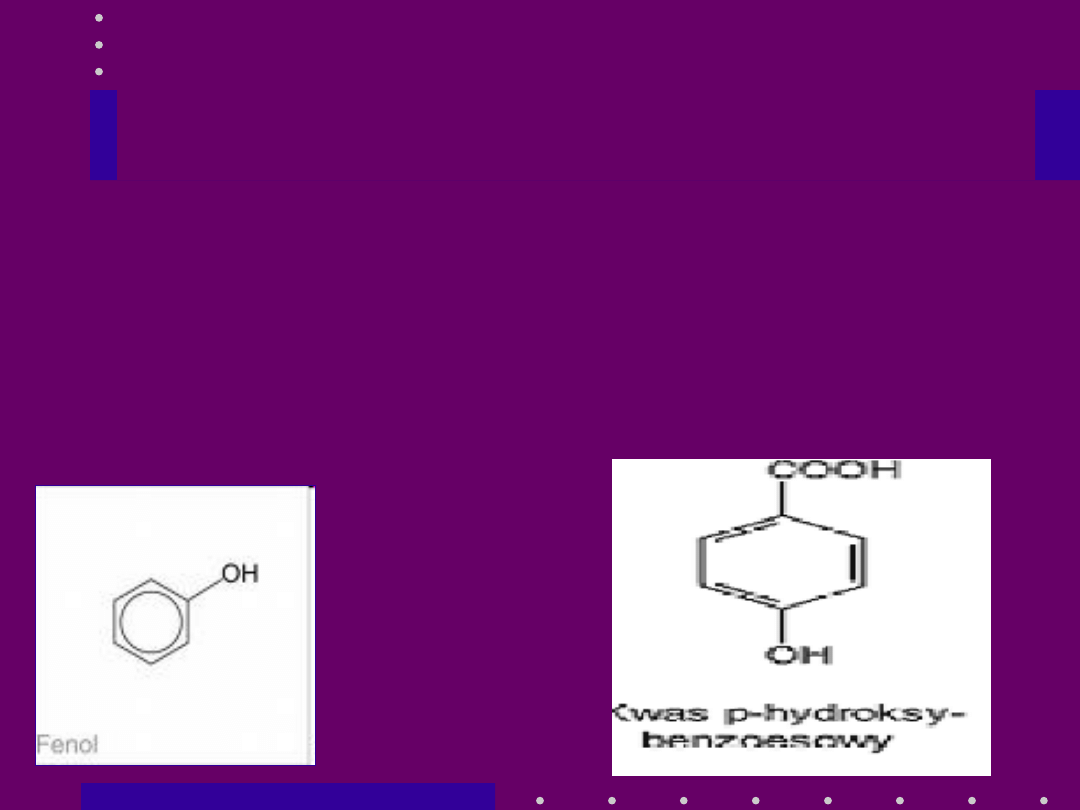
Enzymatyczna karboksylacja
substratów aromatycznych
• cel - karboksylacja fenolu do kwasu 4-
hydroksybenzoesowego (4-HBA)
• biologiczna karboksylacja fenolu jest bardzo
podobna do chemicznej reakcji Kolbego-
Schmitta( służącej m.in. do produkcji 4-HBA)
• ograniczeniem reakcji Kolbego-Schmitta są
występujące w dużej ilości produkty uboczne

Konwersja glukozy do 1,3-
propanodiolu (3G)
• W botransformacji wykorzystuje się rekombinowane
szczepy E.coli, przeprowadzające na dwóch szlakach
metabolicznych konwersję glukozy: najpierw powstaje
produkt pośredni - glicerol, który przekształcany jest
następnie do 3G

Podsumowanie
Przykłady przez nas przedstawione mogą być w
przyszłości stosowane na szeroką skalę w
biotechnologii. Aby wykorzystanie procesów
biotechnologicznych w przemyśle chemicznym
było ekonomicznie korzystne, muszą się one
cechować:
• mniejszym zużyciem energii
•większym stężeniem produktów
•oraz większą wydajnością katalizatorów
Jedną z wad procesów chemicznych jest
długoterminowa potrzeba wysokiej energii a co za
tym idzie wysokie koszty. Wiele procesów
chemicznych prowadzonych w sposób komercyjny
wymaga do swojego przebiegu wysokiej
temperatury i ciśnienia więc zużycie energii jest
bardzo duże, i prawdopodobnie znacznie wyższe
niż porównywalne biologiczne procesy.

Wiele firm chemicznych przechodzi obecnie
restrukturyzację w celu poprawienia wydajności i
zwiększenia zysków. Niektóre z tych firm obierają
biotechnologię jako potencjalną drogę produkcji.
Odkrycia chemiczne z początku XX wieku
zaowocowały wybuchem „syntetyczno-
polimerowej” rewolucji, która polepszyła jakość
życia ludzi na ziemi i stworzyła dobrze opłacalny
przemysł, teraz to biotechnologia jest gotowa do
wprowadzenia podobnej rewolucji w tym stuleciu.

Dziękujemy za
uwagę
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
Wyszukiwarka
Podobne podstrony:
MP 15 Zastosowanie mikroorganizmów w przemyśle chemicznym
operator urzadzen przemyslu chemicznego 815[01] z1 04 n
wyplyw cieczy ze zbiornika, Technologia chemiczna, 5 semestr, Podstawowe procesy przemysłu chemiczne
Największe zastosowanie przemysłowe mają jak dotąd żeliwa szare
operator urzadzen przemyslu chemicznego 815[01] z2 01 u
egzaminA06 2014 08 01 operator urzadzen przemyslu chemicznego 5str
Kompatybilność elektromagnetyczna w zastosowaniach przemysłowych
operator urzadzen przemyslu chemicznego 815[01] z1 03 n
egzaminA06 2013 10 X operator urzadzen przemyslu chemicznego 13str
operator urzadzen przemyslu chemicznego 815[01] z1 02 u
operator urzadzen przemyslu chemicznego 815[01] z2 01 n
Osiągnięcia przemysłu chemicznego po II wojnie światowej
operator urzadzen przemyslu chemicznego 815[01] o1 03 u
operator urzadzen przemyslu chemicznego 815[01] o2 01 n
Miejscowe zastosowanie środków chemicznych wspomagających walkę z płytką nazębną 2
egzaminA06 2014 08 X operator urzadzen przemyslu chemicznego 13str
operator urzadzen przemyslu chemicznego 815[01] o2 02 n
operator urzadzen przemyslu chemicznego 815[01] o2 06 n
więcej podobnych podstron