
RÓWNOWAGI FAZOWE
RÓWNOWAGA CIECZ -
CIECZ

KLASYFIKACJA
ROZTWORÓW
• Z punktu widzenia
termodynamicznego
– Doskonałe
– Niedoskonałe
• Doskonałe - wieloskładnikowe
jednofazowe (prawo Raoulta)
• Doskonałe gazy – spełnienie prawa
Daltona

ROZTWORY DOSKONAŁE
• Trzy warunki:
• Całkowita energia wewnętrzna
układu jednofazowego
dwuskładnikowego jest liniową
funkcją składu
• Objętość ogólna roztworu winna być
liniową funkcją składu
• Zmiana entropii: S=- R T ln X
i

Roztwory niedoskonałe
• Jeżeli jeden z trzech warunków
niespełniony
• Roztwory prawidłowe (regularne)
– War 1 , inne warunki tak
• Roztwory atermiczne
– War 3

Podział ze względu na
właściwości strukturalne
• Mieszaniny gazów
• Roztwory w ciekłych rozpuszczalnikach
• Gazów
• Nieelektrolitów
• Elektrolitów (ścisłą teorię ilościową)
• Związków wielkocząsteczkowych
(technologia organiczna)
• Roztwory stałe
• Układy koloidalne

Procesy nierównowagowe.
Dyfuzja
• Rozpatrzmy cukier w szklance wody
• Zróżnicowanie stężenia w różnych
miejscach - zróżnicowane
parametry stanu
• Dochodzenie do stanu równowagi:
• Szybkość rozpuszczania cukru
• Szybkość odprowadzania
cząsteczek cukru w głąb roztworu

Dyfuzja
• Zjawisko przenoszenia cząsteczek
jednej substancji względem
cząsteczek drugiej substancji
wewnątrz jednej fazy, wywołane
istniejącym w roztworze
gradientem stężenia, nazywamy
dyfuzją

Opis w stanie
nierównowagi
• Objętość fazy na tyle duża, aby
zmiany parametrów stanu można
było traktować jako ciągłe.
• Taka liczba cząsteczek aby można
było stosować elementy statystyki
• Bodziec – gradient stężenia
• Szybkość dyfuzji = - D gradient C
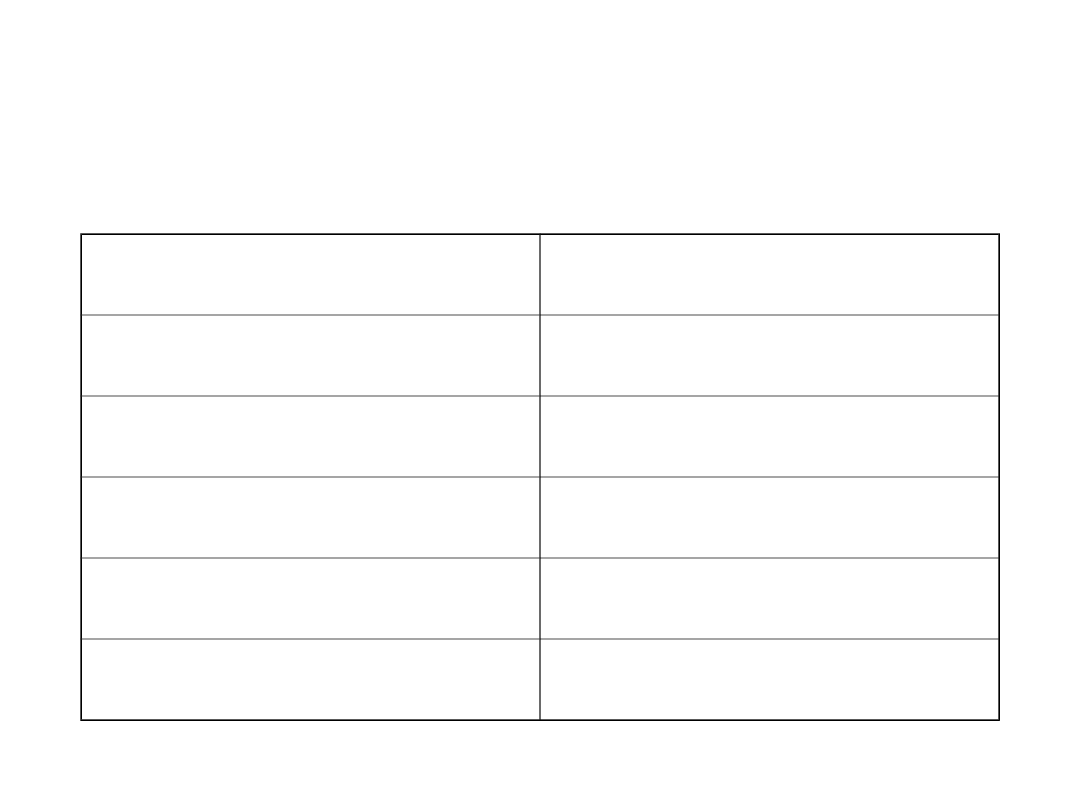
Współczynniki dyfuzji
D/10
-9
m
2
s
-1
w
temperaturze 25° C
Woda w wodzie
2,26
Ar w CCl
4
3,63
Metanol w wodzie
1,58
Sacharoza w wodzie
0,522
Glicyna w wodzie
0,673
Tlen w CCl
4
3.82

Współczynnik dyfuzji
• [D] cm
2
sec
-1
• W gazach - rzędu 10
-2
• W cieczach –rzędu 10
-5
• W ciałach stałych – rzędu 10
-10

Znaczenie D
• Rozchodzenie się zanieczyszczeń
w jeziorach i atmosferze
• Ruch całości – konwekcji
• Ruch cząsteczki:
• Wypadkowa odległość x
2
= 2Dt

Zadanie
• Współczynnik samodyfuzji H
2
O w
wodzie w temperaturze 25°C wynosi
2,26 10
-9
/m
2
s
-1
. Ile czasu potrzebuje
średnio cząsteczka wody, by pokonać
odległość a) 1 cm b) 2 cm od punktu
wyjścia w niemieszanej próbce wody?
• X = 2Dt, t=x
2
/2 D t = 0,01 x 0,01/(2x
2,26 10
-9
). 6,1 h t
2
= (4/4,56) 10
5
=25
h

Równanie Einsteina -
Smoluchowskiego
• Ruch cząsteczek jako błądzenie
przypadkowe D, szybkością,
długością kroków,
• D=
2
/2
• Cząsteczka która wykonuje szybko
długie kroki wykazuje duży
współczynnik dyfuzji

Zadanie
• Przyjmijmy, że cząsteczka wody
pokonuje w procesie samodyfuzji za
każdym przeskokiem drogą równą
swej średnicy (około 200 pm). Ile
czasu wymaga jeden przeskok w
temperaturze 25 °C?
• (2 10
-10
m )
2
= 2 2,26 10
-9
t
• t=4 10
-20
/4,52 10
-9
= 9 ps

Wpływ temperatury
• D wzrasta z temperaturą
• Cząsteczka uwalnia się od sił
przyciągania
• Zwiększa się szybkość
błądzeniazmniejsza się czas błądzenia t
• Jeżeli szybkość błądzenia przypadkowego
spełnia równanie Arrheniusa o energii
aktywacji, to współczynnik dyfuzji
powinien wykazać zależność:

D vs. temperatura
• D e
-(E/RT)
• Szybkość powiązana jest z lepkością
cieczy
• Im większa lepkość tym mniejszy D
czyli:
e
(E/RT)
• Czyli lepkość maleje ze wzrostem
temperatury.

Zadanie
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
Wyszukiwarka
Podobne podstrony:
7 uklady rownowagi fazowej id 4 Nieznany
chem.fiz.równowagi fazowe, Inżynieria środowiska, inż, Semestr III, Chemia fizyczna, laboratorium
Badanie równowagi fazowej w układzie trójskładnikowym 8.3, Technologia chemiczna, Chemia fizyczna, l
7 Analiza termiczna w zastosowaniu do wyznaczania wykresu równowagi fazowej
układy równowagi fazowej
Wykres układu równowagi fazowej, Polibuda, NoM
Analiza termiczna w zastosowaniu do wyznaczania wykresu równowagi fazowej, Studia, SEMESTR 1, NOM
9.RÓWNOWAGI FAZOWE W UKŁADACH TRÓJSKŁADNIKOWYCH, Politechnika Łódzka, Technologia Żywności i Żywieni
Dwuskladnikowe uklady rownowagi fazowej, Księgozbiór, Studia, Materiałoznastwo
9 10 Uklad rownowagi fazowej zelazo cementyt
7 8 Uklady rownowagi fazowej
Wykład Ch F równowagi fazowe
wykład+nr+4+ +Wykresy+równowagi+fazowej+stopów
7.RÓWNOWAGI FAZOWE W UKŁACH JEDNOSKŁADNIKOWYCH, Politechnika Łódzka, Technologia Żywności i Żywienie
wykład+nr+5+ +Wykresy+równowagi+fazowej+stopów+c d
6 Rownowagi fazowe B
Równowagi fazowe, wykład
więcej podobnych podstron