
Teoria skurczu
mięśniowego w
kategoriach biofizyki
Tkacz Weronika, Franków
Iwona , Kiszka Rafał gr.II

• Mięśnie w organizmie żywym przekształcają
bezpośrednio energię chemiczną w energię
mechaniczną (pracę) i (lub) ciepło. Stanowią
swoiste silniki chemiczne, silniki molekularne.
Wspólną cechą mięśni jest zdolność do
odpowiadania skurczem na docierające do nich
sygnały pobudzające. Skurcz jest wynikiem
oddziaływań pomiędzy znajdującymi się w każdej
komórce mięśniowej wyspecjalizowanymi
białkami kurczliwymi. Z białek tych zbudowane są
miofilamenty czyli nitkowate struktury
stanowiące element roboczy tego „silnika
molekularnego” przetwarzającego energię
chemiczną w energię mechaniczną.
• Aby zrozumieć w jaki sposób sygnał docierający
do powierzchni komórki mięśniowej przenika do
jej wnętrza inicjując skurcz, należy poznać
elementy biorące udział w tym zjawisku.
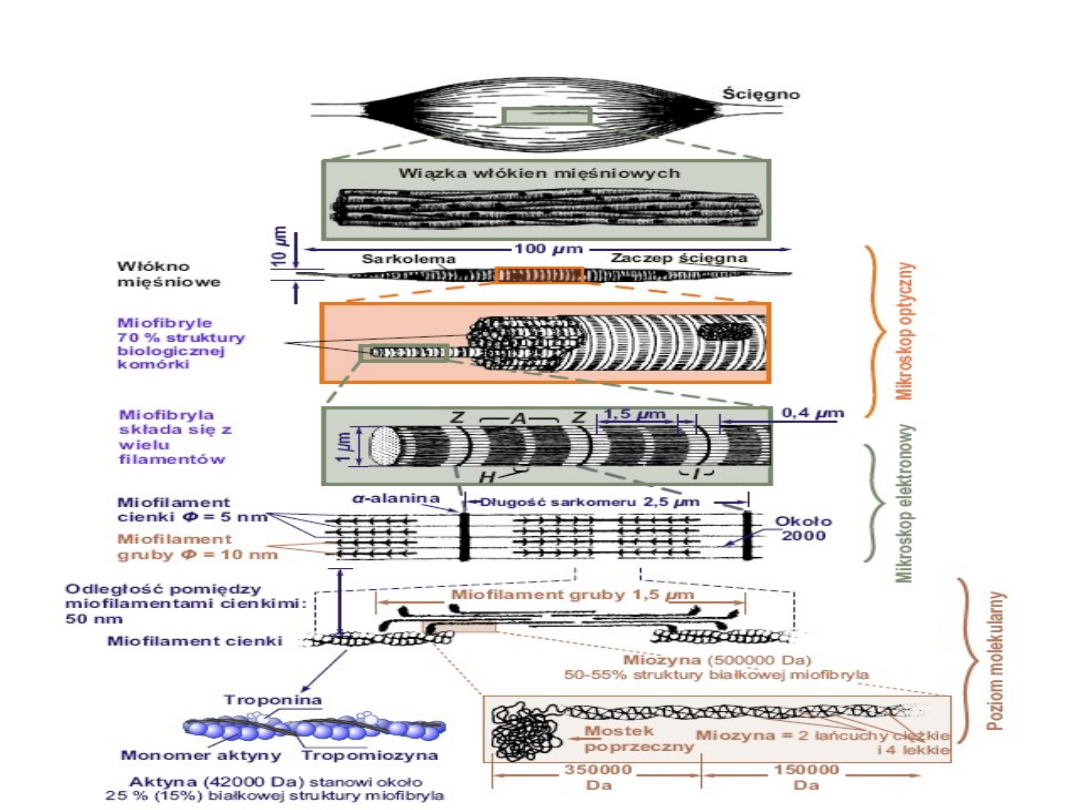
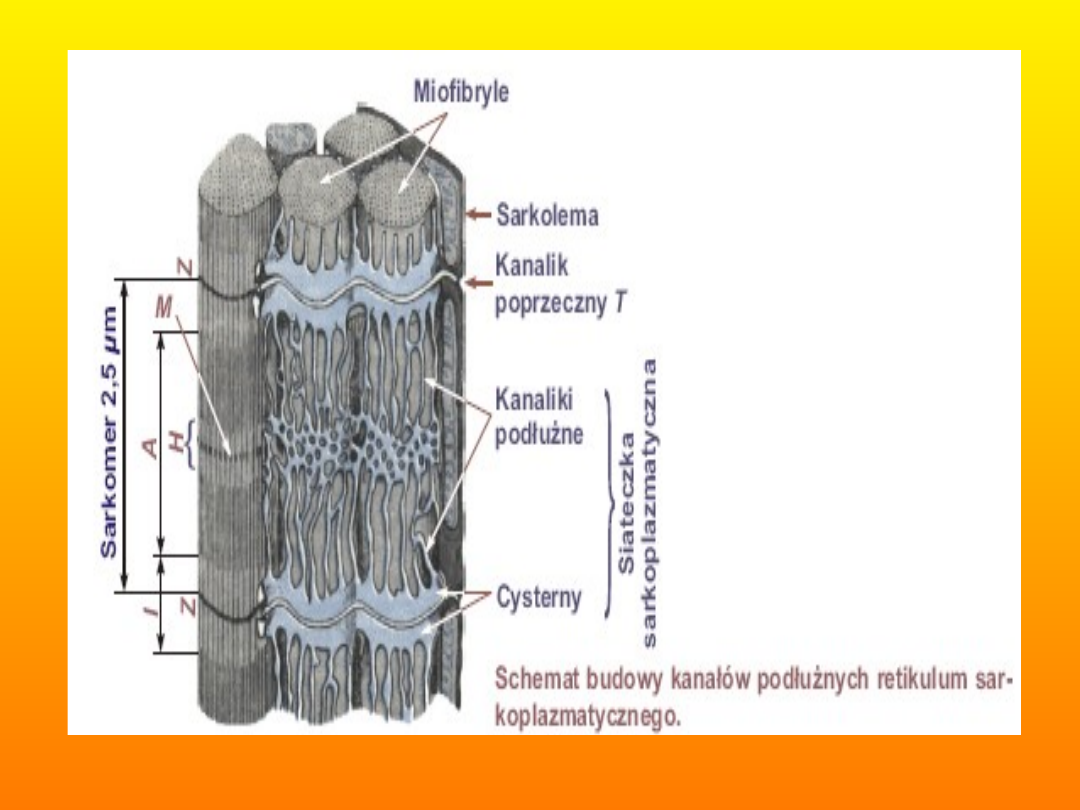
• 1. Mięsień poprzecznie prążkowany

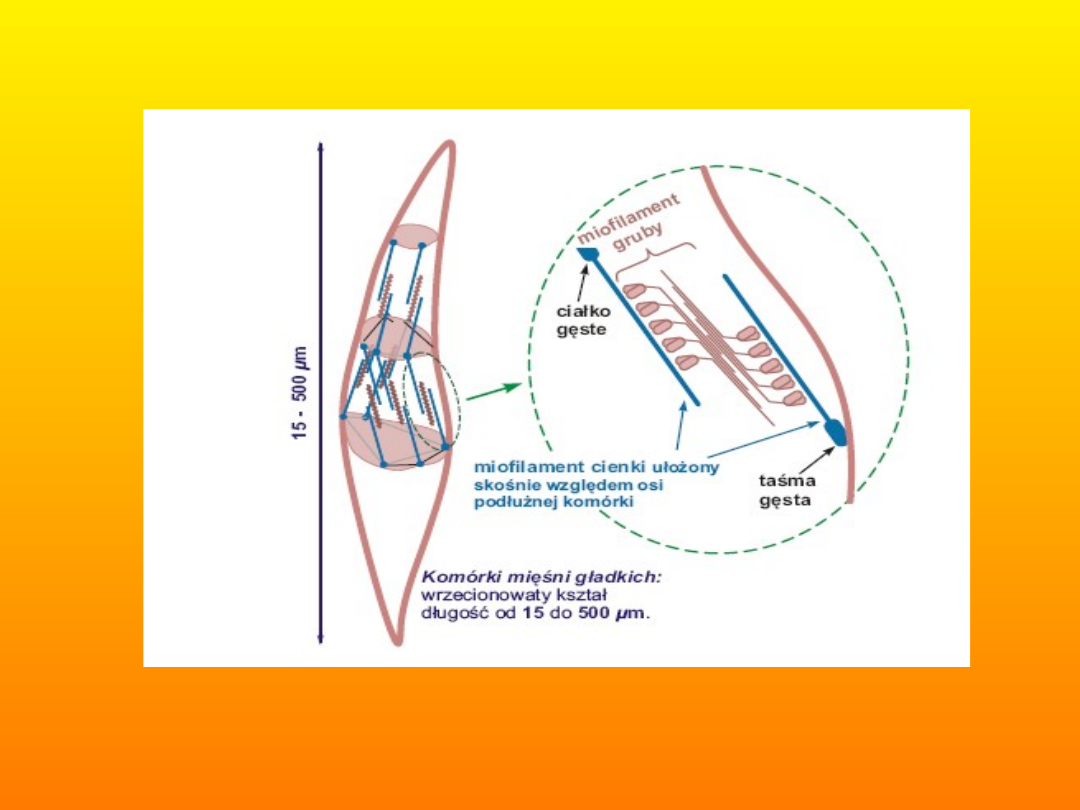
• 2. Komórka mięśnia gładkiego
Miofilamenty aktynowe umocowane są do struktur
znajdujących się pod błoną komórkową (taśma
gęsta) lub w cytoplazmie (ciałko gęste). Między
nimi, równolegle do nich, rozmieszczone są
miofilamenty miozynowe. Stosunek miofilamentów
aktynowych do miozynowych wynosi w tych
mięśniach 15:1. W mięśniach gładkich sposób
ułożenia cząsteczek miozyny w miofilamencie
grubym jest inny niż w miofilamencie mizynowym
mięśni poprzecznie prążkowanych. W mięśniach
gładkich nie występuje kompleks troponinowy. W
mięśniach gładkich oprócz aktyny i tropomiozyny w
skład cienkich miofilamentów mięśni gładkich
wchodzą dwa białka - kaldesmon i kalponina

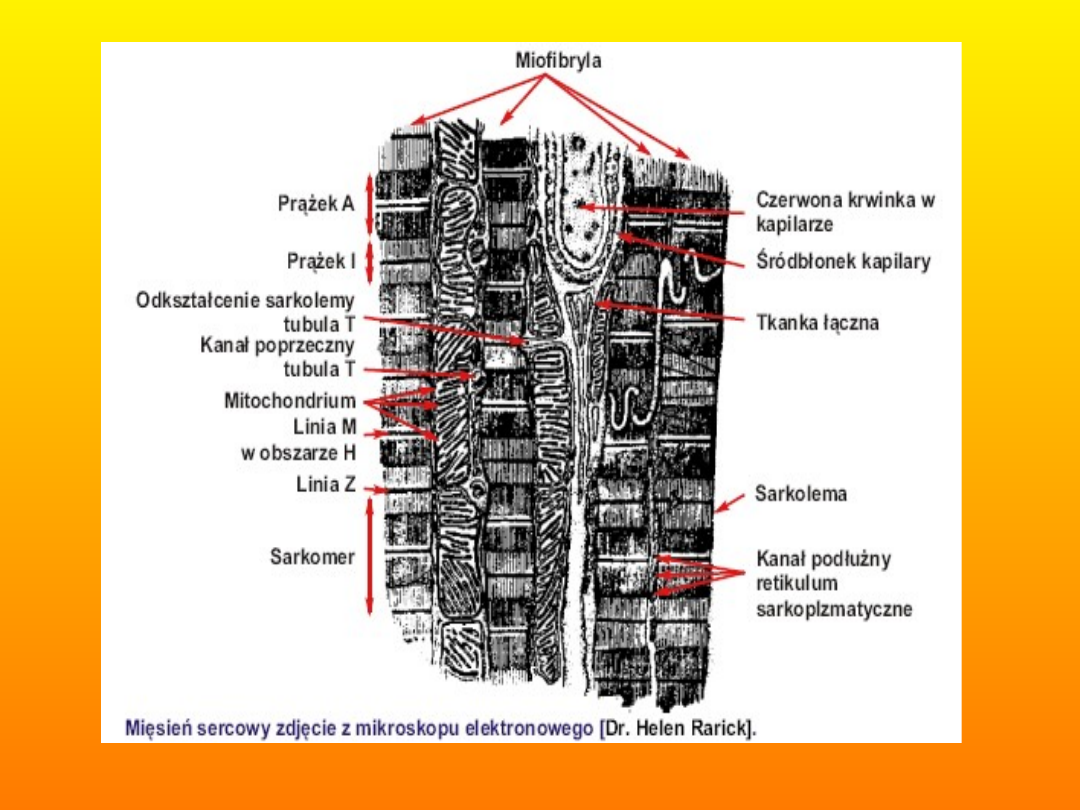
• 3. Komórka mięśnia sercowego
Komórka zawiera wielką liczbę
miofibryli, prążkowanych
podobnie jak w mięśniach
szkieletowych. Dużą część
objętości komórki zajmują
mitochondria (synteza ATP,
źródła energii dla ciągle
pracującego mięśnia). Miofibryle
i mitochondria zajmują 85 %
objętości komórki.
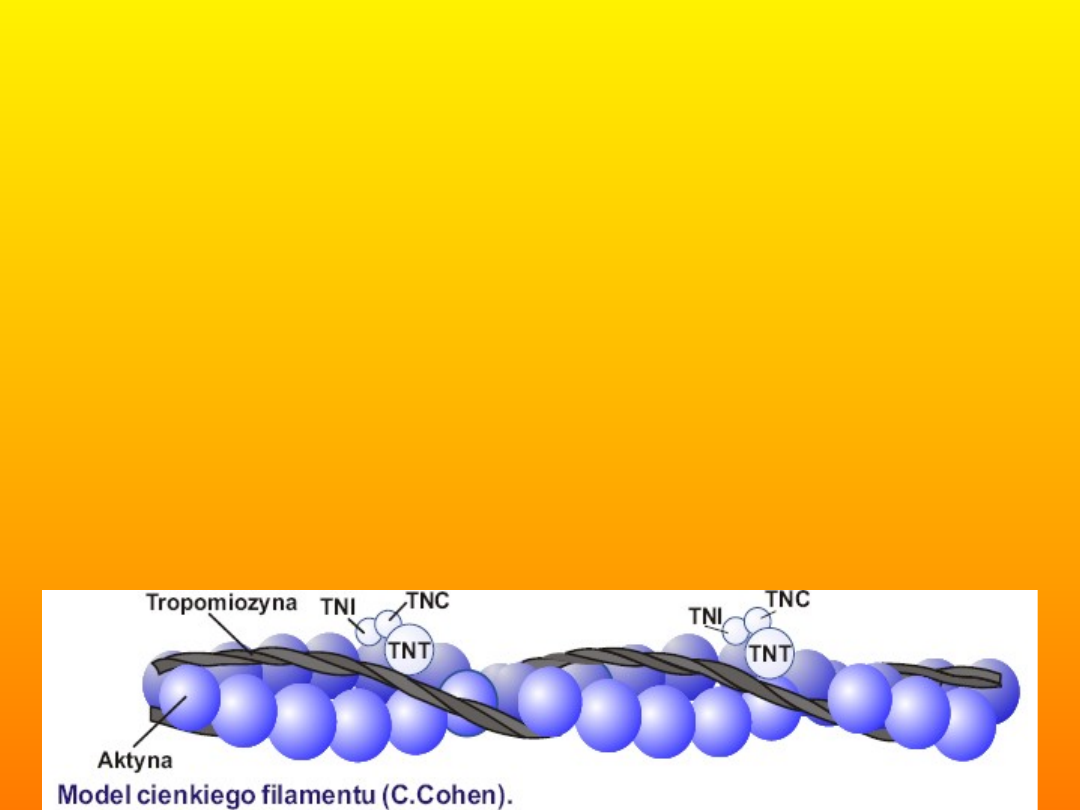
• 4. Budowa miofilamentów .
Komórki tkanki mięśniowej zawierają
aparat kurczliwy zbudowany z
miofilamentów (mikrofilamentów) -
cienkich włókienek białkowych
cytoszkieletu.
Wyróżniamy:
• 4. 1 Miofilament cienki
Miofilamenty cienkie (6 nm),
zbudowane z białka aktyny i białek
towarzyszących przyczepionych do
błony komórkowej.

– Miofilament gruby
Miofilamenty grube (12 nm),
zbudowane z mechanoenzymu
miozyny. W komórkach mięśniowych
kilkaset cząsteczek miozyny tworzy
miofilament układając się w ten
sposób, że ich fragmenty “kroczące”
po powierzchni aktyny wystają na
zewnątrz. Miofilamenty grube
wykorzystując energię z ATP i
“krocząc” po nich przesuwają je
względem siebie (miofilamenty nie
kurczą się!).

• Cząsteczka miozyny ma postać wydłużonej
pałeczki zakończonej z jednej strony
maczugowatym zgrubieniem złożonym z dwóch
podjednostek zwanych głowami miozyny. Część
podłużna ma strukturę podwójnej spirali. Głowy
miozyny mają strukturę globularną. Dwie głowy
cząsteczki miozyny razem tworzą mostek
poprzeczny, który w procesie powstawania
skurczu łączy gruby miofilament miozynowy z
cienkim miofilamentem aktynowym. Na głowach
cząsteczki miozyny znajdują się miejsca wiązania
aktyny i ATP. Miozyna jest ATPazą, czyli enzymem
hydrolizującym
ATP do ADP i nieorganicznego fosforanu.
W skład pojedynczego miofilamentu grubego
wchodzi około 400 cząsteczek miozyny. Sposoby
agregacji różnią się w filamentach grubych mięśni
szkieletowych i gładkich.

• 5. Ślizgowa teoria skurczu
mięśnia
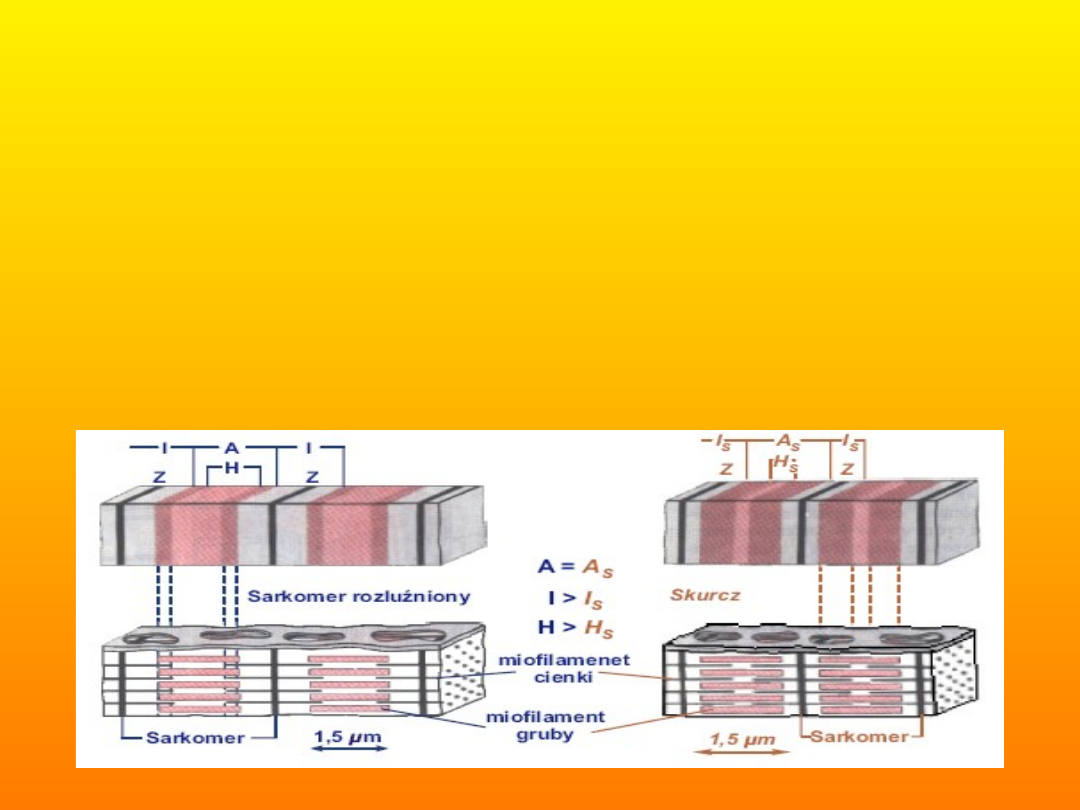
• Skrócenie sarkomeru. Mięsień skraca się w wyniku
skrócenia zespołu sarkomerów połączonych
szeregowo w miofibrylach. Porównując schemat
struktury sarkomeru w dwóch różnych stanach
funkcjonalnych (rysunek poniżej), można zauważyć
zmiany poprzecznego prążkowania i organizacji nici w
czasie jego skrócenia. Przy skróceniu cienkie aktyny
przesuwają się wzdłuż grubych miozyn w kierunku
ośrodka sarkomeru. W czasie nasuwania się aktyn na
miozynę nici cienkie i grube nie ulegają skróceniu,
ale jednocześnie skraca się sarkomer.

• We wszystkich komórkach mięśniowych sygnałem
inicjującym oddziaływanie aktyny z miozyną jest
wzrost stężenia jonów wapnia w sarkoplazmie.
Zwiększenie stężenia wapnia pobudza
oddziaływanie aktyny z miozyną. Powstaje
kompleks
białkowy a szybkość hydrolizowania ATP wzrasta,
ponieważ obecność aktyny
ułatwia odłączenie się fosforanu. Odczepieniu się
fosforanu towarzyszy zmiana konformacji mostka
poprzecznego łączącego aktynę z miozyną
wywołując przesuwanie się miofilamentów
względem siebie. Zsynchronizowane skracanie się
sarkomerów powoduje skracanie się całej komórki.
Jeżeli działania z zewnątrz nie dopuszczają do
zmiany długości zmiana konformacji mostków
poprzecznych wywołuje naprężenie sarkomeru,
generowana jest siła skurczu.

• Cykl mostka poprzecznego i jego relacja z ATPazą
aktomiozyny. Kolejne, główne kroki tego cyklu są
następujące:
• Przyłączenie ATP prowadzi do dysocjacji aktomiozyny na
aktynę i miozynę, następuje odłączenie filamentu grubego
i cienkiego. ATP łączy się z głową miofilamantu grubego,
• Miozyna hydrolizuje ATP, produkty hydrolizy ADP i Pi
przyłączone są do miozyny. Energia uwolniona podczas
rozpadu ATP gromadzi się w molekule miozyny. Kompleks
miozyna, ADP i Pi jest w stanie wzbudzonym, taki stan
mostków poprzecznych dominuje w stanie spoczynku,
• Część głowowa miozyny z ADP i Pi nie oddziałuje z aktynę z
uwagi na hamujące działanie kompleksu białek
regulających to oddziaływanie – troponiny i
tropomiozyny,
• W wyniku stymulacji mięśnia (wzrost stężenia jonów
wapnia w sarkoplazmie) hamujące działanie kompleksu
troponina-tripomiozyna zostaje zawieszone i
miozyna z przyłączonym ADP i Pi łączy się z aktyną.
Istnieje przekonanie, że kąt przyłączenia mostka wynosi
90°.
• Oddziaływanie aktyny z miozyną wyzwala uwolnienie
kolejno Pi i ADP. Energia zgromadzona w miozynie
prowadzi do konformacyjnych zmian w części głowowej
miozyny. Głowa przechyla się o około 45°. W konsekwencji
miofilament aktynowy przesuwa się o około 10-20 nm w
kierunku ośrodka sarkomeru, dopóki energia zgromadzona
w miozynie nie zostanie zużyta.
• Kolejne przyłączenie ATP powtarza cykl, dopóki proteiny
regulujące oddziaływanie nie zatrzymają procesu.
•
Jak widać ATP konieczne jest do rozerwania
kompleksu aktomiozynowego. W przypadku
niedoboru ATP cykl jest wstrzymany. Miozyna z
aktyną są permanentnie złączone, gdy bark ATP
mięsień jest naprężony.
•
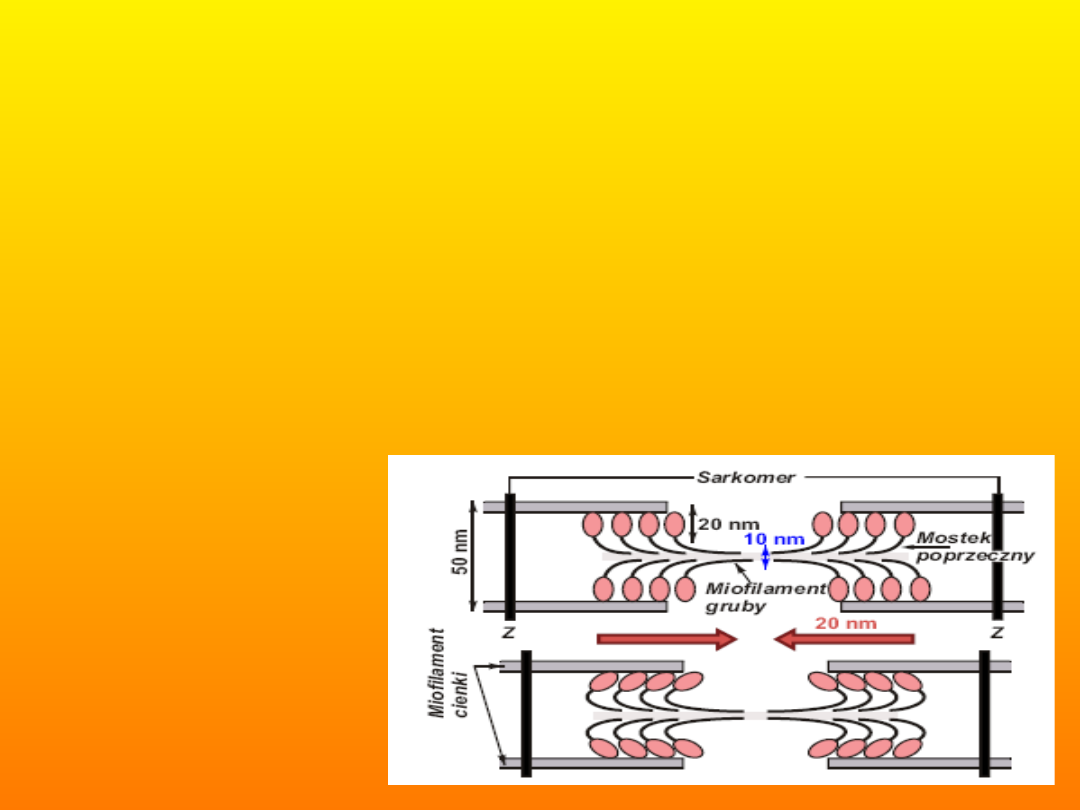
Mostki poprzeczne. Model mechanizmu
przemieszczania: nić miozynowa z mostkami
poprzecznymi przymocowanymi do sąsiednich nici
aktynowych: u góry przed, a na dole w czasie
mostków (w rzeczywistości ruch ten zachodzi
asynchronicznie).
"wiosłowego ruchu"
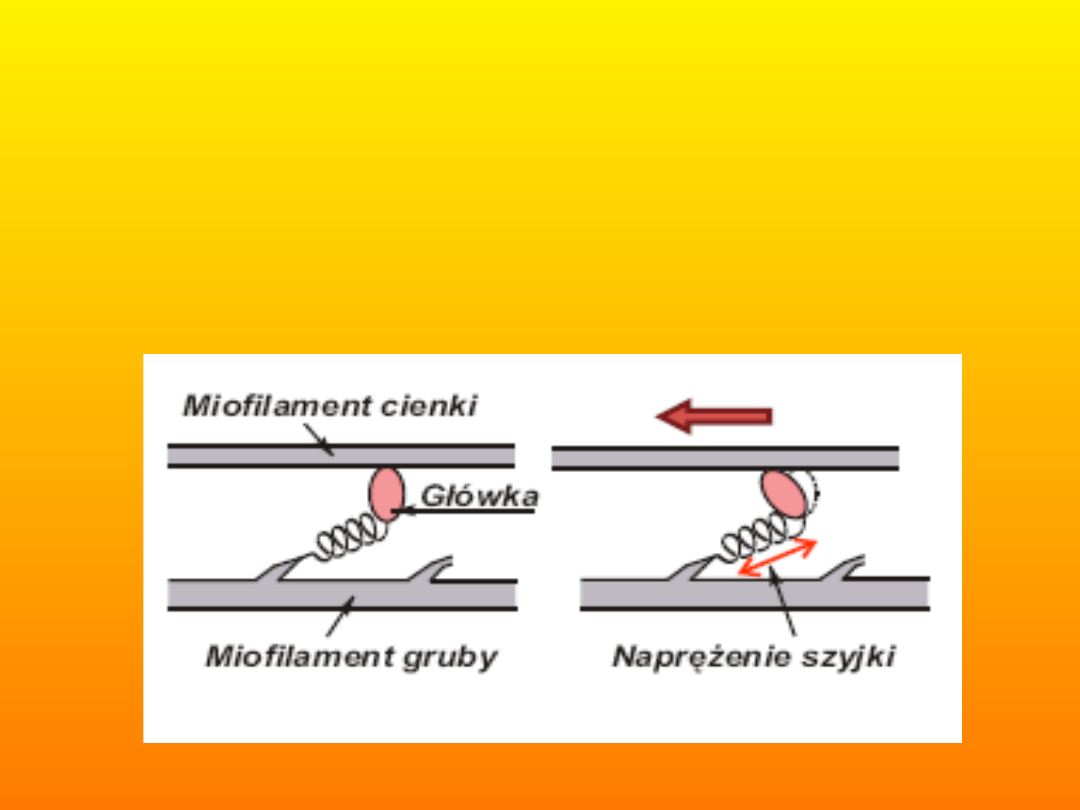
• Model mechanizmu wytwarzania siły przez
mostki poprzeczne. Chemicznie mostki
poprzeczne stanowią pewien fragment nici
miozynowej. Składają się z dwóch
subfragmentów: główki i szyjki. Główki
wiążą się z aktyną w sposób dynamiczny
(częstotliwość od 5 do 10 Hz). Ale układ
wytwarza stałe w czasie naprężenie.

• Rola jonów wapnia
• Istnieje bezpośredni związek pomiędzy
obecnością jonów wapnia w sarkoplazmie i
zdolnością mięśnia do wytwarzania siły.
Dwa podstawowe źródła wapnia
aktywującego skurcz to:
• przestrzeń zewnątrzkomórkowa
• wewnątrzkomórkowe struktury zdolne
gromadzić i uwalniać wapń.
Zewnątrzkomórkowej wapń występuje w formie
zjonizowanej oraz luźno związana z zewnętrzną
powierzchnią błony komórkowej i białkami.
W komórce miejscem gromadzenia wapnia jest
przede wszystkim siateczka sarkoplazmatyczna.
Wewnątrz siateczki sarkoplazmatycznej znajduje
się, białko zdolne do odwracalnego wiązania
dużych ilości jonów wapnia. S
tężenie wolnych jonów wapnia w środowisku
zewnątrzkomórkowym jest około 10 tys. razy
większe
niż
w
cytoplazmie
komórki
nie
pobudzonej.

• Utrzymanie takiego gradientu stężeń wynika z
istnienia bariery jaką stanowi sarkolema i układy
usuwające wapń poza komórkę. Podstawę tych
układów stanowią białka integralne
(transmembranowe) wbudowane w błonę
komórki:
• zależna od ATP pompa wapniowa, obniżająca
stężenie jonów wapnia w cytoplazmie kosztem
energii pochodzącej z hydrolizy ATP (ATPaza
wapniowa)
• wymiennik Na/Ca2+, który sprzęga przenoszenie
wapnia z komórki na zewnątrz ze spontanicznym
napływem jonów sodu, wynikającym z gradientu
ich stężenia (tzw. antyport). Gradient ten
utrzymywany jest dzięki małej przepuszczalności
błony siateczki dla jonów wapnia i występowaniu
w niej pompy wapniowej.
• Udział każdego z wymienionych źródeł jonów wapnia w
procesie aktywacji skurczu zależy od rodzaju mięśnia.
Od typu komórki mięśniowej zależy również mechanizm
prowadzący do aktywacji układu białek kurczliwych.
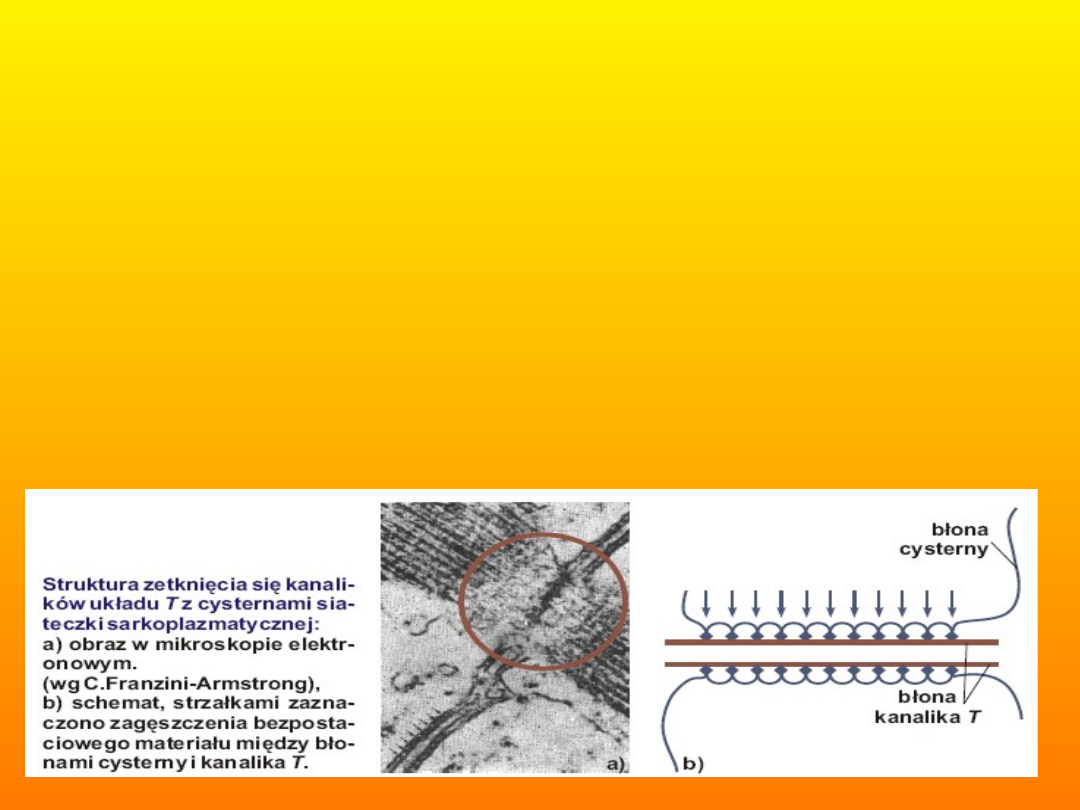
• W błonie komórek mięśni poprzecznie prążkowanych
znajdują się regularnie rozmieszczone zagłębienia
sięgające w głąb komórki i opasujące sarkomery. Jest to
system poprzecznych kanalików T zwanych również
tubulami poprzecznymi T
Kanaliki poprzeczne T umożliwiają dotarcie sygnału do
skurczu z powierzchni sarkolemy do wnętrza włókna.

• 7. Mięśnie szkieletowe
Mięśnie szkieletowe nie kurczą się
spontanicznie. Sygnał do skurczu
przekazywany jest z neuronu ruchowego
poprzez synapsę nerwowo mięśniową.
Prąd przenoszony przez napływające do
cytoplazmy jony Na+ depolaryzuje
błonę, pobudzając sarkolemę do
wytwarzania potencjałów
czynnościowych, które wzdłuż błon tubul
poprzecznych T docierają w głąb komórki
inicjując ciąg zjawisk prowadzący do
aktywacji układu białek kurczliwych,
nazywany sprzężeniem
elektromechanicznym.
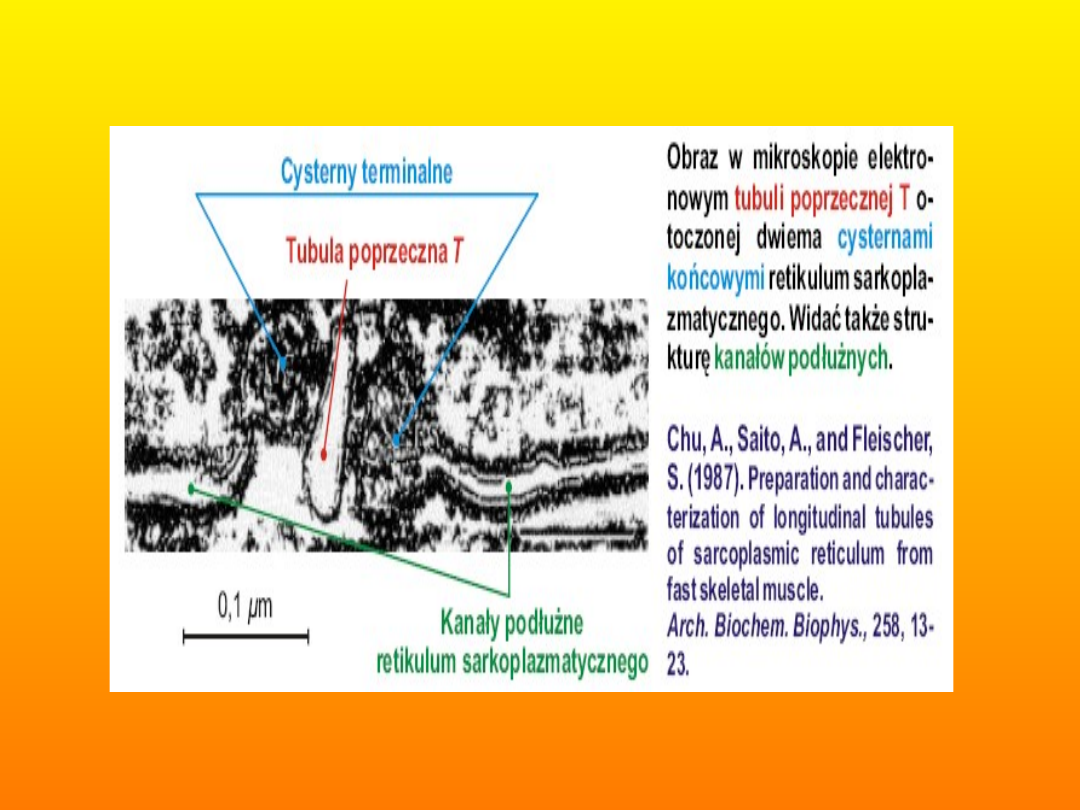
• W mięśniach szkieletowych przekazanie
pobudzenia z sarkolemy do wnętrza komórki
następuje w wyspecjalizowanych obszarach
sąsiadujących ze sobą błon: błony tubuli poprzecznej
T i błony zbiornika brzeżnego (cysterny) siateczki
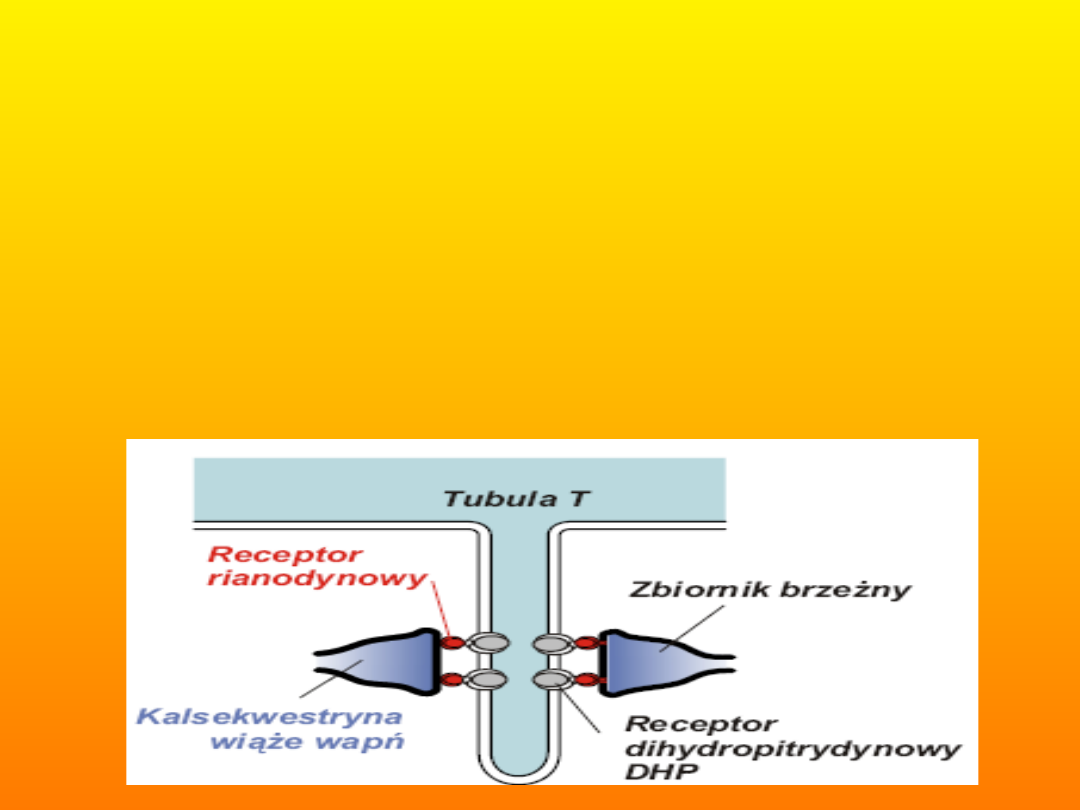
sarkoplazmatycznej. Podstawowymi elementami
struktury przekazującej pobudzenie są bezpośrednio
ze sobą oddziałujące – receptor dihydropirydynowy
wchodzący w skład sarkolemy i receptor
rianodynowy z błony siateczki sarkoplazmatycznej.

•
W komórkach mięśni szkieletowych receptory
dihydropirydynowe spełniają podwójną rolę:
•
są detektorami zmian potencjału sarkolemy,
kontrolującymi uwalnianie wapnia z siateczki
sarkoplazmatycznej i stanowią podjednostkę
przewodzącą zależnego od napięcia kanału
wapniowego. W czasie potencjału czynnościowego,
depolaryzacja kanalików poprzecznych T powoduje
zmianę konformacji receptorów
dihydropirydynowych w sarkolemie.W wyniku
zmiany konformacji białka kanał ten otwiera się, a jony
wapnia napływają do sarkoplazmy. Wzrost stężenia
jonów wapnia jest zjawiskiem przejściowym. Po
chwilowym otwarciu, kanały wapniowe ulegają
inaktywacji hamując napływ jonów wapnia do
sarkoplazmy, a pompy wapniowe i wymiennik
Na+/Ca2+ przywracają niskie stężenie wyjściowe,
aktyna traci zdolność do tworzenia kompleksu z
miozyną i następuje rozkurcz.

• Podsumowanie zjawisk zachodzących w mięśniu szkieletowym
podczas skurczu:
• Pobudzenie:
Sarkolema podlega depolaryzacji, rozchodzi się potencjał
czynnościowy,
Potencjał czynnościowy rozprzestrzenia się wzdłuż tubuli T, Sygna³
przechodzi z tubuli T do cystern końcowych retikulum
sarkplazmatycznego,
Wapń uwalniany jest z retikulum do sarkoplazmy.
• Skrócenie:
Wapń łączy się z troponiną,
W układzie troponina-tropomiozyna zachodzą kooperacyjne zmiany
konformacyjne,
Możliwe jest oddziaływanie miozyny z aktyną,
Mostki poprzeczne miozyny łączą się z filamentem aktynowym,
Przemieszczenie (nasunięcie) aktyny wywołuje naprężenie i / lub
skrócenie mięśnia.
• Rozluźnienie (relaksacja):
Wapń wraca do retikulum sarkoplazmatycznego,
Mostki poprzeczne odłączają się od cienkiego filamentu,
Przywrócone zostaje hamowanie (kontrolowane przez kompleks
troponina-
tropomiozyna) oddziaływań pomiędzy miozyną i aktyną,
Czynne naprężenie zanika, przywrócona jest długość spoczynkowa.

8. Mięsień sercowy
W mięśniu sercowym komórki układu nerwowego i komórki
mięśniowe nie są połączone synapsami. Neurotransmitery
uwalniane przez zakończenia komórek nerwowych do przestrzeni
zewnątrzkomórkowej mogą modulować czynność skurczową przez
oddziaływanie na białka receptorowe znajdujące się w sarkolemie, ale
sygnałem do skurczu nie jest impuls pochodzący z układu
nerwowego lecz potencjały czynnościowe wytwarzane przez
wyspecjalizowany układ bodźcotwórczy.
Pomiędzy komórkami mięśniowymi znajdują się połączenia
szczelinowe rodzaj nie selektywnych kanałów, przez które mogą
przechodzić jony i niewielkie cząsteczki hydrofilowe. System połączeń
międzykomórkowych umożliwia przepływ jonów między komórkami
zapewniając szybkie przenoszenie pobudzenia z komórki na komórkę.
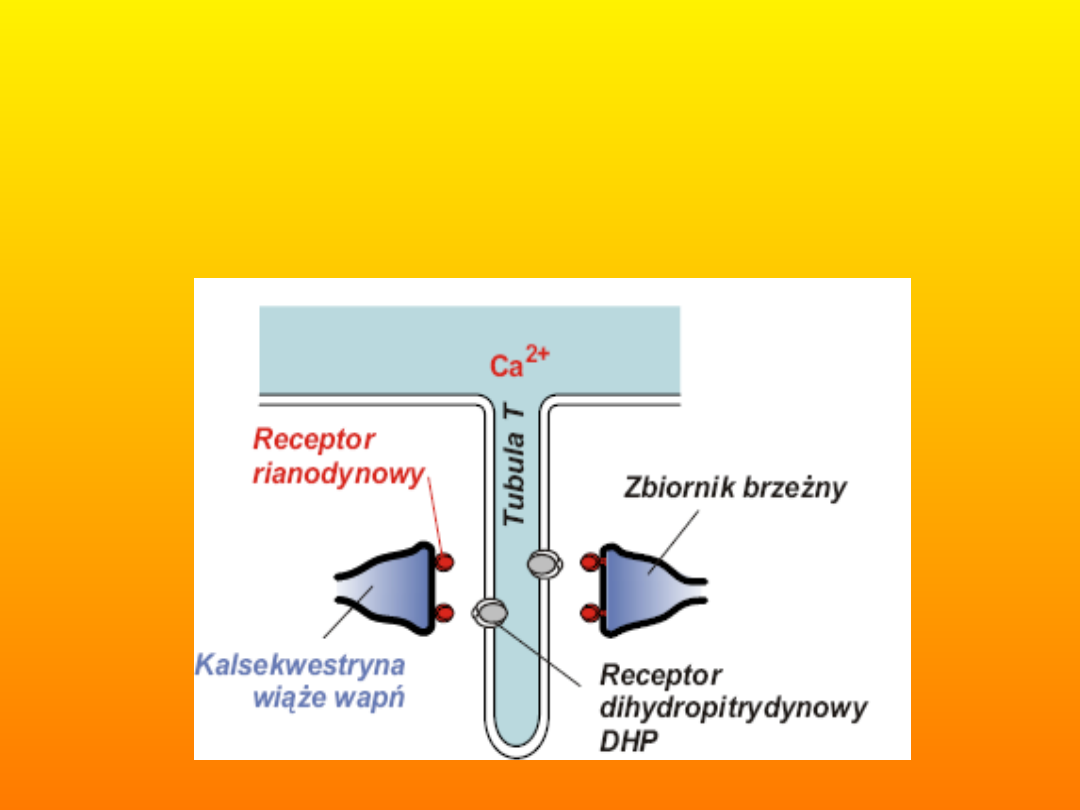
Czynnikiem przenoszącym pobudzenie z sarkolemy na błonę
siateczki są jony wapnia, które pod wpływem gradientu stężeń
napływają przez otwarte, kanały wapniowe do cytoplazmy. Wapń
wchodząca do cytoplazmy z zewnątrz, wiąże się receptorami
rianodynowymi. Związanie wapnia przez makrocząsteczkę receptora
powoduje otwarcie w jej centrum kanału wapniowego i wypływ jonów
wapnia z siateczki do cytoplazmy. Proces ten nosi nazwę zależnego
od wapnia uwalniania wapnia.
•
Wzrost stężenia zjonizowanego wapnia w pobliżu układu
białek kurczliwych inicjuje cykliczne powstawanie i rozpad
połączeń pomiędzy aktyną i miozyną. Zamknięcie
się kanałów wapniowych i usunięcie jonów wapnia z
cytoplazmy blokuje zdolność aktyny do tworzenia
kompleksu z miozyną. Następuje rozkurcz.

• 9. Przenoszenie pobudzenia w komórkach mięśni gładkich
Jedną z cech różniących skurcz mięśni gładkich i mięśni poprzecznie
prążkowanych jest inny mechanizm inicjujący tworzenie się mostków
poprzecznych pomiędzy aktyną i miozyną. W mięśniach gładkich białkiem
reagującym na zmianę stężenia jonów wapnia w cytoplazmie jest należąca
do tej samej rodziny białek co troponina C. Fosforylacja lekkiego łańcucha
miozyny jest procesem inicjującym skurcz mięśni gładkich.
Czynność skurczowa mięśni gładkich nie jest jednoznacznie
przyporządkowana sygnałom płynącym z układu nerwowego. W mięśniach
tych na ogół nie występują struktury typu synapsy nerwowo-mięśniowej.
Zakończenia komórek nerwowych uwalniają neurotransmitery do
przestrzeni między komórkami mięśniowymi. Substancje chemiczne
docierające do powierzchni komórki są rozpoznawane i wiązane przez
receptory błonowe rozmieszczone na całej jej powierzchni. Wiele mięśni
gładkich posiada zdolność spontanicznego wytwarzania potencjałów
czynnościowych, przenoszonych z komórki na komórkę dzięki
niskooporowym
połączeniom międzykomórkowym (połączenia
szczelinowe). Takimi spontanicznie kurczącymi się mięśniami są np.
mięśnie przewodu pokarmowego i mięsień macicy. Pobudzenie
komórki mięśnia gładkiego może powstać w skutek zdepolaryzowania
sarkolemy przez impuls elektryczny przekazany z innej komórki
(sprzężenie elektromechaniczne) lub w wyniku oddziaływania
substancji chemicznej powodującej pobudzenie receptorów
błonowych (sprzężenie farmakomechaniczne).

• 10. Różnice i podobieństwa mechanizmu
skurczu różnych typów mięśni.
Pomimo dużego zróżnicowania budowy i
funkcji, mechanizm skurczu różnych typów
mięśni charakteryzują uderzające
podobieństwa.
We wszystkich komórkach mięśniowych:
Znajduje się układ białek kurczliwych
zbudowany z miofilamentów, których głównymi
składnikami są aktyna (miofilament cienki) i
hydrolizująca ATP miozyna (miofilament gruby)
Skurcz aktywowany jest przez wzrost stężenia
jonów wapnia w cytoplazmie
Sarkolema jest strukturą pobudliwą.

• Oprócz tych podobieństw występują jednak
istotne różnice:
W komórkach mięśnia sercowego i mięśni
gładkich ważną rolę w aktywacji skurczu
odgrywają jony wapnia wchodzące do cytoplazmy
z otaczającej komórkę przestrzeni
W mięśniu sercowym i mięśniach
gładkich występują niskooporowe połączenia
elektryczne między komórkami, nie ma natomiast
bezpośredniego pobudzenia każdej komórki przez
synapsę nerwowo - mięśniową
W mięśniach gładkich proces aktywacji układu
białek kurczliwych przebiega inaczej niż w
mięśniach poprzecznie prążkowanych.

• 11. Regulacja siły mięśnia w organizmie
Bodziec dociera z motoreceptorów do synapsy
nerwowo - mięśniowej i wywołuje mięśniowe
potencjały czynnościowe:
•
1 etap: pobudzenie włókna mięśniowego,
•
2 etap: powstanie potencjału czynnościowego,
•
3 etap: sprzężenie elektromechaniczne:
rozejście się pobudzenia w kanałach poprzecznych T,
uwolnienie jonów Ca2+ z kanałów podłużnych retikulum
sarkoplazmatycznego,
działanie jonów Ca2+ na miofibryle,
•
4 etap: skurcz miofibryli.
• Podobnie reaguje jednostka motoryczna. Jednostka
motoryczna = jeden neuron motoryczny + grupa
unerwianych przez niego włókien mięśniowych. Każda
jednostka motoryczna spełnia zasadę „wszystko albo nic”
dla pojedynczego bodźca ponadprogowego.
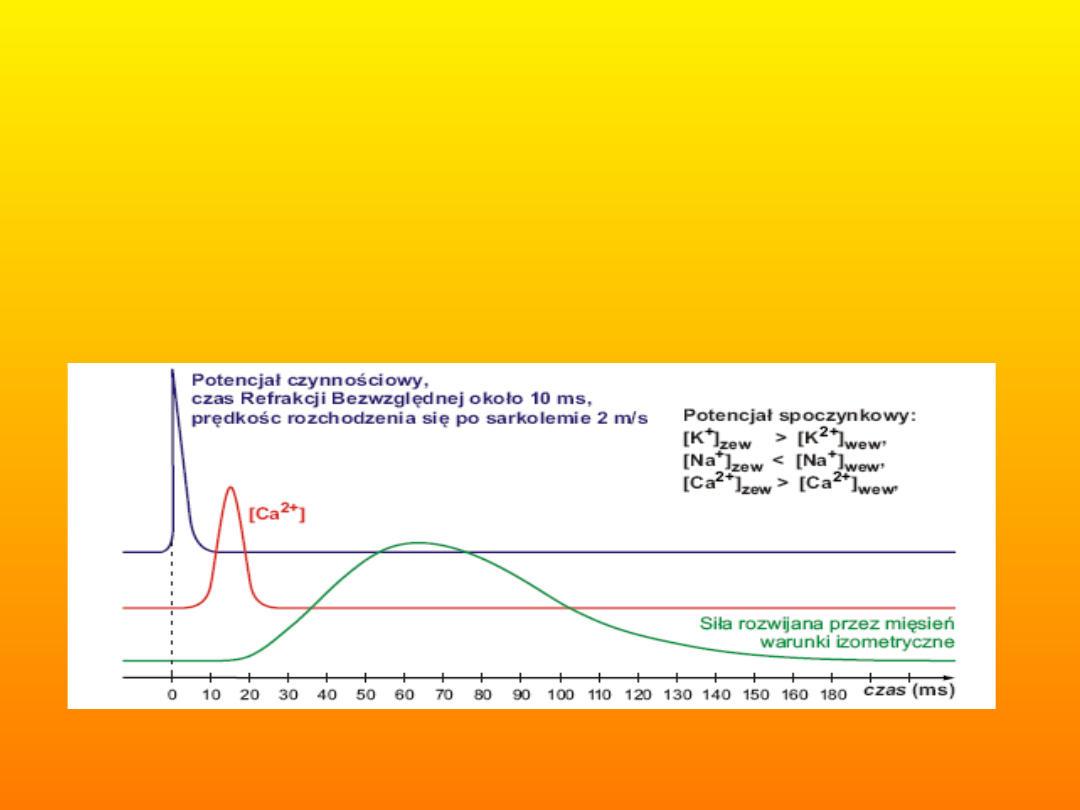
W jaki sposób organizm reguluje wartość siły
mięśnia?
Rozwijana siła jednostki motorycznej zależy od częstotliwości
jej pobudzania i podwaja się w warunkach skurczu tężcowego,
Istnieje możliwość wciągania do skurczu kolejnych jednostek
motorycznych.
czas (ms)
Relacje czasowe pomiędzy potencjałem czynnościowym, stężeniem jonów wapnia i
naprężeniem. Włókienko mięśniowe spełnia zasadę “wszystko albo nic”.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
Wyszukiwarka
Podobne podstrony:
termoregulacja gr II
PIII - teoria, Studia, SiMR, II ROK, III semestr, Elektrotechnika i Elektronika II, Elektra, Elektro
teoria asd, stud, II semestr, ASD
Egzamin z rachunkowsci finansowej gr II, WSFiZ rok 1
pytania fizjo seminaria 2 gr 5, II ROK STOMATOLOGIA SUM ZABRZE, FIZJOLOGIA, SEMINARIUM II
17 kinetyczna teoria gazów i termodynamika II
Teoria ugruntowana, RESOCJALIZACJA (I-II SUM)
teoria polityki skrypt II
PLAN WSPÓŁPRACY gr II
RP Teoria Sciąga, Budownictwo, II TOB zaoczne PP, I sem, Probabilistyka i prawdopodobieństwo, labora
OGÓLNA TEORIA STRATEGII, semestr II, Strategia Bezpieczeństwa Narodowego, Materiały od wykładowcy
czerwiec gr. II 2012, plany miesięczne i inne
testy, s-u¬ba II gr.II, Test egzaminacyjny z prawa służby cywilnej
testy, s-u¬ba II gr.II, Test egzaminacyjny z prawa służby cywilnej
kolokwium z elektroniki 8 12 09 gr ii
pytania 2007 gr II
więcej podobnych podstron