






















































































































































































































































































POLITECHNIKA WARSZAWSKA
LABORATORIUM TERMODYNAMIKI
II
INSTYTUT TECHNIKI CIEPLNEJ
Sprawozdanie z ćwiczenia
Zespół
Nazwiska i imiona
studentów
2004/05
MEL
III
25.11.2004
Rok ak.
Wydział Semestr
Grupa
Data ćwicz.
Ocena
Data
Podpis
I. Temat ćwiczenia
Bomba kalorymetryczna.
Oznaczanie ciepła spalania paliwa stałego Ć
.
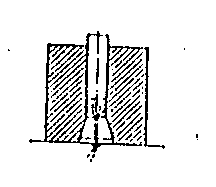
II. Stanowisko badawcze (szkice i krótki opis) A
W
Y
IS
I
P
Pras
elektroda
a S
do przygotowania próbki
doprowadzenie
IE
I
tlenu
N
elektrody
tygielek
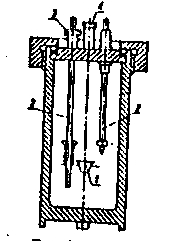
Bomba kalorymetryczna
Opis przebiegu ćwiczenia:
Przebieg ć wiczenia przebiegał nastę pują co: 1. Zerowanie wagi pomiarowej
2. Waż enie drucika (włókna) – md = 6,2 mg = 6,2*10-6 kg
3. Waż enie nitki – mn = 8,3 mg = 8,3*10-6 kg
4. Waż enie tygielka – mt = 5,27 g = 5,27*10-3 kg
5. Zawią zanie pę telki na nitce 6. Wsypanie sproszkowanego wę gla kamiennego do prasy 7. Ubijanie wę gla w prasie 8. Masa ubitego wę gla (brykiecika) – m = 1,01435 g = 1,01435*10-3 kg
9. Rozpię cie włókna i podwieszenie brykiecika 10. Włoż enie zawieszonego brykiecika do bomby kalorymetrycznej 11. Podłą czenie tlenu do bomby 12. Włoż enie bomby do wody i uruchomienie mieszadła 13. OKRES POCZĄ TKOWY:
Pomiar temperatury co 60 s. termometrem Beckmanna. Układ d Ć
ochodzi do
stanu równowagi z otoczeniem.
n
t
1
0,95
A
2
0,955
3
0,96
4
0,96
5
0,96
W
6
0,965
7
0,97
Y
8
10
I00, S
I,98
9
0,98
P 985
11
0,99
12
0,99
S
13 0,99
14
0,995
15
1
16
1,005
IE
I
17
1,01
18
1,01
19
1,01
N
20
1,015
21
1,015
22
1,02
23
1,02
24
1,02
25
1,02
14. OKRES POCZĄ TKOWY:
Zapłon. Pomiar temperatury co 30 s. termometrem Beckmanna.
n
t
1
1,2
2
1,5
3
1,7
4
3,3
5
4,4
4,87
7
5,2
8
5,22
9
5,29
10
5,41
11
5,47
12
5,55
13
5,62
14
5,66
15
5,71
16
5,71
17
5,8
18
5,84
19
5,87
20
5,9
21
5,92
22
5,95
23
5,97
24
5,99
25
6
Ć
26
6,02
27
6,03
28
6,04
29
6,05
A
30
6,06
31
6,07
32
6,07
W
33
6,07
15. OKRES KOŃ COWY – NIE ODBYŁ SIĘ : Y
Układ z powrotem musi dojść do stan
tk = I
u
1, S
I równowagi z otoczeniem. Przyjmuję , ż e koń cowa temperatura wynosi P 2 oC
16.Waż enie tygielka z popiołem – mt+p = 5354,2 mg = 5,3542*10-3 kg
17.Waż enie wody – G = 2,34 kg
Obliczenia:
1. Pojemność cieplna ka S
, gdzie:
G – masa wody w nac IE
I lorymetru: C= G(+ K) c w Nzyniu
K – wartość wodna kalorymetru, K = 0,441 kg cw – ciepło właściwe wody, cw = 4,19 kJ/(kg K) kJ
C = ( 3
,
2 4 + ,
0 44 )
1 ⋅ 1
,
4 9 = 1 ,
1 65239
K
2. Poprawka na wymianę ciepła z otoczeniem: s= n
V − V
−1
1 +
k
p
T
Tn
k
1 = n ⋅ V
−
⋅ ∑ T +
− n ⋅ T
p
s
p )
T − T
k
p
s=2
2
, gdzie:
a) n – ilość odczytów w okresie głównym – n = 33
b) Vp – średnie przyrosty temperatur pomiędzy odczytami w okresie T
T
p
− p
−
1
2
0 9
, 5
,
1 02
początkowym - V
p =
=
= − ,
0 0028
n
25
p
np – ilość odczytów w okresie początkowym
c) Vk - średnie przyrosty temperatur pomiędzy odczytami w okresie T
T
k
−
,
6 07
k
− ,12
końcowym -
1
2
V
k =
=
= 1
,
0 62333
n
30
k
nk – ilość odczytów w okresie końcowym, przyjmuję n = 30 (pomiar co 1
min. przez 30 min.)
T
T
p
+
+
1
9
,
0 5
,
1 02
d) T - średnia temperatura okresu początkowego T
p =
pn =
= 9
,
0 85
p
2
2
T
T
k
+
,
6 07 + ,
1 02
e) T - średnia temperatura okresu końcowego 1
T
k =
kn =
= 5
,
3 45
k
2
2
s= n−1
s= n 1
−
f) ∑ T - suma temp. okresu głównego bez wliczania T
∑ Ts =166,
s
1 i Tn -
19
s=2
s=2
T1 – temperatura początkowa okresu głównego Tn – temperatura końcowa okresu głównego 1
,
0 62333 − (− ,
0 002 )
8
,
1 2 + ,
6 07
k = 33⋅ (− ,
0 002 )
8 −
⋅
+
− ⋅
= −
1
(1661,9
33 ,
1 2)
Ć
5
,
3 45 − 9
,
0 85
2
3. Efekt cieplny powstały w bombie kalorymetrycznej: A, 8 4926 K
Q = C ⋅ ( T
∆ − k )
1
, gdzie
T
∆ - przyrost temperatury w okresie głównym - ∆ TW
Q = 1 ,
1 65239 ⋅ ,
5
( 05 − (− ,
8 4926) Y = ,
6 07 − ,
1 02 = ,
5 05
Q − ∑ q
G
(
+ ) ⋅ ⋅ ∆ + 1 − ∑
i
IS
I =1578, kJ
4. Ciepło spalania:
W
w
i
=
=
m
, gdzie
P K c ( T k) q m
∑ q - suma poprawek na dodatkowe efekty cieplne ∑ q i = Wd ⋅ md + Wn ⋅ mn + Q ⋅ m ⋅ f i
- Wd – ciepło spalania
lania
dr S
utu – Wd = 6700 kJ/kg
- Wn – ciepło spa
∑ q = 6700⋅ ,62⋅10−6 +17400⋅ 3, 8 ⋅10−6 +157 8
, ⋅ ,
1 01435 ⋅10 3
− ⋅ ,
0 0015 = 1
,
0 8572
i
IE
I nitki – Wn = 17400 kJ/kg
- f – współczynnik dla węgla - f = 0,0015
N
kJ
Q − ∑ q
157 8
, − 1
,
0 8572
MJ
W
i
=
=
=155 5
, 336
m
0
,
1 1435⋅10−3
kg
5. Wartość opałowa:
W = W − r ⋅ 9
( ⋅ g
+ g )
u
H 2
w
, gdzie
- g
- zawartość wodoru w paliwie - g H
= ,
0 043
H 2
2
- g - zawartość wilgoci w paliwie - g w =
,
0 05
w
- r – ciepło parowania wody – r= 2500 kJ/kg
−3
MJ
W = 155 5
, 336 − 2500 ⋅10 ⋅ 9
( ⋅ ,
0 043 + ,
0 0 )
5 = 15 ,
4 4411
u
kg
Wnioski:
Wyniki: W = 155,5336 MJ/kg i Wu = 154,4411 MJ/kg znacznie odbiegają od danych tablicowych, może to być spowodowane: 1.
Nie przeprowadzeniem okresu końcowego podczas pomiarów, z związku z czym przyjęcie przybliżonych danych.
2.
Błędy podczas pomiarów (ważenie, odczytów temperatury, itd.).
3.
Zakręcony kran doprowadzający do wodę do kalorymetru, który powinien być otwarty.
4.
Część nitki została ucięta podczas „prasowania” węgla, ta część nie została wzięta pod uwagę podczas obliczeń.
5.
Inne straty np. cieplne w kalorymetrze.
Ć
A
W
Y
IS
I
P
S
IE
I
N
Wyszukiwarka
Podobne podstrony:
A-11CD, W sprawozdaniu b??dnie obliczyli?my Dg poniewa? przyj?li?my b??d pomiaru k?ta Df=5o nie prz
A-11CD 2, W sprawozdaniu b˙˙dnie obliczyli˙my Dg poniewa˙ przyj˙li˙my b˙˙d pomiaru k˙ta Df=5o nie p
2 definicje i sprawozdawczośćid 19489 ppt
PROCES PLANOWANIA BADANIA SPRAWOZDAN FINANSOWYC H
W 11 Sprawozdania
Wymogi, cechy i zadania sprawozdawczośći finansowej
Analiza sprawozdan finansowych w BGZ SA
W3 Sprawozdawczosc
1 Sprawozdanie techniczne
Karta sprawozdania cw 10
eksploracja lab03, Lista sprawozdaniowych bazy danych
2 sprawozdanie szczawianyid 208 Nieznany (2)
Co warto wiedziec o radiestezji Nieznany
Fragmenty przykładowych sprawozdań
Lab 6 PMI Hartownosc Sprawozdan Nieznany
Mikrokontrolery Grodzki Sprawoz Nieznany
biochemia sprawozdanie O (1)
więcej podobnych podstron
