
Alkohole i fenole
Budowa
H
OH
R
OH
Budowa
O
H
Część
hydrofobow
a
Część
hydrofilowa
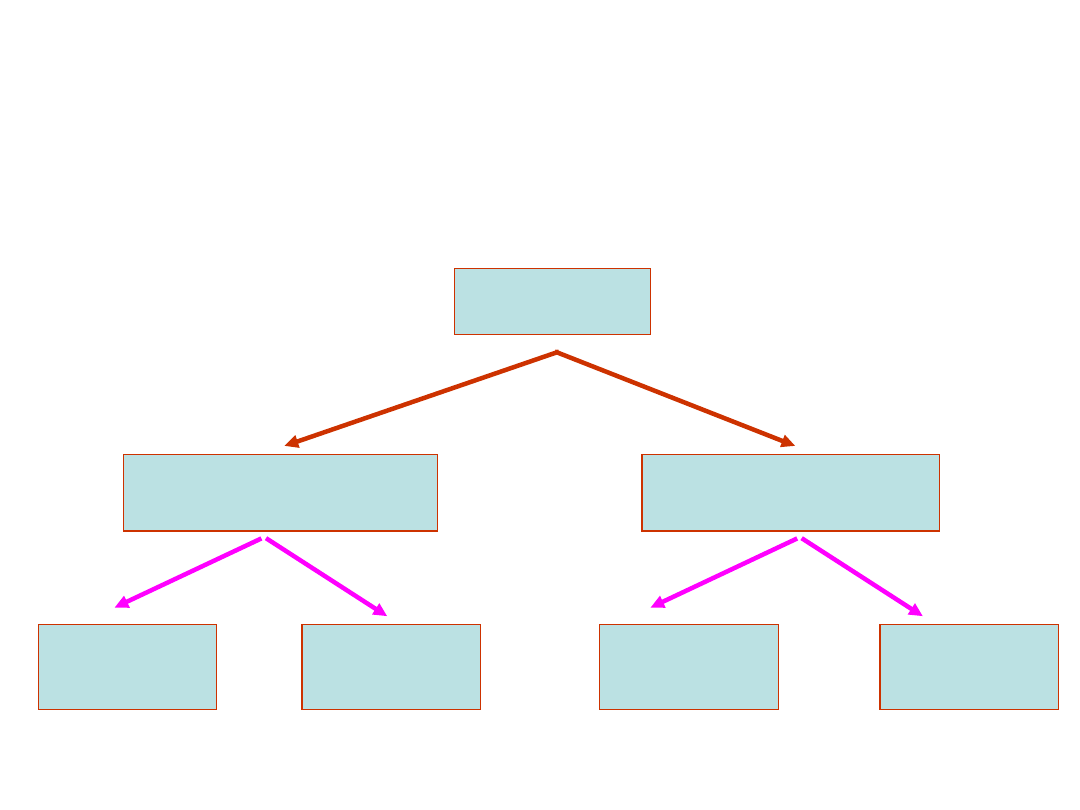
Podział alkoholi
Alkohole
monowodorotlenowe
wielowodorotlenowe
alifatyczne
(nasycone)
alifatyczne
(nasycone)
aromatyczne
(fenole)
aromatyczne
(fenole)
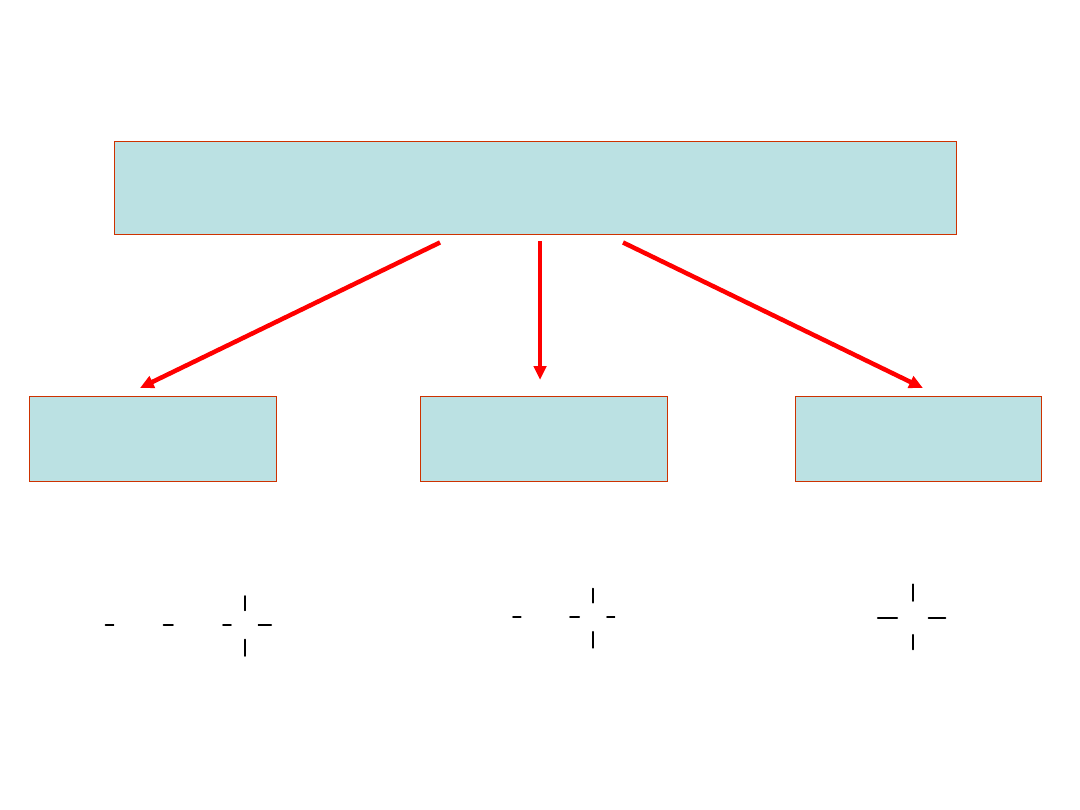
Alkohole alifatyczne
Pierwszorzędowe
1
o
Drugorzędowe
2
o
Trzeciorzędowe
3
o
CH
3
CH
2
CH
2
C
OH
H
H
CH
3
CH
2
C
CH
3
OH
H
CH
3
C
CH
3
OH
CH
3
Nazewnictwo
CH
2
C CH CH
3
CH
3
OH
Cl
Cl
1,2-dichloro-2-metylobutan-3-ol
3,4-dichloro-3-metylobutan-2-ol
O
H
Br
CH
3
2-bromo-1-metylocykloheksan-4-ol
3-bromo-4-metylocykloheksanol
Alkoh
ol
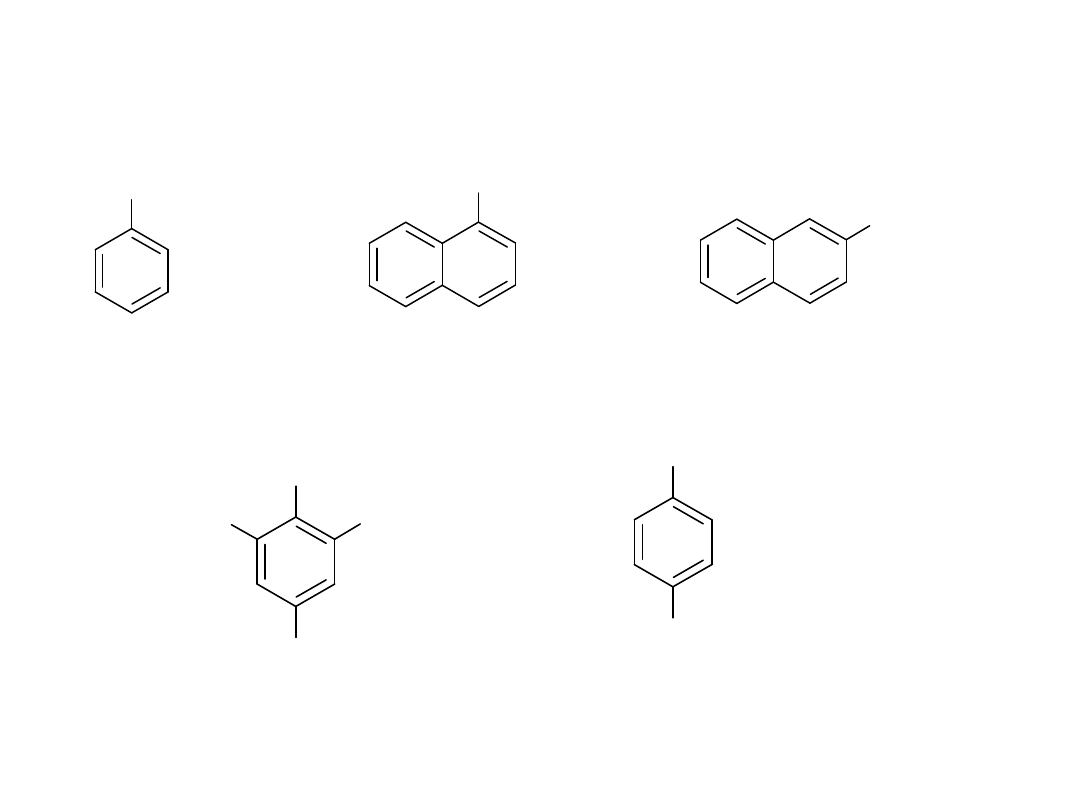
Nazewnictwo
OH
OH
OH
benzenol
fenol
naftalen-1-ol
-naftol
nafalen-2-ol
-nafol
OH
NO
2
NO
2
O
2
N
OH
OH
kwas pikrynowy
hydrochinon
Nazewnictwo
Alkohol
bytylowy
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH CH
3
OH
CH
3
C CH
3
OH
CH
3
CH
3
CH CH
2
CH
2
OH
CH
3
Alkohol tert-
bytylowy
Alkohol sec-
bytylowy
Alkohol
izopentylowy
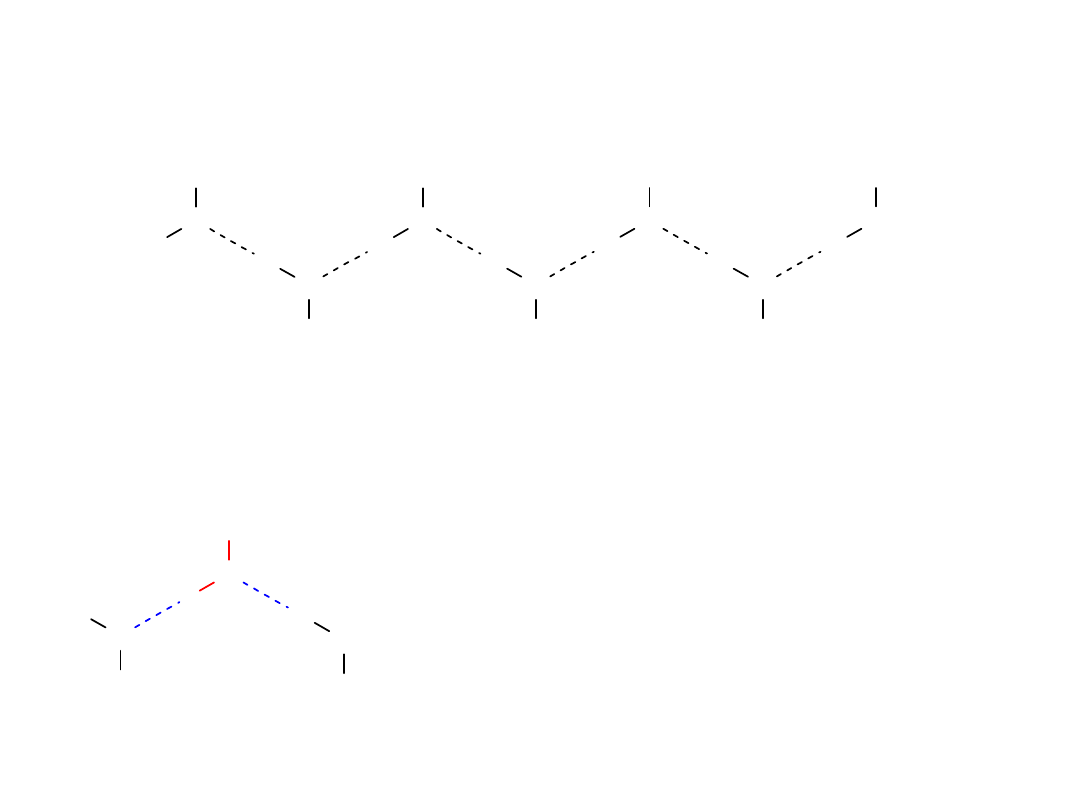
Właściwości fizyczne
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
R
O
H
Tworzenie
wiązań
wodorowych
pomiędzy
cząsteczkami alkoholu powoduje, że mają one wysoką
temperaturę wrzenia. Energia tych wiązań wynosi
20kJ/mol.
H
O
H
R
O
H
H
O
H
Tworzenie wiązań wodorowych
pomiędzy wodą a alkoholem
powoduje,
że
alkohole
zawierające do 4 atomów węgla
doskonale rozpuszczają się w
wodzie
Właściwości chemiczne
R
CH
2
O
H
..
..
>
c.E
c.N
c.E
atom wodoru
o charakterze kwasowym
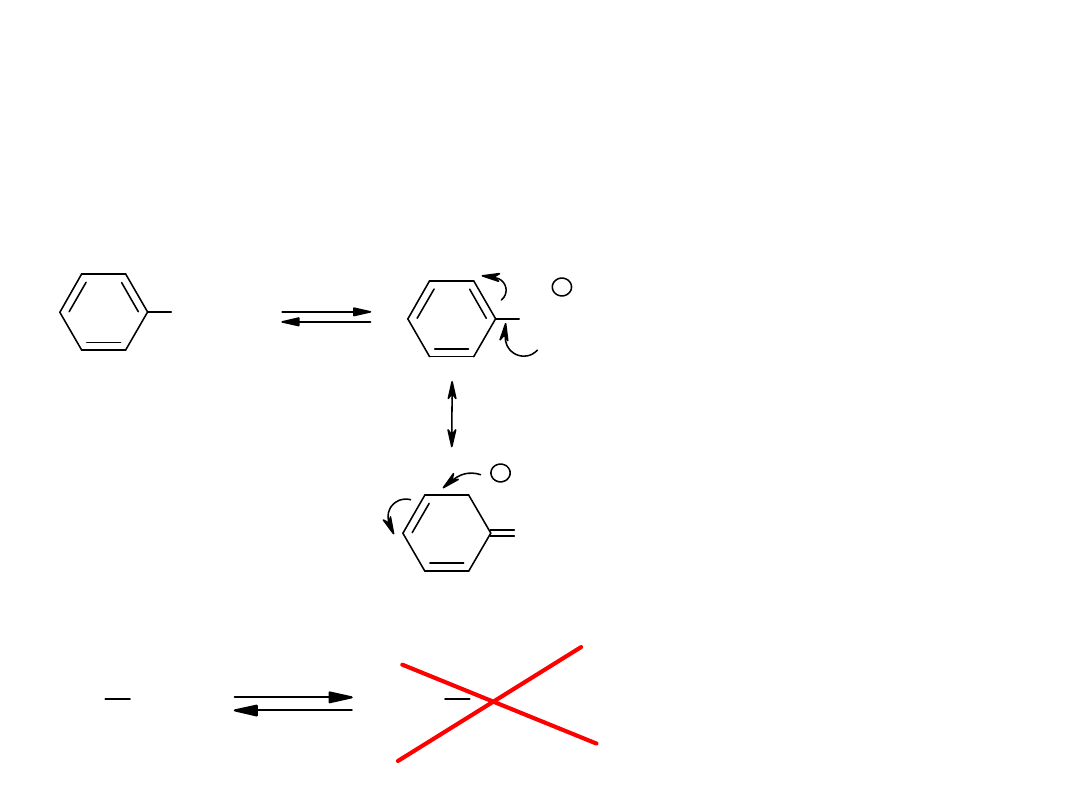
Właściwości kwasowe
Reakcja dysocjacji
OH
O
H
+
-
O
-
+
..
..:
..
..
:
H
2
O
pK
a
=10
-10
R OH
R O
:
..
..
+ H
+
H
2
O
Równowaga
bardzo
silnie
przesunięta
w
lewo
Właściwości kwasowe
OH
ONa
CH
3
OH + NaOH reakcja nie zachodzi
+ NaOH
+ H
2
O
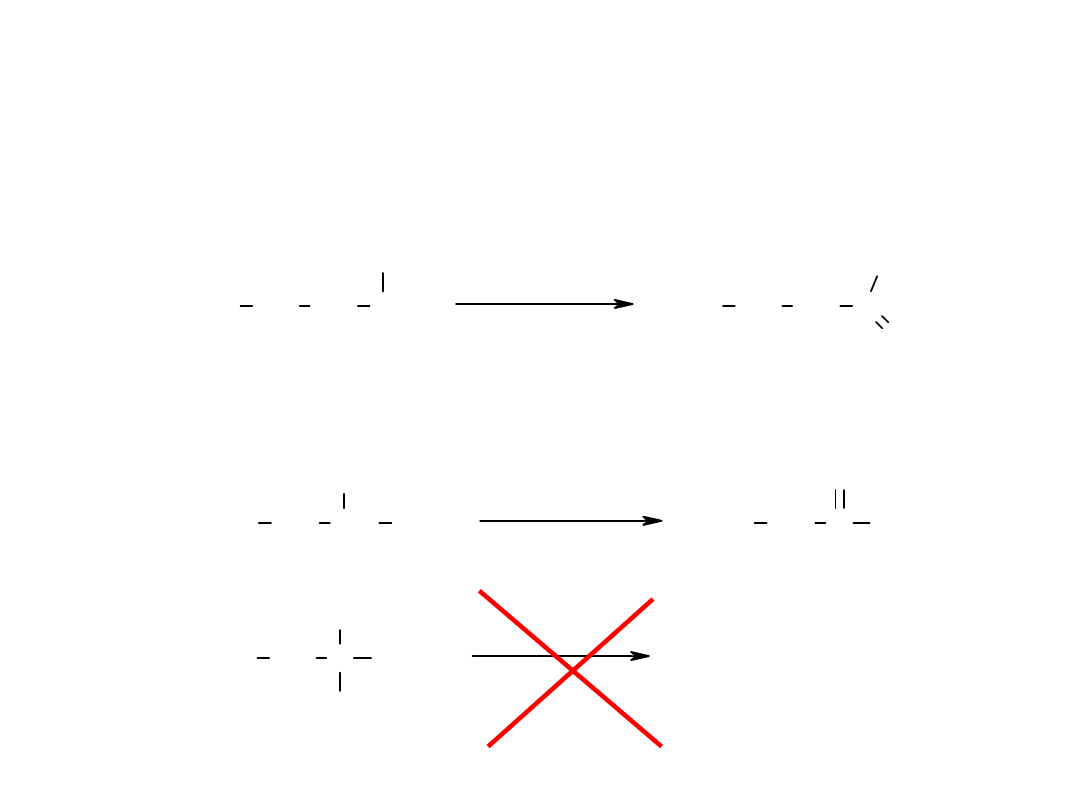
Utlenianie alkoholi
1
o
rzędowe alkohole utleniane są do kwasów karboksylowych
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH
2
C
O
OH
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+
2
o
rzędowe alkohole utleniane są do kwasów karboksylowych
CH
3
CH
2
CH CH
3
OH
CH
3
CH
2
C CH
3
O
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+
CH
3
CH
2
C CH
3
OH
CH
3
KMnO
4
/H
+
Na
2
Cr
2
O
7
/H
+
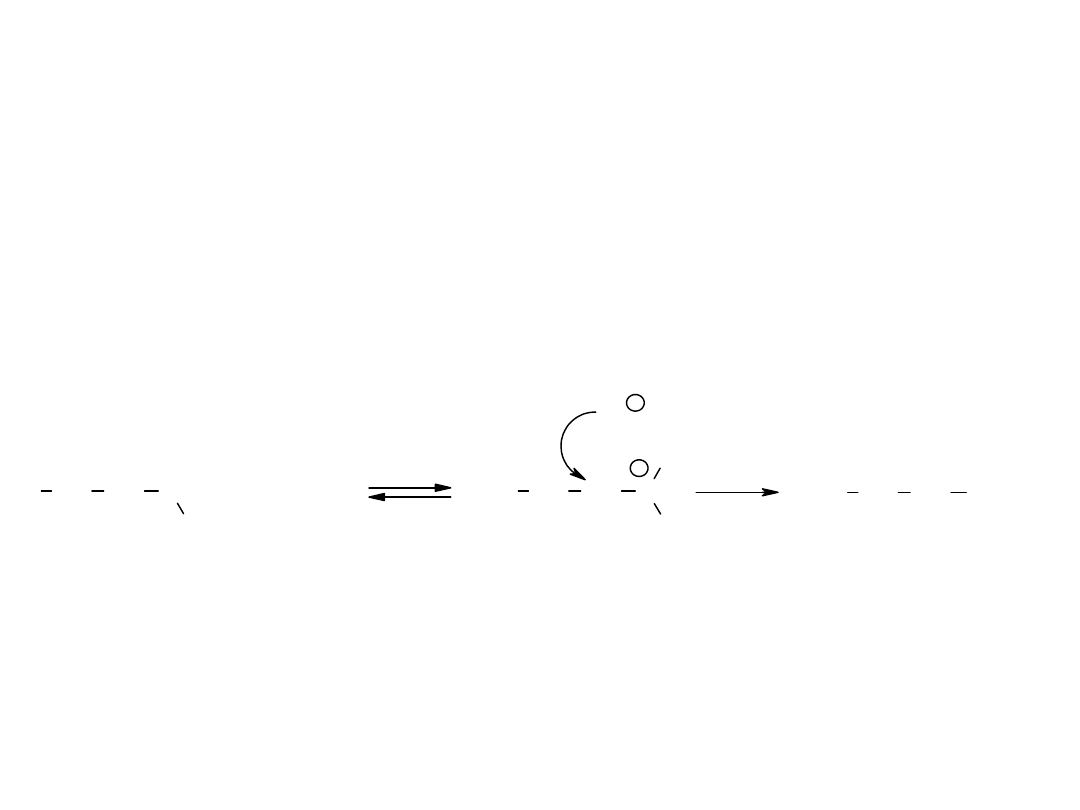
Substytucja nukleofilowa
alkoholi
CH
3
CH
2
CH
2
O
H
CH
3
CH
2
CH
2
O
H
H
+
CH
3
CH
2
CH
2
X
-
+ H
+
+ X
-
X
+ H
2
O
Według mechanizmu S
N
2 ulegają reakcji alkohole 1
o
i 2
o
X=Cl
,
Br, I
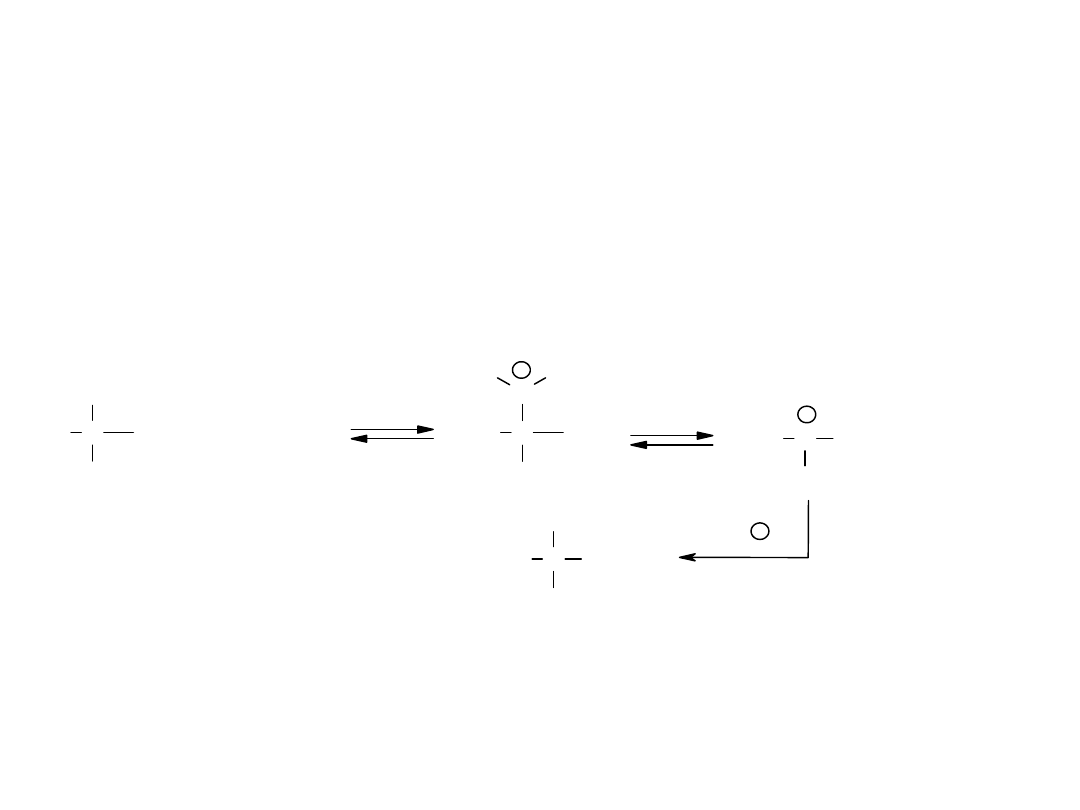
Substytucja nukleofilowa
alkoholi
CH
3
C
CH
3
OH
CH
3
CH
3
C
CH
3
O
H
H
CH
3
+
CH
3
C CH
3
CH
3
+
CH
3
C CH
3
X
CH
3
-
X
+ H
+
+ X
-
+ H
2
O
Alkohole
3
o
reagują
według
mechanizmu S
N
1

Eliminacja alkoholi
W przypadku gdy reszta kwasowa charakteryzuje
się znikomą nukleofilowością, alkohole 2
o
i 3
o
ulegają reakcji eliminacji H
2
O (H
2
SO
4
, H
3
PO
4
CH
3
CH
2
CH
2
CH CH
3
OH
CH
3
CH
2
CH
2
CH CH
3
O
H
H
CH
3
CH
2
CH CH CH
2
H
H
+
+
O
H
H
CH
3
CH
2
CH CH CH
3
CH
3
CH
2
CH
2
CH CH
2
H
2
SO
4
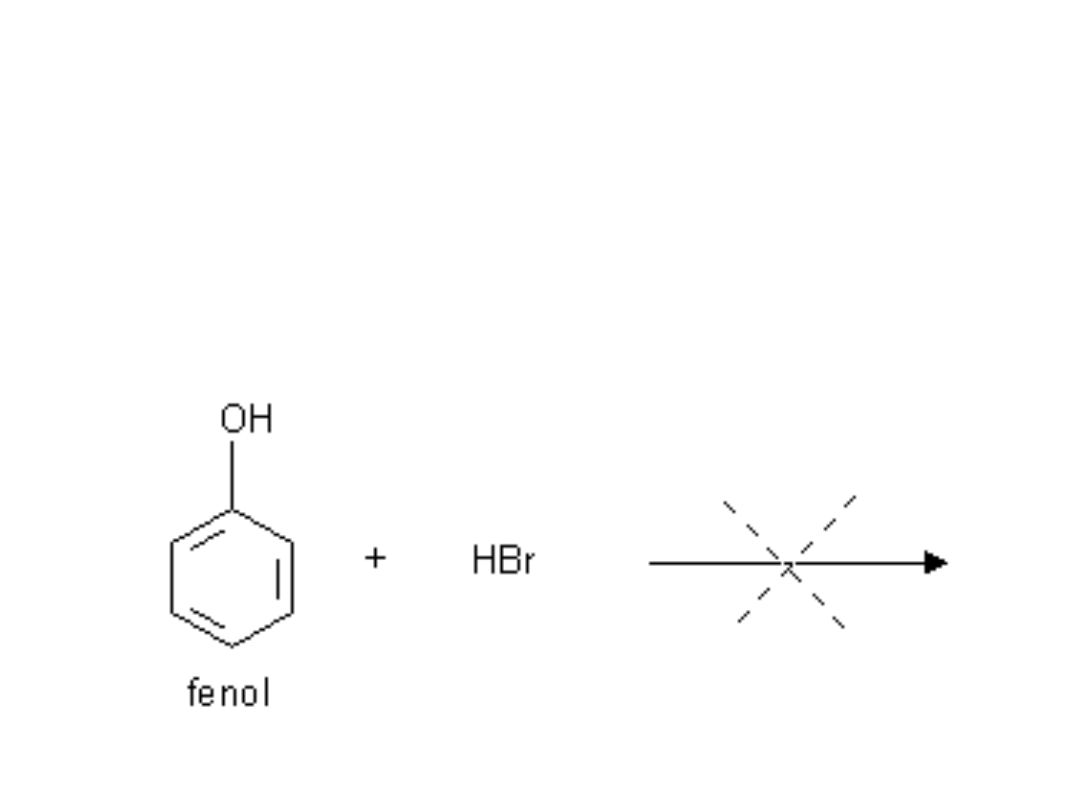
Rozróżnianie alkoholi i fenoli
Reakcja ze stężonym kwasem bromowodorowym
w obecności stężonego kwasu siarkowego
nie zachodzi w przeciwieństwie do alkoholi .
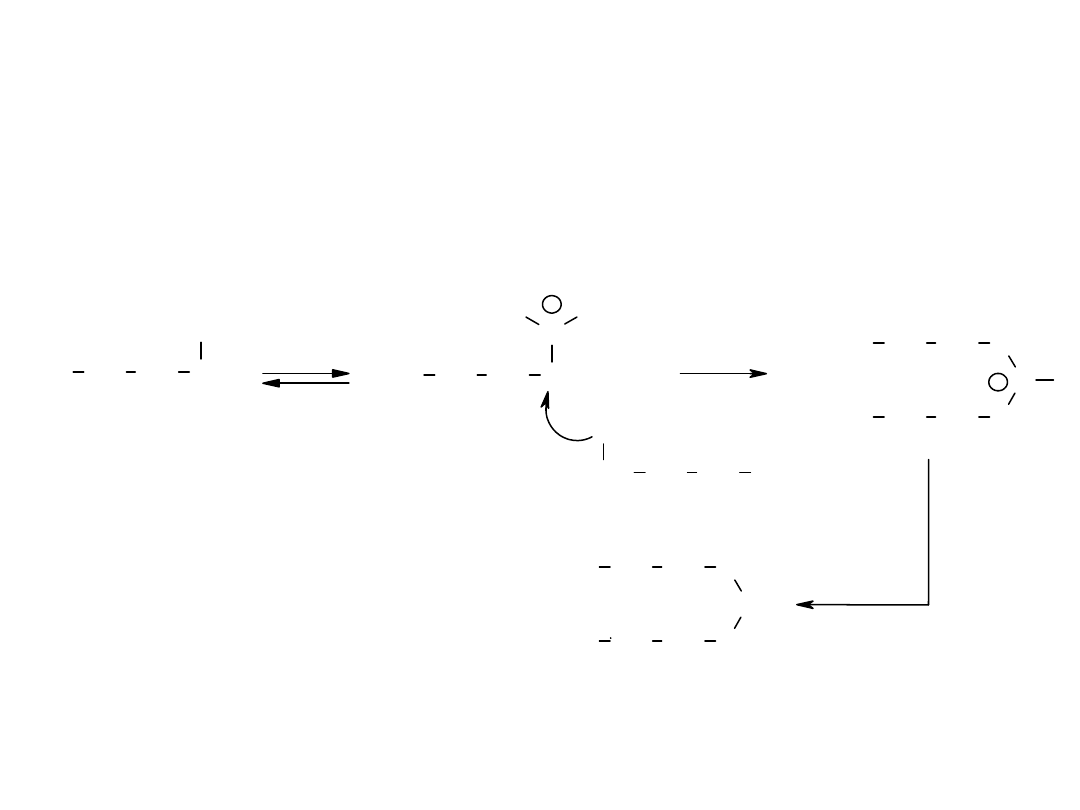
Eliminacja alkoholi
Według
identycznego
mechanizmu
reagują
alkohole 3
o
CH
3
CH
2
CH
2
CH
2
OH
CH
3
CH
2
CH
2
CH
2
O
H
H +
CH
2
CH
2
CH
2
CH
3
OH
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
O H
+
CH
3
CH
2
CH
2
CH
2
CH
3
CH
2
CH
2
CH
2
O
H
2
SO
4
-H
+
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
Wyszukiwarka
Podobne podstrony:
ALKOHOLE, CHEMIA, organiczna
Instrukcja do prób barwnych I (alkohole, Studia, Biotechnologia, Chemia, Chemia organiczna, Wykłady
alkohole fenole cwiczenia, Nauka, CHEMIA, Szkoła, Chemia Organiczna
Chemia organiczna czesc I poprawiona
chemia organiczna wykład 6
Wykład 9 CHEMIA ORGANICZNA
Chemia Organiczna 4
Chemia organiczna IV
CHEMIA- CHEMIA ORGANICZNA, CHEMIA
bromoacetanilid, Studia, Sprawozdania, Chemia organiczna
więcej podobnych podstron