BUDOWA CHEMICZNA ORGANIZMÓW ŻYWYCH
Podział pierwiastków:
makroelementy
węgielwodór
tlenazot
fosfor
siarka
wapń
magnez
sód
potas
chlor
mikroelementy
żelazo
kobalt
miedź
mangan
cynk
molibden
bor
jod
fluor
krzem
ultraelementy
rad
złoto
srebro
platyna
selen
Reguły dotyczące składu pierwiastkowego organizmów żywych
zdolność akumulowania pierwiastków, które stosunkowo rzadko występują w otoczeniu (prócz tlenu)
podobieństwo składu pierwiastkowego organizmów żywych do składu pierwiastkowego wody oceanicznej (stąd wnioski: wszystkie organizmy powstały w wodzie, wszystkie organizmy są spokrewnione)
Funkcje najważniejszych pierwiastków
tworzy szkielet
obniża stopień uwodnienia koloidów
reguluje funkcje błon komórkowych
składnik płynów ustrojowych
udział w krzepnięciu krwi
krzywica, łamliwość kości, choroby zębów, zaburzenia krzepnięcia krwi
tężyczka
rozkład błon plazmatycznych
nieprawidłowy wzrost i martwica organów
tworzy kości
obniża stopień uwodnienia koloidów
składnik chlorofilu
utrzymuje strukturę rybosomów
aktywuje wiele enzymów
zwiększenie pobudliwości nerwowo-mięśniowej, osłabienie, nieprawidłowa praca serca
chloroza liści
więdnięcie
zahamowanie fotosyntezy
bierze udział w przewodzeniu impulsów przez neuron
wpływa na ciśnienie osmotyczne płynów
zanik różnicy potencjałów i brak pobudliwości komórek
zanik różnicy potencjałów i brak pobudliwości komórek
bierze udział w przewodzeniu impulsów przez neuron
podwyższa stopień uwodnienia koloidów
aktywuje wiele enzymów
osłabienie, zmniejszenie kurczliwości serca, osłabienie mięśni
chloroza liści
zwiędły pokrój rośliny
zahamowanie wzrostu korzenia i pędu
martwica organów
składnik białek złożonych transportujących tlen
składnik wielu enzymów np. cytochromów
anemia, osłabienie, bóle głowy, arytmia, zakłócenia procesu oddychania
zakłócenie oddychania i fotosyntezy
chloroza młodych liści
składnik witaminy B12
konieczny dla roślin motylkowych żyjących w symbiozie z bakteriami brodawkowymi
zaburzenia krzepnięcia krwi
zahamowanie procesu wiązania azotu u roślin motylkowych
składnik enzymów cyklu Krebsa
udział w syntezie hemoglobiny i chlorofilu
zaburzenia oddychania komórkowego
bielenie i zasychanie wierzchołków młodych liści
aktywuje wiele enzymów cyklu Krebsa i fazy jasnej fotosyntezy
zaburzenia oddychania
chloroza liści
usychanie liści
składnik insuliny
składnik wielu enzymów
odpowiada za syntezę związków regulujących wzrost i rozwój roślin
powolne gojenie się ran, choroby skóry, łamliwość włosów i paznokci
zaburzenia rozwoju i czynności gonad
chloroza liści
karlenie liści
składnik hormonów tarczycy
obrzęki skóry, wole, kretynizm
tworzy kości i szkliwo zębów
próchnica
Funkcje najważniejszych witamin
współtworzy rodopsynę
wątroba, jaja, masło, mleko, tran
kurza ślepota
zanikanie nabłonków i łuszczenie skóry
składnik enzymów utleniających węglowodany i aminokwasy
wątroba, mięso, drożdże
choroba beri-beri
składnik koenzymu FAD
wątroba, sery, jaja, mleko
zapalenie skóry, pękanie kącików ust
obniżenie sprawności umysłowej
jej pochodna jest koenzymem enzymów przetwarzających aminokwasy
wątroba, mięso, jaja, banany
stany zapalne skóry, pobudliwość
współtworzy niebiałkowy składnik enzymów biorących udział w biosyntezie nukleotydów
flora jelitowa
anemia
wady nerwowe płodu
współtworzy niebiałkowy składnik enzymów przetwarzających zasady azotowe
flora jelitowa
anemia
synteza kolagenu
tworzy istotę podstawową kości i zębów
wchłanianie żelaza
wzmacnia odporność
świeże owoce
obniżenie odporności
szkorbut
gospodarka wapniowa
wzrost kości
wątroba, mleko, jaja, masło, tran, drożdże
krzywica
hamuje utlenianie lipidów ustrojowych i witaminy A
wątroba, jaja, oleje roślinne, orzechy, pszenica, ryby
osłabienie mięśni
obniżenie płodności
krzepnięcie krwi (bierze udział w wytwarzaniu protrombiny)
flora jelitowa
wydłużenie czasu krzepnięcia krwi
krwotoki
składnik koenzymu NAD+ i NADP+
wątroba, sery, jaja, mleko
zmęczenie, depresja, zaburzenia pamięci
Wiązania i oddziaływania chemiczne
wiązania kowalencyjne
polega na uwspólnieniu elektronów
powstaje związek kowalencyjny
podział ze względu na liczbę wspólnych par elektronów:
pojedyncze
podwójne
potrójne
podział ze względu na elektroujemność atomów:
obojętne
spolaryzowane
wiązania jonowe
polega na przeniesieniu elektronów z kationu na anion
powstaje związek jonowy
wiązania wodorowe
polega na łączeniu cząsteczek związanego kowalencyjnie wodoru z innym pierwiastkiem
są słabe, przy dużej ilości silne
oddziaływania van der Waalsa
powstają między grupami chemicznymi o przeciwstawnych znakach
są bardzo słabe, w dużej ilości silne
oddziaływania hydrofobowe
powstają między fragmentami cząsteczek niepolarnych, które są nierozpuszczalne i skupiają się razem np. kropelki tłuszczu
Reakcje
dehydrogenacja - odłączenie H2 od cząsteczki związku
dekarboksylacja - odłączenie CO2 od cząsteczki związku
deaminacja - odłączenie reszty aminowej -NH2 od cząsteczki związku (powstaje amoniak)
transaminacja - przeniesienie reszty aminowej -NH2
uwodornienie - przyłączenie H2 do cząsteczki związku
ufosforylowanie - przyłączenie PO4 do cząsteczki związku (podnosi to poziom energetyczny związku)
kondensacja - reakcja łączenia substratów w większą od nich cząsteczkę i jedną (lub więcej) mniejszych m.in. wody
estryfikacja - reakcja kondensacji, w której powstają estry
Związki nieorganiczne
woda
jest dipolem elektrycznym, co umożliwia asocjację i hydratację
rozpuszczalnik substancji hydrofilowych i niektórych substancji hydrofobowych
substancja obojętna i nieszkodliwa
transportuje różne substancje (jest cieczą i rozpuszczalnikiem)
utrzymuje odpowiednie kształty komórek
warunkuje odpowiedni stan uwodnienia komórek organów roślinnych
funkcje termoizolacyjne i termoregulacyjne (wolno zmienia temperaturę dzięki wysokiemu ciepłu właściwemu, ciepłu parowania i ciepłu topnienia)
zamarzając zwiększa swoją objętość i zmniejsza gęstość (pozwala to na unoszenie się na powierzchni mniej gęstego od wody lodu, co spowalnia zamarzanie głębszych warstw wody i umożliwia życie w zbiornikach)
występują siły adhezji i kohezji
podział:
woda związana
woda wewnątrzkomórkowa
płyn zewnątrzkomórkowy
sole mineralne
2-4% suchej masy organizmu
rozpuszczone w soku komórkowym i płynach pozakomórkowych lub w postaci nierozpuszczalnych elementów
funkcje strukturalne i podporowe (fosforan wapnia i węglan wapnia współtworzą szkielet kręgowców, a krzemionka ściany komórkowe glonów, skrzypów, traw i turzyc)
funkcje biochemiczne (biorą udział w reakcjach, budują enzymy lub są konieczne do ich pracy)
funkcje osmotyczne (utrzymują ciśnienie osmotyczne)
funkcje buforujące (utrzymują odpowiednie pH roztworów komórkowych i pozakomórkowych np. kwas węglowy CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3-, który:
przy kwaśnym pH przyłącza jony wodorowe:
przy zasadowym pH przyłącza jony wodorotlenowe:
Związki organiczne
aminokwasy, peptydy, białka
tworzone przez węgiel, wodór, tlen, azot, siarkę, a białka złożone także przez fosfor, miedź, cynk, molibden i żelazo
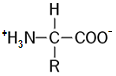
zbudowane z aminokwasów łączących się w łańcuchy polipeptydowe, wzór ogólny aminokwasu:
reagują z kwasami i zasadami (są amfoteryczne)
w roztworze wodnym są zjonizowane (mają więc ładunek elektryczny; występują w zależności od wartości pH w postaci formy kwasowej, zasadowej lub obojnaczej; wartość pH, przy której występuje forma obojnacza nazywana jest punktem izoelektrycznym aminokwasu):
ze względu na wielkość cząsteczek tworzą zole białkowe w wyniku hydratacji
ze względu na posiadany ładunek elektryczny ulegają zjawisku elektroforezy; jej odmianą jest immunoelektroforeza
powszechnie występujące w organizmie aminokwasy:
aminokwasy (prócz najprostszej glicyny) tworzą izomery optyczne typu L lub D (w organizmach występuje tylko forma L-aminokwasów)
aminokwasy łączą się ze sobą wiązaniem peptydowym (w zależności od liczby łączących się aminokwasów powstaje dipeptyd, tripeptyd itd., których nazwy tworzy się przez łączenie nazw aminokwasów) - reakcja kondensacji
białka mają kilka struktur:
pierwszorzędowa
drugorzędowa
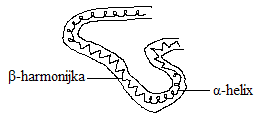
α-helix
β-harmonijka
trzeciorzędowa
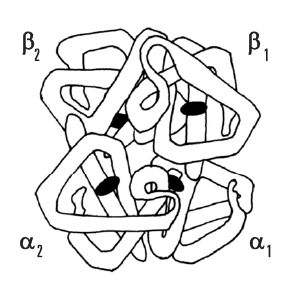
czwartorzędowa
czynniki denaturujące:
temperatura
mocznik
mocne kwasy
mocne zasady
detergenty
jony metali ciężkich
podział białek:
ze względu na kształt cząsteczek:
białka włókienkowe
białka globularne
ze względu na skład chemiczny:
proste
histony
protaminy
albuminy
globuliny
prolaminy
skleroproteiny
kolageny
keratyny
złożone
metaloproteiny
chromoproteiny
glikoproteiny
lipoproteiny
fosfoproteiny
nukleoproteiny
ze względu na liczbę grup funkcyjnych:
obojętne
kwaśne
zasadowe
funkcja budulcowa (współtworzą organelle komórkowe i cytoplazmę)
funkcja katalityczna (tworzą enzymy)
funkcja transportowa (tworzą białka błonowe, które umożliwiają transport do/z komórki różnych substancji i transport daleki jak np. hemoglobina)
funkcja regulatorowa (tworzą hormony peptydowe i białkowe)
funkcja odpornościowa (tworzą immunoglobuliny)
funkcja lokomotoryczna (tworzą miozynę)
funkcja buforująca (utrzymują odpowiednie pH, dzięki oddającej proton grupie -COOH i przyjmującej proton grupie -NH2)
tłuszczowce
tworzone przez węgiel, tlen, wodór i niekiedy fosfor czy azot
zbudowane z kwasów tłuszczowych, alkoholi i niekiedy z innych związków
kwasy tłuszczowe łączą się z alkoholami wiązaniem estrowym - reakcja estryfikacji
nierozpuszczalne w wodzie (rozpuszczalne w rozpuszczalnikach organicznych)
podział tłuszczy:
ze względu na budowę cząsteczki:
tłuszcze proste
tłuszcze właściwe
woski
tłuszcze złożone
fosfolipidy
glikolipidy
ze względu na wiązania:
tłuszcze nasycone
tłuszcze nienasycone
funkcja paliwa biologicznego
funkcja termoizolacyjna
funkcja budulcowa (tworzą błony biologiczne w komórce)
funkcja ułatwiania trawienia tłuszczy (kwasy tłuszczowe)
funkcja regulatorowa (hormony sterydowe, prostaglandyny)
funkcja pomocnicza w fotosyntezie (karoten, ksantofil)
funkcja barwnika (karoten, ksantofil, likopen)
funkcja ochronna (woski tworzą warstwy ochronne na skórze, włosach, piórach, a u roślin na owocach i liściach)
cukrowce
tworzone przez węgiel, wodór i tlen w stosunku 1:2:1
zbudowane z monosacharydów lub są monosacharydami
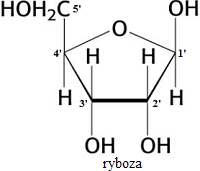
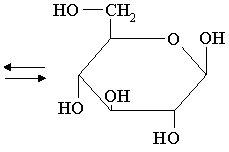
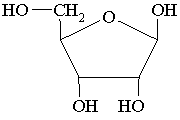
łańcuchy niektórych cukrów (np. glukoza, fruktoza, maltoza, ryboza) tworzą w roztworach wodnych pierścienie - między grupą karbonylową i hydroksylową powstają wewnętrzne mostki tlenowe (trwałe są pierścienie pięcio- i sześcioczłonowe)
cukry tworzą izomery optyczne typu L lub D (organizmy nie przyswajają formy L-cukrów)
monosacharydy łączą się ze sobą wiązaniem O-glikozydowym (w zależności od liczby łączących się monosacharydów powstają różne cukry złożone, których nazwy tworzy się przez łączenie nazw cukrów, choć wiele jest zwyczajowych) - reakcja kondensacji
podział cukrów:
monosacharydy:
ze względu na liczbę atomów węgla:
triozy np. aldehyd glicerynowy
tetrozy
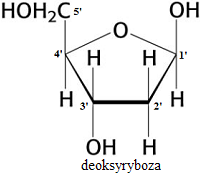
pentozy np. ryboza, deoksyryboza
heksozy np. fruktoza, glukoza
ze względu na rodzaj grupy funkcyjnej:
aldozy
ketozy
cukry złożone:
disacharydy np. sacharoza (glukoza + fruktoza), maltoza (glukoza + glukoza), laktoza (glukoza + galaktoza)
oligosacharydy (3-10 monosacharydów)
polisacharydy (powyżej 10 monosacharydów):
ze względu na rodzaj łańcucha (skrobia jest mieszaniną obu):
amylozy
amylopektyny
ze względu na związki z jakich powstają:
homoglikany np. skrobia, glikogen, celuloza, chityna
heteroglikany np. kwas hialuronowy, chondroityna, heparyna
funkcja wysokowartościowego paliwa biologicznego
funkcja budulcowa (celuloza i pektyny budują ściany komórek roślinnych, a chityna strzępki grzybów i szkielet zewnętrzny stawonogów - cząsteczki tych związków tworzą regularne łańcuchy nadające dużą odporność mechaniczną)
funkcja zapasowa (u roślin skrobia - odkładana w nasionach i bulwach; u zwierząt - glikogen, odkładany w mięśniach i wątrobie)
są składnikami mleka (laktoza) oraz nektaru i pyłku kwiatów - czynnik wabiący owady (maltoza)
kwas hialuronowy i chondroityna są składnikami mazi stawowej i chrząstek
heparyna hamuje krzepnięcie krwi
witaminy
są egzogenne
podział witamin:
rozpuszczalne w tłuszczach (A, D, E, K)
rozpuszczalne w wodzie (pozostałe)
kwasy nukleinowe
wyróżniamy:
kwas deoksyrybonukleinowy
kwas rybonukleinowy
mRNA
tRNA
rRNA
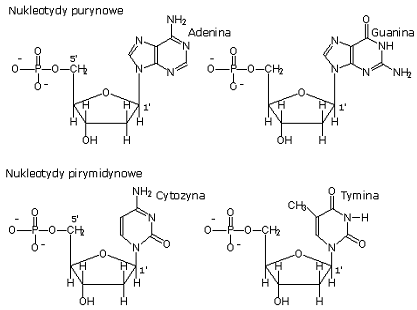
zbudowane z nukleotydów łączących się w łańcuchy polinukleotydowe
zasady azotowe łączą się z pentozami wiązaniem N-glikozydowym (powstają nukleozydy)
nukleozydy łączą się z resztami fosforanowymi (powstają nukleotydy) - reakcja estryfikacji
nukleotydy łączą się ze sobą wiązaniami fosfodiestrowymi (powstają kwasy nukleinowe) - reakcja polimeryzacji
jedna nić DNA łączy się z drugą nicią DNA na zasadzie komplementarności - odpowiednie zasady pasują do siebie i tworzą między sobą wiązania wodorowe: A═T (wiązanie wodorowe podwójne) i C≡G (wiązanie wodorowe potrójne)
funkcja przekazująca i przechowująca informację genetyczną
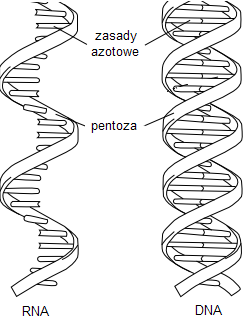
porównanie DNA i RNA:
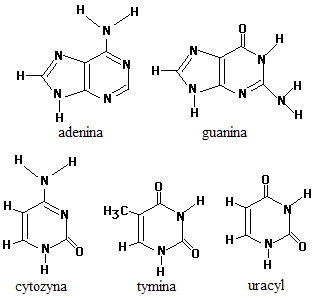
puryny: adenina (A), guanina (G)
pirymidyny: cytozyna (C)
komórka eukariotyczna: jądro, cytoplazma, rybosomy, mitochondria, chloroplasty
komórka prokariotyczna: cytoplazma, rybosomy
komórka eukariotyczna: jądro, mitochondria, chloroplasty
komórka prokariotyczna: genofor, plazmidy
odpowiada za syntezę białek
warunkuje ekspresję informacji genetycznej zapisanej w DNA
jest podstawowym nośnikiem informacji genetycznej (zawiera geny)
przekazuje informację genetyczną z pokolenia na pokolenie
NAZWA |
FUNKCJE |
NIEDOBÓR U ZWIERZĄT |
NIEDOBÓR U ROŚLIN |
wapń (Ca2+) |
|||
magnez (Mg2+) |
|||
sód (Na+) |
|
|
|
potas (K+) |
|||
żelazo (Fe2+) |
|||
kobalt (Co2+) |
|
||
miedź (Cu2+) |
|
||
mangan (Mn2+) |
|
||
cynk (Zn2+) |
|||
jod (J-) |
nie stwierdzono |
||
fluor (F-) |
nie stwierdzono |
NAZWA |
FUNKCJA |
ŹRÓDŁO |
NIEDOBÓR |
A |
|||
B1 |
|||
B2 |
|||
B6 |
|||
B11 |
|||
B12 |
|
||
C |
|||
D |
|
||
E |
|||
K |
|||
PP |
H+ + HCO3- ↔ H2CO3 ↔ H2O + CO2
OH- + H2CO3 ↔ HCO3- + H2O)
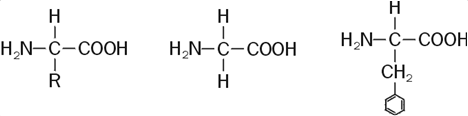
gdzie: R - podstawnik alifatyczny lub aromatyczny, -NH2 - grupa aminowa (zasadowa),
-COOH - grupa karboksylowa (kwasowa)
NH3+-CH2-COO- + H+ ↔ NH3+-CH2-COOH
NH3+-CH2-COO- + OH- ↔ NH2-CH2-COO- + H2O
ENDOGENNE |
EGZOGENNE |
alanina (Ala) asparagina (Asn) asparaginian (Asp) arginina (Arg) glutaminian (Gln) glutamina (Glu) glicyna (Gly) prolina (Pro) seryna (Ser) tyrozyna (Tyr) cysteina (Cys) |
lizyna (Lys) metionina (Met) leucyna (Leu) histydyna (His) fenyloalanina (Phe) treonina (Thr) tryptofan (Trp) izoleucyna (Ile) walina (Val) |


adenina + deoksyryboza → deoksyadenozyna
guanina + deoksyryboza →deoksyguaonozyna
cytozyna + deoksyryboza → deoksycytydyna
uracyl + deoksyryboza → deoksytymidyna
adenina + ryboza → adenozyna
guanina + ryboza → guanozyna
cytozyna + ryboza → cytydyna
uracyl + ryboza → urydyna
deoksyadenozyna + PO43- → deoksyadenozyno-5'-monofosforan
deoksyguaonozyna + PO43- → deoksyguanozyno-5'-monofosforan
deoksycytydyna + PO43- → deoksycytydyno-5'-monofosforan
deoksytymidyna + PO43- → deoksytymidyno-5'-monofosforan
adenozyna + PO43- → adenozyno-5'-monofosforan
guanozyna + PO43- → guanozyno-5'-monofosforan
cytydyna + PO43- → cytydyno-5'-monofosforan
urydyna + PO43- → urydyno-5'-monofosforan
CECHA |
RNA |
DNA |
|
ryboza
|
deoksyryboza
|
reszta fosforanowa |
PO43- |
|
wspólne zasady azotowe |
||
różne zasady azotowe |
pirymidyna: uracyl (U) |
pirymidyna: tymina (T) |
|
pojedyncza nić (chemicznie mniej stabilna od DNA) |
dwuniciowa helisa
|
wielkość cząsteczek |
mniejsze |
bardzo duże |
miejsce występowania |
|
|
funkcje |
||
min. 0,01% suchej masy (masa organizmu bez wody) organizmu
0,01-0,00001% suchej masy organizmu
części bilionowe suchej masy organizmu
tworzenie się i zanik chlorofilu, przy którym następuje rozpad chloroplastów (rośliny żółkną)
inaczej retinol
inaczej tiamina
bóle kończyn, drżenie i osłabienie mięśni, niewydolność układu krążenia
inaczej ryboflawina
inaczej pirydoksyna
inaczej kwas foliowy
inaczej kobalamina
inaczej kwas askorbinowy
witamina C jest wrażliwa na wysokie temperatury
krwawienie dziąseł, wypadanie zębów, obniżona odporność, nieprawidłowe zrastanie się kości
inaczej kalcyferol
inaczej tokoferol
inaczej filochinon
inaczej niacyna
wiązanie się pojedynczych cząsteczek wody w zespoły cząsteczkowe (tworzą się wiązania wodorowe)
inaczej uwodnienie; gromadzenie się dodatnich lub ujemnych końców cząsteczek wody wokół odpowiednich jonów (anionów lub kationów)
elektrolity (są polarne); aniony i kationy łączą się z odpowiednimi biegunami cząsteczek wody, co prowadzi do hydratacji i w efekcie rozpuszczenia
nieelektrolity (są niepolarne); odpychają od siebie cząsteczki wody
określa ilość energii potrzebną do podniesienia temperatury 1g wody o 1°C; jest wysoka ze względu na istnienie wiązań wodorowych (skutek asocjacji) - energia zamiast być przeznaczona na podniesienie temperatury wody służy rozrywaniu wiązań (woda pochłania energię)
określa ilość energii potrzebną do przeprowadzenia w stan pary 1g wody; jest wysoka ze względu na istnienie wiązań wodorowych (skutek asocjacji) - energia zamiast być przeznaczona na podniesienie temperatury wody służy rozrywaniu wiązań (woda pochłania energię, stąd parowanie potu lub transpiracja służy do pozbycia się ciepła)
określa ilość energii potrzebną do stopienia 1g lodu; jest wysoka ze względu na istnienie wiązań wodorowych (skutek asocjacji) - energia zamiast być przeznaczona na podniesienie temperatury lodu służy rozrywaniu wiązań (lód pochłania energię)
siły powierzchniowego przylegania cząsteczek wody do innych cząstek, czego skutkiem są zjawiska kapilarne (wspinanie się wody w wąskich rurkach, umożliwia to m.in. przemieszczanie się zawartej między cząsteczkami gleby wody do korzeni)
siły skupiające cząsteczki wody razem, czego skutkiem jest napięcie powierzchniowe (cząsteczki wody przyciągają się wzajemnie mocniej niż cząsteczki wody z cząsteczkami powietrza)
inaczej woda strukturalna; oblewa lub wchodzi w oddziaływania chemiczne z cząsteczkami związków komórkowych np. z białkami, ścianami komórek, błonami biologicznym (stanowi wówczas składnik budulcowy)
inaczej woda niezwiązana; wraz z rozproszonymi w niej substancjami komórkowymi tworzy koloid - cytoplazmę (stanowi wówczas środowisko wewnątrzkomórkowe lub substrat licznych reakcji)
wraz z rozpuszczonymi w niej substancjami tworzy roztwór otaczający komórki (stanowi wówczas nośnik związków odżywczych i sygnałów przekazywanych między komórkami)
nadmiar jonów wodorowych
nadmiar jonów wodorotlenowych
koloid
wędrówka cząsteczek w polu elektrycznym; szybkość wędrówki cząsteczek zależy od: ładunku, masy i kształtu cząsteczki, rodzaju podłoża (bibuła - elektroforeza bibułowa lub żel - elektroforeza żelowa) oraz napięcia prądu
wędrówka cząsteczek białka w polu elektrycznym po podłożu żelowym, które wysycono przeciwciałami - zetknięcie się przeciwciał z białkiem skutkuje wytrącaniem białka i uzyskaniem obrazu elektroforetycznego
aminokwasy, które organizm ludzki potrafi syntetyzować samodzielnie
aminokwasy, których organizm ludzki nie potrafi syntetyzować samodzielnie, muszą zostać dostarczone w postaci gotowej
związki będące swoim lustrzanym odbiciem (enancjomery)
wiązanie kowalencyjne; powstaje między grupą karboksylową jednego aminokwasu a grupą aminową drugiego (wydziela się także woda)
inaczej pierwotna; opisuje sekwencję (kolejność ułożenia) aminokwasów, która determinuje wszystkie właściwości danej cząsteczki (stąd taka różnorodność białek); stabilizowana przez wiązania peptydowe
opisuje ułożenie struktury pierwszorzędowej w przestrzeni; stabilizowana przez wiązania wodorowe
łańcuch polipeptydowy skręcony w helix (wiązanie wodorowe powstaje wewnątrz tego samego łańcucha); białka o tej strukturze są wytrzymałe i elastyczne np. mioglobina, hemoglobina, keratyna, miozyna
dwa równoległe łańcuchy polipeptydowe (wiązanie wodorowe powstaje między różnymi łańcuchami), zagięcia wynikają ze skręceń wiązań leżących poza ugrupowaniami peptydowymi; białka o tej strukturze są zwarte, nierozciągliwe i nierozpuszczalne w wodzie np. fibroina (w jedwabiu)
opisuje ułożenie struktury drugorzędowej w przestrzeni - α-helix i/lub β-harmonijka zwinięte w przestrzenną bryłę; stabilizowana przez wiązania wodorowe, mostki disiarczkowe, oddziaływania hydrofobowe i oddziaływania van der Waalsa. Kształt, wielkość i właściwości decydują o aktywności biologicznej białka
występuje tylko u białek złożonych z podjednostek; stabilizowana przez wiązania wodorowe, mostki siarczkowe, oddziaływania hydrofobowe i oddziaływania van der Waalsa
polega na zniszczeniu struktury trzeciorzędowej (wiązania stabilizujące tę strukturę są dość słabe)
inaczej białka fibrylarne; cechują się asymetrią cząsteczek (duży stosunek długości do szerokości); są rozciągniętymi łańcuchami polipeptydowymi powiązanymi wiązaniami kowalencyjnymi; mają trwałą strukturę i są nierozpuszczalne w wodzie np. skleroproteiny, miozyna
inaczej białka sferyczne; cechują się kształtem eliptycznym cząsteczek (niewielki stosunek długości do szerokości); są pofałdowanymi i zwiniętymi łańcuchami polipeptydowymi powiązanymi wiązaniami kowalencyjnymi np. histony, albuminy (są rozpuszczalne w wodzie), globuliny (są nierozpuszczalne w wodzie), prolaminy, protaminy, enzymy, immunoglobuliny
zbudowane wyłącznie z aminokwasów
białka zasadowe; wiążą i stabilizują cząsteczkę DNA u eukariotów
białka zasadowe; wiążą i stabilizują cząsteczkę DNA plemników
białka kwaśne; stanowią składnik tkanek stałych i płynów ustrojowych, osocza krwi, mleka, jaj ptasich, nasion
stanowią składnik mięśni (miozyna), mleka, jaj ptasich, nasion
stanowią składnik nasion zbóż
funkcje mechaniczne w tkankach ochronnych i oporowych
po zagotowaniu przechodzą w żelatynę; wyróżniamy kolagen i elastynę
występuje we włosach, piórach, paznokciach, pazurach, łuskach rogowych, kopytach, rogach (nadaje im twardość i odporność mechaniczną)
zbudowane z aminokwasów i składnika niebiałkowego
zbudowane z aminokwasów i metali np. transferyna (magazynuje i transportuje żelazo), ferrodoksyna (przenosi elektrony w fazie jasnej fotosyntezy) - połączenia aminokwasów z żelazem
zbudowane z aminokwasów i barwnika np. hemoglobina, mioglobina - połączenia aminokwasów z żelazoporfiryną (hem)
zbudowane z aminokwasów i cukrowców np. glikokaliks, białka grup krwi
zbudowane z aminokwasów i tłuszczowców np. białka błon komórkowych, HDL (transportują cząsteczki cholesterolu do wątroby, gdzie są one rozkładane), LDL (odkładają cząsteczki cholesterolu we włóknach mięśni gładkich tętnic)
zbudowane z aminokwasów i kwasu fosforowego np. kazeina (stanowi składnik mleka)
zbudowane z aminokwasów i DNA lub RNA; stanowią składnik chromatyny i rybosomów
gdy liczba grup -COOH i -NH2 jest jednakowa
gdy liczba grup -COOH przewyższa liczbę grup -NH2
gdy liczba grup -NH2 przewyższa liczbę grup -COOH
inaczej lipidy
wiązanie kowalencyjne; powstaje między grupą hydroksylową alkoholu a grupą hydroksylową kwasu tłuszczowego (wydziela się także woda)
związki będące połączeniem alkoholu i kwasu tłuszczowego
inaczej glicerydy lub acyloglicerole; związki będące połączeniem glicerolu i kwasu tłuszczowego; ulegają hydrolizie (tłuszcz + woda → kwas tłuszczowy + gliceryna)
związki będące połączeniem wyższych alkoholi monowodorotlenowych i kwasu tłuszczowego
związki będące połączeniem alkoholu, kwasu tłuszczowego i innego związku
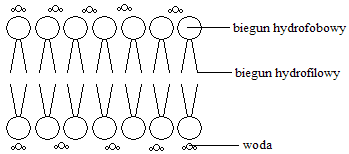
związki będące połączeniem alkoholu, kwasu tłuszczowego i reszty fosforanowej; są amfipatyczne (posiadają hydrofobowo-hydrofilowy charakter dzięki posiadaniu zarazem hydrofobowych łańcuchów bocznych kwasów tłuszczowych oraz hydrofilowego bieguna fosfodiestrowego, czyli zawierającego glicerol i elementy posiadające fosfor). Cząsteczki amfipatyczne tworzą w roztworach wodnych struktury dwuwarstwowe lipidowe, co jest podstawą tworzenia błon biologicznych (biegun hydrofobowy ustawia się do wewnątrz, a hydrofilowy na zewnątrz)
związki będące połączeniem alkoholu, kwasu tłuszczowego i cząsteczek cukrów
kwasy tłuszczowe takich tłuszczy nie mają wiązań wielokrotnych; są stałe, najczęściej zwierzęce
kwasy tłuszczowe takich tłuszczy mają wiązania wielokrotne; są ciekłe (tzw. oleje), najczęściej roślinne
inaczej węglowodany (stosunek wodoru do tlenu jest taki sam jak w cząsteczce wody - 2:1) lub sacharydy
do każdego węgla przyłączone są grupy hydroksylowe (warunkują słodki smak i dobrą rozpuszczalność w wodzie), a do jednego z węgli grupa aldehydowa lub grupa ketonowa
wiązanie kowalencyjne; powstaje między grupą hydroksylową jednego cukru a grupą hydroksylową drugiego (wydziela się także woda)
mają grupę aldehydową -CHO
mają grupę ketonową =CO
rozpuszczalne w wodzie
inaczej wielocukry lub glikany
łańcuch nierozgałęziony, rozpuszczalne w wodzie
łańcuch rozgałęziony, nierozpuszczalne w wodzie (stąd pełnią funkcje zapasowe, strukturalne i podporowe)
powstają z jednego rodzaju monosacharydów
powstają z różnych monosacharydów
DNA
RNA
informacyjny RNA; przenosi informację genetyczną z jądra do cytoplazmy
transportujący RNA; transportuje aminokwasy z cytoplazmy do rybosomów
rybosomalny RNA; współtworzy rybosomy
zbudowane z cukru pięciowęglowego, zasady azotowej i reszty fosforanowej
nukleotydy pozbawione reszt fosforanowych
nadaje nukleotydom silnie kwaśny charakter
aromatyczny związek organiczny zawierający azot
zasada azotowa dwupierścieniowa
zasada azotowa jednopierścieniowa
1
13
pierwiastki biogenne
D-glukopiranoza
D-rybofuranoza
Gly
Ile
Val
Glu
Gln
...
Wyszukiwarka
Podobne podstrony:
Budowa Chemiczna Białek
BUDOWA CHEMICZNA DNA, Genetyka
Budowa chemiczna i synteza lopo Nieznany
Budowa chemiczna
Budowa chemiczna prątka gruźlicy, medycyna, giełdy, interna1, interna j, Ftyzjatria, Ftizjatria, Gru
Budowa chemiczna organizmow, dydaktyka, biologia-praktyki, II gimnazjum
BUDOWA CHEMICZNA, STRUKTURA, FORMY I REPLIKACJA
budowa chemiczna a działanie farmakologiczne, chemia organiczna
Budowa chemiczna prątka gruźlicy-piśmiennictwo, medycyna, giełdy, interna1, interna j, Ftyzjatria, F
Budowa chemiczna
Budowa Chemiczna Białek
BUDOWA CHEMICZNA DNA, Genetyka
Budowa chemiczna i synteza lopo Nieznany
biologia BUDOWA CHEMICZNA RNA
Budowa chemiczna i metabolizm TSH
Wykład 1, budowa atomu, wiązania chemiczne
pdf wykład 02 budowa materii, podstawowe prawa chemiczne 2014
więcej podobnych podstron