![]()
Obliczenie stężenia roztworu NaOH:
cNaOH = 0,058
Obliczanie [a] początkowego stężenia zasady:
![]()
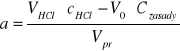
Obliczanie zmiany stężenia jonów OH- [x]:
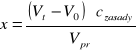
Obliczanie początkowego stężenia estru [b]:
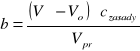
t (min) |
Vzasady (ml ,cm3) |
x |
a-x |
b-x |
|
|
0 |
6,5 |
0 |
0,012 |
0,011 |
0 |
|
|
13 |
0,0075 |
0,0045 |
0,0035 |
0,164 |
|
|
14 |
0,0087 |
0,0033 |
0,0023 |
0,274 |
|
|
14 |
0,0087 |
0,0033 |
0,0023 |
0,274 |
|
|
14,5 |
0,0093 |
0,0027 |
0,0017 |
0,376 |
|
|
14,5 |
0,0093 |
0,0027 |
0,0017 |
0,376 |
|
|
14,7 |
0,0095 |
0,0025 |
0,0015 |
0,424 |
|
|
15,2 |
0,0101 |
0,0019 |
0,0009 |
0,660 |
|
|
15,8 |
0,0108 |
0,0012 |
0,0002 |
1,705 |
|
|
16,4 |
0,011 |
0,001 |
0 |
|
|
![]()
![]()
![]()
t (min) |
|
0 |
0,087 |
|
0,251 |
|
0,361 |
|
0,361 |
|
0,463 |
|
0,463 |
|
0,511 |
|
0,747 |
|
1,792 |
Obliczanie stałej szybkości reakcji:
af - współczynnik kierunkowy
![]()
![]()
Wyliczenie błędu względnego:
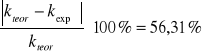
Wnioski:
Na podstawie wyników moich pomiarów stała szybkości reakcji wynosi 10,16![]()
. Porównując otrzymany wynik z danymi teoretycznymi ( 6,5 ![]()
) obliczyłem błąd względny który wynosi 56,31%. Tak duża rozbieżność może być spowodowana niedokładnym odczytywaniem z biurety wartości zużytej zasady sodowej, bądź też samym błędem wynikającym z wykonywania ćwiczenia.