Grupa: 23 Zespół: 9 |
Ćwiczenie: 9 |
Data: 16.03.98 |
1. Marta Stachoń 2.Paweł Janas |
Temat: Ebulioskopia. |
Ocena: |
I. Część teoretyczna.
Prężność pary P nad mieszaniną cieczy o całkowitej wzajemnej rozpuszczalności w przypadku doskonałego zachowania się tych cieczy w roztworze równa jest sumie prężności par poszczególnych składników.
gdzie:
P - ciśnienie całkowite;
PA - ciśnienie składnika A;
PB - ciśnienie składnika B.
Prężność pary nad roztworem jest proporcjonalna do ułamka molowego składnika. Współczynnikiem proporcjonalności jest prężność pary nad czystym składnikiem.
gdzie:
P - prężność pary nad roztworem;
X0 - ułamek molowy składnika;
P0 - prężność pary nad czystym składnikiem
W związku z obniżeniem prężności pary nad roztworem podwyższa się temperatura wrzenia cieczy.
P
Pc
T0 Tr
Podwyższenie temperatury wrzenia roztworu jest wprost proporcjonalne do stężenia molarnego substancji rozpuszczonej.
(A)
gdzie:
Twrz - zmiana temperatury wrzenia
KE - stała ebulioskopowa
m - molalność roztworu
ms - masa substancji rozpuszczonej
mr - masa rozpuszczalnika
n - liczba moli substancji
Stała ebulioskopowa ma wymiar temperatury i oznacza przyrost temperatury wrzenia roztworu w stosunku do temperatury wrzenia rozpuszczalnika zawierającego jeden mol substancji w tysiącu gramach rozpuszczalnika.
Przyrządy służące do dokładnego oznaczania temperatury wrzenia cieczy nazywamy ebuliometrami np: ebuliometr Świętosławskiego.
Rys. Schemat ebuliometru Świętosławskiego
II. Część obliczeniowa.
Ćwiczenie 1.
Obliczamy masę naważki tioacetamidu, której rozpuszczenie w 55 ml acetonu spowoduje wzrost temperatury wrzenia otrzymanego roztworu o około 1K.
Korzystamy ze wzoru (A), z którego wyliczamy ms:
Dane:
Ms=75.14 g.
KE=1480
mr=43.45 g
ΔTwrz=1 K
Po wstawieniu wartości do wzoru otrzymujemy:
ms=1.745 g
Napełniamy ebuliometr 55 cm3 acetonu, następnie doprowadzamy aceton do wrzenia i spisujemy temp. wrzenia. Rozpuszczamy odważkę tioacetamidu w acetonie i ponownie doprowadzamy roztwór do wrzenia, spisując temperaturę.
ρrozp = 0.7899g/cm3
Vrozp = 55.0cm3
pomiar dla 1.745g substancji:
masa substancji [g] |
masa rozpuszczalnika [g] |
molarność roztworu [mol/1000g] |
ΔT [K] |
stała ebulioskopowa [Kg*K/mol] |
1.745 |
43.4445 |
0.5345 |
0.705 |
1.48 |
Ćwiczenie2.
Obliczanie masy cząsteczkowej nieznanej substancji na podstawie różnicy temperatur wrzenia czystego rozpuszczalnika i roztworu zawierającego naważkę substancji o znanej masie.
a) Oznaczanie zmiany temp. wrz.:
ms=1.875g
T1=3.845K
T2=4.685K
ΔT=0.84K
Ze wzoru (A) wyliczamy Ms=76.05[g/mol]
Graficzne przedstawienie wyników:
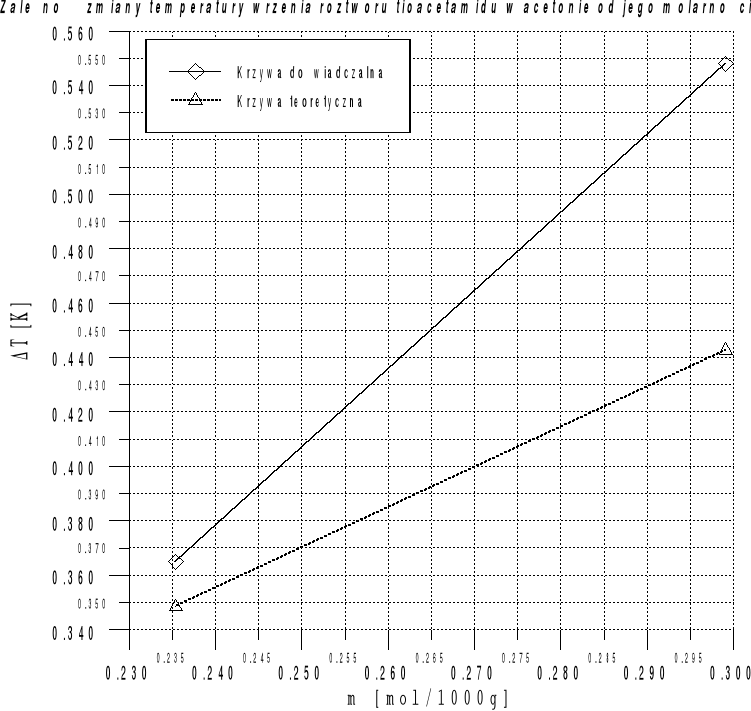
Wnioski:
Doświadczalna masa cząsteczkowa substancji rozpuszczonej w acetonie Ms=76.05[g/mol].Taka wartość masy cząsteczkowej oraz wygląd postaci stałej substancji może sugerować że jest to tioacetamid.
Literatura.
1. Sobczyk L., Kisza A., Gatner K., Koll A.: Eksperymentalna chemia fizyczna. PWN, Warszawa 1982.
Ebulioskopia
- 4 -
Wyszukiwarka
Podobne podstrony:
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
więcej podobnych podstron