Michał Mielnik Gr. 24 09.12.99
Zygmunt Rynduch Gr. 24
Rafał Mierzwa Gr. 24
Tomasz Kapelko Gr. 24
Spektrofotometria absorpcyjna
Podstawy teoretyczne.
Metody spektrofotometrii w świetle widzialnym i nadfiolecie polegają na pomiarze absorpcji promieniowania elektrometrycznego. W podanym zakresie promieniowania zjawisko absorpcji jest związane z przejściami między poziomami elektronów powłok zewnętrznych i zmiana energii cząsteczki lub atomu. W przypadku absorpcji cząsteczka znajdująca się w stanie podstawowym pochłania padające promieniowanie , w wyniku czego wzrasta energia elektronów i cząsteczka przechodzi w stan wzbudzony. W przypadku emisji występuje zjawisko odwrotne , a więc cząsteczka znajdująca się w stanie wzbudzonym emituje energię w postaci promieniowania elektromagnetycznego i cząsteczka wraca do stanu podstawowego. Zmiany energii ΔE w procesie absorpcji lub emisji są proporcjonalne do częstotliwości drgań ν ( a odwrotnie do długości fali λ ) promieniowania elektromagnetycznego:
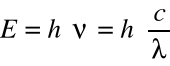
Gdzie: h- stała Plancka
ν- częstotliwość drgań
c- prędkość światła
λ- długość fali
![]()
Gdy wiązka promieniowania monochromatycznego przechodzi przez warstwę roztworu, wówczas wychodzące promieniowanie jest osłabione w stosunku do padającego. Promieniowanie o natężeniu Io ulega częściowo odbiciu lub rozproszeniu i częściowo pochłonięciu, a część tylko przechodzi przez roztwór.
Gdzie: Ir- natężenie promieniowania rozproszonego i odbitego
Ip- natężenie promieniowania pochłoniętego
It- natężenie promieniowania przechodzącego przez roztwór
![]()
W przypadku roztworów nie zawierających zawiesin wartość Ir jest niewielka i można ją praktycznie pominąć. Stosuje się wtedy równanie:
![]()
Znając wartość Io i It można obliczyć Ip. Natężenie światła przechodzącego It zależy od natężenia źródła światła Io i od grubości warstwy roztworu. Zależność tę można wyrazić wzorem LAMBERTA:
Gdzie: k- współczynnik proporcjonalności
b- grubość warstwy roztworu
![]()
Podobna zależność istnieje między natężeniem światła przechodzącego Ir a stężeniem substancji barwnej c w roztworze. Zależność tę opisuje prawo BEERA:
Gdzie: kt- współczynnik proporcjonalności
![]()
Zestawiając równania LAMBERTA i BEERA otrzymujemy:
Gdzie: a- współczynnik absorpcji
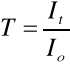
Jest to prawo spektrofotometrii absorpcyjnej. Wyrażenie It / Io nazywamy przepuszczalnością lub transmitancjąT:
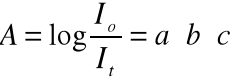
a logarytm odwrotności tego wyrażenia nazywa się ekstynkcją lub absorbancją:
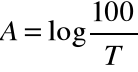
Przy stałej grubości warstwy cieczy, a więc przy stałej b absorbancja A zależy od stężenia substancji. Zależność między absorbancją a transmitancją ( wyrażoną w procentach) można przedstawić wzorem:
Aparatura pomiarowa
Przyrządy do pomiarów spektrofotometrycznych składają się na ogół ze źródła promieniowania, monochromatora, przesłony do regulacji natężenia promieniowania, kuwety z próbką, detektora promieniowania oraz urządzenia pomiarowego lub rejestrującego. W przypadku aparatów do pomiaru w nadfiolecie układ optyczny szklany jest zastępowany kwarcowym, który nadaje się także do pomiarów w świetle widzialnym. Prosty przyrząd służący do wizualnych obserwacji zmiany zabarwienia lub do pomiarów adsorpcji za pomocą urządzenia fotoelektrycznego nosi nazwę kolorymetru lub fotokolorymetru. W prostych urządzeniach światło monochromatyczne uzyskuje się za pomocą filtru szklanego, który przepuszcza stosunkowo szeroką wiązkę promieniowania, co powoduje mniejszą dokładność pomiaru. Przyrządy bardziej precyzyjne są wyposażone w układ rozszczepiający widmo (pryzmat lub siatkę dyfrakcyjną), służący do wydzielania bardzo wąskiej wiązki światła monochromatycznego. Mają one nazwę spektrofotometrów. Rozróżnia się spektrofotometry jedno- i dwuwiązkowe.
Przyrządy jednowiązkowe są znacznie prostsze, lecz mniej dokładne. W bieg wiązki promieniowania wstawia się najpierw odnośnik, a następnie badaną próbkę. W spektrofotometrach dwuwiązkowych jedno źródło światła rozdziela się na dwie wiązki. Jedna z nich przechodzi przez odnośnik, a druga przez badaną próbkę.
Jako źródło promieniowania stosuje się lampy wolframowe, wytwarzające promieniowanie w zakresie 350 - 2500 nm lub lampy wolframowo-jodowe. W zakresie nadfioletu jest stosowana zwykle wysokociśnieniowa lampa wodorowa lub deuterowa, emitująca promieniowanie w zakresie 180 - 380 nm.
Natężenie promieniowania przechodzącego przez roztwór mierzy się różnego typu detektorami. Najczęściej jako detektory stosuje się fotoogniwa, fotokomórki lub rzadziej fotopowielacze.
Fotoogniwa składają się z płytki metalowej (np. Fe), warstwy półprzewodnika (selen lub tlenek miedzi) i cienkiej, przepuszczającej światło warstwy metalu (np. srebro, ołów, złoto). Światło, padając na warstwę półprzewodnika, powoduje wytworzenie się różnicy potencjałów między warstwą półprzewodnika a płytką metalową tworząc ogniwo. Jeżeli ogniwo połączymy z galwanometrem, to w obwodzie będzie płynąć prąd o natężeniu proporcjonalnym do natężenia padającego promieniowania.
Fotokomórki składają się z dwóch metalowych elektrod w bańce szklanej pozbawionej powietrza. Katoda w postaci blaszki metalowej jest pokryta materiałem zdolnym do emitowania elektronów pod wpływem padającego promieniowania. Elektrony dążą do anody i w obwodzie płynie prąd, którego natężenie można zmierzyć galwanometrem.
Podstawową częścią fotopowielacza jest także fotokatoda. Elektrony emitowane z niej pod wpływem padającego promieniowania padają na zestaw wtórnych elektrod (dynod, emiterów), gdzie są przyspieszone i w wyniku wtórnej emisji ich liczba do emitera wykładniczo rośnie.
Metody pomiaru w świetle widzialnym
W spektrometrycznej analizie wody wykorzystuje się najczęściej metodę krzywej wzorcowej. Inne techniki, jak spektrofotometria różnicowa i miareczkowanie spektrofotometryczne, w analizie wody są stosowane bardzo rzadko.
W metodzie krzywej wzorcowej wykonuje się najpierw kilka roztworów wzorcowych zawierających oznaczane substancje o znanych dokładnie stężeniach. Zgodnie z metodą analityczną prowadzi się reakcję w celu wywołania zabarwienia. Sposób postępowania z badanymi próbkami i roztworami wzorcowymi jest taki sam. Następnie mierzy się absorbancję zabarwionych roztworów wzorcowych. Z uzyskanych wyników wykreśla się krzywą wzorcową (stężenie-absorbancja). Mierząc absorbancję zabarwionych próbek, uprzednio przygotowanych w identyczny sposób jak wzorce,odczytujemy na krzywej wzorcowej stężenie oznaczanej substancji.
Wykonanie ćwiczenia
Roztwór wzorcowy o stężeniu 1 mg/ml rozcieńczamy stukrotnie w kolbie miarowej otrzymując roztwór roboczy o stężeniu 0,01 mg/ml. Do pięciu kolbek o poj. 50 ml pobieramy odpowiednio 0, 2, 5, 10, 15 ml roztworu roboczego. Do szóstej kolbki pobieramy 10 ml wody wodociągowej. Następnie do każdej kolbki dodajemy kolejno identyczne ilości następujących odczynników:
2 ml 2 % CaCl2
5 ml 0,05 % żółcieni tytanowej
5 ml 0,5 % żelatyny
delikatnie mieszając miareczkujemy 1 mol/l NaOH do zmiany barwy (od 3 - 10 kropel)
5 ml 1 mol/l NaOH
Uzupełniamy wodą destylowaną do ok. 35 ml, dokładnie mieszamy i dopełniamy do kreski. Otrzymane roztwory pozostawiamy na 15 min.
Prowadzimy pomiar przy długości fali λ = 545 nm.
Do pierwszej kuwety wlewamy tzw. ślepą próbę, czyli roztwór pozbawiony jonów magnezowych. Ustawiamy spektrofotometr w ten sposób, aby dla ślepej próby wskazywał zerową absorbancję. Do drugiej kuwety wlewamy kolejno roztwory wzorcowe odczytując ich absorbancję, powtarzając każdy pomiar trzykrotnie. Tworzymy w ten sposób krzywą wzorcową.
Lp. |
Objętość roztworu roboczego [ml] |
Zawartość Mg w kolbie 50 ml [mg/ml] |
Odczytana wartość absorbancji |
Średnia wartość absorbamcji |
Wartość transmitancji [%] |
||
|
|
|
Pomiar 1 |
Pomiar 2 |
Pomiar3 |
|
|
1. |
0 |
0 |
0 |
0 |
0 |
0 |
100 |
2. |
2 |
0,0004 |
0,075 |
0,075 |
0,075 |
0,075 |
84 |
3. |
5 |
0,0010 |
0,157 |
0,160 |
0,160 |
0,159 |
69 |
4. |
10 |
0,0020 |
0,275 |
0,275 |
0,275 |
0,275 |
53 |
5. |
15 |
0,0030 |
0,380 |
0,380 |
0,380 |
0,380 |
41,5 |
6. |
Próbka badana - 10 ml |
0,195 |
0,195 |
0,195 |
0,195 |
64 |
|
Krzywa wzorcowa
Krzywa wzorcowa jest dana równaniem y = 124.176 x + 0.0188552
Obliczona zawartość Mg w 50 ml próbki badanej wynosi C*Mg = 0,0014185 mg/ml
![]()
Zawartość Mg w samej wodzie wodociągowej (pobranych 10 ml) obliczamy ze wzoru:
w - współczynnik rozcieńczenia 50 ml/10 ml = 5
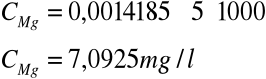
Zawartość magnezu w wodzie wodociągowej wynosi 7,0925 mg/l
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Wyszukiwarka
Podobne podstrony:
Lenovo 3000 N200
Mitsubishi 3000 GT
POTTINGER TERRADISC 3000, 4000 K instrukcja obslugi [PL]
Geodyna 3000 PL (tłumaczone automatem z Szwedzkiego)
22 A 3000 p n e 1400 n e sztuka Indiiid 29435
Konfiguracja VLAN na przelacznikach serii 2000, 3000 i 4000
Instrukcja obsługi TOPCON GPT 3000
8 A 3000 p n e 1279 r n e Chiny
2218 SUNNY BOY 2500 3000 Installationsmanual
3000
1294233750karta kat, E 3000
2008 04 06 3000 14
Kartridże atramentowe Canon BJC 3000
3000
3000
IO 7538 043v3 T 3000 wer 3 0 pl(2)
22 B 3000 p n e 1400 n e sztuka Indiiid 29436 (2)
8 B 3000 p n e 1279 r n e Chiny
więcej podobnych podstron