Marta Miller
Rok 1, gr. 4, Budownictwo
Ćwiczenie C02
Badanie procesu topnienia i krzepnięcia wody
Wstęp :
Celem ćwiczenia jest zapoznanie się ze zjawiskami w trakcie schładzania i podgrzewania wody, jak również wyznaczenie ciepła topnienia wody. Woda występuje w trzech stanach skupienia; stałym, ciekłym i gazowym. Jest to jednak za każdym razem ten sam związek chemiczny, różniący się tylko wzajemnym ułożeniem cząsteczek względem siebie. Przechodzenie związków ze stanu ciekłego w stały i odwrotnie charakteryzują dwie temperatury; krzepnięcia i topnienia. Aby związek mógł przechodzić z jednego stanu w drugi, należy mu dostarczyć lub odebrać energie. Ciepło topnienia jest to ilość ciepła jaką należy dostarczyć jednostce masy ciała stałego, aby zmieniło się ono w ciecz o tej samej temperaturze.
Przebieg ćwiczenia:
Pierwszym etapem jest przygotowanie komputera; uruchomienie programu „Science Workshop”, podłączenie czujnika temperatury do interfejsu.
Wyznaczanie temperatury:
krzepnięcia: przygotowaliśmy zlewkę z mieszaniną wody z lodem, wlaliśmy ok. 5ml wody, włożyliśmy cylinderek do mieszaniny lodu z wodą, do cylinderka włożyliśmy czujnik temperatury, uruchomiliśmy program (w tym momencie temperatura wody w cylindrze spadła do temperatury bliskiej temperaturze wody z lodem w zlewce - ok. 0°C ), następnie wsypaliśmy uprzednio przygotowaną sól kuchenną ( ok. 40ml ) do zlewki i wymieszaliśmy, pomiaru dokonywaliśmy przez 15 min., aż temperatura obniżyła się do ok. -5°C
topnienia: uruchomiliśmy program, wyleliśmy cylinderek wraz z czujnikiem z mieszaniny wody, lodu i soli ( nie poruszając czujnikiem ) i umocowaliśmy go w statywie, w czasie gdy lód ogrzewa się od otaczającego powietrza przygotowałam zlewkę z wodą o temperaturze pokojowej ( w celu przyspieszenia doświadczenia włożyliśmy cylinderek do wody ), pomiar przerwaliśmy gdy temperatura w cylinderku osiągnęła temperaturę wody w zlewce
analiza danych;
uaktywniliśmy okno „Table”. W jednym okienku ustawiliśmy wykres temperatury krzepnięcia w drugim zaś temperatura topnienia
za pomocą kursora precyzyjnego ustaliliśmy temperaturę topnienia i krzepnięcia, wynosiły one odpowiednio 0,623°C i -0,151°C
Wyznaczanie ciepła topnienia lodu:
usunęliśmy dane z poprzedniego doświadczenia, zważyliśmy wewnętrzne naczynie kalorymetru wraz z pokrywą i mieszadłem mk=0,0958 kg, napełniłam kalorymetr ciepłą wodą ( 25°C - 30°C ) i zważyliśmy m1=0,309 kg, włożyliśmy do kalorymetru z woda czujnik temperatury i uruchomiliśmy program, wrzuciliśmy do kalorymetru bryłkę lodu przygotowaną uprzednio i doprowadzoną do temperatury topnienia, zamknęliśmy kalorymetr i zaczęliśmy mieszać, gdy temperatura przestała się zmniejszać wyłączyliśmy pomiar, zważyliśmy kalorymetr z całą zawartością m2=0,347 kg,
na monitorze odczytujemy najwyższą (t0 ) i najniższą ( tk ) temperaturę wody: t0=25,6°C i tk= 12,8°C,
obliczamy:
masę wody mw = m1 - mk = 0,2133kg,
masę lodu: ml = m2 -m2 =0,038 kg,
Ciepło topnienia lodu obliczam ze wzoru:
![]()
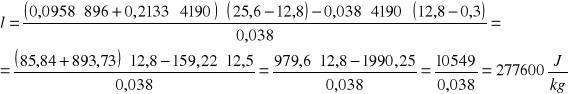
Średnie ciepło topnienia lodu wynosi tyle samo, czyli ![]()
= 277600![]()
, ponieważ doświadczenie wykonaliśmy dla jednego pomiaru.
Rachunek błędów
W wyniku jednego pomiaru niemożliwe jest obliczenie błędu względnego (=0) oraz błędu względnego procentowego (=0%).
Jedynym błędem , jaki mogę obliczyć to błąd procentowy względem wartości tablicowej.
![]()
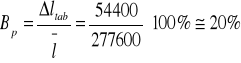
Wnioski:
Z przeprowadzonego doświadczenia wynika, że temperatura krzepnięcia jest niższa od 0°C i wynosi tk= -0,1°C, zaś temperatura topnienia jest wyższa od 0°C i wynosi tt=0,3°C. Pomiary dokonane zostały drogą cyfrową za pomocą komputera, więc powinny być dość dokładne, jednak błąd wyszedł stosunkowo wysoki. Błąd wynika z wpływu ciśnienia i temperatury na badane przedmioty, niedokładności wykonywania doświadczenia i pewnych czynności technicznych. Te same pomiary dokonane w próżni dałyby dokładniejsze wyniki.
Wyszukiwarka
Podobne podstrony:
Ćwiczenie C2, Ćwiczenie C2, Łukasz Rafałowski
Ćwiczenie55, Ćwiczenie 55 (1), Łukasz Rafałowski BUDOWNCTWO rok I
ĆwiczenieC7, Ćwiczenie C7 (2), Łukasz Rafałowski BUDOWNICTWO ROK I GRUPA 4
Ćwiczenie 47, Ćwiczenie 47 (3), Łukasz Rafałowski BUDOWNICTWO ROK I GRUPA 4
Cwiczenie C2
C2, sgsp, Hydromechanika, HYDROMECHANIKA 1, HYDR INSTRUKCJE DO CWICZEN
Laborki Fizyka ćwiczenie C2, SGSP, Fizyka, Fizyka lab, laborki fizyka
Prezentacja tekst, Patofizjologia - C2 Wierzchowiec, Patofizjologia (ćwiczenia)Wierzchowiec
Cwiczenie C2
B2 C2 ozap zalacznik1 cwiczenia pytania
Cwiczenie C2
Spoleczenstwa i kultura Europy - cwiczenia 2009-2010 Semestr Letni V.2, EUROPEISTYKA I ROK, ćwiczeni
więcej podobnych podstron