TPL II - WYKŁAD 10
05.03.2009r.
Parametry wchłaniania substancji leczniczej
w formach leków podawanych na skórę
Barierę hamującą wchłanianie substancji leczniczej przez skórę stanowi warstwa zewnętrzna komórek naskórka - warstwa rogowa - stratum corneum
tworzą ją ściśle ułożone, zrogowaciałe, płaskie komórki, których składnikiem jest przede wszystkim α-keratyna
zawierają one niewielką ilość lipidów i tylko 15 % wody
w przestrzeniach między komórkowych nagromadzone są natomiast głównie substancje lipidowe
Struktura warstw lipidowych w przestrzeniach międzykomórkowych:
strefa lipidowa
HLB: 0 - 10
strefa hydrofilowa
polarne grupy lipidów
HLB: 10 - 20
Szybkość wchłaniania substancji do skóry i przez skórę limituje warstwa rogowa
zwiększenie przepuszczalności tej bariery jest bardzo istotne przy transdermalnej drodze podania leku lub w celu uzyskania efektu leczniczego w skórze.
stąd wynika ogromne zainteresowanie w ostatnich latach promotorami wchłaniania (acelatory wchłaniania)
Promotory wchłaniania:
można je zdefiniować jako związki zmieniające strukturę skóry, tym samym zwiększające jej przepuszczalność
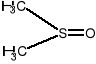
Struktura efektywnych promotorów wchłaniania:
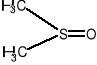
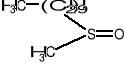
DHSO - dimetylosulfotlenek
bardzo długi okres biotransformacji
utlenia się do tlenku siarki i powoduje zgorzel płuc
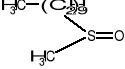
DCMC - decylometylosulfotlenek
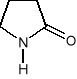
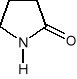
2 - pirolidon
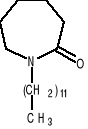
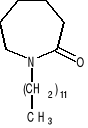
Azon = 1-dodecyloazocyklloheptan - 2 - ondla wszystkich i dla wszystkiego
z wyjątkiem preparatów z suchych ekstraktów roślinnych
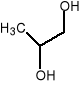
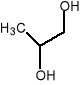
Glikol propylenowy
Kwas olejowy
![]()
Laurylosiarczan sodowy
![]()
związki o charakterze lipidowym:
np. azon, kwasy tłuszczowe
wpływają na struktury międzykomórkowe
umiejscawiają się między hydrofobowymi łańcuchami lipidów
rozluźniają układ warstw lipidów
polarne cząsteczki promotorów
np. DHSO, DCMC, inne
w małych stężeniach - wchodzą w interakcje z białkami wewnątrz komórkowymi
w dużych stężeniach - gromadzą się w przestrzeniach międzykomórkowych
otoczki solwatacyjne tworzą przestrzenie dogodne dla penetracji substancji hydrofilowej
konsekwencją „rozsunięcia” cząstek lipidów jest upłynnianie tej fazy i ułatwianie dyfuzji również związków lipofilowych
promotory wchłaniania o właściwościach amfifilowych
np. tenzydy
zmieniają zarówno właściwości białek jak i lipidów międzykomórkowych
Interakcje promotorów wchłaniania z białkami warstwy rogowej, m.in.:
rozszczepienie wiązań siarczkowych
zmiana konformacji α-keratyny
tworzenie konkurencyjnych kompleksów
zapobieganie wiązaniu substancji penetrującej
Promotory wchłaniania powinny być:
bardzo dobrymi rozpuszczalnikami substancji leczniczej
dobrymi solubilizatorami (pośrednikami rozpuszczalności) substancji leczniczej
powinny zwiększać w skórze (rozumiane jako fazę) współczynnik podziału substancji leczniczej
W technologii form leków podawanych na skórę znacznie mogą mieć jedynie promotory wchłaniania o następujących cechach:
pozbawienie własnego działania farmakologicznego
nie drażniące
nie toksyczne
nie wywołujące uczuleń
działające szybko i długotrwale, przy czym efekt powinien być możliwy do przewidzenia
działające w sposób odwracalny, tj. po usunięciu promotora skóra musi całkowicie odzyskać funkcję bariery
nie ułatwiające przenikania przez skórę substancji z organizmu na zewnątrz
zgodne chemicznie i fizycznie z substancją leczniczą oraz innymi składnikami fazy farmaceutycznej (postać leku)
Wprowadzenie nowych promotorów wchłaniania wymaga kilkuletnich doświadczeń - bardzo skomplikowanych badań in vitro i in vivo.
Wprawdzie wiele związków obdarzonych jest zdolnością zwiększania penetracji, lecz nie są one stosowane, np. syntetyczne lecytyny
Najczęściej stosowane promotory wchłaniania:
Przykłady Zastosowanie:
Alkohole
etanol kortykosterydy, estradiole
izopropanol indometacyna, dietofenole
Glikole
glikol etylenowy metronidazol, estradiol
glikol propylenowy propranolol, hydrokortyzon i inne
z azonem 5-fluorouracyl
z kwasem olejowym acyklowir, kwas salicylowy
z heksadekanolum i oktadekanolum estradiol
z izopropanolem metotreksat
Amidy
mocznik kortykosterydy
dimetyloacetamid ditronal, lidokaina
dimetyloformamid betametazon, kofeina
dimetylotoluamid gryzeofulwina
Alkohole i kwasy tłuszczowe oraz estry
alkohole i kwasy: 5-fluorouracyl
olejowy
mirystynianowy
izopropylowy
Tenzydy - wszystkich kwas
tenzydy jonowe i niejonowe kwas nikotynowy i estry, lidokaina, naproksen,
diklofenak
Pirolidony
2 - pirolidon gryzeofulwina, ibuprofen, insulina, oksytetracyklina,
N - metylo - 2 - pirolidon lindomycyna
Sulfotlenki
DHSO… tetracykliny, 5-fluorouracyl, skopolamina, fizostygmina,
testosteron, naproksen …
Azon
antybiotyki, indometacyna, leki p/grzybicze i leki
p/łuszczycy!!! wazopresyna, 5-fluorouracyl, insulina
Promotory intensywnie badane:
Glikol propylenowy
solubilizuje keratynę
nie wiąże metali
blokuje wiązania wodorowe
brak interakcji ze składnikami lipidowymi
sam jest promotorem dla azonu
DMSO
działanie uzależnione jest od stężenia (40 - 60% bariera)
interakcje z lipidami
w przestrzeni międzykomórkowej tworzą wiązania wodorowe
rozluźnia się struktura lipidów
wada
wydala się drogami oddechowymi
duże stężenie
drażnią skórę
Azon
uznany za najlepszy ze znanych obecnie promotorów
kumuluje się w międzykomórkowej fazie lipidowej warstwy rogowej
zaburza jej strukturę
zwiększa płynność lipidów
zwiększa zdolność wiązania wody przez warstwę rogową
Tenzydy
wiążą się z białkami wewnątrzcząsteczkowymi i lipidami w przestrzeni międzykomórkowej
tworzą kanały umożliwiające penetrację wody i substancji w niej rozpuszczonych
rozkręcają helisę α - keratyny
bardzo dogodna droga penetracji dla związków polarnych
obszar bardzo intensywnych prac badawczych
Dobór promotora
teoretyczne przewidywanie rozpuszczalności
teoria Hildebranda - Scatcharda - Fedora
gdzie:
log x2 - log ułamka molowego substancji rozpuszczonej
ΔHf - entalpia topnienia
Tm - temperatura topnienia substancji rozpuszczonej w ok.
Elementami, które należy obliczyć, aby przewidzieć rozpuszczalność są:
ΔHf
V1
V2
δ1
δ2
Entalpię topnienia ΔHf gaz oblicza się z:
Parametry rozpuszczalności δ1 i δ2 oblicza się metodą Pedorsa (analogicznie jak refrakcję molową) zasada addytywności
ΣΔqi - energia parowania (suma elementów w cząsteczce [cal/mol])
ΣΔvi - objętość molowa [j.w.] w cm3/mol
Obliczoną wartość rozpuszczalności w ułamku molowym można wyrazić w mol/L
Mcz. - M.cz. rozpuszczalnika (promotorów przejścia i każdego innego układu)
bardzo często korzysta się z równania przy założeniu jednostkowego oddziaływania dla rozpuszczalności doskonałej (idealnej)
odtworzenie lipidowego modelu stratum corneum potwierdził słuszność tzw. ścieżki solubilizacyjnej
oparta jest ona na oznaczeniu układu: wodny roztwór solubilizatora - substancja lecznicza
- 45 -
Wyszukiwarka
Podobne podstrony:
wykład 13 - 26.03.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 11 - 12.03.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 12 - 19.03.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 16 - 16.04.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 15 - 09.04.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 14 - 02.04.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 9 - 26.02.2009, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 4 - 23.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 2 - 09.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 16 - 16.04.2009 - cz.2, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 3 - 16.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 17 - 23.04.2009 - cz.3, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 17 - 23.04.2009 - cz.2, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 1 - 02.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 4 - 23.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 2 - 09.10.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 8 - 19.02.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 6 - 06.11.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
wykład 7 - 13.11.2008, FARMACJA, ROK 5, TPL 3, Zachomikowane
więcej podobnych podstron