1.BUDOWA ATOMU, PIERWIASTKI MATERIA gazy, ciecze, ciała stałe(bezpostaciowe- szkliste, osady, krystaliczne- molekularne, jonowe),DEMOKRYT(filozof grecki)”materia musi być zbudowana z niepodzielnych cząstek” "atomas„ (gr.) = niepodzielny. W roku 1986 naukowcy odkryli nowe (mniejsze) cząstki we wnętrzu protonu i nazwali je kwarkami, protony (p) - są to cząstki elementarne posiadające jednostkowy ładunek dodatni +1 oraz jednostkową masę około 1,0073 u Protony i Neutrony tworzą razem Nukleony stanowiąc centralną część atomu neutrony(n)-cząstki elementarne posiadające jednostkową masę około 1,0087 u i są pozbawione ładunku elektrycznego. elektrony (e) - cząstki elementarne obdarzone jednostkowym ładunkiem ujemnym -1 i bardzo małą masą równą 1/1846 u (dokładnie 0,00055 u ) Są więc praktycznie pozbawione masy
WIĄZANIA CHEMICZNE
Aby powstało wiązanie, spełnione muszą być poniższe warunki: reagujące atomy powinny się zderzyć ze sobą, zderzenie to musi być efektywne. Gdy dwa atomy zbliżają się do siebie, zewnętrzne, luźno związane elektrony zostają mocno zaburzone, oddziałując na wszystkie cząstki układu (jony, elektrony). Oddziaływanie to może prowadzić do powstania wiązania, gdy jądra/jony są blisko siebie. Proces powstawania cząsteczki jest korzystny energetycznie - prowadzi do zmniejszenia energii układu. Utworzona cząsteczka jest trwalsza niż poszczególne atomy. Wiązania tworzą elektrony zewnętrznej powłoki elektronowej atomu (walencyjne), przy czym cząsteczki powstają jedynie wówczas, gdy w wyniku reakcji każdy atom osiąga trwałą konfigurację elektronową. Najtrwalsze konfiguracje elektronowe mają atomy gazów szlachetnych (8 elektronów na powłoce walencyjnej) - pierwiastki bierne chemicznie. Cząsteczki dążą do wypełnienia powłoki walencyjnej, czyli obsadzenia jej 8 elektronami(reguła oktetu)Atomy mogą osiągać trwałą konfigurację elektronową przez oddawanie, przyłączanie lub uwspólnianie elektronów. Wiązanie jonowe.
Wiązanie jonowe Powstaje gdy różnica elektroujemności pomiędzy łączącymi się pierwiastkami wynosi więcej niż 1,7. Następuje wówczas przesunięcie elektronów w stronę atomu bardziej elektroujemnego, który staje się anionem, natomiast atom oddający elektrony staje się kationem. Siłą, która utrzymuje dwa atomy ze sobą jest siłą przyciągania elektrostatycznego (brak kierunkowości). Na przykład w związkach pierwiastków z pierwszej kolumny tablicy okresowej z pierwiastkami przedostatniej kolumny (halogenki metali alkalicznych: KCl, LiBr) / pierwiastek elektrododatni - pierwiastek elektroujemny/Cechy związków z przewagą wiązania jonowego: ciała w stanie stałym, zbudowane z kationów i anionów, przyciągających się ze stosunkowo dużą siłą, twarde kryształy o wysokiej temperaturze topnienia i wrzenia, rozpuszczają się dobrze w rozpuszczalnikach polarnych (woda),w stanie stopionym lub w roztworze dobrze przewodzą prąd elektryczny (nośnikiem ładunków są ruchliwe jony),ich reakcje zachodzą stosunkowo szybko.
Wiązania kowalencyjne(atomowe)Jest wynikiem uwspólniena pary elektronowej, przy czym każdy atom dostarcza jeden elektron. Wiązanie koordynacyjne - szczególny przypadek w. kowalencyjnego, gdy uwspólniona para elektronów wiązania pochodzi od jednego atomu (NH4Cl). Mogą powstawać także tzw. wiązania podwójne lub potrójne przez uwspólnienie 4 lub 6 elektronów (np. atomy azotu o konfiguracji 1s22s2p3 - 5 elektronów walencyjnych - tworząc trzy wspólne pary elektronowe uzyskują oktet). Wiązanie ukierunkowane. Na przykładH2,O2/pierwiastek elektroujemny - pierwiastek elektroujemny/Cechy związków z przewagą wiązania jonowego: ich cząsteczki słabo na siebie oddziałują, ich kryształy wykazują niewielką odporność na działanie czynników mechanicznych, mają niskie temperatury przejść fazowych, rozpuszczają się w rozpuszczalnikach niepolarnych (benzen, tetrachlorek węgla),w stanie stopionym lub w roztworze nie przewodzą prądu elektrycznego,reagują stosunkowo wolno.Pośrednie między wiązaniem atomowy i onowym.Tworzy się jeśli różnica elektroujemności łączących się pierwiastków zawiera się w granicach 0,4-1,7.Uwspólniona, wiążąca para elektronów przesunięta jest w stronę atomu pierwiastka bardziej ujemnego. Np. HCl - charakter wiązania jest w ok. 80% atomowy i w 20% jonowy.Cząsteczki w związku z takim nierównomiernym rozmieszcze-niem ładunków tworzą dipole (cząsteczki dwubiegunowe).
Wiązania metaliczne W sieci metalicznej każdy elektron z zewnętrznych powłok znajduje się pod wpływem kilku jąder sąsiednich atomów, co powoduje rozmycie się ściśle określonych poziomów energetycznych w jedno ciągłe pasmo przewodnictwa. Elektrony walencyjne mogą się swobodnie przemieszczać. Materiały o dobrym przewodnictwie elektrycznym. Wiązania wodorowe dwie cząsteczki/jony połączone są jonem wodorowym, szczególne znaczenie ma wiązane -0-H----0-, pełni istotną rolę w utrzymaniu struktury białek i kwasów nukleinowych WĘGLOWODORY- Najprostsze związki organiczne, zawierające tylko atomy węgla i wodoru. mimo tego, że węglowodory składają się tylko z dwóch pierwiastków, jest ich bardzo dużo ze względu na mnogość sposobów łączenia się atomów węgla między sobą.
Podział węglowodorów-Węglowodory alifatyczne (łańcuchowe)- nie zawierają pierścieni benzenowych, Węglowodory aromatyczne - zawierają pierścień benzenowy
Nasycone - węglowodory alifatyczne bez wiązań wielokrotnych
Nienasycone - zawiera jedno lub więcej wiązań podwójnych lub potrójnych Alkany-Węglowodory Nasycone (propan, butan, oktan)
Cykloalkany - alkany o strukturze pierścieniowej (cyklopropan, cyklopentan)
AlkenyWęglowodory z jednym wiązaniem podwójnym węgiel - węgiel (propen, eten)
Alkiny Węglowodory zawierające potrójne wiązanie węgiel - węgiel
PIROLIZA (inaczej destylacja rozkładowa) to proces rozkładu termicznego substancji prowadzony poprzez poddawanie ich działaniu wysokiej temperatury, ale bez kontaktu z tlenem i innymi czynnikami utleniającymi. Zwykle w trakcie pirolizy bardziej złożone związki chemiczne wchodzące w skład pirolizowanej substancji ulegają rozkładowi do prostszych związków o mniejszej masie cząsteczkowej.
Piroliza węgla Przy odgazowaniu 1000 kg (1 tona) węgla otrzymuje się: Gaz koksowniczy 330m3 (20%) o przeciętnym składzie: 50% H2, 34% CH4, 8% CO, 4% olefin, 4% N2, 1% CO2 Koks 650 kg (65%) Smoła węglowa 42 kg (5%) Woda pogazowa (ok. 10%) - zawiera amoniak; Wykorzystywana jest do produkcji soli amonowych stosowanych jako nawozy sztuczne. NH3 + H2SO4 --> (NH4)2SO4
ROPA NAFTOWA - Jest mieszaniną węglowodorów różniących się wielkością i strukturą = parafiny (alkany), cykloparafiny (cykloalkany), olefiny (alkeny), węglowodory aromatyczne. Pozostałość (do ok. 20%) stanowią związki organiczne zawierające tlen, azot, siarkę a także sole nieorganiczne i woda. Parafiny - do 5 atomów węgla (gazy), od 6 do 16 (ciecze), powyżej 17 (ciała stałe). Przerób ropy naftowej-Rafinacja procesy przekształcające ropę naftową w bardziej użyteczne produkty - destylacja frakcyjna, kraking, reforming.
Destylacja frakcyjna oddzielenie ropy na frakcje wg ich temperatur wrzenia (kondensacja wrzącej ropy na odpowiednich półkach - skroplenie).
Frakcja -mieszanina cieczy o podobnych temperaturach wrzenia. Lekkie frakcje mają niskie temp. wrzenia i krótkie łańcuchy węglowodorowe. Frakcje ropy naftowej - Benzyna Ciekła frakcja ropy naftowej powstała po destylacji frakcyjnej. Składa się z alkanów zawierających od 5 do 12 atomów węgla i wrze w przedziale temperatur 40 - 150 stopni. Liczba oktanowa określa odporność benzyny na detonacje (O - 100) i jest podnoszona przez dodatek substancji przeciwstukowych (czteroetyloołów).
Nafta-ciekła frakcja ropy naftowej powstała po destylacji frakcyjnej. Składa się z alkanów zawierających od 9 do 15 atomów węgla i wrze w przedziale temperatur 150 - 250 stopni.
ON-ciekła frakcja ropy naftowej powstała po destylacji frakcyjnej. Składa się z alkanów zawierających od 12 do 25 atomów węgla i ma temperaturę wrzenia wyższą niż 250 stopni. Mazut-olej pozostały po destylacji frakcyjnej. Składa się z węglowodorów zawierających do 40 atomów węgla, wrze powyżej 350 stopni (olej smarowy, parafina, bitumin (asfalt).
Kraking-reakcja rozpadu dłuższych łańcuchów alkanów na krótsze alkany i alkeny. Kraking następuje na skutek działania wysokiej temperatury lub katalizatora.C9H20 --> C7H16 + C2H4nonan (alkan) = heptan (alkan) + eten (alken).
Reforming-proces otrzymywania benzyny z lżejszych frakcji przez rozbicie prostych łańcuchów alkanów i przebudowanie ich w łańcuchy rozgałęzione.
Liczba oktanowa- określa odporność benzyny na detonacje (O - 100) i jest podnoszona przez dodatek substancji przeciwstukowych (czteroetyloołów).
AKUMLUATOR OŁOWIOWY- ogniowo odwracalne akumulujące energię elektryczną Anoda - płyty ołowiowe Katoda - płyty ołowiowe pokryte tlenkiem ołowiu (IV). Elektrolit - wodny roztwór kwasu siarkowego. Pobór prądu-rozładowanie (ogniwo). Podczas rozładowywania wyczerpuje się Pb i PbO2 a stężenie H2SO4 maleje. Ponieważ gęstość zależy od stężenia kwasu, mierząc gęstość można określić stopień rozładowania akumulatora. Anoda(-): Pb = Pb2+ + 2eKatoda(+): PbO2 + 4H+ + 2e = Pb2+ + 2H2O Ładowanie (elektroliza)- W czasie ładowania zwiększa się stężenie H2SO4, tak więc całkowita ilość kwasu w elektrolicie nie ulega zmianie. Naładowany akumulator utrzymuje stałe napięcie ok. 2 V. Anoda(+): Pb2+ + 2e = PbKatoda(-): Pb2+ + 2H2O = PbO2 + 4H+ + 2e
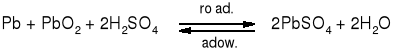
Akumulator ołowiowy-reakcja sumaryczna-
![]()
Wady: duży ciężar, wrażliwość na wstrząsy, konieczność starannej konserwacji (nieużywany akumulator ulega samorozładowaniu). SEM naładowanego akumulatora wynosi 2V, wyładowanego 1.85V.
METALE
Budowa- Sieć regularna przestrzennie centrowana A2, Sieć regularna płaskocentrowana A1,Sieć heksagonalna zwarta A3
Właściwości -Ruchliwość elektronów walencyjnych w metalach warunkuje ich właściwości: połysk, kowalność, ciągliwość, przewodnictwo elektryczne
TEORIA PASKOWA CIAŁ STAŁYCH-Teoria pasmowa dotyczy zasadniczo 2 poziomów energetycznych atomów w ciele stałym: najbardziej zewnętrznego poziomu obsadzonego elektronem i najbliższego mu poziomu wzbudzonego. Poziomy te pod wpływem oddziaływania pól elektrostatycznych pozostałych atomów ulegają rozszczepieniu na dużą liczbę blisko położonych poziomów tworzących pasma energetyczne: walencyjne i przewodnictwa W ramach pasma elektrony poruszają się swobodnie dzięki małym różnicom energii pomiędzy tworzącymi je poziomami. Na każdym poziomie tworzącym pasmo mogą być 2 elektrony.
PÓŁPRZEWODNIKI
Półprzewodnik samoistny - monokryształ półprzewodnika pozbawionego defektów sieci krystalicznej i domieszek, czyli nie zawierający obcych atomów w sieci krystalicznej.
Półprzewodnik typu n - półprzewodnik, w którym elektryczność jest przenoszona przez nadmiar elektronów.
Półprzewodnik typu p - półprzewodnik, w którym elektryczność jest przenoszona przez dziury elektronowe
ALOTROPIA-Polimorfizmem lub alotropią nazywamy występowanie tego samego pierwiastka lub związku w postaci dwóch lub kilku odmian krystalicznych, a odmiany te nazywamy alotropowymi. Przemiany alotropowe zachodzą przy stałych temperaturach i towarzyszy im wydzielanie lub pochłanianie utajonego ciepła przemiany (w zależności od kierunku jej zachodzenia). Odmiany alotropowe nie są różnymi stanami skupienia materii Najbardziej znane pierwiastki tworzące odmiany alotropowe: węgiel występujący w formie diamentu, grafitu, fulerenu fosfor występujący w formie fosforu czerwonego, białego, fioletowego i czarnegosiarka występująca w formie romboidalnej, jednoskośnej i polimerycznej. żelazo o sieci regularnej przestrzennie centrowanej (α i δ) oraz regularnej ściennie centrowanej (γ).
Odmiany węgla - diament: Struktura kubiczna przestrzennie centrowana. Każdy atom węgla otoczony jest 4 sąsiadami, z którymi tworzy wiązania kowalencyjne o tej samej długości tworząc w przestrzeni czworościan foremny (tetraedr);Najtwardszy naturalny minerał, gęstość 3,51 g/cm3;
Izolator, Wiązania o charakterze kowalencyjnym hybrydyzacja sp3
Grafit: Układ płaskich pierścieni heksagonalnych połączonych wiązaniami kowalencyjnymi; W płaszczyźnie hybrydyzacja sp2 stąd są jeszcze niesparowane, swobodne elektrony -materiał jest przewodnikiem elektrycznym; Odległość pomiędzy płaszczyznami ok. 0,3 nm, tj. 2,5 razy więcej niż długość wiązań w pierścieniu węglowym , stąd mała gęstość grafitu 2,25 g/cm3;Pomiędzy płaszczyznami słabe oddziaływanie typu vander Waalsa, stąd kryształ jest typu „soft”
KOROZJA METALI jest to stopniowe niszczenie tworzyw metalowych i niemetalowych pod wpływem chemicznego i elektrochemicznego oddziaływania środowiska w wyniku, którego zmieniają się stan i właściwości niszczonego tworzywa. W przypadku metali możemy rozróżnić korozję chemiczną i elektrochemiczną.
Korozja chemiczna metali następuje w wyniku działania suchych gazów lub cieczy nieprzewodzących prądu elektrycznego. Przykładem korozji chemicznej może być działanie tlenu na metale w podwyższonej temperaturze w rezultacie, którego na powierzchni metalu powstaje warstwa tlenku. Utlenianie metalu do jego tlenków nie zawsze jest procesem szkodliwym. Jeżeli warstwa tlenku jest dostatecznie zwarta i mocno związana z powierzchnią metalu, chroni ona (pasywuje) metal przed dalszym utlenianiem. Glin jak wynika z jego położenia w szeregu napięciowym metali jest metalem nieszlachetnym. Jednak ten metal i jego stopy odznaczają się w środowisku obojętnym dużą odpornością na korozję, wynikającą z utworzenia się pasywnej, trudno rozpuszczalnej warstwy tlenku. Podobne tlenkowe warstewki ochronne tworzy cynk, chrom i nikiel. Do korozji chemicznej zalicza się także czernienie przedmiotów srebrnych na powietrzu. Głównym składnikiem ciemnego nalotu jest siarczek srebra powstający w reakcji srebra ze związkami siarki zawartymi w powietrzu.
Korozja elektrochemiczna jest najbardziej powszechnym rodzajem korozji. Należy do niej powszechnie spotykane zjawisko korozji atmosferycznej, która spowodowana jest działaniem na metale wilgotnego powietrza i zawartych w nim zanieczyszczeń. Korozja metali najczęściej objawia się poprzez powierzchniowe ubytki metalu (plamy i wżery), bądź przez obniżenie wytrzymałości metali. Najczęściej szybkość korozji określa się przez ubytek masy próbki metalu pod wpływem działania czynnika korodującego na jednostkę powierzchni i czasu. Ochrona metali przed korozją: W zależności od rodzaju korozji i charakteru chemicznego czynników korozyjnych istnieje wiele sposobów zapobiegania lub zmniejszania skutków korozji:1. Dobór odpowiedniego materiału do warunków środowiska agresywnego.2. Zastosowanie inhibitorów (opóźniaczy) korozji. Inhibitory tworzą zwykle na powierzchni metalu warstewki ochronne hamujące szybkość korozji. Dla korozji w środowisku alkalicznym jako inhibitory korozji stosowane są sole cyny, arsenu, niklu i magnezu, zaś w środowisku kwaśnym: krochmal, klej lub białko.
3. Ochrona katodowa. Ochrona katodowa polega na połączeniu chronionej konstrukcji z metalem mniej szlachetnym, tworzącym anodę (protektor) ogniwa, natomiast katodą jest obiekt chroniony.4.Powłokiochronne.Powszechnie stosowane powłoki ochronne:- powłoki nieorganiczne: metalowe i niemetalowe
- powłoki organiczne: farby, lakiery, tworzywa sztuczne, smoła i smary. Powłoki metalowe wytwarzane na skalę przemysłową dzielimy na dwie grupy: powłoki anodowe i katodowe. Powłoki anodowe są wykonane z metali o bardziej ujemnym potencjale elektrochemicznym (mniej szlachetnych) niż metal chroniony. Powłoki katodowe są wykonane z metali bardziej szlachetnych niż metal chroniony.- duży ciężar- wrażliwość na wstrząsy
- konieczność starannej konserwacji (nieużywany akumulator ulega samorozładowaniu)SEM naładowanego akumulatora wynosi 2V, wyładowanego 1.85V.
POLIMERY -Związki o budowie łańcuchowej, których cząsteczki zbudowane są z połączonych ze sobą powtarzających się elementów. Najmniejszy powtarzający się element budowy łańcucha polimeru to mer. Cząsteczki polimerów są bardzo długie i mają duże masy cząsteczkowe. Polimery występują w przyrodzie (białka), są też wytwarzane sztucznie.
Typy polimerów - Homopolimer - polimer utworzony z jednego typu monomerów. Kopolimer - polimer utworzony z dwóch lub więcej różnych monomerów.
Otrzymywanie polimerów-Polimery otrzymuje się w reakcji łączenia się ze sobą pojedynczych cząsteczek prostych związków (monomerów) w długie łańcuchy
Reakcje polimeryzacji-Monomery łączą się ze sobą bez powstawania produktów ubocznych. Polimer jest jedynym produktem tej reakcji. Przykłady- polietylen, polichlorek winylu, polistyren, orlon, akrylan, polipropylen, plexiglas, lucie, teflonpoli (tetrafluoroetylen).
Reakcje polikondensacji-Monomery tworząc polimer tracą małe cząsteczki (np. wodę).
Właściwości fizyczne polimerów-Nie mają zdefiniowanej temperatury topnienia (topią się w pewnym zakresie temp.)Polimery o długich łańcuchach mają zwykle dużą lepkość. Wytrzymałość polimerów wzrasta wraz ze wzrostem długości łańcuchów.
Polimery przewodzące-Polimery zdolne do przewodzenia prądu elektrycznego. Są to związki cząsteczkowe niemetali. Właściwości: przewodzą prąd, nie korodują, mają małą gęstość, są elastyczne.(poliacetylen, polianilina).
Budowa polimerów przewodzących-Wszystkie polimery przewodzące mają wspólną cechę: długi łańcuch atomów węgla o hybrydyzacji sp2, często z atomami azotu lub siarki włączonymi w ten łańcuch. Układ sprzężonych wiązań podwójnych - układ wiązań podwójnych oddzielonych wiązaniami pojedynczymi. Układ ten umożliwia przeskakiwanie elektronów.- przewodzą prąd- nie korodują- mają małą gęstość- są elastyczne
SIECIOWANIE POLIMERÓW-proces prowadzący do powstania trójwymiarowej sieci polimerów, na skutek powstawania mostków między ich łańcuchami.(polimer łańcuchowy, polimer usieciowany)
Kauczuki - ogólna nazwa dla nieusieciowanych polimerów o właściwościach elastomerycznych.
Wulkanizacja - Chemiczny proces sieciowania cząsteczek polimeru prowadzący do otrzymania gumy. Polega na ogrzewaniu kauczuku z ok. 3% dodatkiem siarki.
Teoria pasmowa- kwantowo mechaniczna teoria opisująca przewodnictwo elektryczne. W przeciwieństwie do teorii klasycznej punktem wyjścia w tej teorii jest statystyka Fermiego-Diraca i falowa natura elektronów. Najważniejszym pojęciem tej teorii jest pasmo energetyczne - jest to przedział energii, jaką mogą posiadać elektrony w przewodniku. Istnienie ciągłego widma energetycznego jest związane z oddziaływaniem na siebie poszczególnych atomów (jest to zbiór bardzo blisko położonych widm liniowych), natomiast występowanie obszarów zabronionych wynika z warunków nakładanych na periodyczność funkcji falowej elektronów.
Związki z przewagą wiąz. jonowego:[krystaliczne ciała stałe zbud. z jonów] -stan stały, zbudowane z kationów i anionów przyciągających się z dużą siłą ; -kryształy są twarde i mają wysokie temp. iopnienia i wrzenia , -dobrze rozpuszcz. się w rozp. Polarnych [woda] , -stopione lub w roztworze przewodzą prąd , -reakcje zachodzą b. szybko. Cechy zw. z przewag. wiąz. kowalencyjnego [atomowego]:[ gazy, cieczy, ciała stałe zbud. z cząsteczek] -nie przewodzą prądu , -słabo rozpuszcz. się w rozp. polarnych , -niskie temp. wrzenia i topnienia , -cząsteczki słabo na siebie oddziałują , -reagują wolno.
Wiązanie metaliczne - ogólna nazwa dla wszelkich wiązań chemicznych występujących bezpośrednio między atomami metali. Wiązania między atomami metalu, jeśli występują w izolowanej formie (np. w związkach metaloorganicznych) są w zasadzie typowymi wiązaniami kowalencyjnymi, wyróżniają się jednak w stosunku do analogicznych wiązań między niemetalami dwiema istotnymi cechami: *ulegają one łatwiejszej polaryzacji pod wpływem np. pola elektrycznego ze względu na to, że ogólnie w metalach elektrony walencyjne są słabiej związane z jądrami atomów niż w niemetalach ; *nawet jeśli formalnie są wiązaniami pojedynczymi, ze względu na występowanie w metalach dużej liczby walencyjnych orbitali d zachodzi zjawisko ich nakładania się, co powoduje że wiązania te nabierają często charakteru częściowo wielokrotnego.
Piroliza-[destylacja rozkładowa] to proces rozkładu termicznego substancji prowadzony poprzez poddawanie ich działaniu wysokiej temperatury , ale bez kontaktu z tlenem i innymi czynnikami utleniającymi. Ropa naftowa-jest mieszaniną węglowodorów różniących się wielkością i strukturą = parafiny (alkany),cykloparafiny (cykloalkany),olefiny (alkeny),węglowodory aromatyczne. Pozostałość [do 20%] to związki organiczne z tlenem, azotem, siarką , a także sole nieorg. I woda.
Rafinacja-procesy przekształcające ropę naftową w bardziej użyteczne produkty - destylacja frakcyjna, kraking, reforming.
Destylacja frakcyjna -rozdzielenie ropy na frakcje według ich temp. wrzenia.
Frakcja-mieszanina cieczy o podobnych temp. wrzenia. Lekkie frakcje mają niskie temp. wrzenia i krótkie łańcuchy węglowodorowe.
Kraking-reakcja rozpadu dłuższych łańcuchów alkanów na krótsze alkany i alkeny. Kraking następuje na skutek wysokiej temp. lub katalizatora.
Reforming-proces otrzymywania benzyny z lżejszych frakcji przez rozbicie prostych łańcuchów alkanów i przebudowanie ich w łańcuchy rozgałęzione.
Benzyna-ciekła frakcja ropy naftowej powstała po destylacji frakcyjnej. Składa się z alkanów mających od 5 do 12 at. Węgla i wrze w 40-150*C.Frakcje ropy:1)Nafta-ciekła frakcja ropy naft. Powstała po destylacji frakcyjnej. Skład: alkany od 9 do 15 at. Węgla , wrze: 150-250*. 2)ON-ciekł. frak. Ropy naft. powst. po dest. frakc. Alkany od 12-25 at. węgla , wrze >250*. 3)Mazut-olej pozostały po dest. frakc.. Węglowodory do 40 at. węgla , wrze >350* (bitumin, parafina, olej smarowy).
Izotopy-odmiany pierwiastka chemicznego różniące się liczbą neutronów w jądrze atomu (z definicji atomy tego samego pierwiastka mają tę samą liczbę protonów w jądrze). Izotopy tego samego pierwiastka różnią się liczbą masową (łączną liczbą neutronów i protonów w jądrze), ale mają tę samą liczbę atomową (liczbę protonów w jądrze). Dzielą się na trwałe (nie ulegają samorzutnej przemianie na izotopy tego samego lub innych pierwiastków), * nietrwałe, zwane izotopami promieniotwórczymi (ulegają samorzutnej przemianie na inne izotopy, zazwyczaj innego pierwiastka).Wodór: * prot: 1H - ma jeden proton i nie ma neutronów; trwały, * deuter: 2H (D) - ma jeden proton i jeden neutron; trwały, * tryt: 3H (T) - ma jeden proton i dwa neutrony; nietrwały.
Typy centrowania komórek elementarnych -*P(komórka elementarna prymitywna, tzn. mająca węzły tylko w narożach);*S(oznaczane też C, B, lub A, z komórką elementarną mającą dodatkowe węzły na jednej z par ścian równoległych);*I(tzw. przestrzennie, inaczej wewnętrznie centrowane);*F(tzw. płasko, czyli ściennie centrowane).
Odmiany alotropowe węgla: *diament- jest najtwardszy ze znanych minerałów; ^półprzezroczyste ciało stałe; jest bezbarwny lub żółty, błękitny, niebieski, brunatny do czarnego; gęstość wynosi 3,5 g/cm3;^ma właściwości półprzewodnikowe; jest dobrym przewodnikiem ciepła; jest trudno topliwy i odporny na działanie kwasów i zasad; spala się w wysokiej temperaturze.
Stężenia: Stężenie procentowe to udział związków chemicznych w mieszaninach i roztworach wyrażony w procentach.
Stężenie molowe roztworów związków chemicznych to liczba moli danego związku jaką zawiera 1 dm3 danego roztworu.
Stężenie masowe (stężenie masowo-objętościowe) stosunek masy wybranego związku chemicznego do objętości roztworu lub mieszaniny.
Wiązanie wodorowe i van der Waalsa:1) -dwie cząsteczki/ jony połączone są wiązaniem wodorowym; -szczególne znaczenie ma wiązanie H-O-H;- utrzymuje strukturę białek i kwasów nukleinowych.2) -występuje miedzy wszystkimi cząsteczkami; -odpowiada za właściwości fizyczne substancji.
Komórka elementarna i sieć przestrzenna:1) jest to najmniejsza jednostka, z której można zbudować kryształ, poprzez powielanie jej w 3 prostopadłych kierunkach.2) sposób wypełnienia atomami przestrzeni tak, że pewna konfiguracja atomów zwana komórką elementarną jest wielokrotnie powtarzana [ukł.regularny,tetragonalny itd.].
Alotropia-występowanie tego samego pierwiastka chemicznego w 2 lub kilku formach krystalicznych lub cząsteczkowych, zwanych odmianami alotropowymi. Każda z tych odmian jest trwała w pewnym zakresie temperatury i ciśnienia. Zmiana tych warunków może spowodować przemiany alotropowe.
Orbital jest funkcją falową jednego elektronu, której kwadrat modułu (zgodnie z interpretacją Maxa Borna) określa gęstość prawdopodobieństwa napotkania elektronu w danym punkcie przestrzeni.
Węglowodory to org. zw. chem. zawierające tylko atomy węgla i wodoru. Wszystkie składają się z podstawowego szkieletu węglowego i przyłączonych do tego szkieletu atomów wodoru.Są podstawowym składnikiem ropy naftowej, która stanowi ich podstawowe źródło w przemyśle. Inne źródła= sucha destylacja drewna i zgazowywanie węgla [alkany itp.].
Prawo Henry'ego - zależność rozpuszczalności gazu w cieczy od ciśnienia [Mgaz=Kciecz x Pciś. Gaz].Elektroujemność-miara tendencji do przyciągania elektronów przez atomy danego pierwiastka.
Wyszukiwarka
Podobne podstrony:
Chemia materiałów, Polibuda MBM PWR 2012-2016, Sem. I, Chemia
sciaga cad, Polibuda MBM PWR 2012-2016, Sem. V, MES, koło
PKM - sciaga, Polibuda MBM PWR 2012-2016, Sem. V, PKM I, wyklad siara
sciaga cad, Polibuda MBM PWR 2012-2016, Sem. V, MES, koło
MES, Polibuda MBM PWR 2012-2016, Sem. V, MES, koło
TEST OGÓLNY BHP rozwiązania, Polibuda MBM PWR 2012-2016, Sem. III, Ergonomia i BHP
MÓJ, Polibuda MBM PWR 2012-2016, Sem. V, MES, koło
ćwiczenie nr 1, Polibuda MBM PWR 2012-2016, Sem. VI, Hydrostatyczne ukł. nap, Laborki
ver.5 rozkad urzadzenia i systemy wytw. cnc, Polibuda MBM PWR 2012-2016, Sem. VII, CNC i roboty, Wyk
Lab. 7 - wnioski, Polibuda MBM PWR 2012-2016, Sem. V, PKM I, Lab
Ci¦ůgnienie to proces technologiczny obr+-bki plastycznej, Polibuda MBM PWR 2012-2016, Sem. V, Przer
gotowe sciagi, Polibuda MBM PWR 2012-2016, Sem. VI, Podst.elsploatacji i remontów, MM
ZGRZEWANIE, Polibuda MBM PWR 2012-2016, Sem. VI, Tworzywa sztuczne, lab
ergonomia-1, Polibuda MBM PWR 2012-2016, Sem. III, Ergonomia i BHP
przekładnia zębata BYNEK, Polibuda MBM PWR 2012-2016, Sem. VI, PKM II
pkm, Polibuda MBM PWR 2012-2016, Sem. V, PKM I, wyklad siara
wojny, Polibuda MBM PWR 2012-2016, Sem. VII, Wojny
więcej podobnych podstron