Sprawozdanie z ćwiczenia nr 2
z reaktorów chemicznych.
BADANIE PRZEBIEGU PROCESU TECHNOLOGICZNEGO W PRZEPŁYWOWYM REAKTORZE ZBIORNIKOWYM
Opracowali:
Justyna Iwińska
Iza Kaźmierczak
Roman Jędrzejewski
Krzysztof Juszczyk
WSTĘP:
Reakcja zmydlania octanu etylu przebiega według równania
![]()
W reaktorze przepływowym z idealnym mieszaniem stężanie mieszaniny reakcyjnej i jej temperatura są takie same w całej objętości. Jeżeli reaktor pracuje w stanie ustalonym (co ma miejsce poza okresem rozruchu i wyłączania), to akumulacja równa jest zeru:
![]()
gdzie:
qio - przepływ mieszaniny reakcyjnej na wlocie do reaktora [dm3/h]
qik - przepływ mieszaniny reakcyjnej na wylocie z reaktora [dm3/h]
Cio - stężenie składnika i na wlocie do reaktora [mol/dm3]
Cik - stężenie składnika i na wylocie z reaktora [mol/dm3]
νi - współczynnik stechiometryczny składnika i
Vr - objętość reaktora [dm3]
r - równoważnikowa szybkość reakcji [mol · dm-3 · h-1]
τ - czas [h]
Surowce, których różne prędkości przepływu regulowano za pomocą pompy perystaltycznej, doprowadzono do reaktora o objętości 300 ml zaopatrzonego w mieszadło magnetyczne.Po dokładnym wymieszaniu się 0,1n roztworu woorotlenku sodu i 0,1n roztworu octanu etylu w stosunku 1:1 dokonano pomiaru wskazania konduktometru, na podstawie którego obliczono stężenie na wylocie, natomiast na podstawie pomiarów przepływu obliczono stężenie na wlocie strumieni do reaktora. Przewodnictwo mieszaniny reakcyjnej po całkowitym przereagowaniu χ∞ zmierzone zostało poza reaktorem po upływie 20 minut.
Pomiar przewodnictwa na wlocie i wylocie z reaktora oraz po całkowitym przereagowaniu przeprowadzono dla przypadków:
1. CH3COOC2H5 : NaOH = 1:1
2. CH3COOC2H5 : NaOH = 2:1
3. CH3COOC2H5 : NaOH = 3:1
4. CH3COOC2H5 : NaOH = 4:1
Każdy pomiar powtórzono trzykrotnie, a wyniki zapisano w tabelce:
qOE : qNaOH |
C0NaOH [dm3/h] |
C0OE v [dm3/h] |
Przewodnictwo [S/m] |
||||
|
|
|
χ 0 |
χ t |
χ∞ |
||
1:1 |
1 |
0,05 |
0,05 |
1.76 |
0.86 |
0,56 |
|
|
2 |
0,05 |
0,05 |
1.42 |
0,82 |
0,5 |
|
|
3 |
0,05 |
0,05 |
1.26 |
0,79 |
0,56 |
|
|
średnia |
1,48 |
0,8233 |
0,5566 |
|||
1:2 |
1 |
0,033 |
0,067 |
1 |
0,55 |
0,32 |
|
|
2 |
0,033 |
0,067 |
0,99 |
0,55 |
0,32 |
|
|
3 |
0,033 |
0,067 |
0,98 |
0,54 |
0,32 |
|
|
średnia |
0,99 |
0,5466 |
0,32 |
|||
1:3 |
1 |
0,025 |
0,075 |
0,72 |
0,4 |
0,24 |
|
|
2 |
0,025 |
0,075 |
0,70 |
0,39 |
0,24 |
|
|
3 |
0,025 |
0,075 |
0,69 |
0,39 |
0,24 |
|
|
średnia |
0,7033 |
0,3933 |
0,24 |
|||
1:4 |
1 |
0,02 |
0,08 |
0,60 |
0,31 |
0,2 |
|
|
2 |
0,02 |
0,08 |
0,54 |
0,30 |
0,2 |
|
|
3 |
0,02 |
0,08 |
0,56 |
0,30 |
0,2 |
|
|
średnia |
0,5666 |
0,3033 |
0,2 |
|||
Vr= 300ml = 0,3dm3
CNaOH = 0,1n
COE = 0,1n
q = 10ml/min = ![]()
[dm3/s] = 1.66*10-4 [dm3/s]
1.Przepływy
|
qNaOH [dm3/s] |
qOE [dm3/s] |
1:1 |
1,66 · 10-4 |
1,66 · 10-4 |
1:2 |
1,66 · 10-4 |
3,32 · 10-4 |
1:3 |
1,66 · 10-4 |
4,98 · 10-4 |
1:4 |
1,66 · 10-4 |
6,64 · 10-4 |
2. Stężenie na wylocie z reaktora [mol/ dm3]
![]()
![]()
= 0,05 · [(0,8233-1,48)/(0,5566-1,48)] = 0,05 · [(-0,6567)/(-0,9234)]=
= 0.0355[mol/ dm3]
![]()
= 0,033 · [(0,5466-0,99)/(0,32-0,99)] = 0,033 · [(-0,4434)/(-0,67)]=
= 0.02183 [mol/ dm3]
![]()
= 0,025 · [(0,3933-0,7033)/(0,24-0,7033)] = 0,025 · [(-0,31)/(-0,4633)]=
= 0.01672 [mol/ dm3]
![]()
= 0,02 · [(0,3033-0,5666)/(0,2-0,5666)] = 0,02 · [(-0,2633)/(-0,3666)]=
= 0.01436 [mol/ dm3]
![]()
Ci = 0,05 - 0.0355 = 0,0145 [mol/ dm3]
Ci = 0,067 - 0.02183 = 0,04517 [mol/ dm3]
Ci = 0,075 - 0.01672 = 0,05828 [mol/ dm3]
Ci = 0,08 - 0.01436 = 0,06564 [mol/ dm3]
3. Stopień przemiany octanu etylu.
![]()
![]()
= (0,05 - 0,0145)/0,05 = 0.71
![]()
= (0,067 - 0,04517)/0,067 = 0.32582
![]()
= (0,075 - 0,05828)/0,075 = 0.2229
![]()
= (0,08 - 0,06564)/0,08 = 0.1795
4. Szybkość reakcji dla każdego stopnia przemiany.
![]()
[mol/dm3s]
gdzie ![]()
r = (0,05 · 3,32 · 10-4 · 0.71)/0,3 = 3,9286*10-5 [mol/dm3s]
r = (0,067 · 4,98 · 10-4 · 0,32582)/0,3 = 3,62377*10-5 [mol/dm3s]
r = (0,075 · 6,64 · 10-4 · 0,2229)/0,3 = 3,7*10-5[mol/dm3s]
r = (0,08 · 8,3 · 10-4 · 0,1795)/0,3 = 3,9729*10-5[mol/dm3s]
Wykresy:
Lp. |
r |
α |
1. |
3,9286*10-5 |
0,71 |
2. |
3,62377*10-5 |
0,32582 |
3. |
3,7*10-5 |
0,2229 |
4. |
3,9729*10-5 |
0,1795 |
r= f (α)
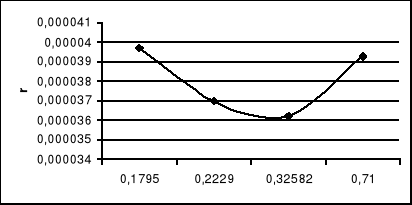
Wnioski:
Wraz ze wzrostem stopnia przemiany octanu etylu równoważnikowa szybkość reakcji początkowo maleje a następnie wzrasta. (zakładając, że pomiary są obarczone dużym błędem, ponieważ wystąpiły zakłócenia procesu reakcji można przyjąć, że równoważnikowa szybkość reakcji wrasta ze wzrostem stopnia przemiany).
Lp. |
qOE/ qNaOH |
r |
1. |
1 |
0,000039286 |
2. |
2 |
0,000036238 |
3. |
3 |
0,000037 |
4. |
4 |
0,000039729 |
r = ƒ ( qOE / qNaOH )
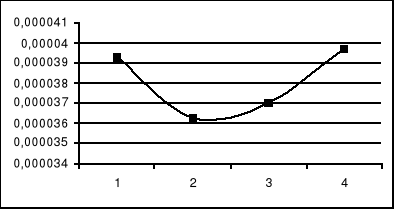
Wnioski:
Wraz ze wzrostem stosunku przepływu OE do przepływu NaOH równoważnikowa szybkość reakcji maleje, a następnie wzrasta. (zakładając, że podczas pomiarów wystąpiły zakłócenia, można przyjąć, że ze wzrostem stosunku przepływu OE do przepływu NaOH maleje równoważnikowa szybkość reakcji).
Wyszukiwarka
Podobne podstrony:
reaktor 3, Studia, Politechnika
reaktory, Studia, Politechnika
Prawo inżynierskie i ochrona własności intelektualnych. Wykład 3, Studia, Politechnika Łódzka - Pend
Testy biodegradacji, Studia, Politechnika
Chf9, Studia, Politechnika
Wyznaczanie stałej reakcji szybkości zmydlania estru, Studia, Politechnika
CH.F.L9, Studia, Politechnika
ZAKAAD CHEMI FIZYCZNEJ, Studia, Politechnika
C15, Studia, Politechnika
podstawowe informacje o ochronie prawnej wzorów przemysłowych, Studia - Politechnika Śląska, Zarządz
Sprawko spawalnictwo 1, studia, studia Politechnika Poznańska - BMiZ - Mechatronika, 2 semestr, obro
dziadek25, Studia, Politechnika
4 2 vademecum echosondy (w tym przykładzie wodnej), studia, studia Politechnika Poznańska - BMiZ - M
LABORKA7, Studia, Politechnika
Wyznaczanie stopnia asocjacji kwasu octowego w rozpuszczalni, Studia, Politechnika
deacon1, Studia, Politechnika
Destylacja wojtek, Studia Politechnika Poznańska, Semestr I, Chemia, Chemia laboratoria, Destylacja
więcej podobnych podstron