Zespół 6 Grupa 34 |
Sprawozdanie 4 |
Data: 16.11.2000 |
Smuła Joanna Makara Joanna Piotr Nylecki |
Równowagi w roztworach buforowych |
|
Wstęp teoretyczny.
Roztworami buforowymi nazywa się roztwory słabego kwasu i jego soli z mocną zasadą oraz słabej zasady i jego soli z mocnym kwasem, wykazujące stałe stężenie jonów wodorowych, które praktycznie nie ulega zmianie podczas rozcieńczania lub po dodaniu niewielkich ilości mocnych kwasów lub zasad (mniejszych od ilości stechiometrycznych w stosunku do składników buforu). Roztworami mogą być również roztwory soli kwasów wieloprotonowych (K2HPO4, Na2HPO4). Według teorii protonowej, roztwory buforowe są to układy zawierające sprzężoną parę kwas - zasada, których stężenie analityczne są wystarczająco duże i mogą być zmieniane niezależnie od siebie.
Roztwory buforowe zachowują podczas rozcieńczania stałe pH, ponieważ zależy ono od stosunku stężeń składników roztworu buforowego, a nie od ich względnych stężeń. Wzory do obliczania pH buforów są następujące:
pH buforu octanowego i fosforanowego wg wzoru
pH= pKHA + lg ![]()
pH buforu amonowego wg wzoru
pH = 14 - pKB +lg![]()
W obu wzorach występuje stężenie zasady (cA-,cB) do stężenia kwasu (cHA,cBH+).
Roztwory buforowe wykazują działanie obustronne, tj. zabezpieczają przed zmianą pH zarówno na skutek dodania mocnych kwasów, jak i zasad. Podczas dodawania mocnego kwasu lub mocnej zasady pH roztworu buforowego powstaje słaby kwas lub słaba zasada. Jeżeli np. do buforu octanowego dodać kwasu solnego, to jony octanowe wiążą jony wodorowe na słabo zdysocjowany kwas octowy
CH3COO- + HCl ⇒CH3COOH + Cl-
Podczas dodawania wodorotleneku sodu reaguje kwas octowy i powstaje słaba zasada (jon octanowe)
CH3COOH + NaOH ⇒ CH3COO- + H2O + Na+
Zdolność przeciwstawiania się wpływom zmieniającym pH charakteryzuje
pojemność buforowa.
Przyjmijmy, że zmiana stężenia mocnej zasady w roztworze dcz powoduje zmianę pH o wartość dpH. Wyrażenie, które określa związek między ilością wprowadzonej zasady i zmianą pH nazywa się pojemnością buforową roztworu
![]()
Zgodnie z podaną definicją β jest zawsze dodatnia, gdyż jeśli dcz > 0, to do dpH>0 (ze wzrostem stężenia zasady pH wzrasta). Jeżeli do roztworu wprowadzi się kwas, to stężenie zasady zmaleje, a więc dcz<0, pH również zmaleje, więc dpH<0 i β>0.
Pojemność buforową wyrażało się dotąd w gramorównoważnikach na litr. Roztwór ma pojemność buforową równą 1, jeżeli po dodaniu 1l roztworu gramorównoważnika zasady lub kwasu zmieni pH o1.
Cel ćwiczenia.
Badanie pH roztworów buforowych oraz ich pojemności buforowej.
Wyniki pomiarów.
Sporządzono 10 roztworów buforowych przez zmieszanie w różnych stosunkach objętościowych 0,2 m. CH3COOH i CH3COONa
W tabeli zestawiono wyniki pomiarów pH r-r buforowych .
Lp |
CH3COOH : CH3COONa |
pH (zmierzone) |
1 |
18,5 : 1,5 |
3,34 |
2 |
|
3,76 |
3 |
17,6 : 2,4 |
3,80 |
4 |
|
3,95 |
5 |
16,4 : 3,6 |
3,82 |
6 |
|
4,09 |
7 |
14,7 : 5,3 |
4,20 |
8 |
|
4,25 |
9 |
12,6 : 7,4 |
4,32 |
10 |
10,2 : 9,8 |
4,61 |
Do trzech wybranych próbek dodajemy 0,2 ml 0,1 m HCL i mierzymy pH , pomiar wykonujemy ponownie po dodaniu do próbek 0,2 ml 1m HCL.
Numer buforu |
pH buforu |
pH ( Po dodaniu 0,2 ml 0,1m HCL ) |
pH ( Po dodaniu 0,2 ml 1m HCL ) |
2 |
3,76 |
3,38 |
3,00 |
4 |
3,95 |
3,55 |
3,10 |
6 |
4,09 |
3,79 |
3,20 |
Mierzymy pH wody destylowanej.
Do dwóch próbek z wodą destylowaną dodajemy kolejno 0,2 ml 0,1m HCL,
oraz 0,2 ml 0,1m HCL
pH wody dest. |
pH ( Po dodaniu 0,2 ml 0,1m HCL ) |
pH ( Po dodaniu 0,2 ml 1m HCL ) |
5,00 |
3,47 |
2,88 |
3.1 Wyznaczenie stałej dysocjacji K kwasu CH3COOH
dla roztworów buforowych na podstawie wykresu pH = f (lgx), x = Cs/Ckw = VH/Vs gdzie Cs,Vs - stężenie, objętość CH3COONa
Ckw,Vkw - stężenie,objętość CH3COOH
Lp |
pH |
lgx |
1 |
3,34 |
1,091 |
2 |
3,76 |
|
3 |
3,80 |
0,8653 |
4 |
3,95 |
|
5 |
3,82 |
0,6585 |
6 |
4,09 |
|
7 |
4,20 |
0,4430 |
8 |
4,25 |
|
9 |
4,32 |
0,2311 |
10 |
4,61 |
0,0174 |
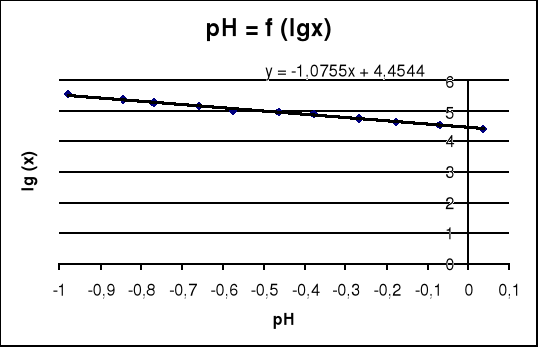
Wartość odciętej dla lgx = 0 daje wartość stałej K = 10 -4,4544
3.2 pH roztworu H2O z HCl
Dla wody destylowanej :
pH= 5,00 ; pH (po dodaniu kwasu 0.1M) = 3.47 - wartość zmierzona
(po dodaniu kwasu 1M ) = 2,88 - wartość zmierzona
Obliczenie teoretycznego pH roztworów buforowych po dodaniu HCl
![]()
![]()
Lp. |
pH(dośw.) |
pH(teor.) |
1 |
3,34 |
|
2 |
3,76 |
|
3 |
3,80 |
|
4 |
3,95 |
|
5 |
3,82 |
|
6 |
4,09 |
|
7 |
4,20 |
|
8 |
4,25 |
|
9 |
4,32 |
|
10 |
4,61 |
|
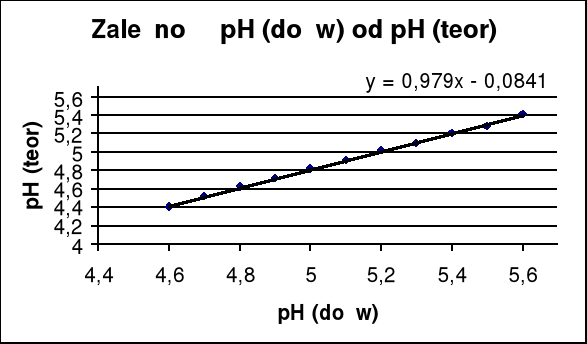
Wykres zależności pH teoretycznego od pH doświadczlnego.
3.4 Obliczenie ΔpHteor(zmiana pH buforu po dodaniu HCl)
![]()
![]()
Lp. |
ΔpHdośw |
ΔpHteor |
-lgx |
1 |
0,19 |
-0,0087 |
|
2 |
0,15 |
-0,00873 |
|
3 |
0,15 |
-0,0090 |
|
4 |
0,15 |
-0,0095 |
|
5 |
0,13 |
-0,010 |
|
6 |
0,14 |
-0,011 |
|
7 |
0,2 |
-0,0129 |
|
8 |
0,13 |
-0,0156 |
|
9 |
0,13 |
-0,0172 |
|
10 |
0,13 |
-0,0195 |
|
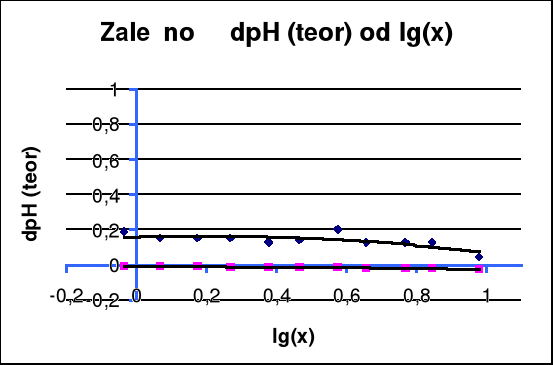
Wykres zależności ΔpH od -lgx.
3.5 Dla stosunku Cs/Cz = uzyskano minimalną (ΔpHmin) wartość pH.
Obliczenie pojemności buforowej β.
β=ΔCHCl / ΔpH
gdzie : ΔCHCl - stężenie HCl po dodaniu do roztworu buforowego
ΔpH - zmiana pH
Lp |
pH |
β |
1 |
4,41 |
0,0165 |
2 |
4,96 |
0,0495 |
3 |
5,54 |
0,0198 |
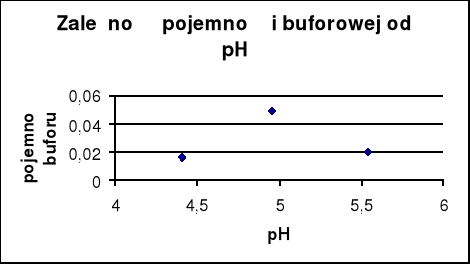
Wykres zależności pojemności buforowej β od pH.
Wartości pH dla buforów wzorcowych
Wartości początkowe: pH = 2,00 i pH = 7,00
Wartości końcowe: pH = 2,10 i pH = 7,11
Wnioski.
Pomimo wprowadzenia do roztworów buforowych niewielkiej ilości mocnego kwasu nie nastąpiły wyraźne zmiany wartości pH,co jest własnością charakterystyczną roztworów buforowych.Analizując wykonane pomiary można zauważyć,że wartość pH sporządzonych roztworów buforowych nieznacznie maleje na skutek dodania mocnego kwasu, ale jest stała pomimo rozcieńczania.W przypadku wody destylowanej dodanie mocnego kwasu powoduje wyraźną zmianę pH o kilka jednostek.Czysta woda destylowana (bez dodatku kwasu) ma pH =5, co odbiega od wartości teoretycznej (pH=7).Przypuszczamy,że spowodowane jest to zakwaszeniem w pewnym stopniu wody destylowanej dwutlenkiem węgla zawartym w powietrzu.
Wyszukiwarka
Podobne podstrony:
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
więcej podobnych podstron