Cel ćwiczenia.
Celem ćwiczenia było oznaczenie lepkościowo średniej masy cząsteczkowej hydroksypropylometylocelulozy (HPMC).
Wykonanie ćwiczenia.
Wykorzystując gotowy roztwór 2% HPMC sporządzono 20 gram roztworu o stężeniu 0,1 % HPMC poprzez rozcieńczenie z wodą.
W pierwszej części ćwiczenia za pomocą wiskozymetru Ubelohde'a zmierzono lepkość 2% roztworu HPMC dla następujących temperatur: 310C, 360C, 410C, 470C.
W drugiej części ćwiczenia również w wiskozymetrze Ubelohde'a umieszczono 10 ml wodnego roztworu HPMC o stężeniu 0,1%. Wykonano pomiar lepkościowy w temperaturze pokojowej, mierząc czas wypływu roztworu z kapilary. Następne pomiary lepkości wykonano rozcieńczając próbkę w wiskozymetrze przez dodawanie po 5 ml wody po każdym pomiarze.
Na końcu zmierzono czas wypływu czystej wody z kapilary.
Wyniki pomiarów.
Czas wypływu 2,0% roztworu HPMC w różnych temperaturach:
Czas wypływu 0,1% roztworu HPMC i jego kolejnych rozcieńczeń:
Obliczenia.
Sporządzenie wykresu η=f(T)
Sporządzenie wykresu ηzred=f(c)
Obliczenie ze wzoru Marka-Houwinka lepkościowo średniej masy cząsteczkowej:
Wnioski.
Lp. |
temp oC |
t[ min] |
t [s] |
1 |
31 |
21,35 |
1281 |
2 |
36 |
20,38 |
1222,8 |
3 |
41 |
18,51 |
1110,6 |
4 |
47 |
18,2 |
1092 |
Obliczając średni czas wypływu roztworu z kapilary odrzucono błędne, nie powtarzające się pomiary.
Lp. |
Rozcieńczenie r-ru |
t 1 [min] |
t2 [min] |
t3 [min] |
t średni [min] |
t średni [s] |
1 |
10 ml 0,1% HPMC |
9,32 |
- |
- |
9,32 |
559,2 |
2 |
plus 5 ml wody |
4,2 |
4,22 |
- |
4,21 |
252,6 |
3 |
plus 5 ml wody |
2,57 |
3,04 |
2,56 |
2,565 |
153,9 |
4 |
plus 5 ml wody |
2,22 |
2,24 |
2,21 |
2,215 |
132,9 |
5 |
plus 5 ml wody |
2,11 |
2,06 |
2,05 |
2,055 |
123,3 |
6 |
plus 5 ml wody |
1,56 |
1,55 |
- |
1,555 |
93,3 |
7 |
plus 5 ml wody |
1,39 |
1,38 |
- |
1,385 |
83,1 |
8 |
czysta woda |
0,4 |
0,4 |
0,4 |
0,4 |
40 |
Nr |
Temp. [oC] |
η [Pa∙s] |
1 |
31 |
1665,3 |
2 |
36 |
1589,64 |
3 |
41 |
1443,78 |
4 |
47 |
1419,6 |
![]()
η - lepkość [kg/(m∙s)]=[Pa∙s]
k - współczynnik wiskozymetru [m2/s2]
ρ - gęstość [kg/m3]
t - czas wypływu [s]
k = 1,3 [m2/s2]
ρ = 1 [kg/m3]
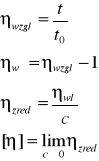
Nr |
c [g/100cm3] |
t [s] |
ηwzgl |
ηwł |
ηzred |
1 |
0,1 |
559,2 |
13,98 |
12,98 |
129,8 |
2 |
0,067 |
252,6 |
6,315 |
5,315 |
79,32836 |
3 |
0,05 |
153,9 |
3,8475 |
2,8475 |
56,95 |
4 |
0,04 |
132,9 |
3,3225 |
2,3225 |
58,0625 |
5 |
0,033 |
123,3 |
3,0825 |
2,0825 |
63,10606 |
6 |
0,029 |
93,3 |
2,3325 |
1,3325 |
45,94828 |
7 |
0,025 |
83,1 |
2,0775 |
1,0775 |
43,1 |
Wykres po odrzuceniu, błędnych pomiarów:
Równanie linii trendu:
y= 544,07+29,805
Wartość y (graniczna liczba lepkościowa):
gdy x=0 to y= 29,805
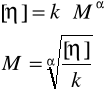
Masa cząsteczkowa M=5924,0 g/mol
Wyznaczona lepkościowo średnia masa cząsteczkowa wodnego roztworu HPMC wynosi M=5924,0[g/mol].
Można zauważyć, że lepkość maleje wraz ze wzrostem temperatury, rośnie natomiast wraz ze wzrostem stężenia roztworu.
ηwzgl - lepkość względna
ηwł - lepkość właściwa
ηzred - lepkość zredukowana
[η] - graniczna liczba lepkościowa (GLL)
[η] - graniczna liczba lepkościowa GLL odczytana z wykresu:
GLL = 29,805
k = 3,71![]()
10-2 [g/100cm3]
α = 0,77
Wyszukiwarka
Podobne podstrony:
INŻYNIERIA REAKTORÓW CHEMICZNYCH (2 termin - zadania) - 9.03.2012, PK - technologia chem, Rok V, Rea
ZADANIE A7(5), Radzion Dorota , technologia chemiczna , rok III , grupa III
13. Miareczkowanie amperometryczne, Technologia Chemiczna, Rok III, Semestr II, Instrumentalne metod
Zakres materiału, Technologia Chemiczna, Rok I, Fizyka, Wykłady fizyka
ZADANIE A7(3), Radzion Dorota , technologia chemiczna , rok III , grupa III
ZADANIE A7(3), Radzion Dorota , technologia chemiczna , rok III , grupa III
ZADANIE A7(10), Radzion Dorota , technologia chemiczna , rok III , grupa III
ZAKRES MATERIAŁU PIM, Technologia Chemiczna, Rok III, Semestr I, Podstawy inżynierii materiałów, Sem
ZADANIE A7(7), Radzion Dorota , technologia chemiczna , rok III , grupa III
Regulamin i terminy laboratorium 2014, Technologia Chemiczna, Rok II, Semestr II, Nauka o Materiałac
ZADANIE A7(6), Radzion Dorota , technologia chemiczna , rok III , grupa III
zagadnienia lab fiz, WIiTCh PK, Technologia Chemiczna, semestr 3, Chemia Fizyczna, laboratorium
Cwiczenie 123g, Technologia Chemiczna, Rok I, Fizyka, Fizyka - laboratoria, 123 - Dioda półprzewodni
Chemia Krzemianów-ściąga egzamin, Technologia Chemiczna, Rok II, Semestr II, Chemia Krzemianów, Egza
03. Roztwarzanie materiałów w kwasach i przez stapianie, Technologia Chemiczna, Rok III, Semestr II,
Zadanie z fizycznej, Technologia chemiczna, rok II
ZADANIE A7(13), Radzion Dorota , technologia chemiczna , rok III , grupa III
04. Metody rozdzielania, Technologia Chemiczna, Rok III, Semestr II, Instrumentalne metody analizy,
ZADANIE A7(12), Radzion Dorota , technologia chemiczna , rok III , grupa III
więcej podobnych podstron