Grupa: 23 Zespół:9 |
Ćwiczenie: 9 |
Data: 07.03.2000 |
Więcaszek Towek Lugowska Barbara Sypula Marcin
|
Temat: Ebulioskopia. |
Ocena: |
I. Część teoretyczna.
Prężność pary P nad mieszaniną cieczy o całkowitej wzajemnej rozpuszczalności w przypadku doskonałego zachowania się tych cieczy w roztworze równa jest sumie prężności par poszczególnych składników.
gdzie:
P - ciśnienie całkowite;
PA - ciśnienie składnika A;
PB - ciśnienie składnika B.
Prężność pary nad roztworem jest proporcjonalna do ułamka molowego składnika. Współczynnikiem proporcjonalności jest prężność pary nad czystym składnikiem.
gdzie:
P - prężność pary nad roztworem;
X0 - ułamek molowy składnika;
P0 - prężność pary nad czystym składnikiem
W związku z obniżeniem prężności pary nad roztworem podwyższa się temperatura wrzenia cieczy.
P
Pc
T0 Tr
Podwyższenie temperatury wrzenia roztworu jest wprost proporcjonalne do stężenia molarnego substancji rozpuszczonej.
gdzie:
Twrz - zmiana temperatury wrzenia
KE - stała ebulioskopowa
m - molalność roztworu
ms - masa substancji rozpuszczonej
mr - masa rozpuszczalnika
n - liczba moli substancji
Stała ebulioskopowa ma wymiar temperatury i oznacza przyrost temperatury wrzenia roztworu w stosunku do temperatury wrzenia rozpuszczalnika zawierającego jeden mol substancji w tysiącu gramach rozpuszczalnika.
Przyrządy służące do dokładnego oznaczania temperatury wrzenia cieczy nazywamy ebuliometrami np: ebuliometr Świętosławskiego.
Rys. Schemat ebuliometru Świętosławskiego
II. Część obliczeniowa.
Wyznaczanie masy molowej doświadczalnej:
Kb=1,48 - wyznaczany doświadczalnie
![]()
Wyznaczanie masy molowej obliczeniowej:
Kb=1,762
![]()
III.Wyznaczanie stałej ebulioskopowej dla acetonu.
W celu wyznaczenia stałej ebulioskopowej dla acetonu wlewamy odmierzoną wcześniej ilościowo próbkę acetonu (55 ml) do aparatu i doprowadzamy do wrzenia.
Podczas, gdy słupek rtęci podnosił się notujemy wskazania termometru co 10 sekund,
Aż do ustabilizowania wahań słupka rtęci. Następnie proces wrzenia prowadzimy jeszcze przez kilka minut i odczytujemy wskazania termometru. Z kolei odważamy na wadze (z dokładnością do 0,001 g) 0,3 g substancji, rozpuszczamy ją w próbce acetonu (55 ml). Roztwór wlewamy do ebuliometru i doprowadzamy do wrzenia. Kiedy słupek rtęci przestaje się wahać odczytujemy jego wartość.
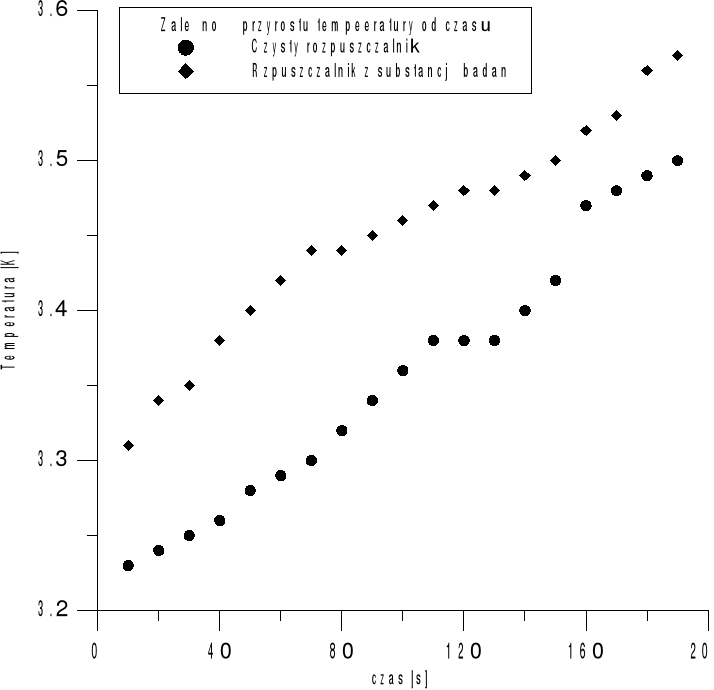
IV.Wykres wrzenia acetonu.
Lp. |
Temp. acetonu T [K] |
Czas t [s] |
Lp. |
Temp. acet.+subst. T [K] |
Czas t [s] |
1 |
2,90 |
15 |
1 |
3,15 |
15 |
2 |
2,92 |
30 |
2 |
3,16 |
30 |
3 |
2,96 |
45 |
3 |
3,18 |
45 |
4 |
2,97 |
60 |
4 |
3,20 |
60 |
5 |
3,00 |
75 |
5 |
3,27 |
75 |
6 |
3,05 |
90 |
6 |
3,30 |
90 |
7 |
3,06 |
105 |
7 |
3,34 |
105 |
8 |
3,10 |
120 |
8 |
3,33 |
120 |
9 |
3,10 |
135 |
9 |
3,33 |
135 |
10 |
3,11 |
150 |
10 |
3,37 |
150 |
11 |
3,11 |
165 |
11 |
3,38 |
165 |
12 |
3,12 |
180 |
12 |
3,39 |
180 |
13 |
3,15 |
195 |
13 |
3,39 |
195 |
14 |
3,20 |
210 |
14 |
3,41 |
210 |
15 |
3,20 |
225 |
15 |
3,41 |
225 |
16 |
3,20 |
240 |
16 |
3,42 |
240 |
17 |
3,21 |
255 |
17 |
3,42 |
255 |
18 |
3,21 |
270 |
18 |
3,42 |
270 |
19 |
3,21 |
285 |
19 |
3,42 |
285 |
Ebulioskopia
-
Wyszukiwarka
Podobne podstrony:
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
Laboratorium sprawozdania cz. 3, Mechanika III semestr, Fizyka, Laboratoria i sprawozdania
więcej podobnych podstron