Wydział Metalurgii i Inżynierii Materiałowej AGH |
||
Rok akademicki: 2003/2004 Rok studiów: II Kierunek studiów: Metalurgia Nr grupy: 4 |
Temat: Lepkość |
Data wykonania ćwiczenia: 5.12.2003
|
Nr zespołu: 11 |
Pastucha Krzysztof Papierz Grzegorz |
Ocena |
1. Oznaczanie lepkości względnej wodnych roztworów gliceryny przy pomocy wiskozymetru Oswalda.
Przyrządy i odczynniki:
Wiskozymetr Oswalda
Statyw metalowy, palnik, siatka, trójnóg, termometr, stoper
Zlewka 500 cm3
Zlewka 100cm3
Pipeta 10cm3
Gruszka gumowa
Woda destylowana (d=0.9982 g/cm3)
60% roztwór gliceryny (d=1.1533g/cm3)
70 % roztwór gliceryny (d=1.1808g/cm3)
80% roztwór gliceryny (d=1.2079g/cm3)
Wykonanie pomiaru:
Przemyty wodą destylowaną wiskozymetr Oswalda, umocowaliśmy w statywie, następnie za pomocą pipety przelaliśmy 10cm3 wody destylowanej do dolnego zbiorniczka. Za pomocą gruszki gumowej zassaliśmy wodę destylowaną do górnego zbiorniczka ponad 2 cm nad górny poziom. Po odłączeniu gruszki gumowej ciecz zaczęła opadać,zmierzyliśmy czas opadania pomiędzy górną kreską a dolną w górnym zbiorniczku. Czynność tę powtórzyliśmy 3 razy. Analogicznie postępowaliśmy z gliceryną notując czasy opadania.
Woda destylowana d=0.9982 g /cm3
50,62s
51,36s
51,08s
średnia 51,02s
δtx =0,2129s
Gliceryna 60% d=1.1533g/cm3
816s
800s
średnia 808s
δtx =4,6188s
Gliceryna 70% d=1.1808 g/cm3
1050s
1028s
średnia 1039s
δtx =6,3508s
Gliceryna 80% d=1.2079 g/cm3
1.1170s
średnia 1170s
δtx =0,98823s
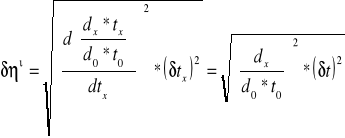
![]()
![]()
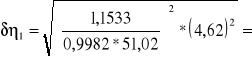
0,7
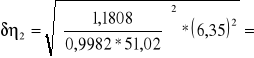
0,96
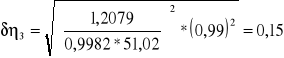
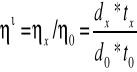
η'1=1,1533*808/0,9982*51,02
η'1=18,29
dx - gęstość badanej cieczy(gliceryna 60% .. 80%)
tx - czas opadania badanej cieczy pomiędzy górną a dolną kreską
d0 - gęstość cieczy wzorcowej (woda destylowana)
t0 - czas opadania cieczy wzorcowej
' - lepkość względna cieczy badanej
x - lepkość bezwzględna
lepkość cieczy wzorcowej
Ciecz |
tśr [s] |
' [Pa∙s] |
δ' |
x [Pa∙s] |
Woda destylowana |
51,02 |
1 |
0 |
0,001 |
60% roztwór gliceryny |
808 |
18,29 |
0,7 |
0,001829 |
70% roztwór gliceryny |
1039 |
23,52 |
0,96 |
0,02352 |
80% roztwór gliceryny |
1170 |
26,49 |
0,15 |
0,02649 |
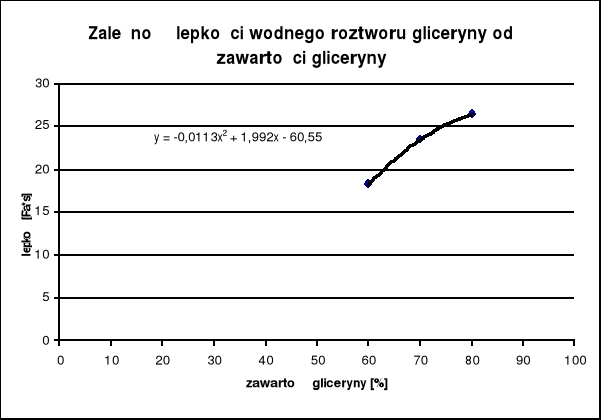
Dla x=100 wartość lepkości będzie równa około 102 [Pa*s]
2. Oznaczanie lepkości względnej roztworów sacharozy za pomocą wiskozymetru Englera
Przyrządy i odczynniki:
Wiskozymetr Englera
cylinder miarowy 300cm3
zlewka 500cm3
20% roztw. Sacharozy d=1.0894 g/cm3
40% roztw. Sacharozy d=1.1765 g/cm3
60% roztw. Sacharozy d=1.2864 g/cm3
Wykonanie pomiaru:
Do suchego wiskozymetru nalaliśmy taką ilość wody destylowanej, aby widoczne haczyki były przykryte (ponad 200cm3), następnie mierzyliśmy czas wypłynięcia 200cm3 wody przez kapilarę. Czynność tę wykonaliśmy 3 razy. Tak samo postępowaliśmy z sacharozą (20%, 40%, 60%) notując czasy.
Woda destylowana
55,5s
52,2s
53s
średnia 53,6s
δtx =0,98s
Sacharoza 20%
60,4s
61s
60,5s
średnia 60,63s
δtx =0,2076s
Sacharoza 40%
80,4s
81s
80,9s
średnia 80,77s
δtx =0,0187s
Sacharoza 60%
295s
291,6s
284,5s
średnia 290,37s
δtx =3,093s
tx - czas wypływu 200cm3 badanej cieczy [s]
tH2O- czas wypływu 200 cm3 wody
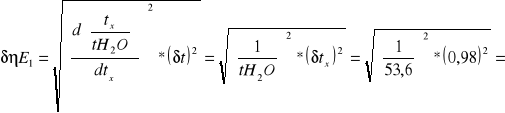
0,018
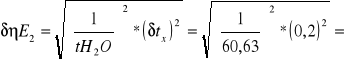
0,033
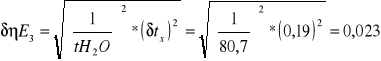
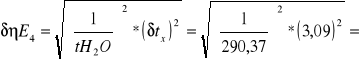
0,01
Ciecz |
Średni czas wypływu [s] |
δtx |
Lepkość [0E] |
δ [0E] |
Woda destylowana |
53,06 |
0,98 |
1 |
0,018 |
20% roztwór sacharozy |
60,63 |
0,21 |
1,13 |
0,033 |
40% roztwór sacharozy |
80,77 |
0,19 |
1,51 |
0,023 |
60% roztwór sacharozy |
290,37 |
3,09 |
5,41 |
0,012 |
3. Oznaczanie lepkości oleju mineralnego za pomocą lepkościomierza Höpplera
Przyrządy i odczynniki:
Wiskozymetr Höpplera,
stoper,
olej mineralny (d=0.928g/cm3)
Wykonanie pomiaru:
Wypoziomowany lepkościomierz Höpplera napełniliśmy olejem o T=294 K. Następnie mierzyliśmy czas opadania kulki pomiędzy dwoma kreskami. Czynność tę wykonaliśmy 3 razy. Tak samo postępowaliśmy z olejem o temperaturze 310 K i 345 K.
T1=294K
104 s
104 s
104,9 s
średnia 104,3 s
![]()
T3=310 K
41,4 s
41,1 s
41,4 s
średnia 41,3 s
![]()
T3=345 K
9,4 s
9,8 s
9,6 s
średnia 9,6 s
![]()
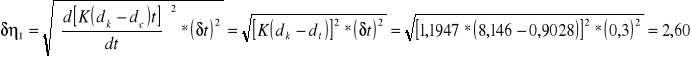
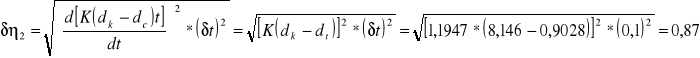
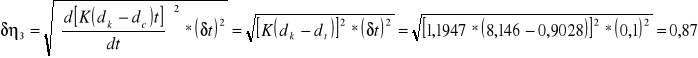
K - stała charakterystyczna dla kulki i wiskozymetru
dk - gęstość kulki = 8.146 g/cm3
dc - gęstość cieczy = 0.9028 g/cm3
K = 1.1947![]()
Temperatura oleju [K] |
t [s] |
δt [s] |
[Pa∙s] ∙10-3 |
δ |
294 |
104,3 |
0,3 |
902,5 |
2,60 |
310 |
41,3 |
0,1 |
357,36 |
0,87 |
345 |
9,6 |
0,1 |
83,07 |
0,87 |
ln η = ln A + (En/R*T)
y = ax + b
a = En/R b = ln A
eb = A
Temperatura (T) |
Lepkość (η) |
x (1/T) |
294 |
902,5 |
0,00340 |
310 |
357,36 |
0,00323 |
345 |
83,07 |
0,0029 |
Wyznaczenie E![]()
.
![]()
R = 8,314 J/mol∙K
Z wykresu ln![]()
(1/T) odczytujemy równanie prostej i obliczamy energie aktywacji:
E![]()
= 39193,86 [J/mol]
A = 2,33*10-5
Wnioski:
Z doświadczeń jakie przeprowadziliśmy wywnioskować można, że lepkość wraz ze wzrostem temperatury maleje. Można zauważyć też, że wraz ze wzrostem stężenia lepkość rośnie
(w przypadku sacharozy i gliceryny).
5
![]()
Wyszukiwarka
Podobne podstrony:
Chemia fizyczna - Ćw. 1 - Lepkość, Chemia fizyczna AGH laborki, lab 1
CHEMIA 12, Chemia fizyczna AGH laborki, lab 12
SPRAWOZ4, Chemia fizyczna AGH laborki, lab 12
napiecie pow nr 2, Chemia fizyczna AGH laborki, lab 2
LABORKA UKASZ 3, Chemia fizyczna AGH laborki, lab 3,4
CHEMIA 12, Chemia fizyczna AGH laborki, lab 12
korozja dla justyny, Chemia fizyczna AGH laborki, lab 21
Wyniki pomiarów ciepła rozpuszczania, Chemia fizyczna AGH laborki, lab 3,4
SPRAWOZ6, Chemia fizyczna AGH laborki, lab 18
Chemia fizyczna (3, Chemia fizyczna AGH laborki, lab 3,4
lab. 05 - baron, Chemia fizyczna AGH laborki, lab 5
Wykresy do 3, Chemia fizyczna AGH laborki, lab 3,4
tekst 7, Chemia fizyczna AGH laborki, lab 6
Chem 1, Chemia fizyczna AGH laborki, lab 1
skoootaaa, Chemia fizyczna AGH laborki, lab 20
Potencjały równowagowe elektrod - siła elektromotoryczna ogniw. polaryzacja, Chemia fizyczna AGH la
więcej podobnych podstron