Egzamin z chemii organicznej.
II termin. 27.06.2007
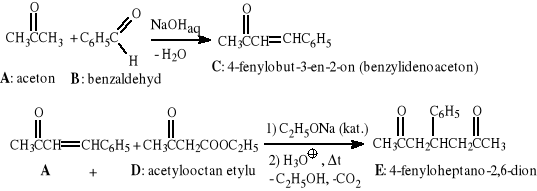
1. Przeprowadzono kondensację aldolową związków A i B otrzymując produkt C posiadający wiązanie C=C. Związek C ze związkiem -dikarbonylowym D w warunkach reakcji Michaela daje produkt E, z którego po hydrolizie i dekarboksylacji otrzymuje się 4-fenyloheptano-2,6-dion. Zapisz schemat powyższych reakcji za pomocą wzorów chemicznych [A + B → C (+ D) → E → 4-fenyloheptano-2,6-dion]. Przedstaw mechanizm kondensacji aldolowej (A+B → [X] → C). Uwaga: stereochemicznych aspektów reakcji można nie rozważać.
2. Przedstaw mechanizmy następujących reakcji:
2,2-dimetylopropan-1-ol + H2SO4/t → 2-metylo-but-2-en,
(S)-2-metoksy-2-fenylobutan + H2O/kat. H2SO4 → metanol + (±)-2-fenylobutan-2-ol,
benzoesan metylu + propanol (nadmiar, kat. H2SO4, t) → benzoesan propylu +?,
p-nitrotoluen + Cl2/Fe →? Wyjaśnij regioselektywność reakcji na podstawie trwałości kompleksów σ.
3. Zaproponuj syntezy następujących związków z podanych i inny substratów organicznych oraz niezbędnych reagentów:
1-fenylobuta-1,3-dienu z toluenu i propenu (proszę wykorzystać reakcję Wittiga),
kwasu 3,5-dibromobenzoesowego z p-toluidyny,
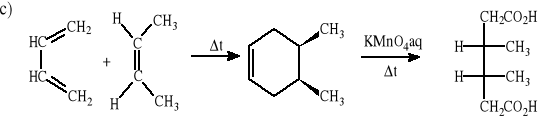
kwasu mezo-3,4-dimetylheksanodiowego z buta-1,3-dienu (jako jeden z etapów syntezy proszę wykorzystać reakcję Dielsa-Aldera),
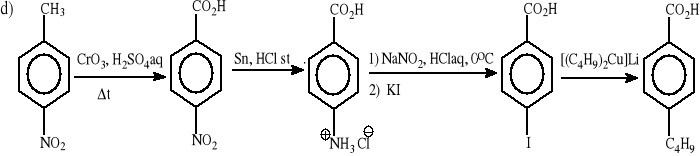
kwas p-butylobenzoesowy z p-nitrotoluenu (jako jeden z etapów proszę wykorzystać reakcję ze związkiem miedzioorganicznym),
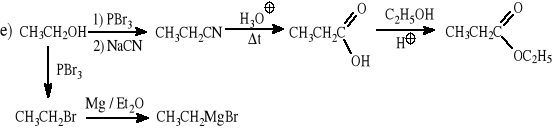
3-etylopentan-3-olu z etanolu jako jedynego substratu organicznego (proszę wykorzystać związki magnezoorganiczne).
4. Narysuj wzory Fischera chiralnych aminokwasów powstających w wyniku hydrolizy tripeptydu Ala-Ser-Gly o wzorze: H2NCH(CH3)CONHCH(CH2OH)CONHCH2CO2H, wiedząc, że wszystkie one mają konfigurację L. Napisz analogiczny wzór tripeptydu: Gly-Ser-Ala. Zaproponuj syntezę racemicznej alaniny (Ala) z kwasu propionowego.
5. Uzupełnij i zapisz za pomocą wzorów chemicznych podane równania reakcji. Podaj nazwy produktów oznaczonych pogrubionymi literami:
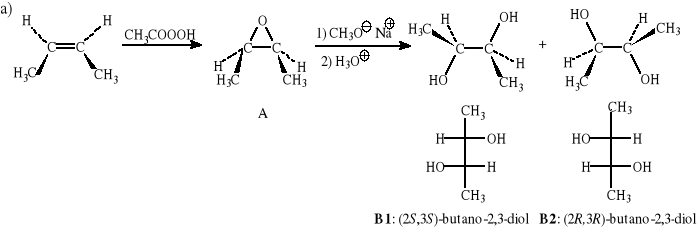
(Z)-but-2-en + CH3COOOH → A [+ 1) CH3O-Na+, 2) H3O+] → B1 + B2; budowę związku A proszę przedstawić za pomocą wzorów przestrzennych a związków B1 i B2 za pomocą wzorów Fischera (w nazwach związków proszę uwzględnić konfiguracje),
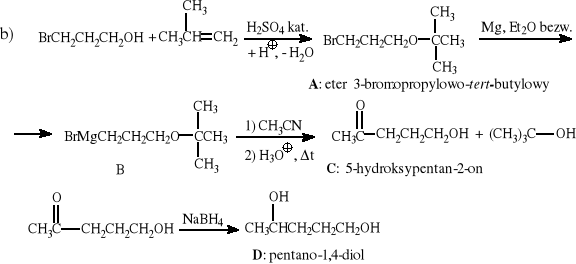
3-bromopropan-1-ol + 2-metylopropen/kat.H2SO4 → A (+ Mg/bezwodny eter) → B (+ 1) CH3CN, 2) H3O+/t, - alkohol tert-butylowy) → C (+ NaBH4) → D,
but-1-en + Br2 → A (+ 2 mole NaNH2) → B [+ 1) NaNH2/NH3 ciekły, 2) bromek etylu] → C (+ Na/NH3 ciekły) → D (+ Cl2) → E; narysuj wzór przestrzenny E, czy jest on optycznie czynny, uzasadnij,
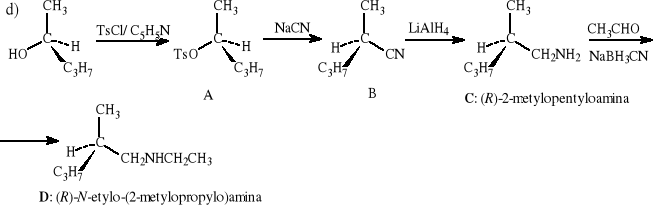
(S)-pentan-2-ol + chlorek tosylu/pirydyna → A (+ cyjanek sodu) → B (+ LiAlH4) → C (+ aldehyd octowy + NaBH3CN) → D (nazwy powinny uwzględniać konfigurację),
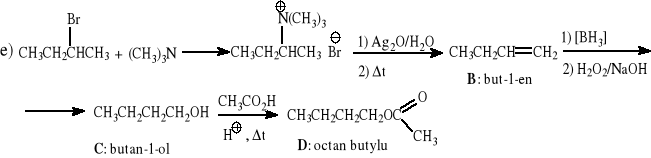
2-bromobutan + trimetyloamina → A [+ 1) Ag2O/H2O, 2) t] → B [+ 1) BH3, 2)/H2O2/NaOH] → C (+ kwas octowy/ kat. H2SO4,stęż., t)→ D,
Egzamin 27.06.07
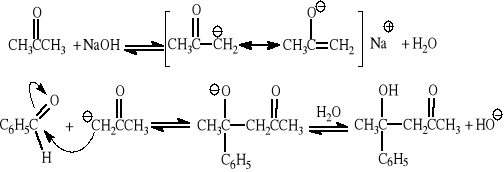
Zadanie1.

Mechanizm kondensacji aldolowej
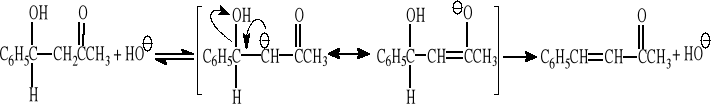
Zadanie 2.
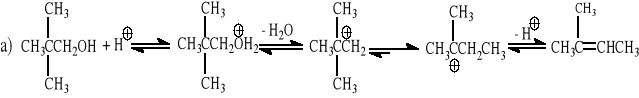
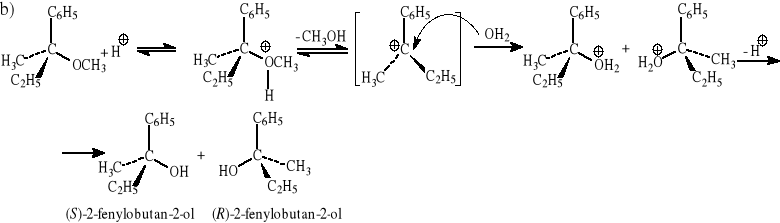
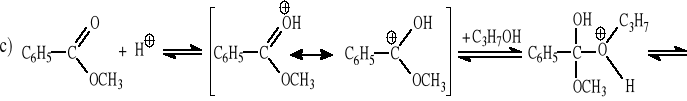
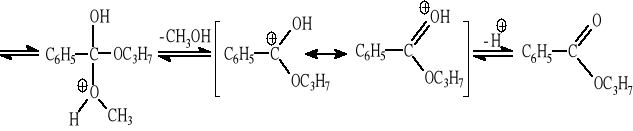
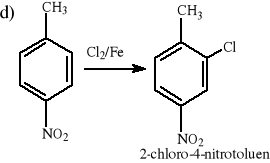
Mechanizm reakcji:
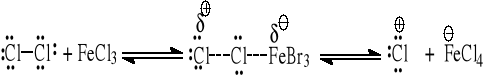
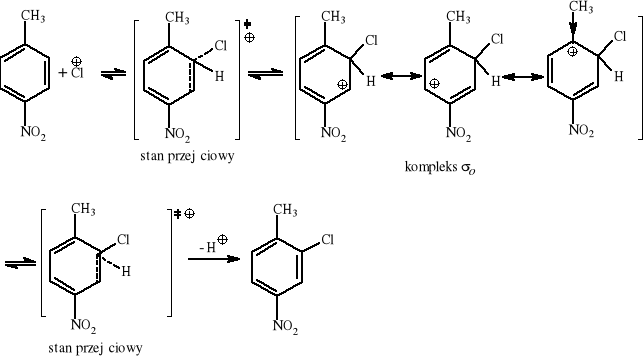
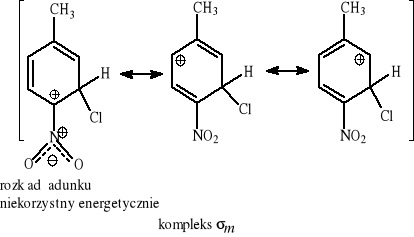
Powstaje 2-chloro-1-metylo-4-nitrobenzen. Drugi izomer praktycznie nie powstaje, ponieważ energia kompleksu σ meta (niekorzystny rozkład ładunku) jest wyższa, co oznacza wyższą energię aktywacji stanu przejściowego (E‡) (postulat Hammonda) dla tego kierunku reakcji.
Zadanie 3.
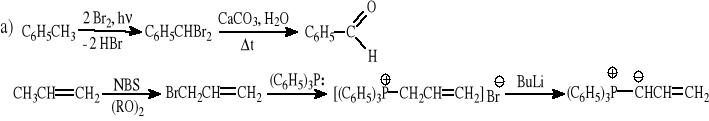
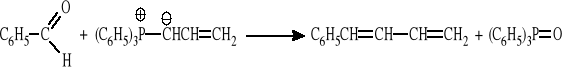
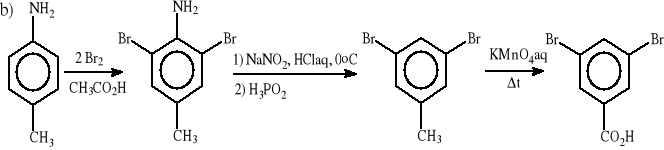
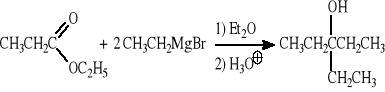
Zadanie 4.
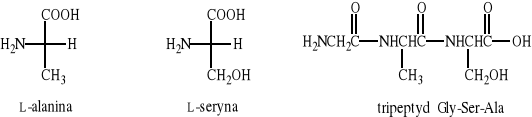
Synteza (+/-)-alaniny:
![]()
Zadanie 5.
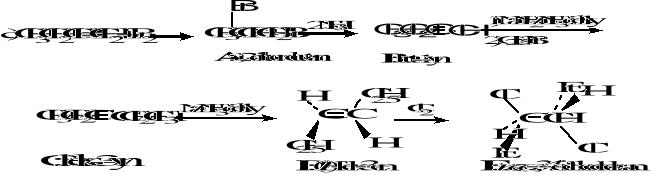
Produkt E jest optycznie niecczynną formą mezo. Posiada środek symetrii .