SPIS TREŚCI
1. BOJOWE ŚRODKI TRUJ¥CE O DZIA£ANIU PARALITYCZNO-DRGAWKOWYM
bojowe środki trujące O DZIA£ANIU PARALITYCZNO-DRGAWKOWYM
CHARAKTERYSTYKA OGÓLNA
Do fosforoorganicznych środków trujących zalicza się wiele związków fosforu o ogólnej budowie:
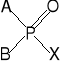
gdzie: A i B = -R, -OR, -NH2
X = reszta kwasowa
Poniżej przedstawiono przykładowe związki posiadające wysoką toksyczność, możliwe do zastosowania jako bojowe środki trujące:
1. i-C3H7 O-alkilo, w tym cykloalkilo-
C3H7 fluorofosfoniany
C2H5
CH3 O
P
C1-10H3-21O F
(i-C3H7)
(C3H7)2
(C2H5)2 O-alkilo, w tym cykloalkilo-
2. (CH3)2 N O cyjanofosfoniany
P
C1-10H3-21O CN
3. (i-C3H7)2
(C3H7)2
(C2H5)2 O-alkilo, w tym cykloalkilo-
(CH3)2 O S- 2 dialkiloaminofosfonotiolany
P
C1-10H3-21O S- CH2-CH2-N(CH3)2
(C2H5)2
(C2H5)2
(C3H7)2
4. Pochodne systoksu
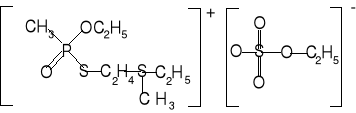
Przedstawione substancje są cieczami, a ich sole ciałami stałymi. Spośród pochodnych chlorowcowych, fluorkowe są z reguły bardziej toksyczne od chlorkowych czy bromkowych, natomiast pochodne cyjankowe bardziej toksyczne od rodankowych.
Dla podstawników alkoksylowych toksyczność wzrasta w szeregu: pochodne metoksylowe, etoksylowe, n-propoksylowe, izo-propoksylowe. ze wzrostem długości łañcucha węglowego w podstawnikach alkilowych toksyczność spada.
Grupy alkiloamidowe powodują tym większe własności trujące, im bardziej rozbudowane przestrzennie są ich grupy alkilowe. Tak więc grupa diizopropyloamidowa będzie bardziej zwiększała toksyczność związku fosforoorganicznego niż grupa dimetyloamidowa.
W niektórych związkach podstawnik X jest grupą fenoksylową. Własności trujące tych pochodnych są jednak mniejsze niż przy w/w podstawnikach X.
Fosforoorganiczne środki trujące przenikają do organizmu przez drogi oddechowe, przewód pokarmowy, błony śluzowe oraz przez skórę. Przenikalność tych środków przez poszczególne wrota organizmu różni się często o dwa rzędy wielkości. Na ogół najtrudniej uzyskać dawkę toksyczną przez skórę, a najłatwiej przez drogi oddechowe. Niektóre z powyższych substancji cechują się jednak podobnymi wielkościami dawek zarówno drogą doustną jak i naskórną.
MECHANIZM TOKSYCZNEGO DZIA£ANIA
Przyczyny powstawania zatruć organizmu.
Podstawą toksycznego działania środków fosforoorganicznych jest unieczynnienie hydrolazy acetylocholiny (acetylocholinoesterazy AChE). Powoduje to nadmierne gromadzenie się acetylocholiny w tkankach, co jest bezpośrednią przyczyną zaburzeñ czynności fizjologicznych organizmu. Acetylocholina jest przekaŹnikiem chemicznym impulsów przesyłanych przez złącze synaptyczne komórki nerwowej. W złączu synaptycznym może występować tylko w czasie przekazywania impulsu. Dłuższe jej pozostawanie w szczelinie synaptycznej powoduje zakłócenie przewodnictwa w komórce nerwowej. Uszkodzona komórka nerwowa w długim czasie nie może odtworzyć normalnych czynności. Uszkodzenie znacznej ilości komórek nerwowych przez środek fosforoorganiczny powoduje szybkie powstanie zaburzeñ czynności wielu układów organizmu stanowiące sumaryczny efekt zatrucia.
Zarys budowy układu nerwowego.
Podstawową jednostką systemu nerwowego jest neuron. Przeciętny neuron ma około 0,1mm średnicy i może osiągać długość kilku metrów. Neuron zasadniczo składa się z trzech części: ciało komórki, akson (neuryt) i dendryt. Akson wychodzi z jednego koñca ciała komórki a krzaczaste dendryty z drugiego koñca. Dendryt jest wyspecjalizowaną częścią neuronu odbierającą bodŹce ze środowiska albo od innej komórki. Akson rozprowadza bodŹce z okolicy dendrytowej. Ciało komórki neuronu odgrywa istotną rolę w utrzymaniu procesów metabolicznych. Może być położone w dowolnym miejscu w stosunku do pozostałych części neuronu. Na podstawie spełnianych funkcji neurony dzielimy na czuciowe, ruchowe i pośredniczące. Neurony czuciowe są receptorami albo łącznikami receptorów. Przewodzą one informacje do centralnego układu nerwowego. Neurony ruchowe przewodzą informacje z centralnego układu nerwowego do mięśni, gruczołów itp. Neurony pośredniczące łączą dwa lub więcej neuronów i znajdują się przeważnie w całości wewnątrz centralnego układu nerwowego. Typowe schematy neuronów przedstawiono na rysunku 1.
Rys 1 . Typy neuronów
Neurony składają się na układ nerwowy organizmu. Dzieli się on na ośrodkowy (centralny) i obwodowy. W skład centralnego układu nerwowego wchodzi mózg i rdzeñ kręgowy. Z mózgu i rdzenia kręgowego wychodzą parzyste nerwy mózgowe i rdzeniowe łączące wszystkie receptory i efektory z mózgiem i rdzeniem tworząc obwodowy układ nerwowy. Nerwy mózgowe i rdzeniowe zbudowane są z neurytów i dendrytów. W układzie obwodowym występują jedynie ciała komórkowe neuronów czuciowych tworzące w pobliżu mózgu i rdzenia skupiska zwane zwojami oraz ciała niektórych neuronów ruchowych układu autonomicznego.
Nerwy mózgowe. Dwanaście par nerwów z różnych okolic mózgu unerwia głównie narządy zmysłów, mięśnie oraz gruczoły występujące w głowie. Oznacza się je numerami od I do XII. Podobnie jak wszystkie nerwy są one zbudowane z neuronów, przy czym pary neuronów I, II i VIII są zbudowane tylko z neuronów czuciowych, pary III, IV, VI, XI, XII - prawie całkowicie z neuronów ruchowych, pary V, VII, IX, X z obu rodzajów neuronów. W tabeli 1 przedstawiono narządy unerwione nerwami mózgowymi.
Tabela 1. Nerwy mózgowe człowieka.
Nr nerwu |
Nazwa nerwu |
Początek nerwów czuciowych |
Efektory unerwione przez nerwy ruchowe |
I |
Węchowy |
śluzówka węchowa nosa (węch) |
- |
II |
Wzrokowy |
siatkówka oka (widzenie) |
- |
III |
Okoruchowy |
mięśnie gałki ocznej (czucie mięśniowe) |
mięśnie poruszające gałką oczną (z nerwem IV i VI), mięśnie zmieniające kształt soczewki, mięśnie zwężające Źrenicę. |
IV |
Bloczkowy |
mięśnie gałki ocznej (czucie mięśniowe) |
inne mięśnie poruszające gałką oczną. |
V |
Trójdzielny |
zęby i skóra twarzy |
niektóre mięśnie żujące |
VI |
Odwodzący |
mięśnie gałki ocznej (czucie mięśniowe) |
inne mięśnie poruszające gałką oczną. |
VII |
Twarzowy |
kubki smakowe przedniej części języka |
mięśnie twarzy, gruczoły podszczękowe i podjęzykowe |
VIII |
Słuchowy |
Ślimak (słyszenie), kanały półkoliste (równowaga) |
- |
IX |
Językowo-gardłowy |
kubki smakowe tylniej części języka, błona wyścielająca gardło |
gruczoły przyuszne, mięśnie gardzieli współdziałające przy połykaniu. |
X |
Błędny |
zakoñczenia nerwowe licznych narządów wewnętrznych: płuc, żołądka, aorty, tchawicy. |
Parasympatyczne nerwy idące do serca, żołądka, tchawicy, jelita cienkiego i przełyku. |
XI |
Dodatkowy |
mięśnie ramienia, (czucie mięśniowe). |
Mięśnie ramienia |
XII |
Podjęzykowy |
mięśnie języka (czucie mięśniowe) |
mięśnie języka |
Jednym z najważniejszych nerwów jest nerw błędny (X). Tworzy on część układu autonomicznego i unerwia wewnętrzne narządy klatki piersiowej i górnej części brzucha.
Nerwy rdzeniowe. Wszystkie nerwy rdzeniowe są nerwami mieszanymi, składającymi się z neuronów czuciowych i ruchowych mniej więcej w równych ilościach.
Z rdzenia człowieka wychodzi 31 par nerwów, z których każda unerwia receptory i efektory jednej okolicy ciała. Każdy nerw wychodzi z rdzenia w postaci dwóch korzonków, które następnie łączą się w jeden nerw rdzeniowy. Włókna czuciowe wchodzą do rdzenia od strony grzbietowej (korzonki grzbietowe czyli tylne), a włókna ruchowe odchodzą od rdzenia jako korzonki brzuszne czyli przednie. Na rys 2 przedstawiono typy neuronów rdzeniowych.
Rys. 2. Typy rdzeniowych neuronów ruchowych i czuciowych i ich połączenia z rdzeniem kręgowym.
W celu uzyskania większej przejrzystości rysunku, neurony czuciowe pokazano po lewej stronie, a neurony ruchowe po prawej, pomimo że znajdują się one po obu stronach ciała.
W przypadku uszkodzenia korzonka czuciowego część ciała unerwiona przez te nerwy zostaje pozbawiona czucia, natomiast nie występuje paraliż mięśni. Jeżeli przetnie się korzonki brzuszne, dana okolica ciała zostaje sparaliżowana, nie jest jednak pozbawiona odczuwania temperatury, dotyku, bólu. Wielkość każdego nerwu rdzeniowego uzależniona jest od wielkości okolicy ciała, którą unerwia. Największe są nerwy koñczyn dolnych. Każdy nerw rdzeniowy na krótkim odcinku poniżej połączenia dwóch korzonków grzbietowego i brzusznego rozdziela się na trzy gałązki:
grzbietową - obsługującą skórę i mięśnie grzbietu;
brzuszną - obsługującą skórę i mięśnie brzucha;
autonomiczną - (wegetatywną) - obsługującą trzewia.
Odruchy i odruchowe łuki nerwowe.
Podstawową czynnością układu nerwowego jest odruch polegający na podświadomym działaniu wywołanym przez jakąś podnietę. O wykonaniu odruchu uświadamiamy sobie dopiero po jego przebiegu. Może to być cofnięcie ręki od gorącego lub kłującego przedmiotu, zamknięcie powiek pod wpływem impulsu świetlnego, odruch kolanowy itp.
Odruch typowy obejmuje jedynie część ciała, nigdy całość. Wyżej podane przykłady należą właśnie do odruchów typowych. Odruchy są funkcjonalnymi jednostkami układu nerwowego i wynikiem ich działania jest większość naszych czynności życiowych. Bardzo ważne w życiu organizmu są między innymi odruchy kontrolujące tętno serca, ciśnienie krwi, oddychanie, wydzielanie śliny, ruchy przewodu pokarmowego. Jeżeli staniemy na coś ostrego lub dotkniemy gorącego przedmiotu, to nie oczekujemy, aby ból został zarejestrowany przez mózg i nie decydujemy się na jakiś ruch dopiero po namyśle, lecz reagujemy natychmiast, podnosząc stopę lub odsuwając odruchowo rękę - przed zarejestrowaniem bólu przez mózg. Wiele bardzo złożonych codziennych czynności jest regulowane w dużej mierze przez odruchy. Wrodzone odruchy nazywamy odruchami bezwarunkowymi, natomiast odruchy nabyte w wyniku doświadczeñ nazywamy odruchami warunkowymi. Minimum anatomicznym wymaganym do wykonania odruchu prostego są: neuron czuciowy z receptorem kontaktujący się za pomocą synapsy z neuronem ruchowym, połączonym z mięśniem lub innym efektorem. Ten typ łuku odruchowego określany jest jako jednosynaptyczny, ponieważ istnieje tylko jedno połączenie synaptyczne między neuronem czuciowym i ruchowym. Większość łuków odruchowych zawiera jeden lub więcej neuronów pośredniczących pomiędzy neuronem czuciowym i ruchowym. Schemat łuku odruchowego przedstawiono na rys. 3.
Rys. 3. Schemat łuku odruchowego.
Odruch prosty, w którym podrażnienie receptora wywołuje skurcz jednego mięśnia jest zwykle demonstrowane na „odruchu kolanowym” Jeśli uderzymy w ścięgno rzepki kolanowej nastąpi podrażnienie jego receptorów. Powstały bodziec popłynie po łuku odruchowym do rdzenia i z powrotem na dół, powodując skurcz mięśnia związanego z tym ścięgnem, w wyniku czego nastąpi gwałtowne wyprostowanie się nogi.
Wiele odruchów obejmuje połączenia licznych neuronów pośredniczących w rdzeniu kręgowym. Rdzeñ kręgowy funkcjonuje nie tylko jako przewodnik bodŹców do i od mózgu; odgrywa on ważną rolę w scalaniu odruchów prostych.
Złożoność odruchów zmienia się wraz z liczbą segmentów rdzenia. Całkowity łuk odruchowy może zawierać się w jednym segmencie rdzenia. Wiele odruchów wymaga jednak połączeñ międzyneuronalnych pomiędzy dwoma lub więcej segmentami rdzenia. Odruchy drapania się, prostowania i chodzenia obejmują włączenie informacji czuciowych z wielu segmentów rdzenia. Odruchy złożone mogą nawet obejmować pewne części mózgu, mianowicie śródmózgowia i rdzenia przedłużonego. W najprostszym rodzaju reakcji bodziec uruchamia mięsieñ bądŹ układ mięśni, które reagują niezmiennie i zgodnie z przewidywaniem.
Tego rodzaju zachowanie uwarunkowane jest jedynie obecnością odpowiednich narządów zmysłowych połączonych z odpowiednim układem mięśni. Na przykład w odruchu kolanowym, który jest odruchem rozciągowym, uderzenie w ścięgno poniżej rzepki kolanowej rozciąga połączony z tym ścięgnem mięsieñ. W neuronie receptorowym powstaje impuls przewodzony wzdłuż jego aksonu do rdzenia kręgowego, gdzie przez synapsę przechodzi na neuron ruchowy pobudzający mięsieñ do skurczu podrywającego podudzie. Jest to więc monosynaptyczny łuk odruchowy przedstawiony na rys.4.
Rys. 4. Schemat monosynaptycznego łuku odruchowego.
W synapsach łączących doprowadzające i odprowadzające odcinki danego obwodu nerwowego może nastąpić modyfikacja reakcji odruchowych zwana opóŹnieniem synaptycznym. Im bodziec jest silniejszy, tym opóŹnienie jest krótsze. Powstaje więc zależność pomiędzy siłą bodŹca, a wystąpieniem reakcji. £uk odruchowy może zawierać dwa i więcej neuronów wstawkowych i tym samym odpowiednią ilość połączeñ (synaps). Na rysunku 5 przedstawiono schemat dwusynaptycznego łuku odruchowego.
Rys. 5. Dwusynaptyczny łuk odruchowy.
Schemat wielosynaptycznego łuku odruchowego przedstawiono na rys. 6.
Rys 6. Wielosynaptyczny łuk odruchowy.
Wielosynaptyczny łuk odruchowy daje możliwość powstawania złożonych reakcji w zależności od siły bodźca.
Połączenia synaptyczne neuronów.
Ponieważ układ nerwowy jest zbudowany z odrębnych jednostek - neuronów - ale działa jak jednolity układ przewodzący, istnieją czynnościowe połączenia między neuronami zwane synapsami. Synapsa (styk) jest okolicą, gdzie jedna komórka - presynaptyczna - łączy się z drugą komórką - postsynaptyczną. W układzie nerwowym kręgowców istnieje wiele synaps, z których większość przewodzi podniety tylko w jednym kierunku, np. z komórek pre- do postsynaptycznych. Okolica synaptyczna aksonu presynaptycznego kręgowców jest wypełniona pęcherzykami synaptycznymi o średnicy 20-60nm. Pęcherzyki zawierają substancje chemiczne uwalniane w czasie pobudzenia aksonu i przewodzą podnietę do komórki postsynaptycznej.
Przewodzenie synaptyczne jest wolniejsze niż przewodzenie wzdłuż nerwu. Stan pobudzenia przenoszony jest tylko w jednym kierunku: w neuronach czuciowych z organu czuciowego do rdzenia kręgowego i mózgu, natomiast w neuronach ruchowych, z mózgu i rdzenia kręgowego do mięśni i gruczołów. Kontrola odbywa się przez aksony, ponieważ tylko zakoñczenie aksonu jest zdolne do wydzielenia substancji chemicznych stymulujących następny neuron. Każde pojedyncze włókno nerwowe może przewodzić impulsy w obu kierunkach; jeżeli jest elektrycznie stymulowane w jego środkowej części, powstaną dwa impulsy idące w przeciwnych kierunkach, ale tylko jeden idący w kierunku aksonu może pobudzić następny neuron. Pobudzenie przenoszone w kierunku dendrytu zostanie zatrzymane po osiągnięciu zakoñczenia. Dalsze przewodzenie sygnału umożliwia złącze synaptyczne pokazane na rysunku nr 7.
Rys 7. Schemat złącza synaptycznego.
W większości złącz synaptycznych występuje szczelina o szerokości około 20 nm, przez którą impulsy przewodzone są przy pomocy przekaŹnika chemicznego. Takim przekaŹnikiem jest acetylocholina. Acetylocholina jest środkiem pobudzającym, wywołującym lokalną depolaryzację błony komórkowej. Przechodzi ona z aksonu do dendrytu na drodze dyfuzji. Na tak małej odległości proces dyfuzji jest wystarczająco szybki, by zapewnić sprawne przewodzenie synaptyczne. Dyfundująca acetylocholina przyczepia się do błony dendrytu w miejscach zwanych receptorami cholinergicznymi powodując wytworzenie nowego impulsu nerwowego przekazywanego dalej wzdłuż dendrytu. Rozróżnia się następujące rodzaje receptorów cholinergicznych:
- receptory muskarynowe w narządach unerwionych przez układ przywspółczulny;
- receptory nikotynowe płytki motorycznej w mięśniach prążkowanych;
- receptory nikotynowe błony postsynaptycznej w zwojach układu wegetatywnego;
- receptory muskarynowe i nikotynowe układu cholinergicznego w ośrodkowym układzie
nerwowym;
Acetylocholina wytwarzana jest w mitochondriach i przechowywana w pęcherzykach synaptycznych. Impuls (potencjał czynnościowy) docierający do aksonu uwalnia zawartość pęcherzyka doprowadzając do przekazania sygnału na płytkę postsynaptyczną. Taka konstrukcja synapsy powoduje, że sygnał przekazywany jest zawsze tylko w jednym kierunku, a nigdy w przeciwnym. Należy przyznać, że acetylocholina nie jest jedynym neurotransmiterem. Znane neurotransmitery to między innymi noradrenalina, serotonia, dopamina.
Po przekazaniu sygnału acetylocholina jest rozkładana przez enzym cholinoesterazę na cholinę i kwas octowy, tracąc w ten sposób własności neurotransmitera. Produkty hydrolizy acetylocholiny tranportowane są do mitochondriów, gdzie następuje powtórna jej synteza.
cholinoesteraza i jej rola w przekazywaniu impulsów nerwowych.
Esteraza cholinowa należy do grupy protein o wysokiej masie cząsteczkowej i składa się ze znacznej ilości α-aminokwasów.
Cząsteczka cholinoesterazy może przyjmować rozmaite kształty: najczęściej spirali. Stwierdzono, że cząsteczka cholinoesterazy posiada jedno centrum aktywne, nadające jej własności katalityczne. Struktura tego centrum jest określona przez skład i kolejność łączących się ze sobą reszt aminokwasów oraz przestrzenne rozmieszczenie spirali.
Centrum aktywne esterazy cholinowej składa się z dwóch części :
- esterazowej - zawierającej grupę nukleofilową np.: grupę OH-;
- anionoidowej - o podwyższonej gęstości elektronowej.
Dla wyjaśnienia katalitycznej aktywności enzymów przyjęto hipotezę, przedstawianą obrazowo jako zasada „zamka i klucza”. Rolę „otworu zamka na klucz”, spełniają w centrum aktywnym enzymu obie części - esterazowa i anionoidowa, których kształt odpowiada „kluczowi” cząsteczce acetylocholiny. Dopasowanie „klucza” do „zamka” odpowiada momentowi utworzenia się kompleksu aktywnego enzym - substrat. W tym momencie, na skutek przejścia acetylocholiny w stan aktywny, następuje gwałtowny wzrost częstości zderzeñ efektywnych cząsteczek wody z acetylocholiną prowadzący do natychmiastowej hydrolizy.
W warunkach normalnych, w organizmie jedynym substratem jest acetylocholina, której hydroliza uwalnia powierzchnię aktywną cholinoesterazy. Dla procesu przekazywania impulsu nerwowego istotne znaczenie posiada nie tylko acetylocholina ale również jej rozkład przez cholinoesterazę. Schemat reakcji hydrolizy acetylocholiny w centrum aktywnym esterazy cholinowej przedstawiono na rys. 8.
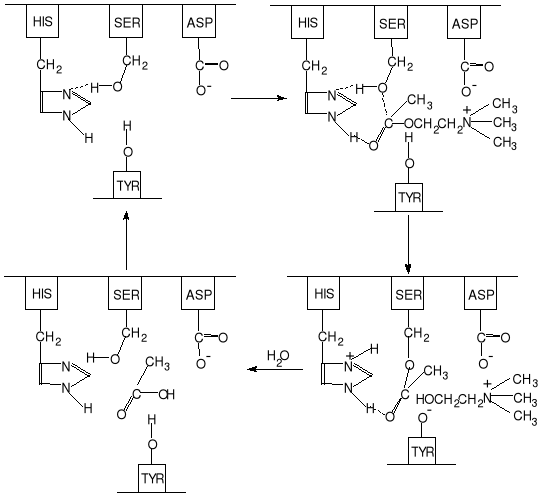
Rys.8. Schemat reakcji hydrolizy acetylocholiny w centrum aktywnym esterazy cholinowej.
Badania nad biochemicznym mechanizmem działania fosforoorganicznych środków trujących na organizm ludzki wykazały, że związki te reagują z cholinoesterazą powodując jej unieczynnienie przez fosforylowanie. Unieczynniony enzym je nie może powodować rozkładu acetylocholiny.
Na rys.9 przedstawiono centrum aktywne esterazy cholinowej, z którego wyprowadzono grupy funkcyjne aminokwasów, wchodzących w jego skład. Opierając się na analogii „zamka” i „klucza” można stwierdzić, że cząsteczka związku fosforoorganicznego stanowi właśnie jakby „klucz”, podobnie jak cząsteczka acetylocholiny. Środek fosforoorganiczny wchodzi do „zamka” na tyle, by nie dopuścić acetylocholiny, nie na tyle jednak aby „otworzyć drzwi”, co prowadzi do zahamowania aktywności enzymatycznej cholinoesterazy.
Obecnie istnieją przekonujące dowody na istnienie takiego właśnie mechanizmu zatruć środkami fosforoorganicznymi. Fakt unieczynnienia esterazy cholinowej przez cząsteczki związków fosforoorganicznych został potwierdzony za pomocą badañ przy użyciu atomów promieniotwórczego fosforu. Stwierdzono, że jeden atom promieniotwórczego fosforu przypadał na jedną cząsteczkę enzymu. W produktach hydrolizy fosforylowanego enzymu znaleziono kwas serynofosforowy, co świadczy o występowaniu reszt seryny w esterazowej części centrum aktywnego cholinoesterazy.
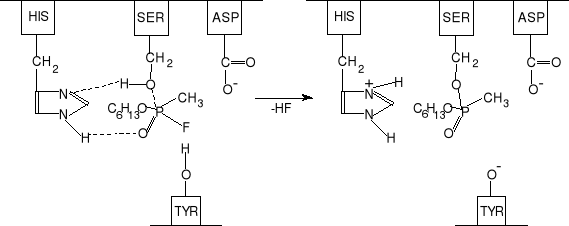
Rys. 9. Schemat blokowania esterazy cholinowej przez soman.
C6H13O- jest grupą pinakolinową. Alkohol pinakolinowy posiada następującą budowę:
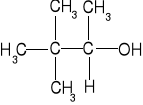
Grupa pinakolinowa podwyższa znacznie toksyczność somanu w stosunku do sarinu, który posiada w budowie cząsteczki grupę izopropylową.
Zablokowanie esterazy cholinowej prowadzi do zwiększenia ilości acetylocholiny w przestrzeni synaptycznej, a włókno nerwowe drażnione przez acetylocholinę zaczyna bez przerwy przekazywać impulsy do mięśni lub gruczołów, unerwianych przez wegetatywny układ nerwowy. Prowadzi to do skurczu mięśni oraz do wzmożonego wydzielania gruczołów. Naruszenie równowagi układu nerwowego wywołuje powstawanie zewnętrznych objawów zatrucia, takich jak: zwężenie Źrenic, ślinotok, skurcze mięśni prowadzące do drgawek i paraliżu.
Jest rzeczą oczywistą, że związki fosforoorganiczne będą wykazać tym większą toksyczność, im bardziej kształt ich cząsteczek będzie dopasowany do „zamka” - centrum aktywnego esterazy cholinowej. Można się więc spodziewać znacznego zwiększenia toksyczności związków fosforoorganicznych, które będą zdolne do blokowania obydwu części centrum aktywnego - esterazowej i anionoidowej. Przykładem mogą być pochodne związki chemiczne fosforylotiocholiny:
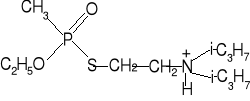
Okazały się one nadzwyczaj silnymi inhibitorami esterazy cholinowej i niezwykle silnymi bojowymi środkami trującymi. W procesie blokowania esterazy cholinowej, udział bierze postać protonowa fosforylotiocholin II , która powstaje w organizmie, na skutek przyłączenia się atomu wodoru do wolnej pary elektronowej atomu azotu w grupie diizopropyloamidowej. W wyniku tego, powstaje ładunek dodatni na atomie azotu, co pozwala na osiągnięcie powinowactwa elektronowego tej grupy do centrum anionoidowego esterazy cholinowej, podobnie jak ma to miejsce w wypadku acetylocholiny:
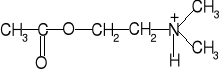
Powstająca w wyniku protonowania grupa amoniowa (i-C3H7)2NH+- charakteryzuje się silnym efektem indukcyjnym, który w znacznym stopniu wzmacnia bezwodnikowy charakter wiązania P-S w cząsteczce fosforylotiocholliny, a co za tym idzie, jej własności fosforylujące. Geometryczne i elektronowe podobieñstwo struktur fosforylotiocholin i esterazy cholinowej prowadzi do specyficznego i trwałego ich wiązania co powoduje inaktywację esterazy cholinowej. Następujące po związaniu fosforylowanie sprawia, że zablokowanie tego enzymu staje się nieodwracalne. Schemat nieodwracalnego blokowania esterazy cholinowej pochodną izopropylową acetylotiocholiny przedstawiono na rys. 10.
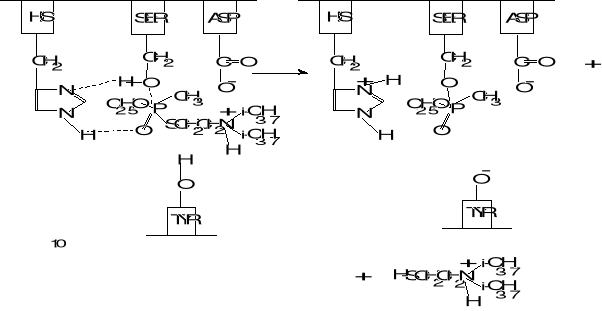
Rys.10. Nieodwracalne zablokowanie enzymu pochodną fosforylotiocholiny
Samorzutne odblokowanie esterazy cholinowej unieczynnionej środkami typu sarin lub V-gazy zachodzi bardzo powoli, względnie w ogóle nie zachodzi (unieczynnienie nieodwracalne).
Nadzwyczaj wysoka toksyczność związków fosforoorganicznych pochodzi stąd, że ilość cholinoesterazy w organizmie jest niewielka, a zdolność fosforoorganicznych środków trujących do blokowania cholinoesterazy jest wyjątkowo duża.
Ratowanie zatrutego wymaga iniekcyjnego podania odtrutek: atropiny i toksogoniny.
Atropina jest alkaloidem o wzorze:
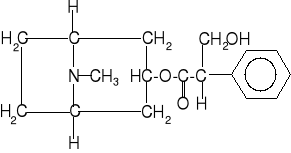
Jest substancją silnie trującą. Połowiczną dawkę śmiertelną (LD50) atropiny ocenia się na 1mg/kg. Jeśli jednak podana jest po zatruciu organizmu inhibitorem esterazy holinowej powoduje rozluŹnienie mięśni, ustąpienie drgawek i paraliżu. Tolerancja zaś organizmu na atropinę wzrasta nawet kilkaset razy. Atropina blokuje receptory holinergiczne, co powoduje brak reakcji w części wykonawczej łuku odruchowego. Uspokajająca działalność atropiny ustaje jednak po okresie około 1 godziny.
Świadczy to o metabolicznych przemianach atropiny w organiŹmie.
Prawdopodobnie hydrolizuje się ona na tropinę i kwas tropowy:
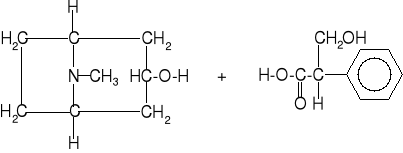
Dla ratowania organizmu podaje się następne dawki atropiny. Atropina spełnia jednak rolę odtrutki działającej skutkowo. Działanie przyczynowe, to odtwarzanie zdolności esterazy cholinowej do hydrolizy acetyloholiny. Takie własności posiadają oksymy. Wypróbowano działanie następujących oksymów: pralidoksym, obidoksym, trimedoksym.
Są to substancje o następujących wzorach:
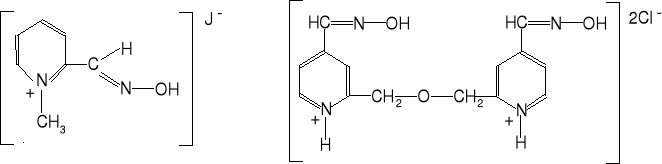
pralidoksym obidoksym
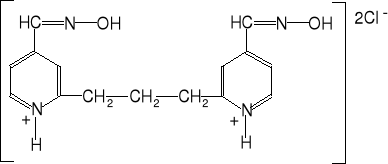
trimedoksym
Konstrukcja tych związków pozwala na wykorzystanie konfiguracji centrum aktywnego cholinoesterazy, umocnienie się w nim, związanie z atomem fosforu, rozerwanie wiązania serynowego i wyciągnięcie związku fosforoorganicznego z centrum aktywnego. Schemat reakcji odblokowywania centrum aktywnego esterazy cholinowej przedstawiono na rys. 11.
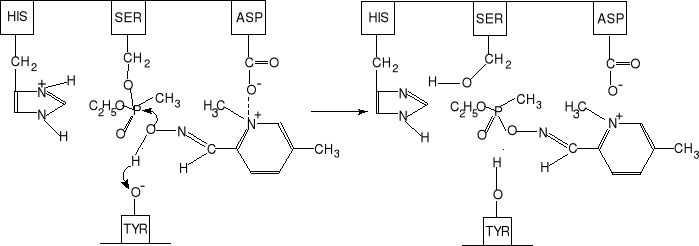
Rys. 11. Schemat reakcji pralidoksymu z estrem kwasu metylofosfonowego w centrum
aktywnym esterazy cholinowej.
Skuteczność reaktywacji centrum aktywnego esterazy cholinowej zależy w znacznym stopniu od czasu podania oksymu i rodzaju grupy alkoksylowej w związku fosforoorganicznym. Po pewnym czasie bowiem następuje nieodwracalne unieczynnienie esterazy. Proces ten wiąże się z odszczepieniem grupy alkoksylowej. Centrum aktywne należy bowiem rozpatrywać jako układ elastyczny, w którym cząsteczka związku fosforoorganicznego ulega po pewnym czasie zakleszczeniu. Podany reaktywator usuwa z centrum aktywnego cząsteczkę fosforanu bez grupy alkoksylowej. Im bardziej rozbudowana jest grupa alkoksylowa, tym szybciej ulega zakleszczeniu i tym szybciej enzym ulega procesowi „starzenia”. Okres, w którym połowa unieczynnionego enzymu przekształca się w formę całkowicie nieodwracalną wynosi dla związku Vx - ok. 40 godzin, dla sarinu - 4 godziny, dla somanu - 2 - 4 minuty. W związku Vx grupą alkoksylową jest grupa etylowa (C2H5O-), w sarinie izopropylowa (C3H7O-), a w somanie pinakolinowa (C6H13O-).
Objawy zatrucia
Objawy zatrucia fosforoorganicznymi środkami trującymi występują w krótkim czasie bez okresu utajenia, a ich nasilenie jest zależne od wielkości pochłoniętej dawki. Trucizna może być podawana do organizmu wielokrotnie w małych dawkach podtoksycznych wywołując w efekcie zatrucie przewlekłe lub jednorazowo w dawkach toksycznych powodując zatrucia ostre.
Zatrucia przewlekłe są powodowane własnością kumulowania się środków fosforoorganicznych w organiŹmie, wskutek czego z małych dawek podtoksycznych uzyskuje się efekt zatrucia. Tym tłumaczy się występowanie zatruć podczas długotrwałego przebywania ludzi w atmosferze o bardzo niskiej zawartości trucizny. Na przykład czterogodzinne przebywanie w atmosferze zawierającej 3* 10-7mg/dm3 somanu wywołuje objawy silnego zatrucia tą substancją.
Zatrucia ostre można podzielić na lekkie, średnie i ciężkie w zależności od wielkości pochłoniętej dawki.
Zatrucia ostre lekkie. W zatruciach lekkich drogą inhalacyjną już po kilkudziesięciu sekundach występują objawy ze strony dróg oddechowych i narządów wzroku. Występuje wodnisty wyciek z nosa, ślinotok, wzmożone wydzielanie śluzu w drzewie okrzelowym, uczucie ciężaru w klatce piersiowej. Pojawia się lekka duszność wskutek skurczu oskrzeli i zalegania w nich wydzieliny. Szczególnie utrudniona jest faza wydechu. Występuje silne zwężenie Źrenic, nie ustępujące w nocy oraz skurcz akomodacji. Występują bóle w gałce ocznej, łzawienie i przekrwienie spojówek. Objawy ze strony narządów wzroku i dróg oddechowych są początkowo wynikiem miejscowego działania trucizny. W dalszym okresie objawy te są wynikiem miejscowego i ogólnego działania trucizny. Objawy ze strony innych narządów, to nudności, wymioty, częste oddawanie moczu, szybkie męczenie się, ogólne osłabienie, niekiedy drżenie włókienkowe mięśni twarzy, wzmożone wydzielanie potu. Zatruty odczuwa bóle i zawroty głowy, uczucie niepokoju, trudności koncentracji.
W zatruciach lekkich drogą doustną objawy ze strony układu pokarmowego rozwijają się po 10 - 20 minutach, natomiast objawy ze strony innych układów po kilkudziesięciu minutach. Pojawiają się nudności, wymioty, biegunka, bóle w jamie brzusznej. Objawy ze strony dróg oddechowych są mniej nasilone niż przy zatruciu drogą inhalacyjną. Mniej nasilone są również objawy zatrucia ze strony narządów wzroku. Zwężenie Źrenic niekiedy nie występuje.
W zatruciach lekkich przez skórę początkowo występuje drżenie włókienkowe mięśni i wzmożona potliwość ograniczona do miejsca wchłaniania środka trującego. Ogólne objawy zatrucia rozwijają się po kilkudziesięciu minutach, a niekiedy po kilku godzinach. Objawy ze strony dróg oddechowych są zwykle mniej nasilone, niż w zatruciu drogą inhalacyjną, natomiast bardziej nasilone mogą być objawy ośrodkowe i osłabienie ogólne.
Zatrucia ostre średnie. Podobnie jak w zatruciach lekkich pierwsze pojawiają się miejscowe objawy działania trucizny na drogi oddechowe lub przewód pokarmowy. Następnie występują objawy związane z ogólnym działaniem trucizny mające zasadnicze znaczenie dla przebiegu zatrucia. Objawy ze strony poszczególnych układów są odpowiednio bardziej nasilone niż w zatruciach lekkich. Występuje silny ślinotok, spłycenie oddechu, częste wymioty, bolesne parcie na stolec. Pojawia się osłabienie, skurcze, drżenie mięśni, zaburzenia mowy, zaburzenia świadomości.
Zatrucia ostre ciężkie. W zatruciach ostrych ciężkich występuje bardzo silna duszność. Z ust wydziela się obfita piana powstająca w wyniku silnego ślinotoku i nasilonego wydzielania się śluzu w oskrzelach. Obserwuje się niedowład mięśni szkieletowych, drgawki kloniczno - toniczne, bezwolne oddawanie moczu i kału, sinicę. Zatruty traci przytomność, popada w śpiączkę. Nasila się niewydolność oddechowa, po czym następuje ustanie oddechu wskutek porażenia mięśni oddechowych. Zejście śmiertelne może nastąpić w ciągu kilkudziesięciu godzin. Przy wysokich stężeniach środka trującego śmierć może nastąpić w czasie kilku minut.
Po ustąpieniu objawów zatrucia może pozostać uszkodzenie mięśnia sercowego, wątroby, zapalenie wielonerwowe, zaburzenia w sferze psychicznej, obniżenie zdolności do wysiłku fizycznego.
LECZENIE
Leczenie zatruć związkami fosforoorganicznymi rozpoczyna się od podania atropiny i reaktywatorów cholinoesterazy oraz zwalczania niedotlenienia. W dalszej kolejności podaje się w miarę potrzeby leki przeciwdrgawkowe, krążeniowe, antybiotyki i inne.
Pierwsza pomoc. Pierwsza pomoc obejmuje: nałożenie maski i wyniesienie z terenu skażonego, przeprowadzenie częściowych zabiegów sanitarnych, podanie atropiny i obidoksymu (toksatr), oczyszczenie jamy ustnej i nosogardzieli z zalegającego śluzu i wymiocin, sztuczne oddychanie.
Zapobieganie dalszemu wchłanianiu trucizny. Konieczne jest usunięcie nie wchłoniętej trucizny z powierzchni ciała i ewentualnie z przewodu pokarmowego. W tym celu należy usunąć skażoną odzież. Skażoną skórę zmywa się dużą ilością wody z roztworem mydła. Miejsca skażone należy dodatkowo przemyć 5 % roztworem kwaśnego węglanu sodowego, wody amoniakalnej lub monoetanoloaminy z IPP. Skażone oczy przemywać 2 % roztworem kwaśnego węglanu sodowego lub strumieniem bieżącej wody. Ważne jest, aby odkażanie rozpocząć jak najszybciej. Przy zatruciu drogą doustną przytomnym chorym należy podawać kilkakrotnie do picia 1-2 szklanki zawiesiny węgla aktywowanego lub 2 % roztworu kwaśnego węglanu sodu i wywoływać wymioty lub przeprowadzać płukanie żołądka. Następnie podaje się 1 - 2 łyżki siarczanu sodowego w 1 - 2 szklankach wody lub 1 - 2 łyżki oleju parafinowego.
Uwaga ! Nie podawać oleju rycynowego, mleka i alkoholu, gdyż substancje te ułatwiają wchłanianie trucizny.
Podawanie atropiny. W zatruciach lekkich podaje się 1 - 2 mg atropiny domięśniowo. Do czasu utrzymywania się objawów podawanie leku ponawia się co 20 - 60 minut.
W zatruciach średniego stopnia podaje się dożylnie 2 - 4 mg atropiny. Działanie leku przejawia się już po kilkudziesięciu sekundach i narasta w czasie kilku minut. Dalsze podawanie atropiny w dawkach 2 mg dożylnie lub domięśniowo powtarza się co 5 - 10 minut aż do ustąpienia objawów muskarynowych.
W zatruciach ciężkich podaje się 4 - 6 mg atropiny dożylnie lub domięśniowo, a następnie po 2 mg co kilka minut aż do ustąpienia objawów muskarynowych.
Podawanie atropiny przerywa się w przypadku wystąpienia objawów przedawkowania. Takimi objawami są: rozszerzenie Źrenic, przyśpieszenie tętna, uczucie suchości w jamie ustnej, trudności w połykaniu i mówieniu.
Podawanie reaktywatorów cholinoesterazy. Stosuje się pralidoksym, obidoksym i trimedoksym w dawkach od 0,2g do 1g. Najczęściej stosuje się obidoksym (toksogonina) w dawce 0,5g dożylnie lub domięśniowo. W razie potrzeby zastrzyk ponawia się po 2 - 3 godzinach.
Stosowanie toksatru zawierającego atropinę wraz z toksogoniną jest skuteczniejsze w działaniu niż oddzielne stosowanie tych leków.
Zwalczanie niedotlenienia. Główną przyczyną śmierci przy zatruciach związkami fosforoorganicznymi jest ostra niewydolność oddechowa. Dlatego zwalczanie niedotlenienia ma istotne znaczenie w utrzymaniu człowieka przy życiu. Pierwszym niezbędnym zabiegiem jest oczyszczenie jamy ustnej i nosogardzieli z wydzieliny i wymiocin oraz odessanie wydzieliny z oskrzeli. Zabieg ten należy powtarzać w miarę potrzeb. Ułożenie chorego na boku lub też na wznak z głową odchyloną maksymalnie do tyłu zapobiega zapadaniu się nasady języka. Przy występujących oznakach niedotlenienia osoby posiadającej zdolność samodzielnego oddychania należy podawać jej powietrze wzbogacone w tlen (40 -60 % tlenu), z krótkimi przerwami co 20 - 40 minut. W przypadku znacznego osłabienia czynności oddechowej należy powietrze podawać z pewnym nadciśnieniem, na przykład metodą usta - usta, usta - nos, lub za pomocą ręcznego aparatu AMBU. W cięższych przypadkach stosuje się wentylację mechaniczną za pomocą respiratora.
BOJOWE ŚRODKI TRUJ¥CE O DZIA£ANIU PARZ¥CYM
charakterystyka ogólna
W drugiej połowie pierwszej wojny światowej, wprowadzono iperyt siarkowy, który posiadał właściwości uszkadzania skóry i błon śluzowych. Powodował ponadto długotrwałe skażenia umundurowania i sprzętu wojskowego. Skażenia skóry iperytem siarkowym w ilości przekraczającej 1,5 - 2,0 g prowadziły ponadto do wystąpienia ogólnego ciężkiego zatrucia. Pod koniec wojny wprowadzono jeszcze inny środek o działaniu miejscowym podobnym do iperytu siarkowego - luizyt.
Ponieważ obraz zmian miejscowych występujących na skórze i błonach śluzowych po skażeniu tymi związkami przypominał zmiany występujące po oparzeniu termicznym, związki te nazwane zostały „parzącymi”. Nazwa ta utrzymała się do dzisiaj, mimo iż mechanizm działania tej grupy związków trujących nic wspólnego ze zmianami termicznymi nie posiada, a polega głównie na alkilowaniu struktur biologicznych komórki. Właściwą nazwą dla tej grupy związków byłaby nazwa „bojowe środki trujące o działaniu alkilującym”. Zdolność do alkilacji kwasów nukleinowych, szczególnie wyrażona w działaniu iperytu azotowego zsyntetyzowanego w 1931 r., spowodowała zastosowanie tego związku do leczenia chorób rozrostowych i nowotworów.
Pierwsze badania biologiczne związków alkilujących prowadzone były na przełomie XIX i XX wieku. Opisano wówczas zmiany występujące po podaniu śmiertelnych dawek tlenku etylenu i etylenoaminy. W pierwszej połowie XX wieku zebrano dalsze informacje o alkilującym działaniu iperytów, a ponadto zsyntetyzowano i przebadano inne związki alkilujące. Wyodrębnia się 4 grupy związków alkilujących:
iperyt i ich pochodne,
pochodne etylenoaminy,
estry kwasów sulfonowych,
epoksydy.
2.2. Charakterystyka iperytu siarkowego.
Iperyt siarkowy posiada następującą budowę cząsteczki:
CH2 _ CH2Cl
S
CH2 _ CH2Cl
dichlorodietylosiarczek
Spośród różnych siarczków posiadających grupę chloroetylową znaczne działanie toksyczne wykazują tylko te, które zawierają chlor w pozycji beta. Siarczki posiadające tylko jedną grupę chloroetylową w pozycji beta działają dwa razy słabiej, a posiadające obie grupy chloroetylowe w pozycji alfa nie posiadają działania alkilującego. Czysty iperyt siarkowy jest bezbarwnym płynem prawie bez zapachu. Techniczny występuje w postaci ciemnego oleistego płynu o zapachu przypominającym musztardę i czosnek (stąd często używana nazwa: gaz musztardowy). Do zapachu tego człowiek bardzo łatwo przywyka, ponieważ pary porażają zakoñczenia nerwowe. Iperyt siarkowy można wykryć po zapachu od stężenia 0,001 - 0,002 mg/dm3. Jego temperatura wrzenia wynosi +217 0C, w temperaturze +13 0C zestala się, w temperaturze 500 0C rozkłada się całkowicie, jednakże krótkotrwałe podniesienie temperatury (w czasie wybuchu pocisku) do 800 0C nie powoduje jego rozłożenia. Maksymalna koncentracja par iperytu siarkowego przy temperaturze +20 0C wynosi 0,6 mg/l, pary są cięższe od powietrza ponad 5 razy. Iperyt siarkowy słabo rozpuszcza się w wodzie, w temperaturze +20 0C zaledwie 0,7 g/l, natomiast dobrze rozpuszcza się w różnych rozpuszczalnikach organicznych i innych bojowych środkach trujących, a także w gumie i tłuszczach.
Iperyt ulega hydrolizie według reakcji:
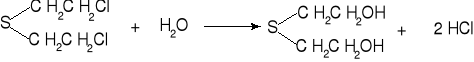
W temperaturze otoczenia +20 0C reakcja ta przebiega wolno ( 50% po około 15-20 godz.), przyspiesza hydrolizę mieszanie oraz podwyższanie temperatury (w temperaturze
100 0C hydrolizuje ponad 95%). Znaczne przyspieszenie hydrolizy uzyskuje się przez usuwanie powstającego kwasu solnego alkalizując środowisko przy pomocy wodorotlenku sodowego itp. Metoda ta ma zastosowanie w usuwaniu iperytu ze spojówek, śluzówek i ran.
Chlorowanie iperytu zachodzi według reakcji:
CH2CH2Cl Cl CH2CH2Cl CHClCH2Cl
S + Cl2 → S → S +HCl
CH2CH2Cl Cl CH2CH2Cl CH2CH2Cl
Monochloroamina B reaguje z iperytem według reakcji:
CH2CH2Cl CH2CH2Cl
S + C6H5SO2N ⋅ NaCl → NaCl + C6H5SO2N = S
CH2CH2Cl CH2CH2Cl
Reakcja ta szczególnie łatwo zachodzi w roztworach wodno-alkoholowych, a także w środowisku kwaśnym.
Reakcja utleniania zachodzi również pod wpływem podchlorynu wapniowego w środowisku wodnym.
CH2CH2Cl CH2CH2Cl
S + CaOCl2 → O = S + CaCl2
CH2CH2Cl CH2CH2Cl
Wymienione wyżej reakcje wykorzystywane są do odkażania iperytu siarkowego.
Toksyczność iperytu siarkowego:
rumieñ - 0,01 mg na 1 cm2 skóry,
pęcherze - 0,1 mg na 1 cm2 skóry,
inhalacja 15-minutowa wywołuje śmierć przy stężeniu 0,1 - 0,2 mg/dm3, lekkie zatrucie przy stężeniu powyżej 0,003 mg/dm3,
stężenie 1 mg/dm3 (powstające po wybuchu pocisków napełnionych iperytem) wywołuje śmierć w ciągu 2 - 3 minut,
15-minutowa ekspozycja powoduje podrażnienie spojówek oczu przy stężeniu 0,005mg/dm3, ciężkie zapalenie spojówek przy stężeniu ponad 0,1 mg/dm3,
dawka śmiertelna naskórna wynosi 50 mg/kg masy ciała.
Charakterystyka iperytu azotowego:
stężenie śmiertelne dla 15 min ekspozycji wynosi 0,2 mg/dm3;
dawka śmiertelna naskórna 20 mg/kg;
rumieñ występuje po dawce powierzchniowej 0,01 mg/cm2 skóry, pęcherze po 0,1 mg/cm2 skóry;
przy stężeniu par 0,1 mg/dm3 po 1-godzinnej ekspozycji występuje rumieñ;
uszkodzenie spojówek występuje po 15 min ekspozycji przy stężeniu par ponad 0,006mg/dm3.
Charakterystyka luizytu
ClCH = CHAsCl2 _ luizyt A,
(ClCH = CH)2AsCl _ luizyt B,
(ClCH = CH)3As _ luizyt C.
reakcja z grupami sulfhydrylowymi:
doustna: dla człowieka 25 mg/kg, dla kotów 15 mg/kg, dla królików 10 mg/kg masy ciała,
inhalacyjna: próg podrażnienia 0,002 mg/dm3 przy 2 min ekspozycji, stężenie śmiertelne przy 15 min ekspozycji 0,15 mg/dm3, przy 2 min ekspozycji 0,9 mg/dm3 ,
działanie par na skórę: rumieñ występuje po 1 godz. przy stężeniu 2 mg/dm3 , pęcherze po 1 godz. przy stężeniu 2,8 mg/dm3; stężenie 0,002 mg/dm3 uszkadza spojówki po ekspozycji 15 min,
działanie kropli na skórę: rumieñ po dawce powierzchniowej 0,2 mg/cm2 skóry, pęcherze po dawce 0,5 mg/cm2 skóry.
MECHANIZM TOKSYCZNEGO DZIA£ANIA ŚRODKÓW TRUJ¥CYCH O DZIA£ANIU PARZ¥CYM
alkilowanie kwasów nukleinowych powodujące zaburzenia biosyntezy białek ustrojowych i podziału komórek,
blokowanie heksokinaz powodujące hamowanie procesu fosforylacji glikozy,
hamowanie esteraz cholinowych,
aktywacja enzymów proteolitycznych,
wiązanie grup sulfohydrylowych (luizyt).
PRZEBIEG ZATRUCIA
LECZENIE
BOJOWE ŚRODKI TRUJ¥CE O DZIA£ANIU DUSZ¥CYM
Charakterystyka ogólna
Mechanizm toksycznego działania
Objawy zatrucia.
leczenie
Bojowe Środki trujące o działaniu ogólnotrującym
charakterystyka ogólna.
mechanizm zatrucia cyjanowodorem i chlorocyjanem
mechanizm zatrucia tlenkiem węgla
objawy zatrucia cyjanowodorem i chlorocyjanem
Objawy zatrucia tlenkiem Węgla.
Leczenie zatrutych cyjanowodorem i chlorocyjanem
ŚRODKI TRUJ¥CE O DZIA£ANIU DRA¯NI¥CYM
charakterystyka ogólna
MECHANIZM TOKSYCZNEGO DZIA£ANIA
silnie wyrażonym działaniem drażniącym w bardzo małych stężeniach, rzędu 0,001 mg/dm3,
wywoływaniem bardziej nasilonych objawów podrażnienia górnych dróg oddechowych niż oczu,
dużą rozpiętością pomiędzy stężeniami wywołującymi silne podrażnienie górnych dróg oddechowych a stężeniami wywołującymi ogólne objawy zatrucia, obrzęk płuc itp.
objawy zatrucia
LECZENIE
ZWI¥ZKI PSYCHOTOKSYCZNE
charakterystyka ogólna
Mechanizm działania toksycznego.
Objawy zatrucia
Leczenie.
BicYKLICZNE ESTRY FOSFOROORGANICZNE
CHARAKTERYSTYKA OGÓLNA
MECHANIZM TOKSYCZNEGO DZIA£ANIA
OBJAWY ZATRUCIA
LECZENIE
FLUOROOCTANY
charakterystyka ogólna
alkohol β-fluoroetylowy;
aldehyd fluorooctowy;
kwas fluorooctowy i jego sole, estry, bezwodniki, amidy;
ω-fluorokwasy tłuszczowe (o parzystej liczbie węgli).
mechanizm toksycznego działania
objawy zatrucia
TRUCIZNY BIOLOGICZNE
JAD KIE£BASIANY (TOKSYNA BOTULINOWA)
Charakterystyka ogólna.
Objawy zatrucia botulinowego (botulizmu).
Inaktywacja toksyny botulinowej.
Leczenie botulizmu.
ENTEROTOKSYNA GRONKOWCA
CHEMICZNE ŚRODKI ROŚLINOBÓJCZE
OGÓLNA CHARAKTERYSTYKA
dokładne usunięcie trucizny (obfite zmywanie skóry wodą z mydłem, płukanie żołądka, usunięcie skażonej odzieży itp.),
zwalczanie hipertermii (oziębianie fizyczne - zawijania zimne, worki z lodem; neuroleptoanalgezja - 2 - 3 cm3 thalamonalu co 3 godziny, ewentualnie 5 mg relanium co 4 godziny)
podawanie dużej ilości płynów w zależności od strat (do 6 dm3 na dobę, w tym 400-500 cm3 40% glukozy),
Metylotiouracyl w dawce 200- 400 mg na dobę,
Sterydy nadnerczowe, szczególnie w przypadku uszkodzenia wątroby (600-1200 mg w przeliczeniu na hydrokortyzon),
W stanach podniecenia haloperidol w dawce 5 mg dożylnie lub domięśniowo lub 10-12 kropli doustnie,
intensywna terapia zachowawcza, objawowa (nie wolno podawać adrenaliny i pochodnych, barbituranów i alkoholu).
POCHODNE KWASÓW FENOKSYKARBOKSYLOWYCH
POCHODNE MOCZNIKA
POCHODNE KWASU KARBAMINOWEGO
TOKSYNY NATURALNE WYSTĘPUJ¥CE W PRZYRODZIE
Trucizny pochodzenia roślinnego
Charakterystyka ogólna
Alkaloidy
Glikozydy
Olejki lotne
Substancje o innej budowie
Leczenie zatruć
Witold Sieñczuk - Toksykologia, PZWL, Warszawa 1990 r.
Claude A. Villee - Biologia, Warszawa 1990 r.
Natalia W. Skinder - Chemia , a ochrona środowiska, Warszawa 1991r.
A. A. Gołubiew, E. I. Lublina, N. A. Tołokoncew, W. A. Fiłow - Toksykologia ilościowa, PZWLek, Warszawa 1978 r.
M. Nikonorow - Pestycydy w świetle toksykologii środowiska, PWRiL, Warszawa 1979r.
Iperyt azotowy posiada następującą budowę cząsteczki:
CH2CH2Cl
N CH2CH2Cl
CH2CH2Cl
trichlorotrietanoloamina
Zsyntetyzowany został w 1931 roku, przy czym nazwa zwyczajowa „iperyt azotowy” dotyczy również związków dwufunkcyjnych (o dwóch grupach alkilujących). Jest jasno-żółtą, oleistą cieczą, bez zapachu, wrzącą w temperaturze 2300C,
temperatura zestalania wynosi - 40C. Nie rozpuszcza się w wodzie, natomiast dobrze rozpuszcza się w rozpuszczalnikach organicznych z wyjątkiem alkoholu etylowego. Maksymalne stężenie par w powietrzu przy 200C wynosi 0,05 mg/dm3, pary te są około 7 razy cięższe od powietrza. Iperyt azotowy wchodzi w reakcje podobnie jak iperyt siarkowy:
Hydroliza iperytu zachodzi bardzo wolno według równania reakcji:
3N (CH2CH2)3 + H2O → HCl ⋅ N (CH2CH2OH)3 + 2HCl ⋅ N (CH2CH2Cl)3
Utlenianie zachodzi według reakcji:
N (CH2CH2Cl)3 + O → O = N (CH2CH2Cl)3
Reakcja z monochloraminą przebiega wolno, efektywność odkażania skóry przy pomocy monochloraminy jest niewielka. Iperyt azotowy jest znacznie trwalszy niż siarkowy, przy czym klasyczne środki odkażające rozkładają go znacznie słabiej. Najlepszymi odkażalnikami iperytu azotowego są silne utleniacze. Spośród dwufunkcyjnych związków jako bojowe środki trujące mogą mieć zastosowanie:
_ HN- 1 - dichlorotrietyloamina:
CH2CH2Cl
N _ CH2CH2Cl
C2H5
_ HN -2 - dichlorodietylometyloamina:
CH2CH2Cl
N _ CH2CH2Cl
CH3
HN-2 charakteryzuje się niską temperaturą zamarzania (-600C), co predysponuje go do używania w zimie.
Toksyczność trichlorotrietanoloaminy:
Luizyt (chlorowinylodichloroarsyna).
ClCH=CHAsCl2
Luizyt zsyntetyzowany został w 1918 roku, był używany w czasie wojny domowej w Hiszpanii oraz wojny włosko-abisyñskiej. Czysty luizyt jest bezbarwnym oleistym płynem, techniczny zabarwiony jest na odcieñ brunatny. Posiada intensywny zapach pelargonii wyczuwalny w bardzo niskich stężeniach, znacznie poniżej działania toksycznego. Luizyt wrze w temperaturze około 200 0C, krzepnie przy - 0,1 0C (techniczny przy - 13 0C). Trudno rozpuszcza się w wodzie , łatwo w rozpuszczalnikach organicznych. Luizyt jest bardziej lotny od iperytów, pary jego są 7 razy cięższe od powietrza.
Luizyt jako pochodna AsCl3 występuje w 3 postaciach:
Jako bojowy środek trujący, ze względu, na najwyższą toksyczność, znalazł zastosowanie luizyt A.
Luizyt łatwo reaguje z szeregiem substancji, nie zawsze jednak produkty reakcji są nietoksyczne:
a) hydroliza
ClCH = CHAsCl2 + H2O → 2HCl + ClCH = CHAsO
Reakcja przebiega szybko (po 20 min hydrolizuje ponad 90 % luizytu), jednakże powstający tlenek chlorowinyloarsyny jest toksyczny i oddziaływuje na skórę podobnie jak luizyt.
b) utlenianie
OH
ClCH = CHAsCl2 + H2O2 + H2O → 2HCl + ClCH = CHAs == O
OH
Reakcja powyższa zachodzi praktycznie ze wszystkimi utleniaczami, a powstający kwas chlorowinyloarsenowy jest nietoksyczny.
OH
ClCH = CHAsCl2 + C6H5SO2N ⋅ NaCl + 3H2O → ClCH = CHAs == O +
OH
+ C6H5SO2NH2 + 2HCl + NaCl
Reakcja ta wykorzystywana jest do odkażania zarówno sprzętu, jak i skóry.
c) reakcja z węglanem sodowym:
ClCH = CHAsCl2 + Na2CO3 → CH ≡ CH + 3CO2 + 3NaCl + Na3AsO3
Reakcję można wykorzystywać do odkażania, szczególnie materiałów tekstylnych, które można gotować. Wyzwalany w czasie reakcji acetylen reagując z azotanem miedzi daje barwną reakcję służącą do wykrywania luizytu.
SH − CH2
| S − CH2
ClCH = CHAsCl2 + SH − CH → 2 HCl + ClCH = CHAs |
| S − CH
OH − CH2 |
HO − CH2
BAL (British Anti - Levisite dimerkaptopropanol)
Nietoksyczny kompleks powstający w tej reakcji wydalany jest z ustroju przez nerki. Luizyt jest jednym spośród bojowych środków trujących o działaniu parzącym, w stosunku do którego istnieje specyficzna odtrutka (BAL). W odróżnieniu od iperytów luizyt posiada właściwości drażniące.
Toksyczność:
Wysoka reaktywność chemiczna związków alkilujących przejawia się zdolnością do tworzenia w środowisku płynów ustrojowych (pH 7,30 - 7,47) cyklicznego jonu sulfoniowego lub amoniowego, który reaguje z dostępnymi alkilacji anionami:
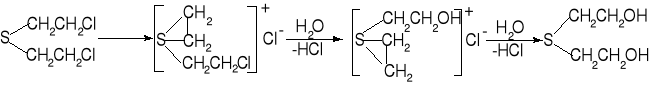
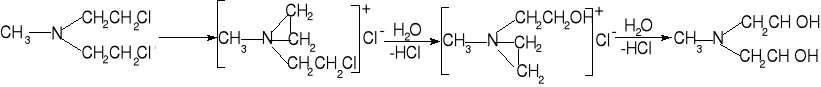
Efektywność alkilowania zależy od pH środowiska i zmniejsza się w miarę jego zakwaszania (np. mała efektywność w odniesieniu do kwaśnych komórek guzów nowotworowych).
Przyjmuje się, że istnieją dwa rodzaje mechanizmów alkilowania składników komórkowych:
- reakcje podstawienia nukleofilowego pierwszorzędowe ( SN1)
Y-
RX → R+ + X- → RY + X-,
- reakcje podstawienia nukleofilowego drugorzędowe ( SN 2)
![]()
gdzie RX - czynnik alkilujący , R - - jon alkilujący, Y- - centrum nukleofiowe.
Reakcje pierwszorzędowe zachodzą w przypadku wolnej jonizacji środka alkilującego i zależą od jego stężenia. Reakcje drugorzędowe przebiegają z przerwaniem wiązania między X i R oraz równoczesnym powstaniem nowego wiązania między jonem alkilującym a centrum nukleofilowym. Przebieg reakcji zależy od stężenia obu tych czynników. Reakcja z ujemnie naładowanymi grupami nukleofilowymi w obrębie cytoplazmy i jądra komórki przebiega nieselektywnie, o jej koñcowej wielkości decyduje stężenie związku alkilującego. Alkilacja dotyczy głównie atomów azotu, siarki i tlenu, tworzących ważne biologicznie grupy: aminowe, tiolowe, hydroksylowe oraz tworzących pierścienie układów heterocyklicznych (np. puryny i pirymidyny). Bardzo łatwo alkilują się reszty fosforanowe nukleotydów, nukleozydy i kwasy nukleinowe. Wrażliwe na środki alkilujące są ponadto białka, enzymy i hormony, głównie polipeptydowe (ACTH, FSH, LH, oksytocyna, wazopresyna, insulina) oraz wolne kwasy tłuszczowe, fosfolipidy i kwasy żółciowe.
Związki alkilujące szczególnie łatwo wiążą się z atomami azotu wchodzącymi w skład pierścieni zasad purynowych i pirydynowych kwasów nukleinowych. Zjawisko to odgrywa podstawową rolę w mechanizmie zatrucia tymi związkami.
Wykazano, że w cząsteczce DNA alkilowaniu ulega najpierw azot N7 guaniny i następnie według malejącej wrażliwości azot N3 i N1 adeniny, azot N1 cytozyny i azot N7 adeniny.
Alkilacja kwasów nukleinowych przez związki alkilujące jedno- i wielofunkcyjne zachodzi podobnie, z tym, że związki wielofunkcyjne - oprócz przyłączania się do azotu N7 guaniny-przyłączają się ponadto do dwu (guanin-7-yl)-pochodnych. Efektem alkilacji azotu N7 guaniny przez związek jednofunkcyjny jest osłabienie lub rozerwanie wiązania między guaniną a resztą cukrową, a następnie oddzielenie guaniny (depurynacja).
Konsekwencją depurynacji jest rozpad wiązania między resztami cukrową i fosforanową. Depurynacja wywołana związkami jednofunkcyjnymi zachodzi wyłącznie w DNA, nie zachodzi w RNA posiadającym trwałą, nieodszczepiającą się 7-alkiloguaninę. Związki wielofunkcyjne wykazują znacznie większą zdolność alkilowania, co wynika ze zdolności tworzenia przez nie śródniciowych i międzyniciowych mostków pomiędzy sąsiednimi cząsteczkami guaniny lub innymi zasadami. TTA może alkilować również DNA poprzez reszty kwasów fosforowych.
Związki alkilujące wielofunfcyjne mogą także mostkować nić DNA z innymi związkami, np. z grupami karboksylowymi kwasu glutaminowego lub asparaginowego białka.
Związane z grupami nukleofilowymi związki alkilujące mogą tworzyć struktury typu „mostek”, „ogon” lub „wiązanie krzyżowe”. Struktury te powodują zaburzenia informacji przekazywanej przez kwasy nukleinowe na drodze wywoływania zaburzeñ replikacji.
Wspomniane wyżej silne odziaływanie związków alkilujących na kwasy nukleinowe i enzymy objawia się efektami świadczącymi o zaburzeniu ich funkcji.
Działanie związków alkilujących na kwasy nukleinowe wywołuje 3 zasadnicze efekty: efekt mutagenny, efekt cytostatyczny i efekt cytotoksyczny. Wystąpienie tych efektów nie zależy w zasadzie od rodzaju środka alkilującego, a głównie jest funkcją jego dawki i reaktywności komórek. Po bardzo małych dawkach, czasowo hamujących mitozę, możliwa jest odnowa komórek często jednak zmienionych, po dawkach średnich zahamowanie mitozy może być trwałe, a po dawkach wysokich wielkość uszkodzeñ zachodzących w komórce, również i w innych strukturach niż kwasy nukleinowe, jest tak duża, że komórka ginie.
Działanie mutagenne może prowadzić do kancerogenezy. Zjawisko to obserwowano w odniesieniu do iperytów i innych środków alkilujących. Działanie cytostatyczne polega głównie na wydłużeniu fazy intermitotycznej, nie obserwowano wpływu środków alkilujących na proces podziału komórkowego.
Działanie cytotoksyczne obserwuje się najczęściej w komórkach szybko dzielących się, jednakże po dużych dawkach środków alkilujących wystąpić może w każdym rodzaju komórek. Podłożem efektu cytotoksycznego są najczęściej: fragmentacja chromosomów, powstawanie jąder gigantycznych i mikrojąder oraz mostkowanie nie pozwalające rozdzielić się chromosomom.
Związki alkilujące posiadają szerokie spektrum działania na żywe struktury. Główne kierunki ich działania to:
Obraz kliniczny zatrucia związkami alkilującymi, jak również obraz ich działania miejscowego, jest wypadkową głównie działania na procesy energetyczne komórkowe i tkankowe. Biologiczne efekty działania związków alkilujących, szczególnie iperytu azotowego, w znacznym stopniu przypominają działanie promieniowania jonizującego.
Właściwość ta została wykorzystana w leczeniu skojarzonym lub uzupełniającym promieniowaniem jonizującym i iperytem azotowym lub jego pochodnymi. Podobieñstwo działania związków alkilujących i promieniowania jonizującego polega głównie na uszkadzaniu lub zmianie struktury kwasów nukleinowych przez oba te czynniki z następowym wystąpieniem efektów cytostatycznych i cytotoksycznych. Różnice w działaniu zależą głównie od sposobu działania na kwasy nukleinowe, różnego oddziaływania na inne struktury komórkowe oraz różnych zdolności oddziaływania mutagennego.
Ze względu na właściwości fizykochemiczne środków trujących o działaniu parzącym, mogą one działać w postaci ciekłej (krople)), par oraz mgieł i aerozoli). Postać działająca zależy od rodzaju urządzenia służącego do ich przenoszenia. Skażenia ciekłymi parzącymi środkami trującymi nastąpić mogą bezpośrednio od wybuchających pocisków, bomb czy głowic rakietowych. Skażenie i zatrucie parami następuje w obrębie wytworzonego obłoku pierwotnego lub wtórnego, szczególnie wtedy, kiedy wytworzone zostały duże powierzchnie terenu skażone płynnymi parzącymi związkami trującymi ( wysoka trwałość iperytów predysponuje je do takiego właśnie sposobu użycia).
Mgły i aerozole wytwarzane mogą być przez specjalne urządzenia, iperyty mogą być mikrokapsułkowane, umieszczone w bombach kasetowych itp. Oddziaływanie tych postaci zbliżone jest do oddziaływania par obłoków pierwotnego i wtórnego.
Działanie na skórę. Związki parzące, ze względu na dobrą rozpuszczalność w tłuszczach, łatwo przenikają przez fizjologiczne bariery ochronne skóry, warstwa rogowa naskórka stanowi pewną niewielką przeszkodę w ich przenikaniu, miejscami najmniejszego oporu są miejsca gruczołów łojowych, potowych oraz mieszki włosowe. Ze względu na powyższe najbardziej wrażliwe są okolice: pachowe, pachwinowe, krocza narządów płciowych, powierzchni wyprostnych przedramion i dłoni oraz okolice o cienkim naskórku: twarz i przestrzenie międzypalcowe. Podwyższona wilgotność skóry czyni ją równieżznaczniebardziej wrażliwą z powodu rozpulchnienia warstwy rogowej. Skażenie kroplowe skóry
środkami o działaniu parzącym powoduje wystąpienie uszkodzenia zbliżonego nieco do obrazu oparzenia termicznego. Od momentu skażenia do czasu wystąpienia pierwszego objawu - rumienia występuje tzw. okres utajenia .Dla iperytów okres ten wynosi od 2 do 12 godzin (średnio 2 - 3 godz ) i zależy od wielkości dawki skażającej. Dla luizytu okres utajania wynosi 15 -20 minut i charakteryzuje się ponadto wystąpieniem swędzenia, a następnie silnego bólu - jest to bardzo ważna wczesna cecha różnicująca. Po okresie utajenia występuje w miejscu skażenia bolesny rumieñ i obrzęk. Obrzęk poiperytowy jest stosunkowo niewielki, poluizytowy znacznie większy niż miejsce skażone i dotyczy głębokich warstw tkanki podskórnej.
Działanie atomu arsenu znajdującego się w cząsteczce luizytu powoduje uszkodzenie śródbłonka naczyniowego oraz blokowanie enzymów cyklu energetycznego. Efektem tego oddziaływania jest wystąpienie licznych wybroczyn w obrębie rumienia, szybko przechodzących w głębokie zmiany martwicze. W kilkanaście godzin po kontakcie w obrębie rumienia pojawiają się pęcherze. Po skażeniu iperytem pojawiają się najpierw w obwodzie rumienia pęcherzyki, które następnie zlewają się w duże, dobrze napięte pęcherze o treści surowiczej. Skażenie luizytem powoduje wystąpienie dużych wiotkich pęcherzy wypełnionych surowiczo-krwistą treścią. Po pęknięciu pęcherzy występują owrzodzenia i nadżerki o różnej głębokości, większe po luizycie. Proces gojenia się owrzodzeñ jest zwykle bardzo powolny (po iperycie 4 - 8 tygodni, po luizycie 2 - 3 tygodnie). Owrzodzenia ulegają z reguły zakażeniom bakteryjnym, a proces ziarninowania jest upośledzony. Powstające blizny są zwykle pozaciągane, przebarwione oraz pokryte cienkim bibułkowatym naskórkiem.
Działanie na oczy. Przebieg uszkodzenia podobny jest do reakcji skóry. Występuje obrzęk i zaczerwienienie spojówek oraz powiek. Pojawiają się szybko punkcikowate, białawe ogniska owrzodzenia i rozpadu. Rogówki ulegają zmętnieniu, czasami z szeregiem mlecznych pasm przedzielających mniej uszkodzoną tkankę. Nasilenie zmian miejscowych osiąga szczyt po 24 - 36 godzinach, gojenie się zmian trwa kilka tygodni. Rokowanie w lekkich i średnio ciężkich uszkodzeniach jest na ogół dobre, ciężkie uszkodzenia dają nieodwracalne zmiany upośledzające widzenie zależne od blizn i zniekształceñ rogówki oraz inne powikłania związane ze zniekształcającym bliznowaceniem powiek.
Działanie miejscowe na drogi oddechowe. Wdychanie par, mgieł lub aerozoli iperytów początkowo nie daje objawów. W krótkim czasie jednak pojawia się ból za mostkiem, chrypka oraz kaszel z odpluwaniem krwawej plwociny, a następnie białawych strzępów tzw. błon rzekomych. Objawy rozwijają się w ciągu 24 - 48 godzin.
Następstwem uszkodzenia nabłonka dróg oddechowych oraz częściowo nabłonka pęcherzykowego są głównie zapalenia o charakterze odoskrzelowego zapalenia płuc - najczęściej dolnych płatów z częstym zwężeniem oskrzeli. Wdychanie par luizytu prowadzić może do wystąpienia toksycznego obrzęku płuc, nie występującego po iperycie.
Działanie miejscowe na przewód pokarmowy. Spożycie skażonego pokarmu lub wypicie skażonej wody, a także przełykanie śliny z rozpuszczonymi środkami trującymi o działaniu parzącym szybko prowadzi do wystąpienia i długotrwałego utrzymywania się zmian chorobowych. Objawy występujące w obrębie przewodu pokarmowego, szczególnie jelit, są wypadkową działania miejscowego oraz ogólnego. Występują kolejno nudności, wymioty, utrata smaku. Pojawiają się owrzodzenia śluzówek jamy ustnej, gardła i przełyku, które przechodząc w zwężenia utrudniają połykanie. Uszkodzenie nabłonka krypt i kosmków powoduje wystąpienie biegunek, często krwawych, prowadzących do odwodnienia i anemii.
Objawy ogólnego zatrucia związkami parzącymi. Dobra rozpuszczalność w tłuszczach sprawia, iż zarówno iperyty, jak i luizyt łatwo wchłaniają się do organizmu poprzez skórę, drogi oddechowe i przewód pokarmowy. Objawy zatrucia ogólnego towarzyszą z reguły zmianom miejscowym. Wchłonięte do organizmu związki trujące o działaniu parzącym znajdują się początkowo w krwiobiegu, skąd szybko znikają. Np. u królików po podaniu dożylnym iperytu siarkowego znakowanego siarką stwierdzono po 20 minutach spadek aktywności we krwi sięgający 90%. Bardzo szybko, bo już po upływie 10 minut, stwierdzono aktywność w moczu. Pozostały w łożysku naczyniowym iperyt siarkowy (około 6%) związany był z plazmą. U szczurów stwierdzono, że 50% dawki całkowitej iperytu siarkowego wydalane jest w przeciągu 6 godzin, 90% po upływie doby, natomiast całkowite wydalanie nastąpiło po 3 dniach. Dystrybucja iperytu azotowego przebiega podobnie. Przechodząc do tkanek iperyty wiążą się z białkiem, głównie z ich grupami tiolowymi oraz alkilują kwasy nukleinowe. Niezwiązana część podlega metabolizmowi (przede wszystkim hydrolizie) i wydalana jest z moczem. Obraz kliniczny zatrucia ogólnego jest wypadkową objawów uszkodzenia narządów i układów zawierających komórki proliferujące. Główne zespoły objawów zależą od uszkodzenia nabłonka przewodu pokarmowego, układu krwiotwórczego i limfopoetycznego oraz związanego z tym stanu septycznego. W 2-3 dni po zatruciu spada gwałtownie liczba płytek krwi oraz limfocytów. Upośledzenie produkcji białek odpornościowych, układu krzepnięcia krwi oraz uszkodzenie śródbłonków naczyñ prowadzi do wystąpienia drobnych wybroczyn szybko zlewających się i przechodzących w septyczne owrzodzenie. Zmiany takie występują w jamie ustnej, płucach, jelicie cienkim, nerkach itp. Występuje dość szybko biegunka, najczęściej krwawa, prowadząca do utraty białka, elektrolitów i wody. Obniżony próg odporności powoduje wystąpienie ciężkiej bakteriemii endo- i egzogennej. Zatrutym wypadają włosy, następuje również zanik komórek rozrodczych. W rozwiniętym okresie zatrucie przypomina postać szpikową choroby popromiennej.
Tabela 2. Charakterystyka działania bojowych środków trujących o działaniu parzącym w zależności od ich stanu skupienia
Stan skupienia bojowego środka |
Droga |
Zasadnicze formy porażenia |
||
trującego o działaniu parzącym |
przenikania |
lekka |
średnia |
ciężka |
1 |
2 |
3 |
4 |
5 |
Para mgła |
Drogi oddechowe |
Nieżyt górnych dróg oddechowych |
Nieżyt górnych dróg oddech. większego stopnia, nieżyt oskrzeli i oskrzelików, odos- krzelowe zapalenie płuc (luizyt) |
Powstawanie błon rzekomobłonicznych w górnych drogach oddechowych, zapalenie płuc odoskrzelowe, rozedma i niedodma ogniskowa, obrzęk płuc (luizyt) |
|
Oczy |
Nieżyt spojówek |
Nieżyt spojówek ropny. Nieżyt spojówek z uszko- dzeniem rogówki bez owrzodzeñ |
Uogólniony nieżyt spojówek z owrzo- dzeniami rogówek, stan zapalno-ropny tkanek około- oczodołowych |
1 |
2 |
3 |
4 |
5 |
|
Skóra |
Rumieñ w okolicach odsło- niętych |
Forma rumie- niowo - pęcherzo- wa na odsłoniętych częściach ciała |
Oparzenia rozwijające się od stadium rumieniowo-pęcherzowego do owrzodzeñ i martwicy na odsłoniętych okolicach ciała. W okolicach osłoniętych odzieżą - lżejsze formy oparzeñ |
|
Przewód pokarmowy |
|
|
Zapalenie błon śluzowych jamy ustnej, przełyku, żołądka |
Kroplisto- ciekły |
Skóra |
Rumieñ |
Rumieniowo- -pęcherzowa forma oparzeñ powierzcho-wnych lub głębokich |
Owrzodzeniowo -martwicze i zgorzelinowe formy oparzeñ
|
|
Oczy |
|
Ropno-martwicze zapalenie spojówek i rogówki |
Martwica rogówki, panoftalmitis |
|
Przewód pokarmowy |
Nieżyt żołądka |
Ostry nieżyt śluzówek jamy ustnej, przełyku, żołądka |
Owrzodzenia w jamie ustnej, przełyku i żołą- dku, krwotoki
|
Tabela 3. Objawy działania bojowych środków trujących o działaniu parzącym na skórę.
Okresy i formy działania |
Iperyt siarkowy |
Iperyt azotowy |
Luizyt |
Kontakt ze środkiem trującym |
Brak działania drażniącego |
Brak działania drażniącego |
Lekkie działanie drażniące (pieczenie, bolesność) |
Okres utajony |
2 -6 godzin |
2 -3 godzin |
15 - 20 minut |
Rumieñ - granice - obrzęk _wybroczyny
- inne
|
dość wyraŹne brak bardzo nieliczne |
dość wyraŹne brak nieliczne
powiększenie mieszków włosowych |
bardzo wyraŹne znaczny liczne i różnej wielkości |
Pęcherze - czas pojawienia się - ilość
- czas gojenia
|
- po około 12 godz. - mnogie, rożnej wielkości
- niezakażone do 3- 4 tygodni
|
- jak po iperycie siark. - drobne, nieliczne
- po 2-3 tygodniach
|
- po 2 do 10 godzin - pojedyncze, duże
- niezakażone do 2 tygodni
|
- pigmentacja |
- ciemnobrązowa |
- brunatna |
- brak |
Okres owrzodzeñ
|
owrzodzenia,płytkie brzegi strome dno blado- sine, wybroczyny
|
mogą nie występować złuszczenia cienkiego strupa
|
owrzodzenia głębokie, kraterowate, dno jaskrawo- czerwone, wybroczyny liczne, krwawienie, znaczna bolesność |
Czas gojenia |
ponad 3 miesiące |
jak po iperycie siarkowym |
przeciętnie 1 miesiąc |
Blizna |
skóra wrażliwa na wtórne uszkodzenia, otoczona rąbkiem pigmentacji |
brak ostrych granic przebarwienia, nadwrażliwość czuciowa skóry |
gruba, gwiazdowata, ściągająca, z mostkami i wypustkami, bez przebarwienia skóry wokół blizny |
Postępowanie w zatruciach i skażeniach iperytami polega na szybkim usunięciu trucizn z powierzchni ciała lub usunięciu ich z przewodu pokarmowego (wymuszone wymioty, płukanie żołądka) oraz na leczeniu wyłącznie objawowym, ponieważ nie są znane specyficzne odtrutki przeciwko tym związkom. W zatruciach i skażeniach luizytem podstawowy schemat postępowania jest podobny jak przy iperytach oraz ponadto stosuje się w leczeniu specyficzną odtrutkę - BAL (British Anti-Levisite) zewnętrznie w postaci maści lub olejowych roztworów oraz wewnętrznie w postaci wstrzyknięć domięśniowych (ampułki 2 cm3 0,1 g). BAL podaje się w dawce 2,5 mg/kg m.c. co 4 godziny przez pierwsze dwa dni, co 6 godzin w trzecim dniu oraz co 12 godzin do koñca leczenia (łącznie 6 - 10 dni). Usunięcia środków parzących z powierzchni ciała i ubrania dokonuje się bezpośrednio po skażeniu przy pomocy znajdującego się w indywidualnym pakiecie przeciwchemicznym, alkoholowego roztworu monochloraminy B. Do roztworu tego dodawany jest środek ściągający i obkurczający naczynia (chlorek cynku) utrudniający wchłanianie trucizny. W razie braku pakietu przeciwchemicznego można użyć 15-20% roztwór monochloraminy B. Odkażenia skóry ze środków parzących można dokonać również przy pomocy 5-10% roztworu diwęglanu sodu, wody utlenionej, 1-2% roztworu nadmanganianu potasu lub słabych roztworów ługów. Powierzchnię śluzówek i ran odkaża się 0,5% wodnym roztworem monochloraminy B lub 5% roztworem diwęglanu sodowego, a spojówki 0,2% wodnym roztworem chloraminy lub 2% roztworem diwęglanu sodowego. Na odkażone miejsca nakłada się jałowy opatrunek. W skażeniach luizytem na odkażone powierzchnie skóry można nałożyć maść z BAL-em. Zmiany miejscowe (pęcherze, owrzodzenia) leczy się podobnie jak oparzenia termiczne stosując jałowe osłanianie zmian, antybiotyki i sterydy miejscowo lub ogólnie. Owrzodzenia spojówek i rogówek wymagają długotrwałego specjalistycznego leczenia mającego na celu niedopuszczenie do wytworzenia się blizn lub zmętnienia w aparacie przeziernym oczu. W przypadku skażeñ inhalacyjnych z uszkodzeniem dróg oddechowych i miąższu płucnego stosuje się głównie antybiotyki i sterydy według ogólnie przyjętych zasad, w celu niedopuszczenia do rozwoju toksycznego zapalenia płuc z następowym powstaniem ich marskości. W większości przypadków skażeñ miejscowych, a z reguły w przypadku zatruć drogą inhalacyjną lub pokarmową rozwija się zespół zatrucia ogólnego.
Postępowanie w tych przypadkach polega głównie na normalizowaniu obrazu krwi obwodowej i zapobieganiu wystąpienia wtórnej infekcji. Z wyboru stosuje się przetaczanie świeżej, pełnej krwi oraz antybiotyki o szerokim spektrum działania. Dodatkowo stosować można środki wspomagające odnowę szpiku kostnego, środki przeciwkrwotoczne, uzupełnianie elektrolitów i białka - w zależności od występujących objawów. Należy podkreślić, że leczenie zatruć środkami parzącymi jest długotrwałe, złożone oraz nie dające często pełnego powrotu do zdrowia.
Jest to grupa bojowych środków trujących, których działanie toksyczne polega na uszkodzeniu i naruszeniu funkcji dolnych dróg oddechowych - zespołu pęcherzyków płucnych.
Najbardziej typowym przedstawicielem środków duszących jest fosgen; analogiczne działanie wykazuje dwufosgen, trójfosgen oraz chlor.
Cl OCCL3 OCCL3
O = C O = C O = C
Cl Cl OCCl3
fosgen difosgen trifosgen
Fosgen jest to bezbarwna, łatwo parująca ciecz o temperaturze wrzenia 8,3oC. W wyższej temperaturze jest bezbarwnym gazem o słabej woni gnijącego siana, łatwo ulegającym skropleniu. Pary fosgenu są około 3,5-krotnie cięższe od powietrza.
Stężenia fosgenu rzędu 0,003 - 0,005 mg/dm3, przy długotrwałym wdychaniu powodują objawy zatrucia. Cl50 wynosi 3,2 [mg min/dm3].
Zatrucie fosgenem następuje w zasadzie wyłącznie przez drogi oddechowe.
Dwufosgen. Cząsteczka dwufosgenu złożona jest z dwu cząsteczek fosgenu. Jest to bezbarwna ciecz o temperaturze wrzenia 127oC. Pary dwufosgenu są około 7-krotnie cięższe od powietrza. Jest znacznie mniej lotny od fosgenu. Toksyczność dwufosgenu jest podobna jak fosgenu. Cl50 wynosi 3,2 [mg min/dm3].
Chlor (Cl). Jest to gaz o barwie zielonożółtej, o gryzącej woni wyczuwalnej już przy bardzo małych stężeniach, około 2,5 razy cięższy od powietrza. W stężeniach rzędu 0,1 mg/dm3 wywołuje silne podrażnienie oczu i dróg oddechowych. Cl50 chloru wynosi 19 [mg min/dm3].
Fosgen z uwagi na charakter fizykochemiczny wnika do ustroju jedynie przez drogi oddechowe. Ulega szybkiemu wchłonięciu przez tkankę płucną, predysponowaną przez swą budowę do wymiany składników gazowych powietrza. Jako dichlorobezwodnik kwasu węglowego ujawnia swą reaktywność już przy pierwszym zetknięciu ze składnikami komórek pęcherzyków płucnych. Reaguje z czynnymi grupami aminowymi i hydroksylowymi białka i cholesterolu błony komórkowej pęcherzyków płucnych, tworząc odpowiednie pochodne węglanowe, np.:
2 białko-NH2+COCl2 → białko-NH-CO-NH-białko+2HCl
2 cholesterol-OH+COOCl2 → cholesterol-O-CO-cholesterol+2HCl
Zmiana struktury białka i cholesterolu pociąga za sobą zmianę półprzepuszczalności błony komórkowej pęcherzyków płucnych i postępującą nekrozę komórek, czego konsekwencją jest przesiąkanie osocza surowicy krwi z naczyñ krwionośnych do wnętrza pęcherzyków płucnych. Wraz z postępującym wysiękiem płucnym zmniejsza się powierzchnia płuc w wymianie gazowej, co pociąga za sobą postępujące niedotlenienie ustroju. Daleko posunięte zmiany w składzie chemicznym białka komórek pęcherzyków płucnych wywołują naturalne dla organizmu procesy proteolizy obcego białka. Jako produkty rozpadu białka pojawiają się we krwi zwiększone ilości aminokwasów białkowych, podatnych w warunkach zatrucia fosgenem na reakcje dekarboksylacji. Wśród tworzących się amin, szczególnie charakterystyczne jest powstawanie histaminy (przez dekarboksylację histydyny - aminokwasu obficie reprezentowanego w białku płuc, hormonu krążenia obdarzonego silnymi własnościami fizjologicznymi.
Stopieñ toksyczności fosgenu określa wartość Lct50= 6,4. Wartość ta jest stała w znacznym przedziale czasu, co związane jest ze znaczną reaktywnością chemiczną fosgenu, zaangażowaniem całej ilości w reakcje bezpośredniej intoksykacji i brakiem zdolności organizmu do naturalnej detoksykacji tego środka trującego.
Małe stężenia fosgenu w powietrzu są wyczuwalne powonieniem, lecz mało charakterystycznie. Wyższe stężenia wywołują podrażnienia śluzówki nosa i gardła (chrząkanie, kaszel). Charakterystyczne objawy zatrucia obserwuje się przy stężeniach i czasach oddychania bliskim wartościom Lct50. W pierwszym okresie występują naturalne odruchy obronne: obok kaszlu, krótki przyspieszony oddech, niepokój i strach skłaniający do ucieczki. Po wyjściu z rejonu skażonego objawy te szybko ustępują i powraca dobre samopoczucie. Jeśli w okresie zatrucia pochłonięta została przez płuca dawka toksyczna wynikająca z iloczynu Lct, okres dobrego samopoczucia jest pozorny, w rzeczywistości jest to okres utajonego działania i trwa zwykle kilka godzin. W tym czasie narasta wysięk płucny. Wraz z nim następuje stopniowe pogarszanie się samopoczucia, wynikające z niedotlenienia ustroju; pojawia się uporczywy i męczący kaszel z obfitą wydzieliną płucną, często krwawą na skutek mechanicznego uszkodzenia pęcherzyków płucnych (przez kaszel), krótki, męczący, przyspieszony bolesny oddech. Spada ciśnienie krwi spowodowane zmniejszeniem objętości krwi (na skutek wysięku płucnego) i wzrostu poziomu histaminy w ustroju (charakterystycznym działaniem histaminy jest rozszerzanie naczyñ krwionośnych). Chory odczuwa chłód, jest bardzo osłabiony; błony śluzowe i skóra przybierają siną barwę. Śmierć następuje po upływie kilku do kilkunastu godzin od wystąpienia pierwszych silnych objawów. Podstawową przyczyną zejścia śmiertelnego jest niedotlenienie organizmu na skutek niewydolności sorpcyjnej płuc, co usprawiedliwia nazwę środków trujących fosgenu jako środków duszących.
Jeśli w ciągu pierwszej doby po zatruciu nie nastąpiło zejście śmiertelne, chory bardzo powoli, w ciągu wielu dni wraca stopniowo do zdrowia, przy czym ogólne osłabienie organizmu i podatność na zakażenia bakteryjne płuc trwa wiele tygodni.
Jeśli zatrucie fosgenem osiągnęło wielkość kilku - kilkunastokrotną wartość Lct50, objawy zatrucia są nie charakterystyczne, a zejście śmiertelne może nastąpić w ciągu pierwszych kilkunastu do kilkudziesięciu minut, na skutek ogólnego porażenia ustroju spowodowanego blokadą enzymów całego układu oddechowego i układu krążenia.
Analogiczne objawy zatrucia i analogiczny stopieñ toksyczności wykazują dwufosgen i trójfosgen, które w warunkach ustroju (prawdopodobnie w procesie katalitycznym) mogą rozpadać się na fosgen
OCCL3 Cl
O = C → 2 O = C
Cl Cl
OCCl3 CL OCCl3
O = C → O = C + O = C
OCCl3 Cl Cl
Pierwsza pomoc przy zatruciu środkami duszącymi polega na maksymalnej ochronie chorego przed wysiłkiem i przemarznięciem - również w okresie utajonego działania, gdzie brak objawów może nie świadczyć o wchłonięciu groŹnej dawki środka trującego. Nie należy stosować sztucznego oddychania i środków pobudzających. Dalsze leczenie wymaga specjalistycznej opieki lekarskiej.
Zwalczanie niedotlenienia. Niedotlenienie tkanek w wyniku niewydolności oddechowej jest głównym objawem zatrucia i przyczyną dalszych zaburzeñ w układzie krążenia, ośrodkowym układzie nerwowym oraz dodatkowym czynnikiem nasilającym obrzęk płuc.
Dlatego stosuje się podawanie mieszanki tlenowo - powietrznej (40 - 60% tlenu). Mieszankę podaje się przez 5 - 10 minut co 15 - 20 minut.
W pierwszym okresie rozwijającego się obrzęku płuc podaje się tlen przez 15 - 20 minut co 10 - 15 minut. Po wystąpieniu sinicy fioletowej mieszankę tlenu z powietrzem podaje się przez cały okres niedotlenienia z przerwami 10 -15 minutowymi co 40 - 50 minut.
Przy objawach sinicy szarej zaleca się stosowanie karbogenu przez 5 - 10 minut (co kilkadziesiąt minut) w czasie których podaje się powietrze wzbogacone tlenem.
Wielu autorów zaleca przy rozwiniętym obrzęku płuc przepuszczanie powietrza wzbogaconego tlenem przez płuczkę z alkoholem etylowym. Pary alkoholu zapobiegają tworzeniu się piany w drogach oddechowych i według niektórych autorów ułatwiają wsysanie się płynu obrzękowego. Inhalację alkoholu etylowego przerywa się co 30 - 40 minut, co zapobiega ogólnemu działaniu alkoholu. Z innych leków, które podobnie jak alkohol zapobiegają pienieniu się płynu obrzękowego, wymienić można tyloxapol (triton WR1339).
W ciężkich przypadkach korzystnie wpływa sztuczna wentylacja pod dodatnim ciśnieniem, po uprzedniej intubacji chorego. Do oddychania stosuje się mieszaninę powietrza z tlenem (40 - 60% tlenu) pod ciśnieniem około 40 cm słupa wody podczas wydechu. W miarę ustępowania obrzęku podczas wdechu należy zmniejszyć. Okresowo odsysa się wydzielinę z drzewa oskrzelowego. Zabieg ten powinien być wykonywany w miarę możliwości krótkotrwale i niezbyt często, ponieważ wytwarzane ujemne ciśnienie w drogach oddechowych sprzyja przesiąkaniu płynu obrzękowego.
Mechaniczna wentylacja poprawia wyraŹnie natlenienie krwi i dzięki temu zapobiega dalszym zaburzeniom czynności organizmu, które są wynikiem hipoksji tkankowej. Ponadto dodatnie ciśnienie podczas wdechu częściowo zapobiega dalszemu przesiąkaniu płynu obrzękowego do światła pęcherzyków płucnych.
Korzystnie w zatruciu fosgenem działają glikosterydy. Podawanie tych leków należy rozpocząć jak najwcześniej i w odpowiednio dużych dawkach. Szczególnie korzystnie wpływa podawanie tych preparatów w aerozolu. Uzyskuje się dzięki temu duże stężenie leku bezpośrednio w chorej tkance.
W razie występowania objawów niewydolności krążenia podaje się Strofantynę (1/8 mg dożylnie). Przy znacznym spadku ciśnienia tętniczego i objawach sinicy szarej oprócz Strofantyny podaje się dożylnie 300 ml 10% roztworu glukozy.
W każdym przypadku zatrucia fosgenem podaje się zapobiegawczo antybiotyki. Przy objawach zapalenia płuc podaje się Penicylinę, Streptomycynę lub inne antybiotyki zależnie od wrażliwości flory bakteryjnej w płucach.
U rannych zatrutych fosgenem zabiegi chirurgiczne należy, w miarę możliwości wykonywać w okresie bezobjawowym lub po ustąpieniu objawów ostrego obrzęku płuc. W okresie obrzęku płuc wykonuje się jedynie niezbędne zabiegi chirurgiczne. Stosowanie do narkozy chloroformu lub eteru jest niewskazane.
Jest to grupa środków trujących, których działanie nie jest związane z zaburzeniami określonego układu biologicznego, a polega na zaburzeniu ogólnych procesów przemian ustrojowych.
Przenikanie związków ogólnotrujących do organizmu odbywa się przede wszystkim poprzez drogi oddechowe, w mniejszym zaś stopniu przez skórę. Jednak w każdym przypadku dostania się ich do organizmu przenikają łatwo do układu krążenia i poprzez krew są rozprowadzane po całym ustroju. W wyższych stężeniach wywołują gwałtowną śmierć przez porażenie układu oddechowego i zahamowanie akcji serca.
Do bojowych środków ogólnotrujących zalicza się: cyjanowodór, chlorocyjan, tlenek węgla.
Cyjanowodór jest bezbarwną bardzo ruchliwą cieczą o charakterystycznym zapachu przypominającym zapach gorzkich migdałów. Pod ciśnieniem normalnym wrze w temperaturze 25,7 oC, krzepnie w temperaturze -13,3 oC.
Gęstość bezwodnego cyjanowodoru w temperaturze 25 oC wynosi 0,682 g / cm3 .
Cyjanowodór jest cieczą zasocjowaną, tworzy asocjaty liniowe o budowie:
...H-C=N...H-C=N...H-C=N...
Cyjanowodór miesza się z wodą w dowolnym stosunku. Rozpuszcza się również w większości rozpuszczalników organicznych (alkohole, węglowodory aromatyczne, estry, chlorowcopochodne węglowodorów). Na powietrzu spala się jasnym fioletowym płomieniem. Ciekły cyjanowodór inicjowany detonatorem wybucha z siłą nitrogliceryny. Mieszaniny cyjanowodoru z powietrzem są wybuchowe ( 5,6-40 % obj.).
Woda powoli reaguje z cyjanowodorem tworząc głównie mrówczan amonowy.
H2O
H - C ≡ N + H2O → HC-NH2 _→ HCOONH4
O
Długotrwałe przechowywanie cyjanowodoru w roztworze wodnym powoduje wypadanie brązowego osadu który, jak stwierdzono jest produktem polimeryzacji.
Chlorowce reagują z cyjanowodorem tworząc odpowiednie chlorowcocyjany:
HCN + X2 → X-CN + HX
Chlorocyjan w warunkach normalnych jest gazem bezbarwnym, który przy ochłodzeniu łatwo skrapla się na bezbarwną, bardzo lotną ciecz, o temperaturze wrzenia 12,5oC. Przy dalszym oziębianiu krzepnie w temperaturze -6,5oC. W wodzie rozpuszcza się z ograniczeniem (7% w temperaturze 15oC). Dobrze rozpuszcza się w rozpuszczalnikach organicznych.
Pod wpływem wody chlorocyjan ulega bardzo powoli hydrolizie do kwasu cyjanowego i chlorowodoru.
Cl-CN + H2O _→ HOCN + HCl
Obok własności ogólnotrujących wykazuje również działanie drażniące. Już w stężeniach 0,003 mg/l drażni boleśnie śluzówkę oczu; przy stężeniach 0,01 mg/1 wywołuje kaszel i mdłości, zapalenie spojówek oka. Iloczyn śmiertelny wynosi:
dla τ = 1 - 5 min. Lcτ50 = 2
τ = 10-20 min. Lcτ50 = 4
Jest więc około dwukrotnie mniej toksyczny od cyjanowodoru.
Mechanizm zatrucia i objawy zatrucia ogólnego są analogiczne jak dla cyjanowodoru.
Tlenek węgla ze względu na charakter gazowy i małą toksyczność nie znalazł zastosowania jako bojowy środek trujący. Jednak w specyficznych warunkach może dojść do zatruć w sytuacjach bojowych i ćwiczebnych, np. gazami spalinowymi silników pojazdów mechanicznych, gazami prochowymi, w których składzie znajdować się może tlenek węgla jako zasadniczy składnik toksyczny.
W warunkach normalnych jest gazem bezbarwnym, bez zapachu i smaku, nieco lżejszym od powietrza. Jego parametry fizyczne są następujące:
- temperatura wrzenia -192oC
-temperatura krzepnięcia -205oC
-temperatura krytyczna -140oC
-ciśnienie krytyczne 3,6 MPa
-gęstość 0,793 g / cm3
Tlenek węgla jest związkiem o własnościach redukujących. Redukuje np. tlenek srebra lub pięciotlenek jodu:
Ag2O + CO → 2 Ag + CO2
J2O5 + 5 CO → J2 + 5 CO2
Jego własności redukujące wykorzystuje się w środkach indykacyjnych (rurki wskaŹnikowe).
Tlenek węgla przenikać może do ustroju wyłącznie przez drogi oddechowe. W płucach ulega szybkiej resorpcji do układu krwionośnego nie wywołując żadnych miejscowych uszkodzeñ tkanek.
Cyjanowodór jako bojowy środek trujący wnika do ustroju głównie przez drogi oddechowe (ze względu na własności fizykochemiczne). Skażenia przez skórę są mało prawdopodobne; skażenia przez drogi pokarmowe są możliwe przy spożyciu wody lub żywności skażonej wolnym cyjanowodorem lub jego solami (cyjankami). W miejscu wnikania do ustroju nie wywołuje żadnych zmian anatomicznych tkanek, ulega łatwo resorpcji do krwi i przez układ krwionośny dociera do tkanek całego ustroju. Wiąże się wiązaniem kompleksowym z enzymami układu cytochromowego o budowie żelazoporfirynowej, znajdującymi się w formie utlenionej:
EFe3+ + HCN → EFe3+ HCN
Z dwóch form tautomerycznych cyjanowodoru
(+) (-)
H - C ≡ N ↔ H - N ≡ C
Formie izonitrylowej (istniejącej w stanie równowagi w ilości ok. 0,6%) przypisuje się znacznie wyższą toksyczność.
Połączenie kompleksowe enzymu z cyjanowodorem traci zdolność katalizowania reakcji utleniania tkankowego w etapie łañcucha oddechowego, przez co zahamowaniu ulegają procesy spalania wewnętrznego. Ponieważ na tej drodze zachodzi ponad 90% wszystkich reakcji oddechowych tkanek, znaczny stopieñ inhibicji enzymów układu cytochromowego prowadzi do znacznych zaburzeñ podstawowych czynności ustroju, aż do zejścia śmiertelnego włącznie. Zatrucie posiada charakter niedotlenienia wewnątrz tkankowego. Krew zatrutego pozostaje w pełni utlenowana. Zahamowane są natomiast procesy odbioru i wykorzystania tlenu przez tkanki.
Inhibicja enzymów jest reakcją odwracalną, stąd przy zatruciach nie śmiertelnych możliwa jest naturalna detoksykacja ustroju.
Procesy detoksykacji po ustaleniu dopływu cyjanowodoru z zewnątrz zachodzą przez rozpad kompleksu i usuwanie cyjanowodoru przez drogi oddechowe oraz na drodze przemian chemicznych:
- hydrolizy do kwasu mrówkowego
HCN + 2 H2O → HCOOH + NH3
- siarkowania do mało toksycznego kwasu siarkocyjanowodorowego (rodanowodorowego)
HCN + S → HCNS
Ostatnia reakcja biegnie przy udziale mono-, i dwusiarczkowych fragmentów białkowych typu: cystyna - cysteina.
Toksyczność cyjanowodoru określa 50% statystycznej śmiertelności wywołanej oddychaniem powietrzem skażonym w warunkach:
C = 1 mg/dm3 przy = 1 min.
C = 0,5 mg/dm3 przy = 2 min.
C = 0,3 mg/dm3 przy = 5 min.
C = 0,2 mg/dm3 przy = 10 min.
Dane te pozostają w dobrej zgodności z iloczynem śmiertelnym Lcτ50 + 0,86 - 0,11 τ. Duży współczynnik czasu świadczy o dość dobrej tolerancji (w porównaniu z innymi środkami trującymi) organizmu, mogącego wiązać cyjanowodór z szybkością odpowiadającą dopływowi 0,11 mg w każdym litrze wdychanego powietrza na minutę.
Dawka toksyczna przez drogi pokarmowe wynosi: LD50 = 1 mg/kg dla cyjanowodoru oraz odpowiednio stechiometrycznie wyższa dla cyjanków.
Tlenek węgla z hemoglobiną krwi tworzy karboksyhemoglobinę - połączenie kompleksowe, blokując miejsce utlenowania hemoglobiny, przez co krew zmniejsza swą zdolność przenoszenia tlenu:
Hb + CO Hb.CO
Reakcja jest odwracalna. Stężenie oksyhemoglobiny i karboksyhemoglobiny we krwi jest wprost proporcjonalne do ciśnieñ parcjalnych tlenu i tlenku węgla w powietrzu wdychanym:
cHb.O2 = k`pO2
cHb.CO = k``pCO
Stosunek znalezionych doświadczalnie wartości k` i k`` wynosi:
k``
= 250
k`
Z czego wynika, że powinowactwo chemiczne tlenku węgla do hemoglobiny jest ok. 250-krotnie większe niż powinowactwo tlenu. Z tego względu tlenek węgla może również wypierać tlen z oksyhemoglobiny w myśl schematu:
Hb.O2 + CO Hb.CO + O2
Nawet przy małych stężeniach CO w powietrzu stopieñ zablokowania funkcji hemoglobiny może być znaczny. Zatrucie tlenkiem węgla jest więc spowodowane niedotlenieniem tkanek poprzez upośledzenie funkcji krwi jako transportera tlenu w ustroju.
Toksyczność tlenku węgla nie daje się wyrazić iloczynem śmiertelnym, brak jest prostej zależności między efektem toksycznym a stężeniem i czasem oddychania skażonym powietrzem. Warunki, przy których dochodzi do 50% statystycznych zejść śmiertelnych są następujące:
c = 30 mg CO/dm3 powietrza przy τ = 2 min.
c = 15 mg CO/dm3 powietrza przy τ = 10 min.
c = 5 mg CO/dm3 powietrza przy τ = 60 min.
c = 3 mg CO/dm3 powietrza przy τ = 200 min.
Jako minimalne stężenie mogące wywołać śmierć przyjmuje się c = 0,7 mg/l. Niższe stężenie wywołują ciężkie objawy zatrucia nie śmiertelne nawet przy dłuższych czasach oddychania.
Istnieje dobra korelacja między efektem toksycznym, a tzw. współczynnikiem zatrucia krwi przez tlenek węgla (k). Wyraża się go jako ułamek stężenia karboksyhemoglobiny we krwi
cHb.CO
k =
cHb
Współczynnik k może być obliczony z ciśnieñ parcjalnych tlenu i tlenku węgla w powietrzu. Jeśli we wzorze stężenia hemoglobiny wyrazić jako sumę stężeñ oksyhemoglobiny i karboksyhemoglobiny i podstawić z wzorów odpowiednie zależności ciśnieñ parcjalnych oraz z wartość liczbową k`` = 250 k`, wówczas:
cHb.CO cHb.CO k``pCO 250 pCO
K = = = =
cHb cHb.O2+cHb.CO k` pO2+k`` pCO pO2+250 pCO
Zależność powyższa jest zgodna z doświadczeniem, pod warunkiem ustalenia się stanu równowagi sorpcyjnej między krwią i powietrzem skażonym, co ma miejsce dopiero po upływie kilku godzin oddychania. Odległe od stanu równowagi, ale toksyczne wartości może osiągać współczynnik zatrucia tlenkiem węgla po stosunkowo krótkim czasie oddychania przy wyższych stężeniach CO, zgodnie z zasadami kinetyki sorpcji. Nawet przy bardzo dużych stężeniach, ale krótkich czasach oddychania (τ < 2`), współczynnik k może nie osiągać wartości śmiertelnych z uwagi na cyrkulacyjny charakter sorpcji.
Zatrucie cyjanowodorem może przebiegać w formie powolnej lub w formie gwałtownej. Jeśli warunki zatrucia zbliżone są do warunków Lcτ50 (lub LD50), w objawach wyróżnić można kilka kolejnych, następujących po sobie stadiów:
1. Stadium objawów początkowych występuje już po 1-2 min. od chwili zetknięcia się z cyjanowodorem: uczucie metalicznego posmaku w ustach, przyspieszony oddech, zawroty głowy, uczucie strachu; jeśli stopieñ zatrucia nie spowoduje wystąpienia dalszych objawów, powyższe stopniowo cofają się, nie pozostawiając po sobie widocznych następstw.
2. Stadium duszności: bolesny przyspieszony oddech, ból w piersiach, duszności, zaburzenia równowagi; z tego stopnia zatrucia pozostaje przez okres kilku dni znaczne osłabienie, ból głowy.
3. Stadium drgawek: utrata równowagi i świadomości, silne drgawki mięśniowe, stopniowy zanik odruchów i reakcji na bodŹce zewnętrzne; przy tym stopniu zatrucia możliwe jest uratowanie zatrutego, ale przy szybkiej interwencji i zastosowaniu odtrutek.
4. Stadium paraliżu następuje dość szybko po stadium poprzednim z objawami stopniowego zaniku akcji serca i akcji płuc, co w krótkim czasie prowadzi do zejścia śmiertelnego. Cały obraz zatrucia trwa od kilkunastu do kilkudziesięciu minut.
Jeśli zatrucie wywołane jest dużą dawką lub dużym stężeniem we wdychanym powietrzu, przebiega forma gwałtowna, przy czym poszczególne stadia zacierają swój obraz, a zejście śmiertelne może nastąpić po upływie kilku minut.
Całkowitą zgodność z doświadczeniem obserwuje się w zależności objawów zatrucia z aktualną w danej chwili wartością k, niezależnie od warunków zatrucia c i τ. Jeśli czas oddychania skażonym powietrzem jest dość długi (kilkadziesiąt minut), obserwuje się pojawianie kolejnych charakterystycznych stadiów zatrucia związanych z wzrastającymi wartościami współczynnika k:
Tabela 4. Objawy zatrucia tlenkiem węgla
k |
Objawy |
0 - 0,1 |
brak objawów |
0,1 - 0,2 |
ból głowy |
0,2 - 0,3 |
uderzenia pulsu w skroniach |
0,3 - 0,4 |
zawroty głowy, zaburzenia równowagi |
0,4 - 0,5 |
przyspieszony oddech, duszność |
0,5 - 0,6 |
zamroczenie, utrata przytomności |
0,6 - 0,7 |
stan śpiączkowy, paraliż układu oddechowego i krążenia, śmierć |
Ponadto charakterystycznym objawem ostatnich stadiów jest ziemiste zabarwienie skóry i błon śluzowych. Przy dużych stężeniach tlenku węgla w powietrzu dochodzi do gwałtownej formy zatrucia, w której zacierają się kolejne stadia i śmierć może nastąpić po kilkunastu minutach.
Z powyższego widać, że zarówno przebieg jak i objawy zatrucia są zbliżone do zatrucia cyjanowodorem. Wiąże się to ściśle z mało swoistą reakcją organizmu na niedotlenienie tkanek, mimo że mechanizm niedotlenienia w obu przypadkach jest odmienny.
Pierwsza pomoc przy zatruciach polega na usunięciu zatrutego z atmosfery skażonej, zastosowaniu w razie potrzeby sztucznego oddychania, a przede wszystkim na zastosowaniu odtrutek. Specyficzną odtrutką na cyjanowodór jest azotyn etylowy lub amylowy podawany w postaci pary przez inhalacje. Podstawą działania odtrutki jest przemiana hemoglobiny krwi w methemoglobinę w reakcji z azotynem
Hb Fe2+ + N3+ → Me+ Hb Fe3+ + N2+
(NO2-) (NO)
Methemoglobina - połączenie żelazoporfiryny z Fe3+ ma zdolność kompleksowego wiązania cyjanowodoru analogicznie jak enzymy układu cytochromowego, przez co zmniejsza się stopieñ blokady tych enzymów. Zachodzi również odblokowanie odwracalnie związanego z enzymami cyjanowodoru w myśl schematu
E.HCN + Met.Hb → E + Met.Hb.HCN
i uwolnienie czynnych katalicznie postaci enzymów zawracanych do naturalnych przemian komórkowych. Ubytek hemoglobiny we krwi, związany z tworzeniem się methemoglobiny nie posiadającej zdolności utlenowania się, w stopniu umożliwiającym skuteczność odtrutki, nie wpływa w sposób dostrzegalnie szkodliwy na funkcje krwi jako transportera tlenu do tkanek.
4.7. LECZENIE ZATRUTYCH TLENKIEM WĘGLA
Przy zatruciach nie śmiertelnych, pierwsza pomoc po usunięciu zatrutego z atmosfery skażonej polega na intensyfikacji naturalnych procesów detoksykacji ustroju drogą usunięcia tlenku węgla z krwi przez drogi oddechowe. W tym celu stosuje się w razie potrzeby środki pobudzające akcję układu oddechowego łącznie ze sztucznym oddychaniem oraz wzbogacenie w tlen powietrza wdychanego. To ostatnie ma na celu przesunięcie stanu równowagi reakcji wiązania przez krew tlenku węgla w kierunku rozpadu karboksyhemoglobiny na oksyhemoglobinę i wolny tlenek węgla desorbowany do powietrza wydychanego.
W trakcie leczenia objawy kwasicy zwalcza się podając 100cm3 8,4% roztworem węglanu sodu. Obrzękowi mózgu zapobiega się przez podanie 100cm3 10% roztworu mannitolu. Podaje się również dożylnie 1g witaminy C. Znaczne podwyższenie temperatury ciała obniża się przez mokre zawijanie lub podawanie odpowiednich leków.
Przebyte zatrucia tlenkiem węgla pozostawiają po sobie po kilku dniach objawy uszkodzenia mózgu. Występuje upośledzenie psychoruchowe, objawy parkinsoidalne, padaczka i porażenia obwodowych nerwów ruchowych. Objawom tym towarzyszy czasem ślepota.
Do tej grupy związków zalicza się: związek CS, adamsyt, dwufenylochloroarsynę, dwufenylocyjanoarsynę oraz związek CR, jakkolwiek ma on również bardzo silne działanie łzawiące. Bardzo silnym działaniem łzawiącym wyróżnia się chloroacetofenon.
Silne właściwości drażniące w małych stężeniach wykazują również metylodichloroarsyna i etylodichloroarsyna. Związki te zaliczane są często do grupy środków parzących z uwagi na właściwości toksyczne zbliżone do luizytu.
Związek CS (dinitryl ortochlorobenzylidenomalonowy): Biała krystaliczna substancja, słabo rozpuszczalna w wodzie, dobrze w rozpuszczalnikach organicznych.
W środowisku alkalicznym ulega hydrolizie, jednakże produkty hydrolizy wykazują również działanie toksyczne. Pod wpływem wodorosiarczanu sodowego traci właściwości toksyczne.
W stężeniach rzędu 0,001 mg/dm3 wywołuje silne podrażnienie dróg oddechowych i oczu. Stężenie 0,005 mg/dm3 uważane jest za granicę wytrzymałości. Cl50 wynosi 25 mg min/dm3.
Adamsyt (DM) chlorek fenarsazyny, difenyloaminochloroarsyna: Jest to żółta lub szarozielona (produkt techniczny) substancja krystaliczna, nierozpuszczalna w wodzie, słabo w alkoholu, benzenie, czterochlorku węgla i dichloretanie, natomiast dobrze w acetonie. Stężenia rzędu 0,001 - 0,002 mg/dm3 powodują silne podrażnienie dróg oddechowych. Stężenie 0,0025 mg/dm3 stanowi granicę wytrzymałości. CL50 wynosi 15 mg min/dm3.
Difenylochlorarsyna: Jest bezbarwną krystaliczną substancją, słabo rozpuszczalną w wodzie i dobrze w rozpuszczalnikach organicznych. Traci właściwości toksyczne pod wpływem środków utleniających (wapno chlorowane, podchloryn wapniowy). W stężeniach 0,001 -0,002 mg/dm3 wywołuje silne podrażnienie górnych dróg oddechowych i w mniejszym stopniu spojówek. Cl50 wynosi 15 mg ⋅ min/dm3. Roztwory difenylochlorarsyny wywołują silne oparzenia skóry.
Difenylocyjanoarsyna (DC): Biała krystaliczna substancja, niemal całkowicie nierozpuszczalna w wodzie, natomiast dobrze w rozpuszczalnikach organicznych. Środki utleniające i alkalia niszczą difenylocyjanoarsynę. Działa drażniąco w stężeniach 0,001 mg/dm3. Cl50 wynosi 10 mg ⋅ min/dm3. Po przeniknięciu do organizmu dużych ilości dwufenylocyjanoarsyny, objawom ze strony dróg oddechowych towarzyszą objawy zatrucia cyjanowodorem powstającym podczas hydrolizy omawianej substancji.
Związek CR Dwubenzo (b,t), (1,4), oksazepina: Jest to ciało stałe o żółtym zabarwieniu, słabo rozpuszczalne w wodzie, dobrze w rozpuszczalnikach organicznych. Wywołuje silne działanie drażniące i łzawiące. Roztwory i pyły związków CR wywołują silne podrażnienie skóry.
Metylodichloroarsyna i etylodichloroarsyna: Są to bezbarwne oleiste ciecze, Źle rozpuszczalne w wodzie, natomiast dobrze w rozpuszczalnikach organicznych. Ulegają zniszczeniu pod wpływem środków utleniających.
Działają silnie drażniąco w stężeniach 0,002 - 0,003 mg/dm3. W dużych stężeniach lub po skażeniu kroplami substancji rozwijają się objawy kliniczne zbliżone do zatrucia luizytem.
Chloroacetofenon jest bezbarwną, krystaliczną substancją nierozpuszczalną w wodzie, dobrze rozpuszczalną w rozpuszczalnikach organicznych. W stężeniach (1 - 3 )* 10-4 mg/dm3 wywołuje silne podrażnienie spojówek. W stężeniach 2*10-3 mg/dm3 wywołuje również działanie drażniące. Wyższe stężenia powodują podrażnienie skóry.
Wszystkie związki z grupy drażniących odznaczają się następującymi właściwościami:
Typowe objawy zatrucia omawianymi związkami związane są z podrażnieniem zakoñczeñ nerwów czuciowych w błonie śluzowej dróg oddechowych i oczu. Duże powinowactwo do tkanki nerwowej związki drażniące zawdzięczają znacznie lepszej rozpuszczalności w tłuszczach aniżeli w wodzie.
Objawy zatrucia środkami o działaniu drażniącym rozwija się po bardzo krótkim okresie utajenia, wynoszącym w zależności od stężenia trucizny od kilkunastu sekund do kilku minut. Pojawia się uczucie pieczenia i drażnienia, bóle w nosogardzieli , kichanie, kaszel, obfity wyciek z nosa, ślinotok, nudności, wymioty. Towarzyszą temu bóle głowy i zębów, bóle w uszach poza mostkiem i niekiedy bóle żołądka.
Podrażnienie górnych dróg oddechowych (zakoñczenia nerwu trójdzielnego) powoduje odruchowe zmniejszenie częstości oddechu i skurczów serca, a podrażnienie dalszych odcinków tych dróg (zakoñczenie nerwu błędnego) - odruchowe pobudzenie ośrodka oddechowego. W wyniku antagonistycznych bodŹców następuje rozkojarzenie czynności oddechowej. W lekkich zatruciach objawy podrażnienia nasilają się w okresie kilkunastu minut po nałożeniu maski przeciwgazowej lub wyjściu ze skażonej atmosfery. Po upływie 1- 3
godzin objawy zaczynają ustępować, a po dalszych kilku lub kilkunastu godzinach następuje całkowite wyzdrowienie.
W ciężkich zatruciach objawy podrażnienia górnych dróg oddechowych są jeszcze bardziej nasilone i męczące. Pojawia się uczucie duszności, występują bardzo silne bóle poza mostkiem, bóle rąk i kręgosłupa. Uczucie duszenia może być tak silne, że zatruty ogarnięty paniką zrywa z twarzy maskę przeciwgazową. Trucizna w dużych stężeniach może powodować odruchowe zatrzymanie czynności oddechowej i serca. Objawom ze strony dróg towarzyszą objawy podrażnienia błony śluzowej oczu zbliżone do tych, jakie obserwuje się przy działaniu związków łzawiących. Niekiedy występują zaburzenia sfery psychicznej.
Objawy ciężkiego zatrucia utrzymują się zwykle kilka godzin. Pełny powrót do zdrowia następuje po 2 - 3 dniach. W wyniku bardzo ciężkiego zatrucia może wystąpić zapalenie krtani, tchawicy, oskrzeli, odoskrzelowe zapalenie płuc, a nawet obrzęk płuc.
Skażenie skóry roztworami lub pyłami środków drażniących powoduje zmiany zapalne, pojawiają się pęcherze wypełnione płynem surowiczym, a następnie owrzodzenia.
W razie zatrucia drogą pokarmową występują bóle w jamie brzusznej, wymioty, biegunka, ogólne osłabienie, zawroty głowy. Dzięki małej rozpuszczalności, a jednocześnie silnemu działaniu drażniącemu (wymioty, biegunka) omawiane związki na ogół szybko zostają usunięte z przewodu pokarmowego i nie wywołują po połknięciu ciężkich, ogólnych objawów zatrucia.
Pierwsza pomoc polega na założeniu maski przeciwgazowej i wyprowadzeniu ze skażonej atmosfery, a następnie przemyciu oczu i przepłukaniu nosogardzieli 2% roztworem wodorowęglanu sodu lub czystą wodą. W miarę możliwości należy zmienić odzież z uwagi na adsorpcję na jej powierzchni dużych ilości środków drażniących. W zależności od nasilenia objawów stosuje się odpowiednie środki przeciwbólowe. Ponadto podaje się środki uspakajające ( Relanium, barbiturany ) i uśmierzające kaszel.
Przy silnym podrażnieniu spojówek dla złagodzenia bólu, oczy można zakropić 2% roztworem nowokainy, 0,3% roztworen lidocainy lub innym roztworem miejscowo znieczulającym. W ciężkich zatruciach podaje się zapobiegawczo antybiotyki. W przypadku obrzęku płuc stosuje się takie same metody leczenia jak w zatruciu fosgenem.
Środki psychotoksyczne, nazwane są również środkami psychozotwórczymi lub halucynogennymi. Poprzez zakłócenie czynności ośrodkowego układu nerwowego i wywoływanie zaburzeñ psychicznych związki te uniemożliwiają wykonanie czynności wymagających dużej sprawności umysłowej, jak np. dowodzenie, prowadzenie pojazdów mechanicznych, prowadzenie celnego ognia.
Związki psychotoksyczne pochodzenia roślinnego i zwierzęcego znane były od dawna. Wykorzystywano je do różnych obrzędów religijnych oraz do wywoływania stanów oszołomienia i halucynacji.
Otrzymanie dietyloamidu kwasu d-lizergowego - przez Stolla i Hoffmanna w 1938 r. przyśpieszyło rozwój badañ nad biochemią ośrodkowego układu nerwowego i chemią leków działających na funkcje psychiczne. Doprowadziło to do syntezy szeregu nowych związków chemicznych o silnym działaniu psychotoksycznym, które mogą być wykorzystane na polu walki jako środki obezwładniające. W ostatnich latach w niektórych grupach społecznych obserwuje się nadużywanie szeregu syntetycznych środków halucynogennych, prowadzące do zależności psychicznej i fizycznej.
Wśród związków chemicznych o działaniu psychotoksycznym wymienia się najczęściej następujące grupy:
- pochodne indolu;
- pochodne kwasu glikolowego;
- pochodne fenotiazyny;
- inne substancje, które mogą być stosowane jako środki psychotoksyczne.
Pochodne indolu. Jest to grupa związków toksycznych obejmująca substancje zawierające w cząsteczce układ indolu. Wiele z tych substancji występuje w roślinach strefy podzwrotnikowej, a część została otrzymana na drodze syntezy. Znanymi związkami z tej grupy są: LSD-25, dimetylotryptamina, bufotenina, psylocybina, harmina, ibogona.
LSD-25 jest środkiem trującym psychotoksycznym otrzymywanym z alkaloidów sporyszu (buławinka czerwona - claviceps purpurea). Sporysz zawiera do 0,1 % alkaloidów, przy czym głównym składnikiem jest ergotoksyna. Najbardziej zbliżonym w budowie cząsteczki do LSD-25 alkaloidem sporyszu jest ergobazyna będąca β-hydroksyizopropyloamidem kwasu
d-lizergowego. Ergobazyna występuje w sporyszu w ilości około 0,01%, a jej zawartość jest bardzo zmienna w zależności od klimatu, nasłonecznienia i sposobu suszenia.
Z chlorku lub estru racemicznego kwasu izolizergowego otrzymuje się działaniem bezwodnej hydrazyny, hydrazyd kwasu lizergowego, który za pomocą kwasu di-p-tolilowinowego rozdziela się na antypody optyczne. Hydrazyd kwasu d-izolizergowego daje pod działaniem kwasu azotowego odpowiedni azydek, który z roztworem dietyloaminy tworzy mieszaninę kwasu
d-lizergowe- go i d-izolizergowego.
LSD-25 jest substancją krystaliczną barwy białej, bez smaku i zapachu, dobrze rozpuszczalną w wodzie, o temperaturze topnienia 83 0C. Zatrucie LSD-25 może nastąpić po przeniknięciu do przewodu pokarmowego, bądŹ przez drogi oddechowe wskutek wdychania aerozolu. Zaburzenia psychiczne mogą wystąpić po przyjęciu doustnie nawet bardzo małych dawek (25-30 μg).
DMT została wyodrębniona z południowo amerykañskich ziół (piptademia peregrina)
Jest to substancja stała, krystaliczna słabo rozpuszczalna w wodzie. Objawy działania toksycznego są podobne do LSD-25. Dawka toksyczna jest jednak znacznie wyższa i wynosi ok. 1mg/kg masy ciała.
Bufotenina występuje w nasionach roślin Piptademia peregrina, grzybie Ammanita mappa oraz w skórze niektórych południowoamerykañskich ropuch i żab. Można ją również otrzymać syntetycznie. Azot grupy aminowej łatwo się czwartorzęduje dzięki czemu tworzą się sole. Bufotenina otrzymana w postaci szczawianu posiada temperaturę topnienia 94oC i jest związkiem łatwo rozpuszczalnym w wodzie. Toksyczność bufoteniny jest wyższa niż DMT i wynosi ok.0,1-0,2 mg/kg. Działanie psychotropowe podobne do LSD-25.
Psylocybina wyodrębniona została z grzyba Psylocybe Mexikana Heim. Występuje również w nasionach Revea Corymboza. Opracowana jest również technologia otrzymywania jej na drodze syntetycznej. Jest substancją stałą, krystaliczną o temperaturze topnienia 173-176oC. Psylocybina jest związkiem fosforoorganicznym, ale nie wykazuje działania blokującego cholinoesterazę. Wywołuje u zatrutego objawy psychotropowe podobne jak LSD-25.
Dawka toksyczna wynosi 0,06-0,08 mg/kg masy ciała.
Harmina została wodrębniona z nasion azjatyckiej ruty stepowej Pegmanum harmala. Jest trucizną drgawkową. W małych dawkach wywołuje drżenie mięśni typu parkinsonoidalnego. W dawkach 2-10 mg/kg wywołuje uczucie kołysania się otoczenia i zmniejszenie wrażliwości na ból.
Pochodne kwasu glikolowego.do pochodnych kwasu glikolowego należą połączenia kwasu glikolowego z alkoholem hinuklidylowym lub hydroksypirymidyną. podstawnikami atomów wodoru w kwasie glikolowym mogą być rodniki fenylowe lub tienylowe. związkiem, który uzyskał zalety bojowego środka trującego jest BZ.
Substancja BZ jest estrem hinuklidylowym kwasu difenyloglikolowego. Jest to substancja krystaliczna, barwy białej, o gorzkawym smaku, słabo rozpuszczalna w wodzie. Jej temperatura topnienia wynosi 165 0C, a temperatura wrzenia 3200C.
Do zatrucia substancją BZ dochodzi najczęściej drogą inhalacyjną przy wdychaniu aerozolu. Możliwe jest także zatrucie drogą pokarmową lub wskutek przeniknięcia przez nieuszkodzoną skórę. Działanie obezwładniające pojawia się przy inhalacji aerozolu w stężeniu 100-200 mg ⋅ min/m3 lub po zażyciu 0,01-0,05 mg/kg masy ciała doustnie.
Pochodne fenotiazyny należą do środków obezwładniających fizycznie. Najbardziej znanym związkiem z tej grupy jest chloropromazyna.
Chloropromazyna jest białym, krystalicznym proszkiem, bez zapachu, o gorzkim smaku, łatwo rozpuszczalnym w wodzie.
Inne związki psychomimetyczne. Meskalina. Otrzymywana jest z kaktusów meksykañskich, np.peyotlu (Anhalonium levinii). Zastosowana doustnie działa uspokajająco, wywołując jednocześnie halucynacje związane z otaczającą rzeczywistością, które są silniejsze przy zamkniętych oczach w ciemności. Objawy psychozy występują najczęściej po przyjęciu 0,4 - 0,7 g meskaliny doustnie.
Haszysz (marihuana). Jest żywicą z włosów gruczołowych kwiatostanów żeñskich konopii indyjskich (Cannabis indica). Zawiera szereg czynnych substancji, m.in. tetrahydrokannabinol, kannabinol, kannabidiol. Wywołuje euforię, uczucie lekkości, omamy wzrokowe i słuchowe, dezorientację w czasie i przestrzeni. W większych dawkach może powodować pobudzenie psychoruchowe. Stan odurzenia trwa kilka godzin i koñczy się snem.
Mechanizm działania toksycznego pochodnych indolu jest niejasny. W oparciu o szereg prac doświadczalnych, wielu autorów wiąże go z działaniem antagonistycznym w stosunku do serotoniny. Inni sugerują, że związki te powodują zaburzenia metabolizmu katecholamin w ośrodkowym układzie nerwowym, prowadzące do nagromadzenia się adrenochromu - związku o silnym działaniu psychomimetycznym.
Substancja BZ łatwo przenika przez barierę krew- mózg i blokuje receptory cholinergiczne w ośrodkowym układzie nerwowym. To działanie antycholinergiczne, podobne do atropiny, leży u podstaw toksycznego działania substancji BZ.
Pochodne fenotiazyny blokują receptory dopaminergiczne i noradrenergiczne w ośrodkach podkorowych mózgu, zwłaszcza w układzie limbiczym, podwzgórzu i układzie siatkowym pnia mózgu. Prawdopodobnie hamują procesy aktywowane przez kompleks jonów wapniowych z kalmoduliną.
Pochodne fenotiazyny łatwo wchłaniają się z przewodu pokarmowego. We krwi ponad 90% substancji występuje w połączeniu z białkami osocza. Przenikają łatwo przez bariery krew-mózg, łożyskową oraz do mleka. W około 70% ulegają wielokierunkowym procesom biotransformacji w wątrobie. W wyniku N-dealkilacji, hydroksylacji aromatycznej, S-oksydacji i N-oksydacji chloropromazyny powstaje około 20 metabolitów, które w postaci wolnej lub w połączeniu z kwasem glukuronowym są wydalane z moczem.
Pierwsze objawy działania LSD-25 pojawiają się po ok. 20-30 minutach od zażycia doustnie; maksymalne działanie występuje po ok. 2-3 godzinach. Objawy zatrucia utrzymują się najczęściej do 1 doby, wyjątkowo trwają kilka dni. LSD-25 wywiera bardzo silne działanie na funkcje psychiczne, ruchowe i wegetatywne.
Zaburzenia psychiczne, występujące pod wpływem LSD-25, polegają na zmianach nastroju, zaburzeniach spostrzegawczości, zdolności myślenia i zaburzeniach osobowości (depersonifikacja). Nastrój jest przeważnie euforyczny, mogą jednak występować naprzemienne okresy euforii i depresji. Występują omamy wzrokowe i słuchowe. Rozwijają się zaburzenia poczucia symetrii ciała. Występuje dezorientacja w czasie, osłabienie, utrudnienie koncentracji uwagi, gonitwa myśli, osłabienie krytycyzmu. Po ustąpieniu halucynacji pojawia się wzmożona senność.
Objawom zaburzeñ w sferze psychicznej towarzyszy równocześnie niezborność ruchów, drżenie mięśniowe. Ponadto obserwuje się „gęsią skórkę” (wskutek skurczu mięśni poruszających włosy), ślinotok, nudności i wymioty, wzrost temperatury ciała, przyspieszenie oddechu, przyspieszenie czynności serca i wzrost ciśnienia tętniczego krwi.
Po przedostaniu się środka trującego BZ do ustroju obserwuje się okres utajenia, wynoszący przeciętnie 30- 60 minut. Szczyt działania występuje po 4-8 godzinach. Natomiast objawy zatrucia mogą utrzymywać się bardzo długo, nawet do 10 dni.
W przebiegu zatrucia obserwuje się dezorientację w czasie i przestrzeni, niepokój ruchowy, niekiedy obniżenie nastroju, czasem nadmierną pobudliwość psychoruchową. Występują omamy wzrokowe i słuchowe. Objawom tym towarzyszy rozszerzenie Źrenic, suchość i zaczerwienienie skóry, suchość śluzówek, wzrost temperatury ciała, przyspieszenie czynności serca i podwyższenie ciśnienia tętniczego krwi. W okresie ustępowania objawów zatrucia może wystąpić wzmożona senność i osłabienie siły mięśniowej.
Pochodne fenotiazyny wywołują w większych dawkach ból głowy, suchość błony śluzowej jamy ustnej, obrzęk błony śluzowej nosa, zaburzenie rytmu serca, zaburzenie orientacji, senność przechodzącą w śpiączkę, drgawki parkinsonoidalne, sinicę. Zgon następuje w wyniku porażenia ośrodka oddechowego. Dawka śmiertelna pochodnych fenotiazyny wynosi 15 - 150 mg/kg.
Objawy zatrucia pochodnymi indolu szybko ustępują po podaniu relanium 5-10 mg domięśniowo. Objawy psychotyczne szybko znosi również frenquel w dawce 20-30 mg.
Wokół zatrutego środkiem BZ należy usunąć z jego zasięgu przedmioty mogące stwarzać zagrożenie dla życia (broñ, ostre przedmioty, leki). Objawy zatrucia ustępują po zastosowaniu fizostygminy. W zależności od ciężkości zatrucia podaje się 0,5 - 3 mg fizostygminy domięśniowo i dawki te powtarza się co 15 - 120 minut. Pobudzenie psychoruchowe można opanować podając relanium lub luminal. Większość autorów uważa za przeciwwskazane podawanie pochodnych fenotiazyny.
Są to bicykliczne estry fosforoorganiczne ( fosforotrioksabicyklooktany ) zwane w skrócie PTBO. Silna toksyczność tych substancji związana jest ściśle z ich budową chemiczną. Najsilniej działającymi związkami wśród bicyklicznych estrów fosforoorganicznych są te, które w pozycji cztery przy węglu posiadają rodnik izopropylowy.
Ogólny wzór cząsteczki
O _ CH2
Y _ P _ O _ CH2 _ C _ Z
O _ CH2
Y - tlen lub siarka, tego podstawnika może też nie być.
Z - bardzo różne podstawniki, z których najbardziej znane to C2H5, i-C3H7 oraz t-C4H9 .
LD50 tych związków wynosi od 0,18 do 500 mg/kg w zależności od rodzaju podstawników Y,Z.
Bellet i Casida stwierdzili, że toksyczność bicyklicznych związków fosforoorganicznych nie jest wynikiem unieczynnienia acetylocholinoesterazy i że nie wywołują one charakterystycznych objawów pobudzenia układu cholinergicznego, typowych dla zatruć związkami antycholinoesterazowymi.
Działanie drgawkotwórcze bicyklicznych związków fosforoorganicznych sugeruje ich interakcję z układem GABA. Porównując działanie dwóch najbardziej aktywnych estrów bicyklicznych: etylowego i izopropylowego ze znanymi antagonistami GABA - bikukuliną i pikrotoksyną na inhibicję presynaptyczną w jądrze klinowym szczura wykazano, że badane estry są efektywnymi antagonistami hamującego działania kwasu gamma-aminomasłowego.
Obecnie powszechnie akceptowana jest hipoteza mówiąca, że bicykliczne związki fosforoorganiczne są antagonistami GABA.
Objawy zatrucia bicyklicznymi fosforanami i tionofosforanami są bardzo podobne do objawów zatrucia związkami typu sarin. Po upływie 2-10 minut od momentu pochłonięcia dawki toksycznej pojawiają się drgawki kloniczno-toniczne o natężeniu proporcjonalnym do jej wielkości. Śmierć następuje w czasie do dwóch godzin.
Znane środki lecznicze stosowane przy zatruciach FOST są nieskuteczne, a wręcz szkodliwe. Czynności drgawkowe osłabiają, a nawet przerywają takie leki jak diazepam i fenobarbital. Działanie przeciw drgawkowe barbituranów i benzodiazepin wydaje się być związane z ich wpływem na kompleks receptora GABA. W zatruciach PTBO fenobarbital podnosi LD50 1.4 razy natomiast diazepam 3.2 razy.
Do fluorooctanów z punktu widzenia toksykologicznego zalicza się wszystkie związki chemiczne, które w biologicznych procesach β-oksydacji kwasów i innych przemianach prowadzą do powstania kwasu fluorooctowego ( jonu fluorooctowego). Są więc nimi przede wszystkim:
Jako bojowe środki trujące mają przede wszystkim znaczenie sabotażowe, mogą znaleŹć (głównie w postaci estrów) także zastosowanie toksyczne.
Do wnętrza ustroju mogą przenikać przez drogi oddechowe, skórę i drogi pokarmowe, nie pozostawiając w miejscu przenikania widocznych śladów. Poprzez krew rozchodzą się po całym organizmie.
Działanie biochemiczne polega na zaburzeniu cyklu przemian kwasów trikarboksylowych (Krebsa) przez swoistą inhibicję akonitazy, enzymu katalizującego przemianę kwasu cytrynowego w kwas izocytrynowy. Substancją inhibitującą akonitazę jest kwas fluorooctowy. Tworzy się on obok kwasu cytrynowego w pierwszej inicjującej reakcji cyklu Krebsa w której miejsce biologicznego kwasu octowego zajmuje kwas fluorooctowy i przy udziale tego samego „enzymu sprzęgającego”.
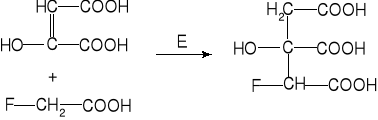
Zgodnie z ogólnym schematem przemian enzymatycznych, biologiczna izomeryzacja kwasu cytrynowego w izocytrynowy biegnie według schematu:
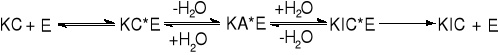
gdzie: KC - kwas cytrynowy;
KA - kwas akonitowy;
KIC - kwas izocytrynowy;
KFC - kwas fluorooctowy.
Jeśli w powyższym schemacie miejsce kwasu cytrynowego zajmie kwas fluorooctowy, powstaje kwas fluorocytrynowy - akonitaza, nie ulegający dalszym przemianom. Cały cykl przemian Krebsa ulega zahamowaniu.
KFC + E _→KFC*E
Ponieważ podstawowe procesy przemian węglowodorów i tłuszczów w ustroju odbywają się przez cykl Krebsa, zahamowanie jego biegu w sposób zasasniczy upośledza funkcję tkanek, co może prowadzić do poważnych zaburzeñ ustroju.
Toksyczność kwasu fluorooctowego (wzorcowego dla grupy fluorooctanów) wyraża się wartością LD50= 2 mg/kg. Toksyczność innych fluorooctanów jest w przybliżeniu stechjometrycznie współmierna do tej wartości ( 2-10 mg/kg, dla estru fluoroetylowego kwasu fluorooctowego nieco poniżej 2 mg/kg.
Interesujące z punktu widzenia toksykologicznego są dane doświadczalne nad toksycznością szeregu kwasów ω-fluorotłuszczowych F(CH2)nCOOH przedstawione w poniższej tabeli w funkcji „n”.
Tabela 5. Toksyczność fluorooctanów
n |
LD50 [mg/kg] |
n |
LD50 [mg/kg] |
1 |
6,6 |
7 |
0,64 |
2 |
60 |
8 |
100 |
3 |
0,65 |
9 |
1,5 |
4 |
100 |
10 |
58 |
5 |
1,35 |
11 |
1,25 |
6 |
40 |
12 |
5,7 |
W tabeli wyraŹnie jest widoczne, że kwasy o „n” parzystym (nieparzystowęglowe) są wielokrotnie mniej toksyczne ponieważ podczas β-oksydacji tworzą kwas fluoropropionowy nie wchodzący do cyklu Krebsa. Drugim interesującym spostrzeżeniem jest znacznie zwiększona toksyczność wyższych parzystowęglowych kwasów ω-fluorokarboksylowych w porównaniu do kwasu fluorooctowego. Przyczyny tego należy dopatrywać się w zwiększonej lipidofilności ułatwiającej przenikanie komórkowe i osiąganie wyższych stężeñ w mitochondriach komórkowych, będących siedliskiem zespołu enzymu cyklu Krebsa.
Charakterystycznym dla działania toksycznego fluorooctanów jest okres utajenia wynoszący zależnie od dawki od 30 minut do 6 godzin. Związany jest z czasem narastania poziomu kwasu fluorooctowego w ustroju, tworzącego się w reakcji enzymatycznej razem z kwasem cytrynowym (przy udziale tego samego enzymu sprzęgającego). Objawami zatrucia po okresie utajenia są stopniowo narastające: niepokój, mdłości, wymioty, ślinotok, drgawki epileptyczno-podobne o nieregularnych nawrotach, skurcze pęcherza i odbytnicy, utrata przytomności, zaburzenia oddychania, zahamowania akcji serca. Śmierć może nastąpić w czasie od 3 godzin do 4 dni zależnie od dawki.
Jad kiełbasiany jest to egzotoksyna produkowana w warunkach naturalnych przez laseczkę jadu kiełbasianego (Clostridium botulinum). Jeśli produkcja ma miejsce w hodowli laboratoryjnej - wówczas stosuje się zazwyczaj nazwę „toksyna botulinowa”. O zatruciu botulinowym człowieka lub zwierząt mówi się wówczas, gdy do organizmu dostaje się zarazek i jego metabolit - toksyna botulinowa. Sam drobnoustrój, tj. laseczka jadu kiełbasianego - powszechna w przyrodzie, szczególnie w glebach - dostaje się do organizmu najczęściej drogą pokarmową i wówczas, co zdarza się rzadziej, może się tam stopniowo namnożyć, wydzielając toksynę o silnym działaniu neuropatogennym. Najczęściej jednak człowiek lub zwierzę ulega zatruciu spożywając zepsuty produkt spożywczy zawierający biotoksynę botulinową z namnożonej bakterii jadu kiełbasianego. Spożycie takiego pokarmu powoduje tzw. botulizm (botulismus) - ciężkie zatrucie wywołane działaniem wchłoniętej neurotoksyny.
Biologiczne działanie jadu kiełbasianego jest bardzo silne. Wrażliwe gatunki zwierząt kręgowych i człowiek reagują na tę toksynę w różnym stopniu, w przypadkach skrajnych porażeniem i śmiercią. Podaje się np. że 1 mikrogram oczyszczonego preparatu zabija 200 000 myszy i może być śmiertelny dla dorosłego człowieka.
Jeśli otrzymaną z hodowli toksynę botulinową podda się dalszemu oczyszczaniu, wówczas z całego botulinowego kompleksu białkowego można wydzielić szczególnie toksyczną cząstkę zwaną „neurotoksyną”, paraliżującą układ nerwowy, a także inną cząstkę „hemaglutyninę”, aglutynującą krwinki czerwone człowieka i zwierząt. Spotykane niekiedy potoczne określenie „botulotoksyna” lub „botulina” dotyczy zazwyczaj takich preparatów jadu kiełbasianego, o których mówi się w kontekście ewentualnego stosowania w działaniu dywersyjno-kryminalnym lub bojowym. Nazwę toksoid (anatoksyna botulinowa) stosuje się wyłącznie do preparatów zdetoksyfikowanych, np. działaniem formaliny, o zachowanych właściwościach immunizacyjnych, wykorzystywanych do produkcji szczepionek.
Jad kiełbasiany jest związkiem natury białkowej o dość znacznym ciężarze cząsteczkowym. Wytwarzany jest przez laseczki jadu kiełbasianego kilku typów biochemicznych i antygenowych, oznaczanych jako Cl. botulinum A, B, C, D, E i F. Uwalniane przez te typy laseczek toksyny mają niemal identyczne działanie farmakodynamiczne, różniąc się jednak nieznacznie budową antygenową. Różnice te są na tyle wyraŹne, iż swoiste surowice lecznicze i diagnostyczne, zawierające przeciwciała skierowane przeciwko poszczególnym typom neurotoksyn botulinowych, mogą zobojętniać wyłącznie ich homologiczne typy.
Powstające w warunkach naturalnego rozwoju różnych typów Cl. botulinum lub w botulinowych hodowlach tych drobnoustrojów, toksyny botulinowe tworzą różnego rodzaju białkowe kompleksy. Kompleksy te mogą być znacznych rozmiarów o ciężarze cząsteczkowym dochodzącym do 900 000 daltonów. Określane są wówczas symbolem „L” lub „LL”, mniejsze kompleksy, o ciężarze od 400 000 do 500 000 - symbolem „M.”, najmniejsze - symbolem „S” tworzą cząsteczki o ciężarze 150 000 daltonów. Taki ciężar wykazują również neurotoksyczne części toksyny botulinowej. Niedawno neurotoksyny laseczki jadu kiełbasianego zostały rozbite na dwie mniejsze części (łañcuchy); łañcuch ciężki (H) o ciężarze zbliżonym do 100 000 i lekki (L) do 50 000 daltonów. Jednołañcuchowe cząstki neurotoksyn, złożone z tych dwóch części mają w początkowym okresie biosyntezy charakter jednolitej cząstki białkowej, ale wykazują słabą toksyczność bądŹ nie są toksyczne. Dopiero „nadgryzione” (nadtrawione) enzymami proteolitycznymi w charakterystycznych punktach, zaczynają wykazywać pełną aktywność neurotoksyczną. I tak np. szczepy Cl. botulinum typu E wytwarzają prawie wyłącznie słabotoksyczne, jednołañcuchowe cząstki neurotoksyny. Takie cząstki protoksyny zwiększają swą toksyczność dopiero po aktywacji silnymi enzymami proteolitycznymi przewodu pokarmowego, np. trypsyny trzustkowej.
Same zarazki - laseczki jadu kiełbasianego - są urzęsionymi, cylindrycznymi tworami długości kilku mikronów, rozwijającymi się tylko hodowlach beztlenowych. Komórki wegetatywne wytwarzają formy przetrwalnikowe - spory (inaczej zarodniki, przetrwalniki). Owalna spora, zniekształcająca komórkę laseczki botulinowej, upodabniając ją do rakiety tenisowej - umożliwia przetrwanie bakterii w niekorzystnych dla nich warunkach fizyko-chemicznych. Spory wytrzymują niekiedy kilkunastominutowe gotowanie, a stopieñ ich termostabilności jest zróżnicowany i zależy od typu drobnoustroju. Jeśli zarodniki znajdują się ponownie w korzystnych dla siebie warunkach, kiełkują do normalnych form wegetatywnych.
U człowieka zatrucie pokarmowe jadem kiełbasianym poczyna objawiać się zazwyczaj po 12 - 48 godzinach od spożycia zepsutego pokarmu albo po kilku - kilkunastu dniach, gdy ilość wprowadzonego jadu nie jest duża, a spożyta potrawa była dostatecznie długo gotowana. Początkowo dominują nieswoiste objawy podrażnienia przewodu pokarmowego (ucisk w żołądku, odbijanie, nudności, wymioty, biegunka). Stopniowo pojawiają się cechy porażenia układu nerwowego - osłabienie, apatia, odurzenie z charakterystycznymi porażeniami gałki ocznej (zaburzenia wzroku, podwójne widzenie, światłowstręt, opadnięcie powiek, zez, rozszerzenie Źrenic, ich nierówność i nieoddziaływanie na światło), a dalej - niedowład - ust., gardła, przełyku z wysychaniem języka, gęstą śliną, zaburzeniem ruchu języka, ochrypłym głosem oraz utrudnienie przełykania. Obok tego występuje maskowatość twarzy, a póŹniej - postępujące osłabienie mięśni tułowia, koñczyn, zwłaszcza górnych i wreszcie niedowład mięśni oddechowych klatki piersiowej i przepony utrudniający i uniemożliwiający oddychanie. Świadomość i temperatura ciała pozostają zazwyczaj niezmienione.
Z praktycznego punktu widzenia zatrucia jadem kiełbasianym można podzielić na dwie grupy: zatrucia naturalne i zatrucia wywołane sztucznie. Zatrucia naturalne rozwijają się najczęściej na skutek spożycia pokarmu skażonego laseczką jadu kiełbasianego, z wytworzoną toksyną botulinową (botulizm pokarmowy). Wyróżnia się ponadto rzadką formę, w której laseczka dostaje się do rany, tam się rozmnaża i wytwarza toksynę wnikającą do krwiobiegu, podobnie jak ma to miejsce przy zatruciu tężcowym (botulizm przyranny). Trzecia grupa zakażenia i zatrucia naturalnego ma miejsce wówczas, gdy do przewodu pokarmowego dostanie się laseczka jadu kiełbasianego, znajdując w nim sprzyjające warunki, rozmnaża się silnie z wytworzeniem toksyny botulinowej. Takie zakażenia, z gwałtownym rozmnażaniem się jadu kiełbasianego w przewodzie pokarmowym, opisywano najczęściej u niemowląt, szczególnie na działanie toksyny (tzw. botulizm niemowlęcy). Niektórzy badacze przypuszczają, że przypadki tzw. zespołów nagłej śmierci niemowląt lub osób dorosłych, mogą mieć związek z przebiegającą skrycie toksoinfekcją botulinową, rozwijającą się w warunkach utrudnionego rozpoznania zatrucia lub zakażenia laseczką jadu kiełbasianego.
Zatrucia jadem kiełbasianym wywołane sztucznie rozważane są teoretycznie w rozmaitych wariantach. Przypuszcza się, że zachodziłyby one wówczas, gdyby rozproszona w powietrzu w postaci aerozolu toksyna botulinowa uległa inhalacji oddechowej i wchłonięciu w płucach. W innym wariancie, skażona opadem toksycznego aerozolu bądŹ innymi sposobami woda mogłaby zostać wypita przez człowieka lub zwierzę i wywołać typowe zatrucie. Wreszcie zawieszony w powietrzu aerozol botulinowy mógłby skażać rozmaite przedmioty, dostawać się do ran, na śluzówki, skórę i wtórnie wywoływać zatrucie. Do sztucznych postaci botulizmu zaliczyć też można wypadki zatruć w trakcie pracy laboratoryjnej z toksyną lub hodowlami Clostridium botulinum.
Konsekwencją omówionych wyżej naturalnych i sztucznych form zatrucia byłyby więc następujące odmiany zatrucia botulinowego: botulizm pokarmowy, botulizm przyranny, botulizm niemowląt oraz mało poznany, a zarazem niebezpieczny ze względu na nienaturalne warunki powstania (atypowe drogi wniknięcia, duże dawki toksyny) botulizm laboratoryjny i inhalacyjny.
Obrona przed atakiem toksyną botulinową, jak również możliwość jej użycia w akcjach dywersyjnych (skażanie wody lub żywnosci ), czy jako środka w jawnej wojnie chemiczno - biologicznej, zależy w dużym stopniu od wytrzymałości tego jadu wobec środowiskowych czynników powodujących jego inaktywację. Od czynników tych zależy również profilaktyka i likwidacja naturalnego botulizmu. Czynniki inaktywacji toksyny botulinowej można podzielić na trzy grupy: fizyczne, chemiczne i swoiste. Do grupy fizycznych należy zaliczyć działanie podwyższonej temperatury, wpływu dziennego światła, promieniowanie ultrafioletowe, podczerwone , jonizujące i nie jonizujące (np. mikrofalowe) oraz ultradŹwięki. Mówiąc o działaniu podwyższonej temperatury, należałoby podkreślić, że proces gotowania w 1000C zdecydowanie niszczy aktywność toksyczną jadu kiełbasianego. Mechanizm unieczynniania toksyny za pomocą wysokiej temperatury polega prawdopodobnie na denaturacji i częściowym rozkładzie cząsteczki białka na proste związki. Czas potrzebny do inaktywacji toksyny w podwyższonej temperaturze zależy od typu toksyny oraz środowiska, w jakim ona się znajduje. Bardziej wrażliwe na działanie podwyższonej temperatury są np. preparaty toksyn oczyszczonych, niż otrzymanych w hodowlach bulionowych. Mniej wrażliwe są preparaty znajdujące się w osłonie rozmaitych składników zawartych w produktach spożywczych oraz w konserwach pochodzenia roślinnego i zwierzęcego. Z badañ różnych autorów nad działaniem podwyższonej temperatury na białko toksyny wynika, że 800C jest temperaturą graniczną, w której inaktywacja toksyny następuje dość szybko, w granicach 4 - 10 min. Poniżej tej temperatury, a więc w granicach 50 - 600C, inaktywacja jest powolna, w ciągu kilku - kilkunastu godzin, a nawet paru dni. W temperaturze 1000C, osiąganej podczas gotowania wody , inaktywacja następuje w ciągu 2 min., przy czym największy spadek miana toksyny ma miejsce już w pierwszej minucie gotowania. Czas ten może się jednak wydłużyć w przypadku toksyny znajdującej w niektórych produktach spożywczych, zawierających rozmaite osłaniające składniki cukrowcowe, solne lub białkowe. Z praktycznego punktu widzenia gotowanie produktu spożywczego lub wody, podejrzanych o obecność toksyny botulinowej, powinno trwać 10 - 30 minut.
Wpływ światła na rozkład toksyny botulinowej jest raczej niewielki. Dotyczy to zarówno światła rozproszonego, jak i ultrafioletu. W dostępnym piśmiennictwie brak jest informacji o wpływie światła podczerwonego.
Nie spotkano również danych pozwalających określić wpływ promieniowania mikrofalowego i jonizującego na inaktywację toksyny. Należałoby spodziewać się działania ultradŹwięków na rozpad toksyny, ale również na ten temat brak jest przekonywujących informacji.
W grupie czynników chemicznych inaktywacji toksyny botulinowej wymienić można związki (kwasy i zasady) wpływające na odczyn środowiska oraz związki utleniające, np. zawierające czynny chlor, jod, nadmanganian potasu i ozon. Trzeba też wymienić związki denaturujące białko, a więc np. alkohole fenol i jego pochodne.
Odnośnie zmian odczynowości środowiska wiadomo, że toksyny botulinowe wytrzymują wahania pH w granicach od 3 do 8. Silna alkalizacja ( powyżej pH 8) lub silne zakwaszenie (poniżej pH 3) wymagałoby zastosowania znacznie stężonych roztworów zasad lub kwasów, co z praktycznego punktu widzenia ograniczałoby możliwości stosowania tych środków w żywności i wodzie . Podobnie przedstawia się sprawa z roztworami alkoholowymi i fenolowymi. Natomiast związki te mogłyby mieć znaczenie w odkażaniu powierzchni rozmaitych przedmiotów, np. naczyñ służących do przechowywania materiałów toksycznych, bądŹ jako środki niszczące tylko toksyczne materiały. Inna grupa związków utleniająca - zawierających czynny chlor, jod lub ozon - może być używana do inaktywacji toksyny w wodzie.
Trudniejszym zadaniem jest odkażanie materiałów skażonych laseczkami jadu kiełbasianego i ich sporami. O ile powszechnie stosowane środki chemiczne, służące do zabijania bakterii oraz fizyczne sposoby dezynfekcji (promienie ultrafioletowe lub gotowanie) niszczą wegetatywne formy laseczki jadu kiełbasianego, o tyle zabicie spor przedstawia pewne trudności. Z praktycznego punktu widzenia z czynników fizycznych wchodziłoby tu w rachubę unieczynnienie materiałów zawierających spory w autoklawie pod ciśnieniem 0,15 Mpa w czasie pół godziny, bowiem niektóre spory wytrzymują nawet kilkugodzinne gotowanie pod ciśnieniem atmosferycznym. Z czynników chemicznych można stosować zanurzanie materiału ze sporami w roztworze lizolu bądŹ 70% alkoholu na 2 -5 godzin.
Do grupy czynników swoistej inaktywacji zalicza się specyficzne surowice antytoksyczne, blokujące i neutralizujące biologiczne centra aktywne toksyn botulinowych. W zasadzie działanie neutralizacyjne antytoksyn obejmuje jedynie układy homologiczne , tzw. surowica - B działa tylko na toksynę botulinową B, antymieszaniny surowic antytoksycznych A, B, C, D, E i F.
Zamieszczone wyżej uwagi i spostrzeżenia wykorzystuje się w praktyce w trakcie postępowania leczniczo - profilaktycznego w naturalnych zatruciach botulinowych oraz obronnego (zabiegi sanitarne i specjalne) w ogniskach masowego zakażenia toksyną botulinową.
Leczenie botulizmu jest nadal problemem bardzo trudnym, pomimo znacznych postępów medycyny w tym zakresie. Efekt terapeutyczny zależy od wchłoniętej przez organizm dawki toksyny, szybkości ustalenia rozpoznania klinicznego i laboratoryjnego oraz terminu wkroczenia z pomocą medyczną.
W wypadku pojawienia się zaburzeñ oddechowych najważniejszym elementem jest stosowanie kontrolowanego, sztucznego oddechu. Respiracja musi być utrzymywana do momentu aż chory zacznie sam oddychać. Trwa to niejednokrotnie, zwłaszcza w ciężkich postaciach zatrucia, nawet do miesiąca i dłużej.
Skuteczne postępowanie przy botuliŹmie musi się wiązać z jak najszybszym usunięciem toksyny i laseczki jadu kiełbasianego z organizmu chorego. Jest więc stosowane płukanie żołądka, podawanie środków działających przeczyszczająco, wreszcie - w przypadku botulizmu przyrannego - chirurgiczne opracowanie rany. Antybiotyki podaje się jedynie w tych przypadkach, gdy w organizmie znajdują się laseczki jadu kiełbasianego, usadowione w przewodzie pokarmowym lub w ranie, zwłaszcza w przypadkach botulizmu niemowlęcego lub przyrannego. Stosuje się wówczas preparaty działające na bakterie gram-dodatnie. Jak wiadomo, antybiotyki nie działają na samą toksynę botulinową.
Głównym środkiem terapeutycznym, który powinien być zastosowany jak najszybciej, jest swoista, wieloważna, antytoksyczna surowica przeciwbotulinowa wiążąca swoiście i neutralizująca jad krążący w ustroju chorego. Surowica powinna być wieloważna, gdyż zazwyczaj nie ma możliwości szybkiego oznaczenia typu toksyny botulinowej, która wywołała zatrucie. Jeśli taka ewentualność zaistnieje, wówczas można przejść na podawanie, swoistych surowic przeciwbotulinowych dla typu A, B, E czy F (chorobotwórczych dla ludzi i zwierząt), typu C (chorobotwórczych głównie dla ptactwa) lub typu D (patogennego przede wszystkim dla bydła). Pamiętać należy, że produkowane obecnie surowice są pochodzenia zwierzęcego, najczęściej otrzymywane od koni uodparnianych toksoidem botulinowym, grożą więc powstawaniem powikłañ, np. choroby posurowiczej. Najlepsze byłoby podawanie przeciwbotulinowej surowicy pochodzenia ludzkiego, a więc od krwiodawców szczepionych toksoidem botulinowym. Surowice takie w chwili obecnej są praktycznie niedostępne i - choć przyszłość leczenia botulizmu powinna się na nich opierać, to bardziej konkretnym wydaje się przeprowadzenie badañ nad odpowiednim oczyszczeniem surowic zwierzęcych oraz otrzymaniem oczyszczonych antytoksycznych globulin przeciwbotulinowych od kilku różnych gatunków zwierząt.
W leczeniu zatrucia jadem kiełbasianym surowica przeciwbotulinowa podawana jest w dużych dawkach i najczęściej długotrwale. Wiadomo, że immunoglobuliny antytoksycznych przeciwciał surowiczych mogą inaktywować jedynie toksynę wolno krążącą w ustroju, nie neutralizują natomiast cząstek jadu, które uległy związaniu z odpowiednimi receptorami tkanek ustrojowych i wywołały charakterystyczny efekt neuropatogenny. W literaturze spotyka się również doniesienia o możliwości stosowania środków działających antagonistycznie w stosunku do toksyny botulinowej, zwłaszcza cholinomimetycznych, ponieważ zatrucia jadem kiełbasianym powoduje blokowanie działania neurotransmitera acetylocholinowego na synapsach zakoñczeñ nerwowych płytki nerwowo-mięśniowej. Opisywano podawanie środków cholinomimetycznych i antagonistycznych w doświadczalnym botuliŹmie zwierząt, a także próby stosowania tych środków w leczeniu zatrutych ludzi. W tym celu stosowano m.in. 4-aminopirydynę lub 3-, 4-dwuamino-pirydynę, guanidynę i germinę. Niektóre z nich grożą powikłaniami i na ogół nie spełniały nadziei, jaką w nich pokładano.
Profilaktyka botulizmu.
Szczególny nacisk powinien być skierowany na uświadomienie konieczności szybkiego orientowania się o grożącym zatruciu, bowiem skuteczność postępowania leczniczego zależy w sposób zasadniczy od czasu zneutralizowania i usunięcia toksyny z ustroju. Celowi temu służy m.in. tzw. ekspresdiagnostyka, to jest szybkie metody polowej i laboratorylnej detekcji, indykacji i identyfikacji toksyny.
Swoista profilaktyka zatrucia jadem kiełbasianym polega na szczepieniach anatoksyną (toksoidem). W światowym piśmiennictwie przedmiotu opisywane są liczne badania nad otrzymywaniem poliwalentnego toksoidu przeciwbotulinowego, który mógłby mieć zastosowanie: w laboratoriach pracujących z jadem kiełbasianym; w środowiskach i na terenach, gdzie szczególnie często występują zatrucia oraz w tych wszystkich warunkach obrony cywilnej i wojskowej, w których zaistniałoby uzasadnione niebezpieczeñstwo zastosowania przez nieprzyjaciela toksyny botulinowej jako bojowego środka chemicznego. Szczepienie toksoidem botulinowym, podobnie jak toksoidem tężcowym, pozostawia długotrwałą odporność antytoksyczną, utrzymującą się co najmniej przez kilka lat.
W sytuacjach doraŹnych należy przewidzieć profilaktyczne stosowanie surowicy przeciwbotulinowej, przede wszystkim w wypadkach podejrzenia o spożycie skażonego pokarmu lub zagrożenie innymi formami zatrucia.
Jest to egzotoksyna produkowana przez gronkowce. Znane są cztery typy antygenowe tego jadu: A, B, C, D. Pod względem budowy chemicznej są to proteiny proste. Najlepiej przebadany jest typ B. Otrzymano go w stanie wysokiej czystości.
W porównaniu z toksyną batulinową enterotoksyna B jest bardziej stabilna. Rozkłada się dopiero powyżej 30 min gotowania. Enterotoksyna B wywołuje efekt chorobowy po dostaniu się do organizmu drogą pokarmową lub oddechową. Zatrucie objawia się gwałtownymi symptomami ogólnymi i ze strony układu pokarmowego. Okres inkubacyjny wynosi od 0,5 do 6 godzin. Organizm zostaje całkowicie obezwładniony na okres 24 godzin. Ryzyko śmierci jest na ogół niewielkie (do 5%).
Chemiczne środki roślinobójcze są to substancje stosowane w rolnictwie do niszczenia chwastów lub ułatwiania zbiorów. Oddziaływanie środków roślinobójczych może powodować opadanie liści, wysychanie całej rośliny, przyspieszenie lub zwolnienie wzrostu, opadanie kwiatów itp. Na podstawie głównego efektu działania środki roślinobójcze podzielono na grupy:
Herbicydy. Są to substancje dezorganizujące wzrost i metabolizm roślin i doprowadzające do ich zniszczenia. Herbicydy mogą być selektywne - niszczące tylko niektóre rośliny lub totalne - niszczące wszystkie gatunki roślin; mogą oddziaływać kontaktowo lub systematycznie po wniknięciu do rośliny; wchłaniać mogą się z liści lub z gleby. Do herbicydów zaliczane są także syntetyczne regulatory wzrostu roślin, tzw. heteroauksyny, w małych dawkach przyspieszające wzrost roślin, w dużych - powodujące ich więdnięcie; pod względem chemicznym herbicydy są najczęściej pochodnymi węglowodorów, związków nitrowych, fenoli, aromatycznych kwasów karboksylowych, kwasów aryloksytłuszczowych, amin i tiazyn.
Defolianty. Są to substancje powodujące opadanie liści. Mechanizm ich działania przypomina działanie hormonów roślinnych. Małe dawki defoliantów polepszają rozwój liści, duże powodują ich niszczenie i działają podobnie jak herbicydy. Do defoliantów zalicza się: azotniak, chlorek cynku, sole amidu kwasu cyjanowego, chlorany i borany oraz niektóre estry kwasu monochlorooctowego.
Desikanty. Powodują szybkie żółknięcie i wysychanie liści lub całych roślin. Należą do nich sole kwasu rodanowodorowego i tiocyjanowego, pentachlorofenolan sodowy oraz niektóre herbicydy i defolianty.
Arborycydy. Sa to związki typu herbicydów używane do niszczenia roślin zdrewniałych, przyspieszają one także usychanie.
Środki roslinobójcze mogą być stosowane do niszczenia zasiewów roślin uprawnych, a także do niszczenia szaty roślinnej w celu utrudnienia maskowania, zwiększenia skuteczności działania środków zapalających, w celu utrudnienia działañ partyzanckich itp.
Środki roślinobójcze, głównie defolianty i herbicydy, używane były masowo w wojnie wietnamskiej w latach 1961 - 1966. Na terenach skażonych obserwowano występowanie bardzo licznych zatruć ludzi i zwierząt, głównie wskutek spożywania zatrutych produktów roślinnych i wody.
Celem zwiększenia toksyczności trucizn roślinnych do stosowania opracowano ich mieszanki:
Mieszanka purpurowa:
-kwas 2,4-D 50 %
-kwas 2,4,5-T 30 %
-ester izobutylowy kwasu 2,4,5-T 20 %
Mieszanka pomarańczowa:
-kwas 2,4-D 50 %
-kwas 2,4,5-T 50 %
Mieszanka biała:
-kwas 2,4-D 80 %
- picloram 20 %
Mieszanka niebieska: - kwas dimetyloarsenowy
Środki niszczenia roślin różnią się znacznie budową chemiczną i toksycznością. Mechanizm oddziaływania toksycznego jest różny dla poszczególnych grup związków, z których ważniejsze będą omówione poniżej.
DiNITROALKILOFENOLE Związki te łatwo wchłaniają się przez drogi oddechowe, skórę i przewód pokarmowy. Nasilenie działania toksycznego dinitroalkilofenoli wzrasta wraz ze wzrostem temperatury otoczenia (wprowadzono zakaz pracy z tymi związkami w temperaturze powyżej 250). Bardzo powoli metabolizują do mono- i diaminopochodnych, które wydalane są z moczem w postaci sprzężonej z kwasem glukuronowym (ostre objawy po jednorazowym zatruciu mogą utrzymywać się nawet do kilku tygodni).Związki te hamują procesy oksydacyjnej fosforylacji, pobudzają glikozę często aż do całkowitego zniknięcia glikogenu w wątrobie i mięśniach oraz wybitnie pobudzają przemianę materii.
Objawy zatrucia występują po kilku minutach od wchłonięcia trucizny. Występuje niepokój, osłabienie, podwyższenie temperatury ciała nawet powyżej 410C, zaczerwienienie twarzy, zlewne poty, pragnienie nudności, wymioty i biegunka, a następnie drgawki kloniczno-toniczne, zapaść i śpiączka. Obserwuje się również uszkodzenie wątroby, nerek, mięśnia sercowego, methemoglobinemię i żółtaczkę hemolityczną, rozwija się kwasica metaboliczna. Wzrost podstawowej przemiany materii może sięgać do 400%.
Pochodne kwasów fenokarboksylowych posiadają wzór ogólny ArO(CH2)nCOOH. Aktywność kwasów fenokarboksylowych zależna jest od budowy podstawnika aromatycznego i długości łañcucha alifatycznego. Do najlepiej poznanych należą kwasu fenoksyoctowe zawierające w pierścieniu aromatycznym chlor i grupy metylowe. Aktywność pochodnych wzrasta w szeregu kwasy < sole kwasów < estry. Orientacyjna dawka śmiertelna dla człowieka przy podaniu doustnym wynosi około 10g. Ostre zatrucie manifestuje się działaniem narkotycznym oraz wzmagającym przemianę materii. Najpierw występuje pobudzenie psychoruchowe i drgawki, a następnie śpiączka i śmierć. Leczenie zatruć jest wyłącznie objawowe ( podobne jak w zatruciach dwunitroalkilofenolami).
Pentachlorofenol.
Pentachlorofenol (PCP) stosowany może być jako herbicyd, defoliant, insektycyd oraz fungicyd. £atwo wchłania się do organizmu. Mechanizm toksycznego działania polega powodowaniu zaburzeñ procesów fosforylizacji i przemiany materii. Działa drażniąco na skórę i błony śluzowe. Przy wielokrotnym działaniu powoduje uszkodzenie spojówek, trądzik i czyraczość. Bardzo wolno metabolizuje i kumuluje się w organizmie. Dawka LD50 dla szczurów wynosi 210 mg/kg per os. W ostrych zatruciach występuje podrażnienie śluzówek i spojówek, nudności, duszność z przyspieszeniem oddechu, zlewne poty, pragnienie, ślinotok, podwyższenie temperatury oraz osłabienie mięśniowe. Obserwuje się ponadto hyperglikemię oraz cukromocz. Niekiedy występuje toksyczny obrzęk płuc.
Leczenie zatruć PCP jest wyłącznie objawowe (podobnie jak w zatruciu dwunitroalkilofenolami).
Pochodne mocznika (diuron, linuron, monuron) mają bardzo duże zastosowanie jako herbicydy. Związki te są bardzo mało toksyczne (np. dla diuronu DL50 dla szczura wynosi 3,4 g/kg per os). Utrzymują się bardzo długo w glebie (1 - 2 lata). Ostre zatrucia zwierząt doświadczalnych charakteryzują się zaburzeniami ze strony ośrodkowego układu nerwowego, jak: pobudzenie a następnie obniżenie aktywności ruchowej, śpiączka, drgawki. Leczenie zatruć tymi związkami jest objawowe.
Związki tej grupy stosowane mogą być jako insektycydy (sevin, karbotox, vapam, propoksur) oraz jako herbicydy (profam, chlorprofam, chlorbufam). Należą do związków hamujących czynność esterazy acetylocholinowej. Działanie ich jest krótkie, ponieważ łatwo ulegają rozkładowi w organizmie. Herbicydy karbaminianowe są mało toksyczne (LD50 dla szczurów wynosi dla profamu 1,0 g/kg, dla chlorprofamu 3,8 g/kg, a dla chlorbufamu 5,9 g/kg per os). Objawy zatrucia są zupełnie podobne do objawów wywołanych przez związki fosforoorganiczne. Odróżnienie zatrucia karbinianami i związkami fosforoorganicznymi nie jest możliwe ani na podstawie objawów klinicznych, ani na ocenie aktywności esterazy acetylocholinowej. Jedyną wskazówką, stwierdzaną jednakże ex post, że nastąpiło zatrucie karbaminianami różni się od leczenia zatruć związkami fosforoorganicznymi niemożnością stosowania oksymów, które są całkowicie nieskuteczne, a nawet mogą pogłębiać przebieg zatrucia. Okoliczność powyższa oraz trudności w rozpoznaniu rodzaju zatrucia były podstawą koncepcji syntezy wysokotoksycznych karbaminianów, potencjalnych bojowych środków trujących (dla niektórych z nich DL50 dla myszy wynosi 0,005 - 0,05 mg/kg i.v.).
Podstawą leczenia zatruć karbaminianami jest atropinizacja i intensywna terapia zachowawcza. Jeśli nie można ustalić, która grupa związków wywołała zatrucie, należy rozpoczynać leczenie wyłącznie atropiną. W razie podania w takim przypadku oksymów (częste postępowanie rutynowe), dalsze ich stosowanie należy uzależnić od badania wzrostu aktywności esterazy acetylocholinowej.
HERBICYDY O RÓ¯NEJ BUDOWIE CHEMICZNEJ
Dikwat (NN - etyleno-2, 2-dwupirydylian). Może być stosowany jako herbicyd, desikant i defoliant. DL50 dla szczurów wynosi 215 - 235 mg/kg p.o. Bardzo słabo wchłania się w jelitach. Jednorazowe podanie szczurom wywiera działanie embriotoksyczne; ekspozycja przewlekła psów i szczurów prowadzi do powstania zaćmy.
Parakwat (Gramoxon - dwuchlorek 1,1-dmumetylo-4,4-dwupirydylowy). Stosowany jest jako herbicyd, fugicyd i insektycyd. DL50 dla szczurów wynosi 120 - 150 mg/kg p.o. Śmiertelna dawka dla człowieka wynosi 15 - 30 cm3. Wchłania się słabo w przewodzie pokarmowym, nie kumuluje się. Wodne roztwory parakwatu przybierają intensywną purpurową barwę, roztwory stężone korodują stal, cynk i aluminium, a także wywołują oparzenia chemiczne powłok. Wdychanie par parakwatu powołuje znaczny, nieodwracalny rozrost nabłonka płuc. Spożycie parakwatu powoduje oparzenie chemiczne błony śluzowej jamy ustnej i przełyku, wymioty. Po dwóch dobach od zatrucia rozwija się ostra niewydolność nerek, a po 5 - 10 dniach śródmiąższowe zapalenie płuc z dużą tendencją do włóknienia, co prowadzi do śmierci.
Leczenie jest wyłącznie objawowe, w przypadku rozwijającego się zapalenia płuc podaje się duże dawki antybiotyków i sterydów.
Trichlorooctan sodowy (TCA - CCl3COONa). Działa silnie drażniąco na skórę i błony śluzowe. W miejscach kontaktu powstają szybko owrzodzenia. Spożycie TCA powoduje ciężkie uszkodzenie przewodu pokarmowego. DL50 dla szczura wynosi 3,3 g/kg p.o. Podobnym, lecz znacznie słabszym działaniem charakteryzuje się dwuchloropropionian sodowy (dalapon - CH3CCl2COONa). Leczenie jest wyłącznie objawowe. Duże znaczenie zapobiegawcze posiada wczesne usunięcie TCA (zmycie powłok wodą z dodatkiem dwuwęglanu sodu, wczesne płukanie żołądka, wymuszone wymioty itp.).
Cyjanamid wapnia (azotniak - CaNCN). Stosowany jest jako defoliant, herbicyd lub sztuczny nawóz. Produkt techniczny jest ciemnoszarym proszkiem zawierającym około 60% cyjanamidu wapniowego. Cyjanamid wapnia rozkłada się w organiŹmie na węglan wapniowy i cyjanamid. Mechanizm działania toksycznego tego związku polega prawdopodobnie na wiązaniu grup sulfhydrylowych cysteiny i glutationu oraz hamowaniu aktywności dehydrogenezy alkoholowej. Cyjanamid wapnia działa miejscowo na skórę i błony śluzowe dróg oddechowych, powodując zmiany typu uczuleniowego oraz podobne do oparzeñ termicznych. Zmiany te są bardzo swędzące, łatwo infekują się oraz trudno goją. Ze strony dróg oddechowych obserwuje się podrażnienie śluzówki nosa, katar , kaszel, a następnie objawy ostrego nieżytu oskrzeli. Działanie uogólnione cyjanamidu wapniowego wywołuje zaczerwienienie twarzy i górnej części tułowia, bóle i zawroty głowy, przyspieszenie tętna i oddechu, obniżenie ciśnienia tętniczego krwi, rzadziej śpiączkę i drgawki. Przy zatruciu doustnym mogą wystąpić wymioty i biegunka. Toksyczność cyjanamidu wapniowego wzrasta wybitnie po spożyciu alkoholu (o ile doustna dawka śmiertelna wynosi 35-50 g, to po spożyciu alkoholu obserwowano przypadek śmiertelny po dawce około 0,35 g),przypuszczalnie z powodu hamowania aktywności dehydrogenezy alkoholowej.
Leczenie zatrucia jest głównie objawowe. Przy równoczesnym spożyciu alkoholu zmniejszenie reakcji antabusowej następuje po dożylnym podawaniem 500-1000 mg witaminy C oraz 100 mg żelaza. W zatruciu cyjanamidem wapniowym obserwowano korzystne działanie chlorowodorku cysteiny podawanego kilkakrotnie domięśniowo w dawce 0,2 g.
Chlorany (magnezowy, sodowy, potasowy).Używane są jako defolianty i desikanty. Zatrucie następuje najczęściej drogą pokarmową, rzadziej wziewną przy rozpylaniu. Działanie toksyczne chloranów polega na wytwarzaniu methemoglobiny, która wytrącając się (szczególnie w kwaśnym moczu ) w kanalikach nerkowych wywołuje ostrą niewydolność nerek. Spożycie doustne chloranów powoduje ponadto uszkodzenie błon śluzowych przewodu pokarmowego. W zatruciu chloranami stosuje się płukanie żołądka roztworem dwuwęglanu sodowego, wczesną alkalizację w celu niedopuszczenia do zakwaszenia moczu, transfuzję wymienną przy wysokiej methemoglobinemii, a w przypadku bezmoczu - dializę pozaustrojową. Korzystne działanie wywiera ponadto tionina (helthion - 0,2% roztwór tioniny w 10% glukozie ) podawana dożylnie i domięśniowo w dawce 10 cm3.
Związki arsenu. Używane są głównie jako insektycydy; wśród herbicydów znajdują się związki z grupy kadodylu, pochodne kwasu arsenowego oraz trójtlenek arsenu. Wysoką toksycznością odznaczają się związki arsenu trójwartościowego, znacznie mniejszą arsenu pięciowartościowego. Niektóre organiczne związki arsenu pięciowartościowego nie wywierają bezpośrednio działania toksycznego, a dopiero po ich przemianie na związki arsenu trójwartościowego. Arsen łatwo wiąże się z grupami sulfhydrylowymi aminokwasów białek , w tym różnych enzymów jak esterazy, lipazy, fosfatazy, oksydazy i inne, powodując utrudnienie przebiegu procesów życiowych w tkankach. Małe dawki arsenu mogą pobudzać rozrost tkanek (rogowacenie skóry) lub powodować powstawanie nowotworów (rak płuc, rak „arsenowy” skóry). Związki arsenu stosowane miejscowo w większych stężeniach powodują martwicę tkanek na drodze zaburzeñ metabolizmu komórek i uszkodzenia komórek śródbłonkowych naczyñ. Arsen gromadzi się w układzie siateczkowo-śródbłonkowym wątroby, nerek i śledziony, w kościach, skórze, włosach i paznokciach (w keratynie). Wydala się wolno, tak, że nawet po kilku latach od zatrucia można go wykryć we włosach i kościach. Zatrucia arsenem mogą być ostre , podostre i przewlekłe. Ostre zatrucia dużymi dawkami arsenu przebiegać mogą gwałtownie, tzw. postać porażenia zatrucia. Po 1/2 - 1,0 godzinie występują silne, piekące bóle w przewodzie pokarmowym, ostre bóle głowy, zapaść i śmierć na skutek porażenia ośrodków krążenia i oddychania. W przypadkach zatruć o wolniejszym przebiegu, występuje postać żołądkowo-jelitowa charakteryzująca się silną biegunką, stąd też nazywana bywa „postacią choleryczną”. W 1 - 2 godziny od przyjęcia trucizny występują bóle i pieczenia w przewodzie pokarmowym, wymioty oraz wodnisto-śluzowata obfita biegunka prowadząca do odwodnienia i utraty elektrolitów. Szybko rozwija się wstrząs toksyczny i kwasica. Śmierć następuje po 6 - 8 dniach od zatrucia. Przebieg zatrucia podostrego jest nie charakterystyczny, występuje szereg objawów prowadzących do wyniszczenia i śmierci. Pierwszą cechą rozpoznawczą może być łamliwość paznokci i wypadanie włosów oraz rogowacenie dłoni i podeszw.
Zatrucia przewlekłe charakteryzują się zapaleniami wielonerwowymi, osłabieniem mięśniowym, upośledzeniem wzroku i słuchu. Liczne są zmiany skórne: rumienie, łuszczenia naskórka, hyperkeratoza, przebarwienia - tzw. melanoza arsenowa, wypadanie włosów i łamliwość paznokci.
Przy przewlekłej ekspozycji na arsen obserwuje się występowanie odporności i przyzwyczajenia, prawdopodobnie na skutek upośledzenia wchłaniania arsenu (tolerancja może sięgać dawek kilkakrotnie przekraczających śmiertelne). Leczenie zatruć arsenem jest trudne i złożone. Ważną rolę odgrywa zapobieganie wchłaniania się trucizny poprzez płukanie żołądka z jednoczesnym podaniem przez zgłębnik 100 ml antidotum metallorum sauteri (stabilizowany roztwór siarkowodoru wytrącający metale w postaci nierozpuszczalnych siarczków). W celu przyspieszenia usunięcia arsenu z organizmu stosować można środki helatujące (BAL i Sulfactim) oraz wiążące arsen (tiosiarczan sodowy). BAL i Sulfactim dzięki
obecności w cząsteczce grup sulfhydrylowych wiążą wolny arsen oraz związany z białkami, prowadząc do reaktywacji szeregu enzymów. Oba w/w. leki podaje się domięśniowo w dawce 2 - 3 mg/kg masy ciała co 4 godziny przez pierwsze dwie doby, co 6 godzin przez trzecią i czwartą dobę, a następnie co 12 godzin do koñca leczenia, trwającego zazwyczaj 6 dni. Leki te posiadają właściwości uszkodzenia nerek, dlatego też w czasie leczenia należy wykonywać codziennie badanie moczu na obecność białka i krwinek czerwonych. Tiosiarczan sodowy podaje się dożylnie, powoli, w postaci 30 % wodnego roztworu w dawce 50 cm3. Ponadto należy podawać pozajelitowo duże dawki witamin B1 i C, których poziom w zatrutym ustroju gwałtownie obniża się. Większość autorów poddaje w wątpliwość skuteczność dializy pozaustrojowej.
W ciągu całego okresu zatrucia stosuje się leczenie objawowe.
W świecie roślinnym można się spotkać z wielu przykładami występowania związków trujących. Różnorodność tych trucizn pod względem chemicznym, jak również duża rozpiętość rodzin i gatunków, w których spotyka się substancje toksyczne, uniemożliwia przeprowadzenie klasyfikacji, czy systematyki toksykologicznej roślin trujących.
Najczęściej występującymi związkami trującymi w roślinach są: alkaloidy, glikozydy, saponiny, olejki i żywice. Wiele z tych substancji ma zastosowanie jako ważne i cenne leki, inne są używkami i narkotykami. Wiele roślin trujących zostało wycofanych ze współczesnego lecznictwa i zastąpionych przez związki syntetyczne. Są także rośliny trujące, w których substancje czynne, ze względu na swą nietrwałość, zmienną zawartość lub wysoką toksyczność utrudniają dawkowanie i z tych względów nie są obecnie wykorzystywane przez człowieka.
Rośliny trujące powodują najczęściej zatrucia ostre, przypadkowe lub omyłkowe, jakkolwiek znane są przypadki wykorzystania ich niekiedy w celach przestępczych. Szczególnie wyciągi i odwary roślin trujących były szeroko stosowane w starożytności i średniowieczu dla celów trucicielskich bądŹ też do wykonywania sądowych wyroków śmierci. Wśród plemion pierwotnych wyciągi z roślin trujących i odurzających używane są do zatruwania strzał, obrzędów tyrualnych lub wykonywania „wyroków boskich”.
Trucizny roślinne należą do silnie i gwałtownie działających, a dawki śmiertelne dla człowieka wynoszą niekiedy już kilkadziesiąt miligramów. Mechanizm działania trującego jest różnorodny: alkaloidy najczęściej pobudzają lub porażają układ nerwowy, glikozydy - mięsieñ sercowy, saponiny uszkadzają krwinki czerwone itp.
Alkaloidy należą do silnie toksycznych substancji roślinnych, działających głównie na ośrodkowy lub wegetatywny układ nerwowy. Nieliczne wykazują działanie protoplazmatyczne (np. chninika) lub mięśniowe (np. weratryna). Zatrucia alkaloidami nie dają charakterystycznych zmian anatomopatologicznych i z tych względów wykrycie substancji trującej i ustalenie przyczyny zatrucia opiera się przede wszystkim na analizie chemicznej. Alkaloidy są zwykle substancjami stałymi, mają smak wybitnie gorzki i są trudno rozpuszczalne w wodzie, dobrze natomiast, z niewielkimi wyjątkami, w rozpuszczalnikach organicznych. Nie mają na ogół charakterystycznej barwy ani zapachu. Tylko nieliczne alkaloidy, nie zawierające tlenu w swej cząsteczce (nikotyna, koniina, sparteina, arekolina, peletieryna i inne) są zwykłymi płynnymi, lotnymi, rozpuszczalnymi w wodzie, często z lekkim swoistym zapachem. Z kwasami alkaloidy tworzą krystaliczne połączenia, co ma duże znaczenie dla ich identyfikacji. W zwłokach większość alkaloidów ulega rozkładowi, niektóre jednak można wykryć po kilku, a nawet kilkunastu latach.
Zatrucia alkaloidami występują przy stosowaniu ich jako leki, lub omyłkowe, a niekiedy są one używane dla celów przestępczych.
Pierwsza pomoc i leczenie zatruć alkaloidami powinny być wykonywane jak najszybciej. Wywołuje się wymioty lub stosuje się płukanie żołądka wodą z dodatkiem roztworu nadmanganianu potasowego, podaje węgiel aktywowany, antidotum universale, taninę oraz środki działające antagonistycznie pod względem farmakologicznym. W celu poprawienia czynności układu oddechowego lub krążenia podaje się leki cucące i pobudzające oraz tlen z dwutlenkiem węgla. Przy występujących drgawkach - domięśniowo lub doodbytniczno wodzian chloralu, paraldehyd lub chloropromazynę.
Alkaloidy tropinowe występują w wielu roślinach (liście, owoce, korzenie) rodziny psiankowatych (Solanaceae). Najbardziej wśród nich są rozpowszechnione: pokrzyk wilcza jagoda (Atropa belladonna), bieluñ dziędzierzawa (Datura stramonium), lulek czarny (Hyoscyamus niger), alraune (Atropa mandragora). Z roślin tych wyodrębniono kilka alkaloidów, z których największe znaczenie toksykologiczne mają atropina i skopolamina.
Zatrucia alkaloidami tropinowymi oraz nadużywanie ich dla celów mistycznych znane już były w starożytności. F*hner w swych studiach historyczno-etnologicznych opisuje rolę alkaloidów psiankowatych w przepowiedniach Pytii, dla wywoływania ekstaz i w tañcach oddających kult religijny, jako składnika maści lub napojów czarownic itp. Obecnie zatrucia zdarzają się wskutek pomyłkowego spożycia jagód pokrzyku lub przy stosowaniu jako leku. Stosunkowo często można się także spotkać z nadwrażliwością na przetwory zawierające atropinę, przy czym już dawki poniżej 1 mg atropiny mogą wywoływać objawy toksyczne. U dzieci, które są szczególnie wrażliwe na atropinę, już po zjedzeniu kilku jagód wilczej jagody może nastąpić zejście śmiertelne, natomiast u ludzi dorosłych po spożyciu 15-20 jagód.
Atropina jest estrem heterocyklicznego aminoalkoholu - tropiny z kwasem tropowym, o smaku gorzkim. Nie jest związkiem trwałym i łatwo ulega hydrolizie, szczególnie w środowisku zasadowym. Zwierzęta roślinożerne (królik, niektóre ptaki, ślimak i inne) mają enzymy rozkładające szybko atropinę (tropinoesterazy), wskutek czego są one odporne na zatrucia. Opisano nawet przypadki zatruć człowieka po zjedzeniu mięsa zwierząt, które żywiły się liśćmi wilczej jagody. Atropina wchłania się szybko z przewodu pokarmowego, ale tylko niewielkie ilości są wydalane z moczem. Przy dłużej trwającym leczeniu atropiną organizm może się do niej przyzwyczaić, stwarzając potrzebę zwiększenia przyjmowanych dawek.
Atropina jest silnie działającą trucizną protoplazmatyczną wywołującą zatrucie u człowieka dorosłego już po przyjęciu doustnym 0,01 g, a zejście śmiertelne po 0,1-0,12 g. Atropina wywiera silne działanie porażające układ nerwowy parasympatyczny, a w dalszym etapie działanie pobudzające - na ośrodkowy układ nerwowy. Zatrucia atropiną powodują liczne charakterystyczne objawy, jak silne rozszerzenie Źrenic z porażeniem akomodacji i światłowstrętem oraz utrudnionym widzeniem, znaczną suchość błony śluzowej w nosie, gardle, krtani i związane z tym pragnienie, trudności w połykaniu i mówieniu. Skóra staje się zaczerwieniona, sucha i gorąca. Czynność serca ulega przyspieszeniu, a potem staje się niemiarowa. Do charakterystycznych objawów rozwijających się w wyniku działania atropiny na ośrodkowy układ nerwowy należą: potęgujący się niepokój ruchowy, objawy niezborności, bóle i zawroty głowy, silne pobudzenie psychiczne i pomieszanie myśli aż do bredzenia, napady nadmiernej gadatliwości i wesołości, halucynacje i omamy. Niekiedy dochodzi do napadów szału. Po tym okresie następuje znużenie, przygnębienie, senność i otępienie. Zjawia się duszność, niewydolność krążenia, śpiączka, bezdech i drgawki. Śmierć następuje wskutek porażenia ośrodka oddechowego.
Leczenie zatrutych atropiną przyjętą doustnie wymaga możliwie natychmiastowego płukania żołądka. Ze względu na suchość błony śluzowej przełyku sonda powinna być naoliwiona. Do płukania stosuje się zawiesinę węgla zwierzęcego i taniny. Przy trudnościach wprowadzenia sondy podaje się podskórnie apomorfinę w ilości 10 mg. W okresie silnego pobudzenia podaje się luminal domięśniowo w ilości 0,2 g lub 3 g wodzianu chloralu doodbytniczno. Nie jest wskazane podawanie morfiny jako środka uspokajającego, gdyż stwarza to niebezpieczeñstwo potęgowania działania porażającego na ośrodek oddechowy.
Skopolamina (Hioscyna) jest również estrem kwasu tropowego z heterocyklicznym aminoalkoholem - stropiną, która jest pokrewna tropinie. Na układ nerwowy parasympatyczny działa podobnie do atropiny, natomiast różni się od niej w oddziaływaniu na ośrodkowy układ nerwowy. Podobnie do morfiny wywiera działanie hamujące na ośrodki ruchowe mózgu i stosowana jest w psychiatrii przy nadmiernym pobudzeniu ruchowym dla spotęgowania działania morfiny. Już w małych dawkach powoduje stan senności, znacznego uspokojenia, stany otępienia psychicznego, co znacznie osłabia własną wolę i samodzielność myślenia. W dużych dawkach może powodować zejście śmiertelne przez porażenie ośrodka oddechowego. Przeciętna dawka śmiertelna skopolaminy waha się w granicach 0,1-0,2 g przy podaniu podskórnym, a doustnie może przekraczać niekiedy 0,5 g, niebezpieczeñstwo zaś zatruć występuje przede wszystkim przy stosowaniu jej łącznie z morfiną.
Nikotyna (1-metylo-2-pirydynopirolidyna) jest głównym alkaloidem liści tytoniu wielu odmian Nicotiana tabacum L. Liście w stanie świeżym zawierają od 2 do 8% nikotyny, w zależności od gatunku, warunków klimatycznych, glebowych itp. Po fermentacji ilość nikotyny spada do 0,2_4%. Nikotyna jest bezbarwnym lub lekkożółtawym płynem, higroskopijnym, silnie zasadowym. Na powietrzu i świetle szybko brunatnieje, przypominając charakterystyczny zapach pirydynowy. Rozpuszcza się w każdym stosunku w wodzie, alkoholu, olejach i rozpuszczalnikach organicznych.
Nikotyna ma smak piekący oraz działa żrąco na błonę śluzową. Ulega ona niesłychanie szybko wchłonięciu przez błonę śluzową oraz łatwo rozpuszcza się w lipidach ustrojowych. Dobrze wchłania się przez skórę, jakkolwiek wolniej niż przez błonę śluzową. Borzelleca wykazał na psach, że nikotyna wchłania się także z pęcherza moczowego.
Działanie nikotyny jest nadzwyczaj szybkie i pod tym względem zbliżone do cyjanowodoru. Dawka śmiertelna dla człowieka wynosi 0,06-0,1 g, przy czym zgon następuje w ciągu kilku minut wskutek porażenia ośrodka oddechowego. W ostrych zatruciach mniejszymi dawkami występuje uczucie pieczenia w ustach, ślinotok, bóle i zawroty głowy, nudności i wymioty, biegunka, silne poty i osłabienie, utrudnione oddychanie, niemiarowość tętna, omdlenie, a w cięższych przypadkach utrata przytomności, drgawki i śmierć przez porażenie ośrodka oddechowego. U ludzi nie przyzwyczajonych objawy te występują już po wypaleniu pierwszych papierosów, wkrótce jednak organizm się przyzwyczaja do nikotyny i może znosić ilości przekraczające średnią dawkę śmiertelną.
Zatrucia przewlekłe nikotyną (nikotynizm) są wynikiem rozwoju nałogu palenia tytoniu. Liczne badania doświadczalne i kliniczne wykazały, jak wielkie niebezpieczeñstwo i szkodliwe następstwa są wynikiem zatruć przewlekłych nikotyną.
Obok zatruć powstających w wyniku nadużywania tytoniu jako używki występują także zatrucia nikotyną, które mogą być przestępcze lub samobójcze, jak również przypadkowe i zawodowe. Zatrucia o podłożu kryminalnym zdarzają się rzadko, ze względu na silny i przykry smak oraz zapach nikotyny. Zatrucia wypadkowe zdarzały się zwłaszcza dawniej, gdy stosowano nikotynę do zwalczania pasożytów. Opisano przypadki zatruć, nawet śmiertelnych, przede wszystkim wśród dzieci, wskutek nadmiernie gorliwego wcierania w skórę naparów z tytoniu lub roztworów nikotyny. Opisano także przypadek śmiertelnego zatrucia człowieka, który zasnął w magazynie z belami tytoniu, jak również zatrucia wśród przemytników, którzy dokoła ciała owinięciu byli liśćmi tytoniowymi. Ważniejszym jednak zagadnieniem są zatrucia zawodowe ze względu na zastosowanie roztworów nikotyny w rolnictwie przy zwalczaniu pasożytów bydła i drobiu lub jako środka owadobójczego stosowanego do gazowania w szklarni. Najczęściej zatrucia występują wśród ogrodników, którzy nie przestrzegają zasad ostrożności przy pracy z roztworami nikotyny. Wprawdzie lotna nikotyna szybciej od innych insektycydów ulatnia się, ale jest opisany przypadek zatrucia siedmioosobowej rodziny po zjedzeniu sałaty spryskiwanej roztworem nikotyny.
Wiele innych roślin zawiera również alkaloidy o podobnym do nikotyny działaniu na zwoje wegetatywne. Australijczycy żuli, a obecnie także palą liście rośliny Duboisia hopwoodii, zawierającej alkaloid piturynę. Z rośliny Anabasia aphilia wyodrębniono alkaloid anabazynę, o działaniu podobnym do nikotyny i stosowanym jako środek owadobójczy. Krzew rosnący u nas w ogrodach i parkach - złotokap pospolity (Cytisus laburnum L.), o długich złocistych kwiatostanach, zawiera trujący alkaloid cytyzynę, pobudzający ośrodek oddechowy i naczynioruchowy. Zatruciu cytyzyną ulegają najczęściej dzieci, które zjadają nasiona podobne do grochu lub żują korzenie o słodkim smaku. Już 10-30 nasion może spowodować ciężkie zatrucie z bólami w jamie brzusznej, wymiotami, biegunką, zimnymi potami. Po okresie zwolnienia następuje przyspieszenie tętna, silne uczucie senności, drgawki kloniczno-toniczne i śmierć przez porażenie ośrodka oddechowego. Liści złotokapu używa się niekiedy jako domieszki lub namiastki liści tytoniowych.
Koiina (α-propylopiperydyna) jest głównym alkaloidem pietrasznika plamistego (Conium maculatum L.). Koiina jest substancją płynną i lotną, silnie alkaliczną, na powietrzu ulega szybko brunatnieniu i żywicowaceniu. Ma przykry zapach, przypominający mocz mysi. Rozpuszcza się w wodzie, alkoholu i rozpuszczalnikach organicznych. Koiina łatwo wchłania się przez błony śluzowe i skórę. Działa najpierw drażniąco, a potem porażająco na wegetatywne zwoje obwodowe oraz, podobnie do kurary, na zakoñczenie nerwów ruchowych. Porażenia te obejmują najpierw koñczyny dolne, a następnie wyższe odcinki ciała. Objawami zatrucia koiiną są: rozszerzenie Źrenic i światłowstręt, silny ślinotok i biegunka. Wkrótce następuje utrata sił fizycznych i senność z całkowitym zachowaniem świadomości. Gdy porażenie obejmuje przeponę i mięśnie klatki piersiowej, następuje śmierć przez uduszenie. Taki przebieg miała śmierć Sokratesa, opisana przez Platona. Zatrucie koiiną następuje bardzo szybko. Dawka śmiertelna dla człowieka wynosi 0,4-0,6 g koiiny.
Sparteina, alkaloid żarnowca (Spartium scoparium L.), w działaniu swym podobna do koiiny, a według niektórych autorów jest nawet silniej trująca. Alkaloidy sparteina i lupinina znajdują się także w łubinie żółtym i jego odmianach. Najczęściej zatruciu ulegają małe dzieci, które są bardziej wrażliwe na sparteinę. Już kilka nasion łubinu było przyczyną śmierci dzieci. Szmidt opisuje zatrucie śmiertelne 2,5-letniego dziecka po spożyciu 10 tabletek leku zawierającego sparteinę.
Lobelina. Głównym alkaloidem rośliny stroiczka rozdęta (Lobelia inflata L.), jest α-lobelina, która poprzez pobudzenie chemoreceptorów kłębka szyjnego wywołuje na drodze odruchu krótkotrwałe przyspieszenie i pogłębienie oddechu. Wywiera poza tym działanie nikotynowe na zwoje układu wegetatywnego. W lecznictwie stosowana jest w celu pobudzenia oddechu oraz przy kuracjach odwykowych od palenia tytoniu, ze względu na podobieñstwo działania farmakologicznego do nikotyny. Stosowana jest obecnie coraz rzadziej z powodu licznych objawów ubocznych.
Jest jeszcze wiele innych roślin zawierających alkaloidy o bardzo silnym działaniu trującym, które były używane jako leki bądŹ używki, ale ze względu na ograniczone obecnie zastosowanie nie przedstawiają większego niebezpieczeñstwa toksykologicznego. Można tu m.in. wymienieć alkaloidy:
Akonityna, główny alkaloid tojadu mordownika (Aconitum napellus L.), byliny z niebieskimi kwiatami, często hodowanej w ogrodach. Akonityna jest substancją krystaliczną, słabo zasadową, łatwo wchłania się przez błonę śluzową i skórę. Należy do najsilniej działających trucizn roślinnych, gdyż już w ilości 0,25 mg wywołuje u ludzi ostre zatrucia, a 1-3 mg - śmierć. Zatrucia mogą nastąpić po spożyciu kilku gramów bulw podobnych do pietruszki, lub też przedawkowaniu jako leku. Obecnie, ze względu na trudne jej dawkowanie, stosuje się akonitynę niezmiernie rzadko. Dawniej akonityna była często używana jako trucizna mordercza. Feketi* opisuje przypadek zatrucia śmiertelnego proszkiem w opłatku z akonityną, wydanym z przepisu lekarskiego, w którym omyłkowo opuszczono jedno zero, tj. zamiast 0,0003 g znajdowało się w proszku 0,003 g akonityny.
Akonityna w dawkach toksycznych wywołuje zaburzenia czucia języka, gardzieli, twarzy, koñczyn, rozprzestrzeniające się szybko po całym ciele, zmniejszając wrażliwość na ból i dotyk. Pojawiają się niepokój, podniecenie i lęk, obfite poty, trudności w połykaniu, bóle żołądka, wymioty i biegunka oraz drżenia włókienkowe. Czynność serca oraz ośrodki oddechowy i naczynioruchowy po początkowym pobudzeniu ulegają szybkiemu zahamowaniu, doprowadzając do zgonu, przy czym świadomość pozostaje zachowana aż do śmierci.
Kolchicyna, alkaloid jednoliściennej rośliny ziemowit jesienny (Colchicum autumnale L.). Zatrucia zdarzają się najczęściej wśród dzieci, które zjadły owoce, cebulki lub liście ziemowitu, albo też po przedawkowaniu jako leku stosowanego w dnie. Weil i współpr. opisują przypadek śmierci w ciągu 24 godzin dwojga starszych ludzi, którzy w posiłku zjedli cebulki ziemowita, sprzedane razem z czosnkiem. Kolchicyna i jej pochodne (Demecolicin, Colcemid i inne) mają działanie antymitotyczne, przy czym pochodne kolchicyny stosowane w lecznictwie są do 50 razy mniej toksyczne. W dawkach trujących kolchicyna wywołuje bóle żołądka i jelit, wymioty, biegunkę, leukopenię, uczucie palenia i drapania w jamie ustnej, utrudnione połykanie, a przy większych dawkach uszkodzenie wątroby i nerek, białkomocz, odwodnienie organizmu i bezmocz. Opisano także przypadki wypadania włosów po 10-14 dniach, podobnie jak w zatruciu talem. Dawka śmiertelna dla dorosłego człowieka wynosi 0,02-0,4 g.
Weratryna jest zespołem alkaloidów zawartych w jednoliściennej roślinie ciemierzyca biała (Veratrum album L.) i innych jej odmianach, jak również w kichawcu (Sabadilla off. L.). Preparaty z ciemierzycy lub czyste alkaloidy są używane jako leki hipotensyjne oraz w rzucawce porodowej. Ze względu na małą rozpiętość pomiędzy dawką leczniczą a toksyczną stosowanie tych preparatów jest ograniczone. W lecznictwie kuchawiec stosowany był dawniej jako ocet sabadylowy do zwalczania wszawicy. Zatrucia zdarzają się omyłkowe lub przez rozmyślne wypicie octu sabadylowego. Dawka śmiertelna weratryny wynosi około 20 mg, wskutek jednak szybkiego występowania wymiotów rzadziej zdarzają się zatrucia śmiertelne niż po kolchicynie. Weratryna silnie drażni błonę śluzową, a w większych dawkach pobudza do silnego kichania i wymiotów oraz wywołuje bolesną krwawą biegunkę. Charakterystyczne są także skurcze mięśni prążkowanych, mrowienie i świąd na całym ciele z uczuciem zimna, spadek ciśnienia tętniczego krwi i zwolnienie czynności serca. Śmierć następuje przez porażenie oddechu lub serca.
Kurara jest to wyciąg z roślin gatunku Strychnos, przygotowywanego przez Indian Ameryki Południowej do zatruwania strzał. Kurara zawiera kilka alkaloidów, przede wszystkim kurarynę. Działają one porażająco na zakoñczenia nerwów ruchowych (blok depolaryzacyjny płytki motorycznej), powodując zwiotczenie wszystkich mięśni szkieletowych i przepony. Zwierzę zranione zatrutą strzałą, gdy trucizna dostanie się do krwi, bardzo szybko pada bezwładne wskutek porażenia mięśni oddechowych i ginie z uduszenia. Kurara działa jedynie po podaniu pozajelitowym, gdyż przyjęta doustnie wchłania się powoli i szybko wydala, co uniemożliwia osiągnięcie stężenia toksycznego.
Alkaloidy kurary oraz leki o podobnym działaniu (D-tubokuraryna, Curarin, Myostatin, Tubarin i inne) są stosowane w chirurgii w celu wywołania pełnego zwiotczenia mięśni szkieletowych. Po przedawkowaniu tych alkaloidów mogą występować: podwójne widzenie, niedowład powiek, ślinotok, trudności w połykaniu i oddychaniu. Swoistym antagonistą farmakologicznym alkaloidów kurarynowych jest fizostygmina i prostygmina, które znoszą porażenia mięśniowe zatrutych zwierząt.
Taksyna, alkaloid zawarty w szpilkach i nasionach cisu (Taxus baccata L.). Już w starożytności napar ze szpilek cisu był stosowany jako środek poronny, a i obecnie zdarzają się z tego powodu zatrucia. W czerwonych owocach cisu, zjadanych chętnie przez dzieci, toksyna znajduje się jedynie w twardych nasionach, natomiast mięsista osnówka nie jest trująca. Czerwek i Fischer opisują śmiertelny przypadek zatrucia samobójczego 20-letniej kobiety, która wypiła napar ze szpilek cisu w ilości 3 łyżek stołowych i zjadła pozostałość naparu. Już po godzinie wystąpiły zawroty głowy, silne bicie serca, szum w uszach i pieczenie całego ciała oraz częste wymioty i biegunka połączona z silnymi bólami żołądka i jelit. Znaczne przyspieszenie czynności serca, a następnie zapaść krążeniowa doprowadziły do zgonu.
Arekolina jest głównym alkaloidem owoców palmy Areca catechu L., rosnącej w południowo-wschodniej Azji. Ludność miejscowa żuje w celach euforyzujących tzw. betel, przyrządzany z orzeszków areki z wapnem i liśćmi pieprzowca. Arekolina jest alkaloidem płynnym, pobudza zakoñczenia nerwów parasympatycznych, wywołuje ślinotok, wzmaga ruchy robaczkowe jelit. Zejście śmiertelne może nastąpić już po przyjęciu 50 mg arekoliny, jednakże zatrucia ostre zdarzają się rzadko, natomiast bardziej szkodliwe jest żucie areki jako używki.
Pilokarpina, alkaloid wyodrębniony z liści Pilocarpus jaborandi L., jest stosowana w okulistyce i niekiedy w innych specjalnościach. Przy przedawkowaniu mogą wystąpić: rumieñ, obfite poty, łzawienie, ślinotok, zwężenie Źrenic, nudności, wymioty i zwolnienie czynności serca. Śmierć następuje przez porażenie ośrodka oddechowego. Objawy zatrucia pilokarpiną znosi atropina, która jest antagonistą tego alkaloidu.
Fizostygmina (ezeryna), alkaloid z nasion Physostigma venenosum L., stosowana jest w okulistyce (powoduje silne i długotrwałe zwężenie Źrenic). Fizostygmina wywiera działanie hamujące na esterazę cholinową, powodując objawy zatrucia acetylocholiną. Zatrucie śmiertelne może nastąpić już po przyjęciu 10 mg, przy czym występują objawy lęku, porażenia mięśni, zapaść oraz porażenie ośrodka oddechowego. Śmierć następuje przy zachowaniu pełnej świadomości.
Cykutotoksyna, alkaloid występujący w szeroko u nas rozpowszechnionej roślinie - szaleju jadowitym (Cicuta virosa L.). Podobnie do pikrotoksyny działa pobudzająco na ośrodkowy układ nerwowy. Pfeiffer opisuje zatrucie śmiertelne dwóch chłopców, którzy zjedli korzenie szaleju. Objawy zatrucia z utratą świadomości wystąpiły bardzo szybko, a zgon w ciągu jednej godziny. Marcinkowski i Porawski opisują zatrucie 4 chłopców szalejem jadowitym. Chłopcy wykopali na łące kłącza przypominające marchew i zjedli na surowo. Jeden z nich, lat 16, który zjadł 1/2 kłącza już po 50 minutach doznał silnego napadu drgawek, wymiotów, wydzielania piany i utraty przytomności. £ącznie w ciągu 100 minut chłopiec miał 11 napadów drgawek, po których zmarł. Pozostali, którzy zjedli mniejsze ilości, zostali uratowani.
Strychnina. Alkaloid otrzymywany z rośliny rodzaju kulczyba (Strychnos). Biały, krystaliczny proszek bez zapachu o bardzo gorzkim smaku. Silna trucizna powoduje sztywność mięśni twarzy, szyi i kolan. Typowym objawem jest występowanie skurczów tonicznych po bodżcach dŹwiękowych lub świetlnych. Skurcze nasilają się, aż do wystąpienia ciągłego skurczu tężcowego, podczas którego ciało zatrutego tworzy łuk. Dochodzi do zahamowania ruchów oddechowych. Śmierć następuje w wyniku uduszenia. Dawka śmiertelna strychniny wynosi 15 do 20mg.
W wielu roślinach znajdują się związki o budowie glikozydowej. są to eterowe połączenia cukru prostego z aglikonem zawierającym w swej cząsteczce grupę hydroksylową (alkaloid, fenol, kwas organiczny itp.). w organizmie glikozydy ulegają łatwo rozkładowi pod wpływem swoistych enzymów. glikozydy mają bardzo różną budowę chemiczną, zarówno cząsteczki aglikonu jak i cukru. działanie farmakologiczne i toksykologiczne glikozydów jest również bardzo różnorodne. największe znaczenie toksykodynamiczne wykazują glikozydy nasercowe.
Glikozydy nasercowe znajdujące się w roślinach różnych rodzin składają się z aglikonów o budowie sterydowej oraz swoistej części cukrowej. Mają one doniosłe znaczenie w lecznictwie, szczególnie glikozydy naparstnicy, strofantusa, miłka wiosennego, konwalii i inne. Glikozydy nasercowe silnie wiążą się z białkami mięśnia sercowego i w wyniku kumulacji mogą powodować zatrucia. Opisane przypadki zatruć dotyczą stosowania glikozydów w lecznictwie, rzadko zdarzają się przypadki samobójcze. Przy przedawkowaniu lub zwiększonej wrażliwości występują bóle i zawroty głowy, przyspieszone tętno, szum w uszach, senność, oszołomienie, uczucie osłabienia, nerwobóle, widzenie w żółtych barwach na skutek podrażnienia odpowiednich elementów siatkówki oka, upośledzenie, łaknienia, ślinotok, nudności, wymioty, biegunka, duszność i sinica. Objawy te nasilają się, przy czym może nastąpić zapaść i śmierć. Dawkę śmiertelną dla człowieka określa się na 3-10 mg digitoksyny lub 2,5-6 g liści naparstnicy.
W przypadku wystąpienia objawów toksycznych należy odstawić podawanie naparstnicy oraz ewentualnie podawać małe dawki atropiny. Działanie toksyczne naparstnicy można zmniejszyć przez jednoczesne podawanie jonów potasowych. Ostatnio opisywano przypadki pomyślnego leczenia zatruć naparstnicą środkami blokującymi wybiórczo β-receptory adrenergiczne.
Wiele roślin wytwarza olejki lotne, które wywierają silne i często toksyczne działanie. Skład chemiczny olejków jest bardzo złożony, przy czym każda roślina wytwarza olejek charakterystyczny dla swego gatunku. Mogą to być estry zawierające siarkę (olejek gorczyczny), estry wielowodorotlenowych fenoli (anetol, eugenol, safrol), pochodne terpenowe (olejek terpentynowy, eukaliptusowy, jałowcowy) i inne. Działanie toksykodynamiczne jest funkcją zespołu jego składników.
Olejki lotne są na ogół bezbarwnymi i ruchliwymi cieczami, o charakterystycznym przyjemnym zapachu, nierozpuszczalnymi lub trudno rozpuszczalnymi w wodzie, dobrze natomiast w alkoholu, tłuszczach i rozpuszczalnikach organicznych. Wprowadzone doustnie wywierają silne działanie drażniące na błonę śluzową, wywołując przekrwienie i stany zapalne. W większych dawkach powodują zapalenie i zwyrodnienie tłuszczowe wątroby i nerek. Wskutek przekrwienia narządów miednicy małej w większych dawkach mogą powodować poronienie. Z tych względów w medycynie ludowej olejki są nadużywane jako środki poronne, choć w dawkach skutecznych wywierają działanie silnie drażniące, a niekiedy niebezpieczne dla życia. Na serce i naczynia krwionośne mogą działać pobudzająco, niekiedy powodować zwiotczenie mięśni gładkich i ślinotok. Niektóre olejki mogą działać drażniąco, a potem porażająco na ośrodkowy układ nerwowy. Podane na skórę wywołują podrażnienie, rozszerzenie naczyñ i ich przekrwienie oraz uczucie pieczenia. W organizmie olejki lotne ulegają przede wszystkim utlenieniu, a następnie po sprzężeniu z kwasem glukuronowym lub siarkowym są wydalane razem z moczen. W niewielkich ilościach olejki lotne są wydalane w stanie nie zmienionym przez nerki i płuca, co po swoistym zapachu umożliwia często szybkie ustalenie przyczyny zatrucia.
W zatruciach olejkami należy jak najszybciej przeprowadzić płukanie żołądka z dużą ilością węgla. Przeciwwskazane jest podawanie mleka, olejów lub alkoholu. Gdy występuje bolesna biegunka i parcie na stolec, podaje się środki śluzowe, kleiki, a w razie dużej utraty płynów wykonuje wlewki dożylne. Przy występujących drgawkach podaje się domięśniowo luminal (0,1-0,2 g), a w przypadkach ciężkiego wstrząsu dożylnie noradrenalinę 95-10 mg na 300 cm3 wlewki) i hydrokortyzon, przy niebezpieczeñstwie zaś porażenia oddechu - lobelinę, środki cucące i sztuczne oddychanie.
Olejki lotne łatwo wchłaniają się przez skórę i dlatego przy pracy z nimi należy używać rękawic ochronnych oraz beztłuszczowego kremu, w celu zapobieżenia występowaniu podrażnieñ i zapaleñ skóry.
Spośród wielu olejków, jakie znajdują zastosowanie w życiu człowieka, częściej spotykane bywają zatrucia następującymi roślinami olejkowymi:
Jałowiec sawina (Juniperus sabina L.) zawiera 3-5% olejku lotnego, którego 50% stanowi alkohol terpenowy sabinol. Już w starożytności jałowiec sawina był stosowany jako środek poronny. Wykazuje on silne działanie drażniące, moczopędne oraz kurczące na macicę. Niebezpieczeñstwo zatruć spowodowane jest tym, że działanie poronne występuje dopiero po podaniu dawki zbliżonej do dawki śmiertelnej. Już 6 kropel może stanowić ilość śmiertelną dla człowieka. Podany w większych ilościach (0,1-0,2 g olejku lub 10-20 g szyszko-jagód) wywołuje ciężkie zapalenie nerek, jelit i żołądka. Występuje silne parcie na mocz, krwiomocz, a potem skąpomocz i bezmocz. Rozwijają się drgawki, śpiączka i porażenie ośrodkowego układu nerwowego.
Olejek terpentynowy (Oleum Terebinthinae) jest otrzymywany z żywic drzew szpilkowych. Opisano przypadki zatruć samobójczych terpentyną. Dawkę śmiertelną ocenia się na 100 cm3, przy czym olejek stary, częściowo utleniony, wykazuje silniejsze działanie toksyczne.
Olejek terpentynowy przyjęty doustnie powoduje zaburzenia żołądkowo-jelitowe oraz ostre zapalenie nerek z białko- i krwiomoczem, a póŹniej skąpomocz, bóle i zawroty głowy, odurzenie, afazja, po czym występuje śpiączka i śmierć prze porażenie ośrodka oddechowego. Nawet gdy zatruty zostanie uratowany, rozwija się zwykle znacznie niedokrwistość prawdopodobnie w wyniku uszkodzenia szpiku. Mocz po przyjęciu olejku terpentynowego ma zapach podobny do fiołków. Przy wdychaniu występuje podrażnienie dróg oddechowych aż do stanów zapalnych płuc.
Podobne działanie toksyczne wykazuje także olejek eukaliptusowy, ale ze względu na ograniczone jego stosowanie, praktycznie nie bywa przyczyną zatruć.
Olejek gorczyczny (Oleum Sinapis), CH2=CH-CH2-NSC, allilotiocyjanek, występuje w nasionach gorczycy w formie glikozydowej (sinigryna). Olejek gorczyczny oraz podobne estry znajdują się w chrzanie, rzepie, czosnku i cebuli. Olejek gorczyczny bywa stosowany w lecznictwie jako środek drażniący skórę i powodujący jej przekrwienie. W nadmiernych ilościach może powodować pęcherze na skórze, a nawet martwice. Przyjęty doustnie jako ludowy środek poronny powoduje silne przekrwienie narządów podbrzusza. Wdychany silnie drażni drogi oddechowe i może powodować obrzęk płuc. Pary olejku gorczycznego drażnią śluzówkę i mogą wywołać uszkodzenie oczu.
Większe ilości olejku gorczycznego wywołują nudności i wymioty, uszkodzenie nerek z białko- i krwiomoczem, osłabienie czynności serca i zapaść.
Bagno zwyczajne (Ledum palustre L.) zawiera silnie aromatyczny olejek w ilości 0,3-2%, którego głównym składnikiem jest trujący alkohol seskwiterpenowy - ledol. W lecznictwie ludowym stosowano go dawniej jako środek poronny, co bywało nieraz przyczyną silnych zatruć. Bagno przechowywane w mieszkaniu jako środek przeciw molom może powodować bóle i zawroty głowy. Przyjęte w dawkach toksycznych silnie drażni narządy moczowo-płciowe, wywołuje wymioty, bóle jelitowe i biegunkę oraz działa porażająco na ośrodkowy układ nerwowy.
Głuszkow opisuje przypadki zatrucia miodem wiosennym, gdy pszczoły wraz z nektarem z kwiatów pobierały substancje toksyczne. Obserwowano następujące objawy zatrucia: zawroty głowy, chwiejny chód, nudności, a nieco póŹniej wymioty, zaburzenia wzrokowe, obrazy były niewyraŹne i mało widoczne. Autor uważa, że pasieki powinny być oddalone co najmniej 5-6 km od miejsc, gdzie rośnie bagno.
Tuja wschodnia (Thuja orientalis L.) jest rośliną drzewiastą, wiecznie zieloną, często hodowaną dla celów dekoracyjnych. Zawiera olejek lotny, którego głównym składnikiem jest tujon (CH3.C6H6O.C3H7). W lecznictwie ludowym odwar z igieł tui bywał również stosowany jako środek poronny. Po wypiciu większej ilości tujonu następują ostre zaburzenia żołądkowo-jelitowe, utrata przytomności, drgawki toniczno-kloniczne, uszkodzenie nerek i mocznica.
Piołun (Artemisia absinthium L.) zawiera obok glikozydów goryczkowych olejek lotny w ilości około 0,5%, którego najważniejszym składnikiem jest absyntol (do 70%) i tujon. Olejek piołunowy potęguje działanie odurzające alkoholu, i dlatego bywa używany do sporządzania napoju, zwanego absyntem (obecnie jego produkcja jest prawnie zabroniona). Nadmierne picie absyntu doprowadza szybko do zaburzeñ nerwowych i psychicznych halucynacji, omamów i napadów padaczkowych (absinthinismus). W niektórych krajach (zwłaszcza Francja i Szwajcaria) absynt był pity w dużych ilościach, powodując znacznie cięższe objawy alkoholizmu niż po samym alkoholu etylowym.
W niektórych roślinach znajdują się związki chemiczne połączone z białkiem o silnych właściwościach trujących zwane fitotoksynami. Fitotoksyny są wrażliwe na ogrzewanie, podobnie jak białka, i w wyższej temperaturze tracą swe właściwości toksyczne. W przewodzie pokarmowym pod wpływem soków trawiennych, większość fitotoksyn jest szybko inaktywowana. Wprowadzone zwierzęciu kilkakrotnie podskórnie powodują powstawanie swoistych przeciwciał (antygenów). Fitotoksyny aglutynują krwinki w bardzo dużych rozcieñczeniach, niektóre zwiększają krzepliwość krwi lub wywołują jej hemolizę. Fitotoksyny powodują zatrucia ostre zwykle bardzo ciężkie z groŹnymi następstwami, a zwłaszcza ciężkie schorzenia nerek.
Rycyna, fitotoksyna znajdująca się w ilości 3-5% w nasionach rącznika (Ricinus communis L.). Przy wytłaczaniu oleju powstaje ona w wytłokach i nie przechodzi do oleju stosowanego w lecznictwie. Rycyna jest silną trucizną, a dawka śmiertelna dla człowieka wynosi 30 mg przy podaniu doustnym lub 3 mg podskórnie. Jeden gram rycyny może zabić 1,5 miliona świnek morskich. Również silnie trujące są nasiona rącznika i już 20 nasion może być śmiertelne dla człowieka dorosłego.
Rycyna jest polipeptydem, wchłanianym w jelitach, o silnych właściwościach proteolitycznych. Jest substancją bezbarwną, bez smaku i zapachu, i - podobnie jak jad węża lub grzybów - trucizną krwi. Nawet w znacznym rozcieñczeniu (dla człowieka 1 : 2 milionów) aglutynuje czerwone krwinki większości zwierząt. U człowieka wywołuje także częściowo hemolizę krwinek. Spożycie większej ilości nasion rycynusa powoduje bóle i zawroty głowy, ogólne osłabienie, uszkodzenie wątroby i nerek (białkomocz, urobilinuria, żółtaczka), porażenia naczyniowo-ruchowe. Zatrucia następują najczęściej wśród dzieci, które przez nieostrożność zjadły nasiona rącznika podobne do fasoli. Kaszas i Papp opisują przypadek zatrucia 10 uczniów, w wieku 11-12 lat, po spożyciu 1-6 nasion jako rzekomych orzeszków. Zastosowane leczenie opierało się na płukaniu żołądka, zwalczaniu bólów, podawaniu leków pobudzających krążenie oraz wylewów dożylnych. Po zjedzeniu 10-15 nasion rycynusa u ludzi dorosłych występowały biegunki typu cholerycznego, kurcze rąk i nóg, odwodnienie, przyspieszenie czynności serca, bezmocz, 20 nasion uważa się za dawkę śmiertelną dla człowieka dorosłego, a 5-6 dla dziecka.
Abryna, fitotoksyna znajdująca się w nasionach modligroszka (Abrus praecatorius L.) wykazuje podobne działanie aglutynujące do rycyny. Dawka śmiertelna wynosi 1 mg na kg ciężaru ciała zwierzęcego.
Fitotoksyny znajdują się jeszcze w wielu innych gatunkach roślin; występujące w grzybach i roślinach strączkowych zostały omówione w rozdziale o toksykologii artykułów spożywczych.
Oprócz omówionych grup związków toksycznych rośliny wytwarzają wiele innych substancji, często o nie ustalonej budowie chemicznej, ale o silnym działaniu farmakodynamicznym, jak np. ruta, wilczomlecz, liczne odmiany jaskrów, pierwiosnki, sumak. Wywierają one silne działanie drażniące na skórę i błonę śluzową. Odczyny i uszkodzenia organizmu wywołane przez te rośliny mogą być nieraz bardzo przykre i niebezpieczne, ale na ogół nie powodują one zatruć śmiertelnych
Aflatoksyny. W ostatnich latach na terenie wielu krajów Europy silnie rozprzestrzeniła się choroba o nieznanej początkowo etiologii, od której ginęło w znacznych ilościach młode bydło hodowlane i ptactwo domowe. Intensywnie przeprowadzone badania wykazywały, że wiąże się to ze sprawdzoną śrutą arachidową, cenną paszą białkową dla zwierząt, a
Formy B2 i G2 są to uwodornione postacie aflatoksyn B1 i G1, u których jest zredukowane podwójne wiązanie w zewnętrznym pierścieniu dehydrofuranowym. Oprócz tych czterech aflatoksyn znane są jeszcze dwie tzw. hydroksyaflatoksyny występujące w małych ilościach głównie w mleku i moczu zwierząt, żywionych makuchami arachidowymi. Otrzymały one nazwę aflatoksyn M1 i M2 i różnią się od poprzednich występowaniem grupy hydroksyn w pozycji 4 w skrajnym pierścieniu furanowym. Prawdopodobnie są to produkty przemian metabolicznych aflatoksyny B1 i B2.
Aflatoksyny mogą powstawać i na innych produktach roślinnych porażonych tą pleśnią (kukurydza, zboża, owies, rzepak, otręby, groch itp.), ale optimum wzrostu Aspergillus flavus jest w temperaturze 30-33oC oraz przy zawartości wilgoci 18-20%, a więc w warunkach, które występują w krajach tropikalnych.
W czystej postaci chemicznej aflatoksyny są bardzo wrażliwe na temperaturę, światło, utlenienie tlenem powietrza oraz na działanie kwasów lub zasad. Natomiast w warunkach naturalnych w roślinie bądŹ w organizmie zwierzęcym związki te są dość trwałe. Aflatoksyny dobrze rozpuszczają się w chloroformie, metanolu, acetonie i tłuszczach, natomiast nie rozpuszczają się w wodzie i w eterze naftowym. Tylko w niewielkich ilościach gromadzą się w wątrobie i nerkach (6-9%). Wydalają się aflatoksyny z moczem, kałem i mlekiem, przy czym głównie w formie M1 i M2, a tylko około 8% w nie zmienionej postaci.
Zatrucia aflatoksynami zarówno ostre jak i przewlekłe, są opisane dotychczas jedynie wśród zwierząt hodowlanych i ptactwa domowego karmionego paszą porażoną tą pleśnią. Różna jest toksyczność aflatoksyn zależnie od gatunku zwierząt. Przy podaniu per os dawka LD50 dla kacząt i pstrągów, które są szczególnie wrażliwe na aflatoksyny, wynosi 0,3 mg/kg, dla szczura, świnki morskiej, psa i świni - około 1 mg/kg, a dla chomika około 10 mg/kg. Do mało wrażliwych na te związki należą owce i myszy. Znacznie silniej reagują na aflatoksynę zwierzęta młode, zwłaszcza w początkowym okresie swego życia, dlatego też
biologiczną ocenę toksyczności wykonuje się na kaczątkach 1-dniowych, dla których dawka LD50 wynosi dla aflatoksyny: B1 18,2 μg, G1 - 39,2 μg, B2 - 84,4 μg, G2 - 172,5 μg na kg.
Do objawów występujących w ostrych zatruciach aflatoksyną należą: brak łaknienia, apatia, wyczerpanie, drgawki, przykurcze, porażenia, biegunka (nieraz krwawa), obrzęki, wodobrzusze, wybroczyny pod skórą, żółtaczka. W zatruciach przewlekłych występują głównie ogniska zapalne, zaburzenia czynnościowe wątroby oraz zmiany nowotworowe. U kaczek stwierdzono zmiany zwyrodnieniowe komórek miąższu wątrobowego i proliferację komórek wyścielających kanaliki żółciowe oraz nabrzmienia i zmiany morfologiczne mitochondrii. Przy dłuższym podawaniu aflatoksyny występuje silna hiperplazja kanalików żółciowych oraz stwierdza się typowy obraz raka wątroby. Przypuszczalnie aflatoksyny są inhibitorami syntezy białek, wiążą DNA i hamują syntezę RNA zależną od kwasu desoksyrybonukleinowego.
Aktywność rakotwórcza aflatoksyny jest bardzo duża i określa się ją na 10 μg dziennie. Analogiczne dawki dla innych silnie działających środków rakotwórczych wynoszą: dla dwumetylonitrozoaminy 750 μg dziennie, a dla żółci masłowej (p-aminoazobenzen) 9000 μg dziennie.
Brak jest doniesieñ o zatruciach wśród ludzi, można jednak przypuszczać, że organizm człowieka jest wrażliwy na aflatoksyny. Badania Zuckermana i współpr. przeprowadzone na ludzkich komórkach wątrobowych in vitro wykazały ich wielką wrażliwość na działanie rakotwórcze, podobne do wrażliwości wątroby szczura. Działanie cytotoksyczne aflatoksyny B1 wynosiło 1 ppm, dla G1 - 5 ppm i dla G2 - 16 ppm, ilości wywołujące zmiany nowotworowe w wątrobie 1-dniowych kacząt. Istnieje przypuszczenie, że częste występowanie raka wątroby u ludności zamieszkującej rejony Afryki Centralnej i inne kraje
Rozpoznanie zatruć aflatoksyną jest bardzo trudne, gdyż brak wyraŹnych swoistych objawów. Pomocne są tu badania laboratoryjne oraz wczesne usunięcie porażonego pokarmu. Zatrucia przewlekłe dają zmiany nieodwracalne i dlatego wielkie znaczenie ma ochrona człowieka i zwierząt przed spożywaniem orzechów arachidowych i innych produktów porażonych przez kropidlaka żółtego. Leczenie zatruć jest tylko objawowe.
JADY ZWIERZĘCE
W świecie zwierzęcym znajdują się wiele organizmów, które wytwarzają substancje trujące, często o niezmiernie silnych właściwościach toksykodynamicznych. Zwierzęta te można podzielić na powodujące zatrucia czynne lub bierne. Zwierzęta czynnie toksyczne mają odpowiednie narządy wytwarzające truciznę oraz mechanizmy, za pomocą których zwierzę potrafi przenieść jad na człowieka lub inny organizm. Natomiast zwierzęta biernie toksyczne wytwarzają nie w specjalnych narządach, lecz w całym organizmie toksyny, które działają dopiero po spożyciu zwierzęcia.
Na całym świecie zatrucia jadami zwierzęcymi zdarzają się dość często, szczególnie w krajach strefy tropikalnej. Statystyki Światowej Organizacji Zdrowia podają, że rocznie jest notowanych około 500 tysięcy ukąszeñ przez węże, z tego blisko 40 tysięcy koñczy się śmiercią, W samej Azji notuje się około 35 tysięcy zgonów, w tym w Indiach 11 tysięcy. W Ameryce Południowej rocznie ginie od 3 do 4 tysięcy osób, a w Ameryce Północnej 300-500 osób. W Europie notowanych jest rocznie około 50 przypadków śmiertelnych od ukąszeñ przez żmije.
Pod względem chemicznym jady zwierzęce stanowią wielką różnorodność i w większości nie są jeszcze dostatecznie poznane. Na ogół należą one do toksalbumin, które działają jedynie po wprowadzeniu pozajelitowym, w przewodzie pokarmowym bowiem ulegają szybko rozkładowi pod względem soków trawiennych. Tylko niektóre jady zwierzęce należą do związków szeregu tłuszczowego lub organicznego kwasów czy zasad.
Zatrucia jadami zwierzęcymi mają przebieg ostry i gwałtowny, o szybkim rozwoju objawów. Są to zatrucia samobójcze lub mordercze.
Jady zwierzęce podawane pozajelitowo w małych dawkach wytwarzają w organizmie ciała odpornościowe, neutralizujące działanie trucizny. Umożliwia to wytwarzanie odporności biernej u ludzi i zwierząt oraz produkcję surowic odpornościowych, stosowanych przy ukąszeniach zwierząt jadowitych (antisera).
Niekiedy mogą wystąpić zatrucia wywołane przez produkty rozkładu białka zwierzęcego. Szybkość i siła rozwoju zatrucia tymi produktami zależna jest od składu i budowy białka zwierzęcego, jak również czynników zewnętrznych wpływających na rozkład.
Wiele jest gatunków zwierząt wytwarzających substancje trujące, począwszy od najprostszych jednokomórkowych (ameby) i bezkręgowców (owady, pająki, skorpiony, mięczaki i inne) aż do kręgowców (ryby, płazy, gady).
W naszych warunkach geoklimatycznych spotyka się tylko nieliczne gatunki zwierząt jadowitych, jak kantarydy, pszczoły, szerszenie, osy, ropuchy, żmije. W innych krajach większe znaczenie toksykologiczne przedstawiają także niektóre gatunki pająków, skorpionów, ryb i węży.
Toksyczność jadów zwierzęcych jest bardzo duża i różni się zależnie od gatunku zwierzęcia.
Toksyczność niektórych jadów zwierzęcych przedstawiono w tabeli 6.
Tabela 6. Toksyczność niektórych jadów zwierzęcych
Rodzaj jadu |
Dawka w mg/kg |
Rodzaj zwierzęcia |
Sposób podania |
Przypuszczalna dawka śmiertelna dla człowieka (70 kg) w mg |
Jad pszczeli |
3,5 |
Mysz |
Dożylnie |
245,0 |
Bufotoksyna (Bufo vulgaris) |
0,3 |
Kot |
Dożylnie |
21,0 |
Krotaktyna (z jadu grzechotnika) |
0,065 |
Mysz |
Dootrzewn. |
4,55 |
Krotamina (z jadu grzechotnika) |
1,0 |
Mysz |
Dootrzewn. |
70,0 |
Krotoksyna (z jadu grzechotnika) |
0,1 |
Mysz |
Dootrzewn. |
7,0 |
Neurotoksyna (z jadu kobry) |
0,021 |
Gołąb |
Domieśn. |
1,47 |
Jad ryby Fugu |
0,008 |
Mysz |
Dootrzewn. |
0,56 |
Salamandaryna |
3,4 |
Mysz |
Podskórnie |
238,0 |
Butotoksyna (z jadu skorpionów) |
0,5 |
Mysz |
Dożylnie |
35,0 |
Jad małży |
0,05 |
Mysz |
Dootrzewn. |
3,5 |
Jady żmij |
1,5 - 2,5 |
Mysz |
Podskórnie |
105 - 175,0 |
Fosfolipazy (z jadu grzechotnika) |
5,0 |
Mysz |
Domieśn. |
350,0 |
Owady. W dużej klasie owadów jest wiele gatunków, które mają bierne lub czynne właściwości toksyczne. Gąsienice niektórych motyli wydzielają toksyczne substancje, które mogą powodować schorzenia skórne u człowieka. Drobne, kruche włoski gąsienic, w formie pyłu lub przenoszone brudnymi rękoma, mogą wywoływać pokrzywki, stany zapalne skóry, zapalenie spojówek, dychawicę oskrzelową. Objawy takie mogą występować u osób mających zawodowy kontakt z owadami (obróbka kokonów jedwabnika). Wśród błonkoskrzydłych są owady kłujące, które w czasie użądlenia wydzielają substancje toksyczne. Inne znów, jak mrówki, wydzielają substancje toksyczne w czasie ukąszenia. Niektóre gatunki chrząszczy wytwarzają także związki o silnych właściwościach toksykodynamicznych (kantarydy).
Ponadto liczne owady, jak komary, muchy, pchły, wszy, pluskwy, są biernie niebezpieczne, gdyż są przenosicielami drobnoustrojów chorobotwórczych (malaria, śpiączka tropikalna, tyfus plamisty, dżuma i wiele innych). Ukłucia tych owadów mogą spowodować lokalne podrażnienia skórne, obrzęki, swędzenia, niebezpieczne zwłaszcza przy nadwrażliwości ustrojowej.
Pszczoły, osy, szerszenie. Objawy występujące po ukąszeniu tych owadów przebiegają podobnie, jednakże najlepiej jest poznana toksykologia jadu pszczelego. Wytwarzany on jest jedynie u pszczół robotnic i u królowej, gromadzony w pęcherzyku jadowym, w ilości około 0,3 mg i wydalany jednorazowo wraz z ukłuciem. W jadzie tym wykazano obecność histaminy, substancji białkowych, toksalbumin, działających hemolitycznie i silnie kurcząco na jelito cienkie świnki morskiej, oraz kwasu mrówkowego. W działaniu swym jad pszczeli, podobnie do jadu węży, czynny jest tylko pozajelitowo. Substancje hemolityczne saponinowe obniżają krzepliwość krwi i mogą powodować krwiomocz oraz krwawienie maciczne. Wyodrębniona neurotoksyna jest trucizną drgawkową i ulega unieczynnieniu pod wpływem enzymów, środków utleniających itp.
Toksyczność jadu pszczelego jest odmienna dla różnych gatunków zwierząt. Zimnokrwiste i jeż wykazują dużą odporność, człowiek zaś i inne ssaki są bardziej wrażliwe. U człowieka użądlenie pszczoły powoduje silny ból i obrzęk. U osób wrażliwych już 3-5 użądleñ może wywołać odczyny ogólne, jak wzrost temperatury ciała, przyspieszenie tętna, bóle i zawroty głowy, mdłości, wysypki, obrzęki. U ludzi zdrowych dopiero powyżej 500 użądleñ może spowodować zejście śmiertelne. Ale znane są również przypadki, że po jednym lub kilku użądleniach już po 10-15 minutach następowała zapaść, uczucie lęku, biegunka, duszność i porażenie oddechu. Występowało to u osób szczególnie wrażliwych lub też w przypadku nakłucia większych naczyñ krwionośnych. O nagłej śmierci mężczyzny 53-letniego od jadu pszczoły donosi Dascaln. Pierwsze użądlenie, wywołało silny odczyn alergiczny. W miesiąc póŹniej drugie użądlenie - podobne objawy, ale z większym nasileniem. W trzy tygodnie póŹniej po trzecim użądleniu nastąpiła śmierć. Jad pszczeli może łatwo wywołać odczyny miejscowe wskutek zwiększenia przepuszczalności tkankowej. Przypuszczalnie jest to wynikiem zawartej w jadzie hialuronidazy, jak również uszkodzenia naczyñ włosowatych. Szczególnie niebezpieczny jest obrzęk w obrębie krtani, co może powodować nawet zejście śmiertelne. Zwykle objawy użądleñ ustępują po 4-5 godzinach, niekiedy jednak uczucie znużenia i bóle głowy mogą trwać przez kilka dni.
W ciężkich objawach wstrząsu należy jak najszybciej podać dożylnie glukonian wapniowy (20 cm3 20% roztworu) oraz 0,5-1 mg adrenaliny podskórnie. W razie obrzęku krtani może być niezbędna tracheotomia. Ostatnio z dobrym wynikiem stosuje się preparaty kortyzonowe, w postaci maści jak i wstrzyknięć. Świeże ukłucia należy natychmiast zwilżyć amoniakiem, roztworem wodorowęglanu sodowego lub też słabym roztworem nadmanganianu potasowego.
Kantarydyna. Majka lekarska, zwana muchą hiszpañską lub kantarydą (Lytta vesicatoria). W starożytności była używana w lecznictwie jako środek moczopędny i poronny. W postaci maści, nalewki i plastrów jeszcze do niedawna były stosowane w lecznictwie w celu wywołania miejscowego przekrwienia skóry. Chrząszcze te powinny zawierać co najmniej 0,7% kantarydyny w suchej masie owada. Jest to substancja krystaliczna, rozpuszczalna w tłuszczach i praktycznie nierozpuszczalna w wodzie. Największą wrażliwość na kantarydynę wykazuje człowiek. Wiele zwierząt może bez szkody dla zdrowia jeść te owady (np. jeże, kury, kaczki). Już 0,1 mg kantarydyny wywołuje na skórze człowieka zaczerwienienie, uczucie bólu, a po kilku godzinach pęcherze. Przyjęta doustnie w ilości powyżej 5 mg kantarydyna wywołuje pieczenie i powstawanie pęcherzy w ustach, obrzmienia gruczołów ślinowych, bóle w przełyku, kurcze żołądka, wymioty i krwawą biegunkę. Kantarydyna wywołuje krwotoczne zapalenie nerek i ciężkie uszkodzenie kanalików nerkowych, a ponadto silne przekrwienie i podrażnienie narządu moczowo-płciowego. Opisano przypadki śmierci w czasie 18 godzin po omyłkowym spożyciu 65-130 mg kantarydyny. Dla człowieka dawka śmiertelna much hiszpañskich, zawierających około 2% kantarydyny, wynosi 2-3 g, natomiast substancji krystalicznej 40-80 mg.
Do leczenia zatruć kantarydyną brak jest swoistych odtrutek. We wcześnie stwierdzonych przypadkach zatruć drogą pokarmową stosuje się płukanie żołądka, węgiel lub antidotum universale. Celowe jest podawanie dużych ilości wodorowęglanu sodowego aż do osiągnięcia odczynu zasadowego moczu oraz obfite podawanie płynów, aby ułatwić wydalenie kantarydyny z moczem.
W przyrodzie, a zwłaszcza w krajach tropikalnych, znajduje się jeszcze wiele innych gatunków owadów, jak mrówki, muchy, komary, bąki, kleszcze, gąsienice motyli i inne, które poprzez ukłucia wprowadzają jad lub też działają biernie przy zetknięciu się z parzydełkami, czułkami itp. Toksyny tych owadów wywołują reakcje miejscowe na skórze w postaci stanów zapalnych, opuchnięć, pęcherzy, swędzenia i bólu, miejscowych krwawieñ itp. Wskutek silnego drapania często następują uszkodzenia skóry i wtórne zakażenia. Przy nakłuciach owady te mogą nieraz wprowadzić do krwi chorobotwórcze wirusy lub pasożyty.
Skorpiony. Rząd skorpionów należy do najstarszych żyjących odmian zwierzęcych. Użądlenia przez skorpiony występujące w Europie powodują jedynie miejscowe, krótkotrwałe odczyny, natomiast gatunki żyjące w krajach tropikalnych jak Tityus czy Buthus, wytwarzają jad bardzo silnie trujący. Toksyczność tego jadu ulega dużym wahaniom w zależności od pory roku i gatunku zwierzęcia. Skład chemiczny jadu skorpionów nie jest jeszcze poznany, ale wywiera on silniejsze działanie na organizmy o wyższym zróżnicowaniu układu nerwowego i to jedynie po wprowadzeniu pozajelitowo. Jady poszczególnych gatunków skorpionów różnią się znacznie między sobą i wykazując pewne podobieñstwo do jadu węża nie są jednak z nimi identyczne. Wyizolowana toksyna jest bardzo zbliżona do neurotoksyny jadu wężów. Ponadto jad skorpionów zawiera niedializujące toksyczne substancje białkowe, które wywierają działanie hemolityczne, proteolityczne oraz pobudzające lub hamujące krzepliwość krwi. W jadzie niektórych skorpionów stwierdzono także obecność serotoniny, hialuronidazy lub substancji o działaniu antybiotyków.
Ukłucia mniej jadowitych skorpionów powodują miejscowe odczyny zapalne, bardziej jadowitych dają w miejscu ukłuć ropiejące ogniska zapalne oraz wymioty, omdlenia, drżenia i drgawki mięśniowe. Objawy zatrucia po jadach o silnym działaniu trującym rozwijają w czasie od 10 minut do 20 godzin. W miejscu ukłucia powstaje obrzęk i bolesność, która przechodzi w silne promieniujące bóle. W ciągu kilku godzin występują bóle głowy, wymioty, przyspieszenie tętna i oddechu, wzrost temperatury ciała, krwotoki żołądkowo-jelitowe i dróg oddechowych, obniżenie czucia skóry, osłabienie odruchów ściągnistych, odurzenie, niepokój, uczucie lęku, drgawki, śpiączka i obrzęk płuc, co doprowadza do zejścia śmiertelnego. Niekiedy mogą wystąpić: bolesna sztywność mięśni szyi, bóle gardła, drgawki tężcowe, przy czym może nastąpić śmierć przez zatrzymanie oddechu. Szczególnie wrażliwe na ten jad są dzieci.
Przy ratowaniu zatruć jadem skorpionów podaje się swoistą surowicę, przy czym optymalne jej działanie występuje do 4 godzin po ukłuciu. Surowice takie są produkowane w Algierii, Brazylii i Meksyku z jadu miejscowych gatunków skorpionów. Korzystne jest również leczenie kortyzonowymi lekami stosowanymi zarówno miejscowo, jak i ogólnie.
Pająki. Jady pająków nie są jednakowe pod względem immunologicznym i różnią się od jadów skorpionów i węży. Dla człowieka tylko niektóre gatunki tropikalnych pająków są toksyczne, przy czym szczególnie niebezpieczny jest pająk zwany „czarna wdowa” (Latrodectus mactans), którego ukłucia mogą powodować zejścia śmiertelne.
Jad pająków jest cieczą zwykle bezbarwną i lekko oleistą, przy czym jej toksyczność ulega wahaniom zależnie od pory roku. Skład chemiczny nie jest jeszcze poznany, stwierdzono obecność neurotoksyny o charakterze lipoproteidów, wolne aminokwasy z dużą ilością kwasu glutaminowego, silnie zasadową substancję oraz enzym proteolityczny podobny do trypsyny, hialurodnidazę i inne.
W miejscu ukłucia przez pająki gatunku Latrodectus powstają tylko nieznaczne odczyny lub brak ich w ogóle, natomiast wyraŹnie występują objawy ogólne. Z miejsca nakłucia rozchodzą się promieniujące bóle, występują drżenia mięśni koñczyn, poty, dreszcze, uczucie niepokoju, zawroty głowy, hipotermia, drgawki kloniczno-toniczne oraz zaburzenie, a nawet zahamowanie oddechu, lub obrzęk płuc.
Inne gatunki pająków, jak krzyżak, tarantula itp., wywołują przede wszystkim objawy miejscowe. Początkowo powstaje mała brodawka z czerwoną obwódką i obrzęk na dużej powierzchni, który po wielu dniach lub tygodniach powoduje zmiany martwicze tkanki, rozprzestrzeniające się nieraz na całą koñczynę. Ból występuje zwykle dopiero po pewnym czasie. Obok tego mogą występować objawy ogólne, jak gorączka, pokrzywka, krwiomocz i białkomocz, ale nie są one groŹne dla życia.
W zatruciach jadem pająków stosuje się swoistą surowicę odpornościową, która powinna być podana najpóŹniej w ciągu 24 godzin od ukąszenia. Stosuje się również miejscowo i ogólnie leki kortyzonowe i antyhistaminowe.
Różne gatunki mięczaków, jak ślimaki, małże itp., wytwarzają silne jady, przy czym toksyny niektórych ślimaków (Aplysia depilans L.) już w starożytności były używane jako trucizny do celów morderczych.
Budowa chemiczna jadów tych zwierząt nie jest jeszcze poznana. Ślimaki z rodziny Muricidae wytwarzają substancję, zwaną mureksyną, która przy hydrolizie rozkłada się na cholinę i kwas urokaninowy (kwas β-imidazoliloakrylowy). Mureksyna wykazuje silne działanie nikotynowe i kurarynowe.
Zatrucia ostre nagłe, nieraz masowe i śmiertelne, występują po spożyciu małży z gatunku Mytilus californianus, co zostało opisane w rozdziale o toksykologii produktów spożywczych.
Niektóre gatunki meduz mają parzydełka zawierające jad parzący. Przy zetknięciu ze skórą ludzką już po 10-15 minutach mogą występować objawy przykrego i bolesnego pieczenia, swędzenia oraz tworzenia się pęcherzy. W ciężkich zatruciach stwierdza się niekiedy także objawy ucisku w klatce piersiowej, kurcze mięśni oddechowych, duszność, uczucie znużenia, bóle głowy, drgawki, rzadziej biegunkę i zapaść.
Ryby. Z dużej klasy ryb, liczącej około 20 tysięcy gatunków, przeszło 600 rodzajów wytwarza substancje trujące. Mogą się one zbierać w specjalnych gruczołach pod płetwą grzbietową lub przy ogonie i wydzielać przez specjalne narządy po zranieniu swojej ofiary (ryby czynnie trujące) lub też działać szkodliwie dopiero po spożyciu ryby zawierającej substancje trujące w swym organizmie (ryby biernie trujące).
Budowa chemiczna jadu ryb nie jest jeszcze poznana, są to jednak substancje o budowie białkowej i tylko nieliczne wywołują zatrucia przez przewód pokarmowy.
Przebieg zatruć jest odmienny dla różnych gatunków ryb, można jednak odróżnić cztery zasadnicze rodzaje działania toksycznego:
1. Zatrucia gatunkiem Fugu - ryby kule (Tetrodontidae i pokrewne rodziny), żyją w morzach Japonii, gdzie są używane jako pokarm. Ustalenie, które ryby zawierają substancje trujące, jest bardzo trudne, ponieważ są one toksyczne tylko w określonych okolicach i w różnym czasie. Rocznie w Japonii zdarza się przeszło 100 wypadków zatruć tymi rybami, przy czym śmiertelność wynosi około 60%. Już po 30 minutach po spożyciu trującej ryby występują charakterystyczne objawy ciężkiego porażenia - znieczulenie warg, języka, koñców palców, bóle i zawroty głowy, nudności, wymioty, bóle brzucha. Śmierć następuje przez porażenie mięśni oddechowych nieraz po 1 godzinie, zwykle zaś w ciągu 20-40 godzinach. Substancję trującą jest ciepłostała tetrodotoksyna. Wywołuje ona porażenie ośrodkowego układu nerwowego oraz działanie kurarynowe na płytkę motoryczną. Dawka śmiertelna podskórna dla myszy wynosi 0,01 μg na 1 g.
Badania przeprowadzone z tetrodotoksyną wykazują, że silniejsze niż na mięśnie jest jej działanie na ośrodek oddechowy, co stanowi zwykle przyczynę śmierci. W zatruciach zaleca się sztuczne oddychanie oraz podawanie środków pobudzających oddech.
2. Zatrucia gatunkiem murena (rodzina Muraenidae, zwłaszcza rodzaj Gymnothorax). Ryby te żyją w morzach tropikalnych i zawierają substancje trujące w błonie śluzowej podniebienia, wydalane przy ukąszeniu swej ofiary. Toksyny te znajdują się także w mięśniach i narządach wewnętrznych, wywołując zatrucia po spożyciu. Ukąszenia mureny są nadzwyczaj bolesne, wywołują miejscowe obrzmienie i martwice. W cięższych przypadkach zatruć rozwijają się objawy ogólne, jak zaburzenia krążenia i oddechu, drgawki o charakterze padaczkowym itp., a w przypadku spożycia ryby - zawroty głowy, wymioty, ślinotok oraz objawy porażenia układu nerwowego. Śmiertelność wynosi około 10%.
3. Zatrucia makrelami (rodz. Scombridae) zbliżone są do zatruć histaminą. Objawy toksyczne charakteryzują się bólem głowy, wymiotami, uczuciem gorąca na twarzy i nieco póŹniej wysypkami pokrzywkowymi. Zatrucia te nie powodują groŹniejszych następstw.
4. Inne zatrucia rybami wywołują objawy żołądkowo-jelitowe: wymioty, biegunkę, silne bóle brzucha i gorączkę. Śmiertelność wynosi około 2-3%. Zatrucia tego rodzaju powodują między innymi brzany ( Barbus fluviatilis), o których była mowa w rozdziale o zatruciach produktami spożywczymi.
Niektóre ryby, jak węgorze, liny, tuñczyki, zawierają silnie toksyczną surowicę krwi, działającą hemolitycznie. Obok nie zidentyfikowanej toksyny niekiedy w małych ilościach znajduje się także 5-hydroksytryptamina. Śmierć przez porażenie oddechu, poprzedzane krótkotrwałym pobudzeniem, następuje tylko po wprowadzeniu tych toksyn pozajelitowo.
Niekiedy zatrucia mogą wystąpić po spożyciu ikry wielu gatunków ryb. Wskutek szybkiego rozkładu pod wpływem enzymów mogą powstać substancje o budowie polipeptydowej, które podane pozajelitowo działają toksycznie, Są to protaminy, zawierające dużą zawartość argininy, oraz serynę, prolinę, alaninę, walinę i inne aminokwasy. Najbardziej znanymi przedstawicielami protamin są wyodrębnione z ikry łososia - salmina i ze śledzia - klupeina. Do czynnie jadowitych ryb należą także żyjące w Morzu Północnym i na Atlantyku ryby gatunku Trachinoidae (Trachinus draco i inne). Pod płetwą grzbietową i pod pokrywą skrzelową mają one gruczoły jadowe, które przy zetknięciu lub ukłuciu wydzielają silnie toksyczny jad. W miejscach ukłucia, zwykle nogi lub ręki, następuje obrzęk i ból, a gdy nie nastąpi szybki ucisk koñczyny, stan zapalny rozszerza się na tułów, powodując ogólne osłabienie, gorączkę, sinicę, zawroty głowy i przyspieszoną czynność serca. Niekiedy w miejscu ukłucia może powstać martwica nie tylko tkanek miękkich, ale i kości.
Leczenie zatruć wywołanych jadem ryb prowadzi się podobnie do zatruć jadami innych zwierząt. Podaje się dożylnie glukonian wapniowy, a w przypadku spożycia ryby trującej postępuje się podobnie jak przy zatruciach pokarmowych. Ponadto stosuje się leczenie objawowe oraz terapię kortyzonową.
Płazy. Wśród płazów znajduje się wiele gatunków wytwarzających jady w gruczołach rozmieszczonych pod całą skórą lub w niektórych częściach ciała, z niekiedy może oddziaływać toksycznie także śluz, którym są one zawsze pokryte. Wydzielina śluzowa zawiera substancje białkowe i jest bardzo słabo toksyczna, wydzielina zaś gruczołów jadowych jest barwy mlecznej, o odczynie kwaśnym i często swoistym zapachu. Płazy nie mają specjalnych narządów do wprowadzania trucizny i są one toksycznie bierne, tj. odstraszają głównie swych wrogów i chronią się tym przed pożarcie. Jady płazów należą do najlepiej poznanych pod względem chemicznym i w wielu przypadkach mają już ustaloną budowę strukturalną.
W jadzie salamandry zostały wyodrębnione 3 substancje: samandaryna, samandaron oraz samandarydyna. Obok tych związków znajdują się wielkocząsteczkowe substancje przypuszczalnie o budowie białkowej, które działają hemolitycznie i miejscowo drażniąco.
Samandaryna jest silną trucizną kurczową, o działaniu ośrodkowym z głównym punktem uchwytu w rdzeniu przedłużonym.
Dokładnie poznany jest także jad ropuchy (różne gatunki z rodziny Bufonidae) Lecznicze działanie nasercowe skóry lub całej ropuchy w postaci wysuszonej i sproszkowanej było znane już w starożytności. Substancja ta jest jeszcze stosowana w lecznictwie w Chinach i Japonii.
Głównymi składnikami jadu ropuchy są:
1) substancje bezazotowe o budowie sterydowej bardzo zbliżonej do aglikonów glikozydów naparstnicowych. Noszą one ogólną nazwę bufogeniny, przy czym istnieje duża ich różnorodność u różnych gatunków ropuch;
2) bufotoksyna, która jest bufoteniną, w której grupa wodorotlenowa przy atomie C-14 jest zestryfikowana przez kwas korkowy;
3) zasady organiczne, głównie pochodne indolowe, niekiedy 5-hydroksytryptamina, a także adrenalina i noradrenalina;
4) substancje śluzowe nieznanej budowy, o działaniu hemolitycznym i aglutynującym; występują one u niektórych ropuch;
5) substancje redukujące, jak kwas askorbinowy, glutation oraz cholesteryna, ergosteryna.
Jady ropuch są truciznami działającymi na serce w sposób podobny do glikozydów nasercowych.
Węże jadowite. Zatrucia jadami węży stanowią największe niebezpieczeñstwo dla człowieka spośród wszystkich zatruć zwierzęcych. W około 2500 istniejących gatunków węży blisko 360 jest trujących. Większość jadowitych węży żyje w krajach o klimacie gorącym, w Europie spotyka się jedynie gatunki żmij (Viperidae). W piśmiennictwie podana jest duża rozpiętość toksyczności, ilości i składu chemicznego jadu węży nawet w obrębie jednego gatunku. Zależy to w dużym stopniu od pory roku, żywienia, wieku zwierzęcia, miejsca i warunków bytowych itp.
Ilość jadu grzechotnika wydalana przy jednym ukąszeniu jest wystarczająca do zabicia 4 świñ lub 12 psów, albo też 46 małp rezus. Dawka śmiertelna jest bardzo różna dla zwierząt, np. dla psów i małp wynosi 0,64 mg na kg, dla świñ i świnek morskich 3,2 mg na kg, dla szczurów 25 mg na kg.
Siła toksykodynamiczna jadu węży znacznie przewyższa najbardziej gwałtownie działające trucizny chemiczne. Podczas gdy 1 g strychniny może zabić 5 ludzi, a 1 g cyjanowodoru do 16 osób, to 1 g jadu niektórych węży stanowi dawkę śmiertelną dla 150 ludzi.
Skład jadu węży nie jest jeszcze całkowicie poznany. Jest to kompleks zawierający różne biotoksyny, ulegające rozkładowi w sokach trawiennych. Jedne z nich wywierają głównie działanie miejscowe, a inne po wchłonięciu silnie działają neurotoksycznie. Według Sloffa jady węży pod względem działania farmakologicznego można podzielić na trzy grupy:
1. Jady o działaniu kurarynowym. Wywołują one przede wszystkim zaburzenia nerwowe i w działaniu swym są podobne do kurary, podczas gdy wpływ na układ krążenia ma znaczenie uboczne. Jady te nie działają ośrodkowo, ale wywołują zaburzenia w przenoszeniu impulsów z włókien nerwowych do narządów wykonawczych. Jad kobry indyjskiej - okularnika (Naja naja) poraża mięśnie poprzecznie prążkowane jeszcze w stężeniu 1 : 100 tysięcy. Działanie kurarynowe niektórych jadów wężowych opiera się w dużej mierze na zawartości w nich esterazy cholinowej. Przedstawicielem grupy węży o tym działaniu są kobry oraz w słabszym stopniu węże grupy Solenoglypha z rodzaju Echis (rodz. Viperidae) oraz Crotalus i Bothrops (rodz. Crotalidae).
2. Jady działające na serce i układ krążenia. Ukąszenie węży tej grupy wywołuje objawy często podobne do wstrząsu anafilaktycznego, niektóre zaś jady działają bezpośrednio na czynność serca. Obok toksyn o działaniu na układ krążenia jady te zawierają silnie aktywne enzymy, jak fosfolipazy A, proteazy, adenozynotrójfosfatazy. Tego rodzaju jady wydzielają węże należące do rodziny Elapidae (kobry), Viperidae (żmije) i Crotalidae (grzechotniki).
3. Jady o działaniu miejscowym względnie wpływające na krzepliwość krwi. Jady te obok swoistych toksyn zawierają liczne enzymy, jak proteazy, fosfolipazy, hialuronidazy, koagulazy, dehydrogenazy aminokwasów i inne. Jady tego rodzaju są wydzielane przez węże z rodziny Cortalidae (grzechotniki).
Russell opisuje objawy zatruć po ukąszeniach przez 9 gatunków grzechotników spotykanych w południowej Kalifornii, przy czym objawy te mogą mieć różny przebieg. Zawsze jednak występują obrzęki, wybroczyny krwawe, bóle i obrzmienia miejscowe gruczołów limfatycznych. Obok tego powstają: osłabienie, hipotermia i silne poty, zamroczenie, mdłości albo wymioty, mrowienie lub odrętwienie języka, krwotoki i spadek hemoglobiny.
Efrati i Reif wyodrębnili bezazotowe glikozydy saponinowe z jadu kobry: ofiotoksynę C17H26O10 oraz z jadu żmij krotaloksynę C34H54O21. Ponadto stwierdzili obecność hialuronidazy we wszystkich jadach, co niewątpliwie sprzyja szybkiemu ich wchłanianiu. Obok zaburzeñ w krzepliwości krwi niektóre jady zawierają lizyny (fosfolipazy, hemolizyny), które działają na składniki morfologiczne krwi, zwłaszcza na krwinki czerwone, powodując ich hemolizę, Jady wężów mogą także wywierać działanie na ośrodkowy układ nerwowy, wywołując zawroty głowy, nudności i wymioty, hipotermię, zaburzenia oddechowe, spadek ciśnienia tętniczego krwi.
Westermann i Klapper, podając dożylnie zwierzętom jad kobry indyjskiej (Naja naja, N. nivea), stwierdzili już po kilku sekundach zwolnienie czynności serca, spadek pojemności minutowej serca oraz bezdech. Objawy te wywołują nie dializujące składniki jadu. Działanie występujące póŹniej i utrzymujące się około 30 minut przejawia się przyspieszeniem czynności serca i wzrostem jego pojemności minutowej, co jest wywołane przez frakcję dializującą. Przypuszczalnie spowodowane to jest uwolnieniem histaminy z tkanek, gdyż stężenie jej we krwi wzrasta trzykrotnie. PóŹniejsze działanie toksyczne prowadzące do zapaści i śmierci jest również wywołane przez małocząsteczkowe dializujące składniki jadu kobry.
Rozwój i nasilenie objawów zatrucia jadem węży zależą nie tylko od ich właściwości toksykodynamicznych, lecz także od warunków, w jakich nastąpiło ukąszenie, Silniejszy przebieg zatrucia wykazują ukąszenia w górnej części tułowia, w okolicy większych naczyñ żylnych lub ukąszenia w dzieñ parny i gorący. Ukąszenia węży pozostawiają charakterystyczny ślad dwóch nakłuć w odległości około 1 cm. Zależnie od rodzaju jadów objawy mogą mieć różny przebieg, ogólnie jednak zatrucia te charakteryzują się następującymi objawami: w miejscu ukąszenia występuje obrzęk z niebieskawym zabarwieniem i silną bolesnością, Wkrótce lub w ciągu godziny występują ogólne objawy zatrucia, jak krwawienia z nosa i podskórne, zawroty i bóle głowy, spadek ciśnienia tętniczego krwi, odurzenie, uczucie lęku, duszność, hipo- lub hipertermia, postępujący obrzęk płuc, nudności, a także krwawe wymioty i krwotoczna biegunka, krwiomocz, drgawki, objawy porażenia języka, krtani i oddechu. W dalszym przebiegu mogą rozwinąć się powikłania septyczne i rozległe martwice, niejednokrotnie z przebiegiem śmiertelnym.
W Europie ukąszenia żmij mają przebieg śmiertelny tylko wśród małych dzieci i ludzi starszych lub też wskutek nagłej zapaści przy dostaniu się jadu wprost do żyły. Rozległe obrzęki, bóle, wybroczyny krwotoczne i inne objawy mogą utrzymywać się przez 1-2 dni, po czym stopniowo cofają się.
Ratowanie zatrutych jadem węży opiera się na stosowaniu środków miejscowych i ogólnych. Miejscowo stosuje się natychmiast opaskę uciskową dośrodkowo od miejsca ukąszenia, najwyżej na 1 godzinę, Celowe jest wyssanie jadu z rany, ale osoba wysysająca nie może mieć żadnych skaleczeñ w jamie ustnej. Niekiedy stosuje się nacięcia nożem skóry i naczyñ pomiędzy śladami ukąszeñ. Zabiegi te są celowe przy natychmiastowym zastosowaniu, gdy jad nie został jeszcze wchłonięty do ogólnego krwiobiegu.
Należy możliwie najszybciej w okolice ukąszenia zastosować surowicę wieloważną przeciw jadowi węży w ilości 10 cm3, a w ciężkich przypadkach - do 40 cm3 dożylnie. Im póŹniej jest stosowana surowica, tym większa jej ilość musi być podana.
Poza tym, stosuje się leczenie objawowe: podanie środków antyhistaminowych jest bardzo celowe, gdyż hamują one działanie hialuronidazy. Również korzystne wyniki daje terapia lekami kartyzonowymi, począwszy od 100 do 200 mg dziennie w postaci dożylnych wlewów kroplowych. W razie potrzeby stosuje się środki cucące (koramina, kardiazol, kofeina), środki uspokajające (luminal, chloropromazyna itp.).
Silne właściwości farmakologiczne jadu węży znalazły także zastosowanie w lecznictwie. Małe dawki jadu kobry wyraŹnie zwiększają wyniki testów psychologicznych (liczenie pamięciowe). Według Machta jad kobry ma również działanie podobne do alkaloidów opiumowych z opóŹnionym okresem działania, ale za to dłużej utrzymującym się działaniem przeciwbólowym. Według Klobusitzky'ego bardzo silnie toksyczny jad węży z gatunku Bothrops, żyjących w Brazylii jest skuteczny w leczeniu krwawieñ różnego pochodzenia. Opracowany przez Klobusitzky'ego lek Botropase z wydzieliny gruczołów jadowitych grzechotników Bothrops jararaca oraz Reptillase z mieszaniny jadów Bothrops atrox i Lachesis ma działanie podobne do trombiny i trombokinazy. Lek ten wpływa na przepuszczalność naczyñ krwionośnych oraz zmniejsza kruchość ich ścian, przez co znajduje zastosowanie przy krwotokach na różnym tle. Candura, de Nicola i inni opisują podobnie korzystne działanie enzymu zwiększającego krzepliwość krwi, otrzymywanego z jadu węży Bothrops jararaca (preparat Botropase).
Ssaki. W klasie ssaków znajdują się nieliczne gatunki zwierząt wytwarzających także jady. W Australii i Nowej Gwinei żyje dziobak (Ornithorrhynchus anatimus), którego samce mają na tylnych łapach ruchomą ostrogę połączoną z gruczołami jadowymi. Skaleczenie człowieka wywołuje bóle, opuchnięcie i objawy wstrząsu. Według Kellawaya i Le Messuriera jad ten wykazuje słabe działanie koagulujące oraz hemolityczne i wywołuje objawy podobne do jadu żmij.
W rodzinie Soricidae są również gatunki podobne do myszy (Blarina brewicauda i inne), żyjące w Ameryce. Wydzielają one jad z gruczołów podszczękowych. Przy jednorazowym ugryzieniu wydzielana ilość jadu wystarcza do zabicia 200 myszy lub kilka kotów. Pod względem farmakologicznym jad ten wykazuje podobieñstwo do trypsyny. Wstrzyknięty zwierzętom powoduje spadek ciśnienia tętniczego krwi i porażenie oddechu.
LITERATURA
1. Stanisław Podhorecki, Stefan Michałek, Marian Lodowski - Bojowe środki trujące
WSOWChem. Kraków 1973r. Część I i II.
2. Stanisław Głozak - Chemia bojowych środków trujących, WAT, Warszawa 1973 r.
3. Michał Krauze, Ireneusz Nowak - Broñ chemiczna. MON, Warszawa 1985 r.
4. Jerzy Grochowski, Józef Woliñski - Bojowe środki trujące, Warszawa 1960 r.
5. W. Konig - Chemische Kamfstoffe, Berlin 1966 r.
6. R. Stochr - Chemische Kampfstoffe und Schutz vor chemischen Kampfstoffen,
Berlin 1977 r.
7. Aleksandra Stachlewska-Wróblowa - Analiza skażeñ chemicznych, Warszawa 1981 r.
8. Eugeniusz Szczucki - Chemia środków trujących. Część III. Chemia toksykologiczna,
WAT, Warszawa 1973 r.
9. Mieczysław Sokołowski - Problemy analizy niektórych wysokotoksycznych związków
chemicznych, Biuletyn WIChiR nr 1/18/91.
10. W. Raszewski - Nowa grupa wysokotoksycznych związków - bicykliczne estry fosfo-
roorganiczne, Biuletyn WIChiR nr 1/18/91.
11. J. Legocki, D. Bukowska, D. Markiewicz - Synteza niektórych bicyklicznych fosfora-
nów i tionofosforanów, Biuletyn WIChiR nr 1/18/91.
12. J. Legocki, M. Czajka, H. Nowacka-Krukowska - Rozkład hydrolityczny bicyklicznych
fosforanów i tionofosforanów w środowisku zasadowym, Biuletyn WIChiR nr 1/18/91.
13. Zarys toksykologii wojskowej. Podręcznik, MON, Warszawa 1988 r.
14. Tadeusz Dutkiewicz - Chemia toksykologiczna, PZWL, Warszawa 1968 r.
357.242.1 Środki trujące PODSTAWY BIOCHEMII I TOKSYKOLOGII WSO-TK cz. II j. pol. TOKSYKOLOGIA SZCZEGÓ£OWA
|
K. Szyszka: Podstawy biochemii i toksykologii. cz. II. Toksykologia szczegółowa Wrocław. Wyższa Szkoła Oficerska im. Tadeusza Kościuszki 1997r. s. 146, rys. 11. Skrypt zawiera materiał teoretyczny z przedmiotu „Podstawy biochemii i toksykologii” dostosowany do programu kształcenia słuchaczy WSO. Obejmuje charakterystyki toksykologiczne bojowych środków trujących i toksyn naturalnych występujących w przyrodzie. Opisane w skrypcie środki trujące ułóżone są według systematyki toksykologicznej. Każda grupa środków trujących zawiera charakterystykę ogólną, mechanizm działania toksycznegoobjawy zatrucia i podstawowe metody leczenia.
K. Sz. 10 / 97 |
Druk WSO - WIW zam......................./ 97
2
Wyszukiwarka
Podobne podstrony:
Metodyka oceny strat i zniszczeń OPBMR, Podręczniki Wojskowe, Opracowania, podręczniki i instrukcje
Metodyka szkolenia pododdziałów z broni masowego rażenia WP, Podręczniki Wojskowe, Opracowania, podr
Obrona ABC w NATO, Podręczniki Wojskowe, Opracowania, podręczniki i instrukcje Militarne
Metodyka szkolenia ogniowego WP, Podręczniki Wojskowe, Opracowania, podręczniki i instrukcje Militar
wyklad 25 bojowe srodki trujace
Bojowe środki trujące, Chemia, Biochemia
Psychotoksyczne bojowe środki trujące
wyklad 25 bojowe srodki trujace
Bojowe środki trujące
PO bojowe srodki trujace i zapalajace
Bulow Trixi von Mezczyzni Podreczna instrukcja obslugi
Środki gaśnicze i podręczny sprzęt gaśniczy, Materiały z Ostrowa
podreczna instrukcja Linksys PAP2T EU[1]
Bojowe i przemysłowe środki trujące
podreczna instrukcja Linksys PAP2T EU
T von Bulow Mężczyżni podręczna instrukcja obsługi
więcej podobnych podstron