156 3

312
Zadanie 338.
wilgotny
papierek
wskaźnikowy
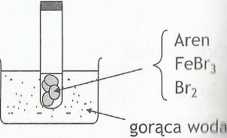
Zaprojektuj doświadczenie pozwalające udowodnić charakter aromatyczny węglowodoru w reakcji substytucji elektrofilowej z bromem. W opisie doświadczenia uwzględnij sprzęt, odczynniki, czynności, spostrzeżenia oraz wnioski.
Odpowiedź
|
Sprzęt |
Probówka, zlewka, pipeta, korek z rurką odprowadzającą gaz |
|
Odczynniki |
Węglowodór o charakterze aromatycznym (na przykład benzen, toluen), l>i<> mek żelaza(lll), brom, papierek uniwersalny, woda |
|
Opis czynności |
Do probówki zawierającej bromek żelaza(lll) wprowadzić brom i kilka kropli węglowodoru o charakterze aromatycznym. Probówkę zamknąć korkiem z rur-ką odprowadzającą wydzielany gaz i wstawić do zlewki z gorącą wodą. Do wylotu rurki odprowadzającej wydzielany gaz zbliżyć wilgotny uniwersalny pa pierek wskaźnikowy. |
|
Spostrzeżenia |
Obserwuje się odbarwienie czerwonobrunatnego roztworu bromu, uniwersalny papierek wskaźnikowy umieszczony u wylotu rurki zabarwił się na czerwono, |
|
Wniosek |
Węglowodór o charakterze aromatycznym (Ar) w obecności katalizatora I eUt, ulega reakcji substytucji elektrofilowej z bromem z wydzieleniem kwasowego produktu ubocznego reakcji. Ar + Br2 -» Ar-Br + HBr |
Zadanie 339.
Zaprojektuj doświadczenie pozwalające wykazać różnice w reaktywność i związku aromatycznego z łańcuchem alifatycznym w zależności od wamm ków reakcji na przykładzie reakcji toluenu z chlorem. W opisie doświ.uk ^ nia uwzględnij sprzęt, odczynniki, czynności, spostrzeżenia oraz wnioski.
Odpowiedź
|
Sprzęt |
2 probówki z rurką boczną, pipety, korki, źródło światła |
|
Odczynniki |
Toluen, chlor, chlorek żelaza(lll), papierki uniwersalne |
|
Opis czynności |
Należy wykonać dwie próby: 1. Do probówki z toluenem, na którą skierowano promieniowanie ulliafinlfMu we, wprowadzić chlor. W pobliżu rurki bocznej probówki umieścić zwilżony papierek uniwersalny. 2. Do probówki z toluenem dodać chlorek /elnza(lll) i wprowadzić chlnt Pin bówki zamknąć korkami l zawaitośr miewać W pnbli u tutki bm -me) pe = bówki umieścić zwilżony uniwersalny papierek wskaźnikowy |
|
'.( H r.ł l --e .T-nin |
w obu próbit h obi§twuje się zanik żółtozielonego zatrat wienia chloru, /wilło ne uniwerialne papierki wskaźnikowe umieli* zona w pobliiu rutek bo* inyrh ifebówik ' ierwiinitł ijf. |
W zależności od warunków reakcji aren z tańcuchem ,tłumy /nym z chlorem reaguje różnie. W obecności światła zachod/i trakt ja ij rodnikowej w łańcuchu bocznym, na przykład dla toluenu.
Wnioski
C6H5CH3+ Cl2 UV > C6H5CH2Cl + HCl
chlorofenylometan
W obecności katalizatora zachodzi reakcja substytucji elekt rofilowij kład dla toluenu:
C6H5CH3+ Cl2 - - FeCl3 > C6H4CICH3 + HClt
o- i p-chlorometylobenzen
Reakcji substytucji elektrofilowej towarzyszy powstawanie gazowia tu reakcji o charakterze kwasowym, który w obecności wody libflfl rek wskaźnikowy, gdyż dysocjuje zgodnie z równaniem trakt ij
Hci(aq) + h2o -> cr + H30+
Ro/ióżmenie węglowodorów
mimie 340.
/^projektuj doświadczenie pozwalające rozróżnić etan i etyn v i inanganianem(VII) potasu. W opisie doświadczenia uw/ylędnt odczynniki, czynności, spostrzeżenia oraz wnioski.
* łfjptlwied/
|
i SpOft |
Probówki, butla z badanymi gazami, rutki doprowadza)qf e ya?y. pipt |
|
r,,,! wirniki |
Etan, etyn, manganian(VII) potasu |
|
Ofitś , /yttnośt l |
Należy przygotować dwie probówki / rozciefu/tinyffl inriwmmtt rj nu(VII) potasu, a następnie do probówek wprowadzić badana wiglnd |
|
1 leżenia |
Etan nie reaguje z manganianem(Vli) potasu. Pi/epuiz- ..«ni• • t ,n,, p bówke z rozcieńczonym roztworem manganlanu(VI!) potasu powoduj |
|
Wlenie fioletowego roztworu i wytrącenie brunatnego osadu | |
|
j Wnioski |
Etan nie reaguje / mfliiganlanem(VII) potasu, en potwltrdza i«-y charakter. Liyn w tral« jt / mnnyaiiiaimtM(VII) potasu ulega uilemetmi igodnis Hieni tealu |i 1 KMn©4 * I H-( =' II > 1 Mn( >, l r 1 l<0QC-CQQK + 1 KOH + I Hj§ 2 c' 2 C + R * 3 Mn * 3 e > Mn /1 R |
Wyszukiwarka
Podobne podstrony:
84 2 ! i mlt wi > - ii .• - i suhitam i*7«dan1© 169. Zaprojektuj doświadczenie pozwalające na
166 3 332Zadanie 369.Zaprojektuj doświadczenie pozwalające rozróżnić sacharozę od skrobi. W opisie
ftidanip wlaśc(Cl2, Bn i , ( ! U I) zwlą/kóvZadanie 188. Zaprojektuj doświadczenie pozwalające na
jednofunkcyjne pochodne węglowodorów 1. Zaprojektuj doświadczenie, by: a), odróżni
Wykład 2 Pomiar pH 1. pH-metr 2. papierki wskaźnikowe 3.
weglowodory�8 Węglowodory Zadanie 588 (3 pkt.) Y/2007/A2 Zaprojektuj jedno doświadczenie pozwalające
chemiafilmowy�9 Zadanie 2. Zaprojektuj doświadczenie, za pomocą którego wykażesz, że wodorotlenek gl
roztwór, którego odczyn, chcemy zbadać uniwersalny - papierek wskaźnikowy
CHjNHjCI chlorowodorek metyloaminy, chlorek metyloamoniowy uniwersalny papierek wskaźnikowy Czy za
Zaprojektuj doświadczenie (hipotezę, pytanie badawcze, przebieg eksperymentu,
Segregator2 Strona!8 Zadanie 16. 5 pkt Zaprojektuj doświadczenie, w którym wykażes
więcej podobnych podstron