1tom307

12. ELEKTROCHEMIA 616
Sumaryczne reakcje prądotwórcze zachodzące w poszczególnych rodzajach akumul torów są następujące:
w ogniwie o schemacie PbO, | H,S04aq | Pb
a-
Pb + PbO, + 2H,SOj.
wyładowanie
ładowanie
2PbS04 + 2H,0
— w ogniwie o schemacie NiO(OH)| KOHaq |Cd
Cd + 2NiO(OH) + 2H,0 Cd(OH), + 2Ni(OH),
— w ogniwie o schemacie Ag,01 KOHaq | Zn Ag20 + Zn U 2Ag + ZnO Akumulatory ołowiowe
W naczyniu kwasoodpornym z ebonitu, polipropylenu, poliakrylostyrenu lub szklą znajdują się płyty akumulatorowe z substancjami czynnymi. Stosuje się płyty wielko-powierzchniowe (Plantego) z masą czynną wytworzoną z materiału płyty, pastowane (Faure’a) z masą czynną osadzoną w kratce z ołowiu twardego (stopu Pb + Sb + Se lub Pb + Ca + Sn) oraz pancerne z masą osadzoną w osłonach rurkowych z tworzywa. Płyty w naczyniu łączy się w zespoły dodatnie i ujemne. Rozdziela sieje separatorami z materiału mikroporowatego (np. polietylenu, impregnowanego papieru) lub prętami ebonitowymi. Naczynie zamyka uszczelnione wieczko, z otworem wlewowym zaopatrzonym w korek wentylacyjny lub bez otworu z zaworem bezpieczeństwa.
Jako elektrolit stosuje się wodny roztwór kwasu siarkowego o gęstości zależnej od rodzaju akumulatorów'. Właściwości elektrolitu przedstawiono na rys. 12.5. Właściwości poszczególnych rodzajów akumulatorów zestawiono w tabl. 12.4. W tablicy podano charakterystyczne wielkości akumulatorów, np.:
— sprawność elektryczną — stosunek pojemności elektrycznej akumulatora do ładunku potrzebnego do jego naładowania;
— sprawność energetyczną — stosunek uzyskanej z akumulatora energii do energii potrzebnej do jego ponownego naładowania;
— wskaźnik energetyczny — stosunek energii akumulatora do jego masy lub objętości. Wymienione nazwy, jak również, pozostałe użyte określenia zawiera norma PN-88/E-01004. Charakterystyczny przebieg napięcia wyładowania widać na rys. 12.6.
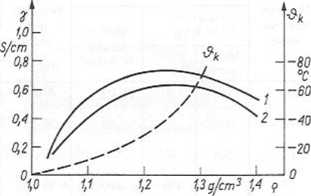
Rys. 12.5. Zależność parametrów elektrolitów od ich gęstości
1 — przewodności właściwej H2S04, 2 — przewodności właściwej KOH, >9k -- temperatury krzepnięcia H2S04 i KOH
U
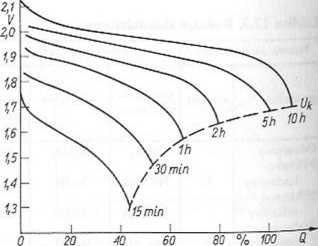
Rys. 12.6. Charakterystyki wyładowania akumulatorów trakcyjnych z dodatnimi płytami pancernymi o pojemności 100 A h: 10 h prądem 11,2 A, 10-godzinnym; 5 h — prądem 20 A, 5-godzinnym;
2 h prądem 40 A, 2-godzinnym; 1 h — prądem 66 A, 1-godzinnym; 30 min — prądem 106 A; 15 min — prądem 170 A
12.1. CHEMICZNE ŹRÓDŁA PRĄDU
s.cSS
2
n
Ol Ol _ —
2 I I
<s *>0» _' Ołcs
|
O e M |
O OJ |
00 | |||
|
o >. |
2" |
<s *>0» |
_ — oo ©_ 1 i |
O o S ^ - NO § | |
|
■o c o“ |
* |
_r Oj c-i o" |
2 = |
<* ™ c> |
n *-.Oł _' Oł <N
s?
o gd cn Ol ~
1 - co
“ I
r- w-i cc r--© o"
o S.O> NCł-
i i
o o
t*'. oo 7 ‘O ' OC no ! I t o' o' © o ■
fN CO
■5 Z 9 %
- S *£
o u
—
©„ 2 Oj »0> <n 0>—< *- oc
fN — CO
Cn f'
o o' o
o
CS Ol fN
o - O r- rs nOIn —
: _• WO © OC C"-
1 o' ©
.1 'i S ~ « 2 c s es s f3 o
§
S *
%<
•s§
2 S ? S
.2- E * g..2,
« ^ l: Z ft. Ł
o rt
II I
Ł
«-® « z > 2
i2
* C c/:
; bo >, !■-?. 8 : > os
8 s i >> —
I &
cg i oo I
3
1
2 :S o-§-
I I
-i ^
.EL cs S>j£
£ c M >io
i.„ I !s U'
•s.§| £?-5 .§ £. J2 > « c «
tł <S O V ^ O O.
00
I i i
^ 1 .2 S. c ... - o
o 2
>* cg

Wyszukiwarka
Podobne podstrony:
1tom306 12. ELEKTROCHEMIA 614 — bateria srebrowa Ag20
1tom308 12. ELEKTROCHEMIA 618 Akumulatory ołowiowe dzieli się wg zastosowania na rozruchowe (samocho
DSC01332 (12) ELEKTRONÓW W komórce transfer elektronów w reakcji redoks z donora na akceptor zachodz
Sumaryczna reakcja przebiega na obu elektrodach podczas procesu elektrolizy jest reakcja utleniania-
img104 (18) Znaczny jest też u dziecka w wieku 11-12 lat stopień kontrolowania reakcji emocjonalnych
skanuj0038 (12) PCR-RFLP - etapy: 1) reakcja PCR - powielenie badanego fragmentu&n
skanuj0341 (2) PHP i MySQL dla każdeg: PHP i MySQL dla każdeg: Rysunek 12.6. Zapytanie pobierające s
Skanuj 8 Elektrokardiografia (EKG) podczas pracy serca zachodzą w nim zmiany potencjałów elektryczny
s che 1H Miedź natomiast reaguje z kwasem azotowym^), ale jest to reakcja udenienift i redukcji. Rea
kinetyka chemiczna 2 półczynniki dobierz metodą C) Napisz równanie reakcji, jaka zachodzi w obu nacz
więcej podobnych podstron