Image51 (15)

189 Rozwiązania zadań ze zbioru "MENDLA"____
W3 = n.R.^.T2-nR -
T2 t2
T3 Ti
W3 = n • R • T3 - n • R • 1
T2
W ostatniej przemianie ochłodzono gaz zachowując stałą objętość, więc praca W4 = 0.
Ostatecznie praca W całego cyklu będzie:
W = Wi + W2 + W3 + W4
W = - n • R • (T2 - Ti) + 0 + n • R • T3 - n ■ R • + 0
• 2
W = n • R • (T1 - T2 + T3 - )
12
W=1 mol• 8,31 ^ J ■.. (300K- SOOK + 800K-
K■ mol 600K
W = 8,31p- 100/C
A
W = 831 J
Odp.: W tym cyklu nad gazem wykonano pracę 831 J.
Zadanie 691 str.138
Dane: Szukane:
S, m, Ti, p, M, Q, po, cv Ft = ? - siła tarcia
m — masa azotu M — masa odważnika
Fi, F2 — siły parcia azotu na tłok Q — ciężar odważnika F — siła parcia atmosferycznego na tłok
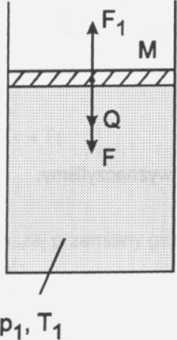
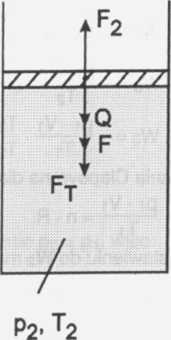
Z równowagi sił w II przypadku otrzymamy: F2 = Q + F + Ft /: S
ś
f2 q f fi
S " s + s + s
Z definicji ciśnienia wiadomo, że p = ^ , więc:
Fi F2 F
p1 ” S ’ P2~ S ' Po_S
Po podstawieniu pi, p2 i po do wcześniejszego równania wyznaczymy siłę tarcia Ft. Q _ Ft
/•s
P2 • S = Q + po • S + Ft Ft = P2-S-Po-S-Q Ft = S • (p2 - po) - Q
W równaniu nie znamy wartości p2, ale możemy je wyznaczyć. Ponieważ azot pobrał ciepło Q zachowując stałą objętość, więc:
Q = Cv ■ m • ńT i fŁ-B _> _ Pi_j2
Ti T2 Ti
oraz AT = T2 - Ti Po podstawieniu:
Q = cv • m • (T2-T1) /: cv • m
Przekształcając to równanie obliczymy T2.
Q
cv • m
T2 =
= T2-Ti
Q
cv • m
+ Ti
Wyznaczoną T2 podstawiamy do równania p2 =
P1 • (
Q
skąd p2 =
cv • m
+ Ti)
Pi
Ti
Q + cv • m • Ti
P2 =
Cv • m
P2 =
Pi -(Q + cv • m • Ti)
cv • m • Ti
Wreszcie P2 możemy podstawić do siły tarcia Ft
*pi -(Q + Cvm-Ti)
cv • m • Ti f Q *
FT = S • stąd Ft = S •
-Po
Pi
+ 1
-Po
- Q , -M -g
ale Q = Mg
Wyszukiwarka
Podobne podstrony:
Image5 (57) 90 Rozwiązania zadań ze zbioru "MENDLA Podobnie: T2 = Ti + AT Zgodnie z treścią zad
18469 Image45 (15) 177 Rozwiązania zadań ze zbioru "MENDLA 177 Rozwiązania zadań ze zbioru &q
18469 Image45 (15) 177 Rozwiązania zadań ze zbioru "MENDLA 177 Rozwiązania zadań ze zbioru &q
Image45 (15) 177 Rozwiązania zadań ze zbioru "MENDLA 177 Rozwiązania zadań ze zbioru "ME
Image48 (15) 183____Rozwiązania zadań ze zbioru "MENDLA"_ W przemianie B-C praca W2 = O, w
Image54 (16) 195 Rozwiązania zadań ze zbioru "MENDLA Ostatecznie pobrane ciepło jest równe: 195
Image56 (12) 199 Rozwiązania zadań ze zbioru "MENDLA" Sprawność silnika Carnota określona
Image5 (58) 64 Rozwiązania zadań ze zbioru "MENDLA V1(T) V2(T) temperatura jest stała TT, 3T(Za
Image50 (16) 187 Rozwiązania zadań ze zbioru "MENDLA" Objętość końcową V2 obliczymy korzys
Image52 (16) 191 Rozwiązania zadań ze zbioru "MENDLA Zadanie 692 str.138 Szukane: P2, Vi, V3 Da
więcej podobnych podstron