Maśliński4970

Zarówno czynniki wzrostu, błonowe białka receptorowe, jak i cytoplazma-tyczne oraz jądrowe białka regulatorowe (odpowiednio EGF, erbBl, ras oraz myc i fos) są kodowane przez protoonkogeny występujące we wszystkich prawidłowych komórkach, a których obecność i prawidłowa funkcja jest niezbędna do przenikania informacji ze środowiska do komórki oraz zapewnienia właściwych kontaktów międzykomórkowych.
Z danych doświadczalnych wynika, że zaktywowane (zmutowane) protoonkogeny uzyskują aktywność onkogenów, co przejawia się m.in. nadmiernym wytwarzaniem ich białkowych produktów i/lub zwiększonym wydzielaniem ich poza obręb komórki. Prowadzi to z kolei do wzmożonej transmisji sygnałów przez czynniki wzrostu z powierzchni do jądra komórki i stymulowania niekontrolowanej proliferacji, a w konsekwencji do rozwoju nowotworu.
Wśród onkogenów komórkowych (protoonkogenów) na szczególną uwagę zasługują te, które są odpowiedzialne za wytwarzanie białek (enzymów) o podstawowym znaczeniu dla procesów wzrostu i rozwoju komórki, przede wszystkim dotyczy to fosforylacji białek, której zaburzenia stanowią główny mechanizm naruszenia regulacji cyklu komórkowego, co następuje w proliferacji nowotworowej. W fosforylacji białek istotną rolę odgrywają kinazy zależne od cyklin (ang. cyclin-dependent kinase - CDK). W onkologii klinicznej wykorzystuje się obecnie specyficzne inhibitory kinaz tyrozy-nowych (np. imatynib), które hamują ich zdolność do przenoszenia sygnału prolifera-cyjnego do jądra komórki, wstrzymują rozplem komórek nowotworowych i zwiększają ich apoptozę.
Biorąc pod uwagę typ kodowanego białka i jego lokalizację, można wyróżnić następujące grupy onkogenów (ryc. 17.3, tab. 17.3):
1. Onkogeny kodujące czynniki wzrostu.
2. Onkogeny sterujące wytwarzaniem białek receptorowych, zarówno tych o aktywności kinaz białkowych (ERBB, SIS, RET), jak i tych, które nie wykazują aktywności kinazy tyrozynowej (TGFR), bądź receptorów meta-botropowych - związanych z białkiem G. Do podstawowych białek z tej grupy należą kinazy białkowe. Większość z nich występuje w błonie komórkowej w pobliżu płytek kontaktowych, niektóre zaś (białka adapterowe, czyli niereceptorowe kinazy tyrozynowe, takie jak SRC i ABL) występują w cytoplazmie. Obecnie znanych jest ponad 100 kinaz białkowych. Wiele z nich odgrywa istotną rolę w regulacji wzrostu i różnicowania komórek.
3. Onkogeny kodujące białka cytoplazmatyczne biorące udział w przekazywaniu sygnałów mitogennych z błony komórkowej do jądra komórki, np. H-RAS, K-RAS i inne. Należą do stosunkowo najmniej poznanych, choć wytwarzane przez nie białka są białkami regulacyjnymi komórki.
4. Onkogeny kodujące białka jądra komórki o charakterze czynników trans* krypcyjnych, np. MYC, FOS, JUN. Wywierają one zasadniczy wpływ na ekspresję innych genów oraz transkrypcję RNA.
Duże nadzieje wiąże się obecnie z intensywnie prowadzonymi badaniami nad możliwością uzyskania takich polipeptydów, które blokowałyby na błonie komórkowej receptory dla czynników wzrostu, hamując w ten sposób ich stymulacyjny wpływ na proliferację komórek i proces nowotworzenia. Badania dotyczą m.in. blokerów dla TGF-fi, które mogłyby zahamować angiogenezę w guzie, doprowadzając do jego martwicy. Wyniki części z tych badań są na tyle obiecujące, iż znalazły praktyczne zastosowanie w leczeniu chorych na wybrane nowotwory, np. u części choiych na raka piersi z nadekspresją białka HER2/neu (białko błonowe z rodziny EGFR) stosuje się humanizowane przeciwciało skierowane przeciw temu receptorowi na powierzchni komórek rakowych.
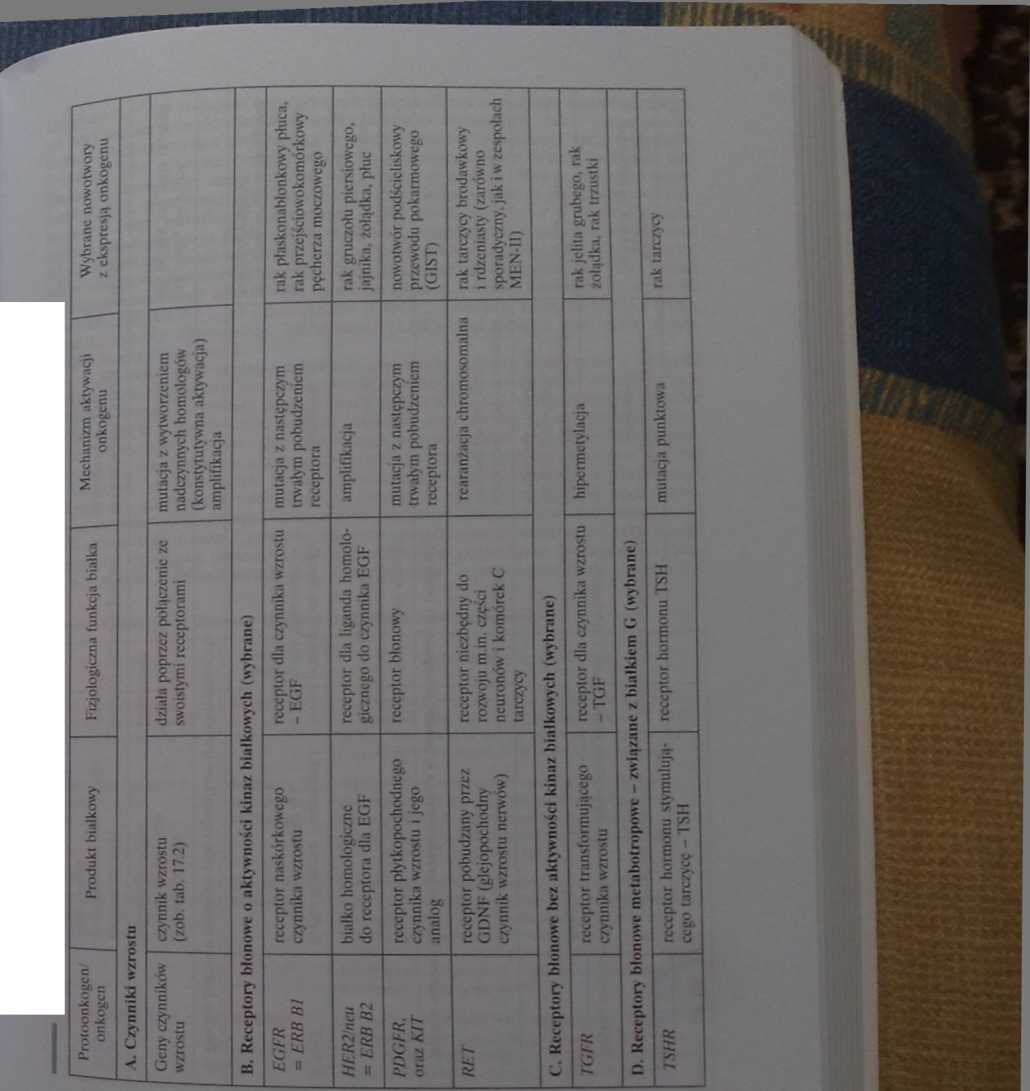
Tabela 17.3. Podział onkogenów i ich produktów białkowych występujących w nowotworach u człowieka
915
Wyszukiwarka
Podobne podstrony:
CCF20080410�003 Inne czynniki wzrostowe to interleukiny (IL-3, IL-9, IL-11) oraz czynnik wzrostowy n
Slajd22 (18) ACHONDROPLAZJA Przyczyną choroby są mutacje w genie FGFR3 (gen receptora czynnika wzros
Maśliński4971 Odrębny rozdział stanowią czynniki wzrostu specyficzne dla układu krwiotwórczego, ale
wewnątrztarczycowego niedoboru jodu, zwiększa się uwalnianie miejscowych czynników wzrostowych takic
IMAG0090 (5) Czynnik wzrostu, którego aktywność jest związana aktywacją receptora TrkA oraz NGF
Obecność receptora typu 2 dla ludzkiego naskórkowego czynnika wzrostu ocenia się w błonach komórek
Zmiany popytu mogą być efektem oddziaływania zarówno czynników rynkowych jak i nierynkowych; czynnik
skanuj0019 (10) Czynniki wzrostu lub spadku tpoHoki Najprawdopodobniej pozytywnie wpływają na nią ta
Hormonozależność Czynnik wzrostu Receptor czynnika wzrostu genów Onkogeny Synteza
Zdjęcie514 Część I) Zadanie 1. Jaki rodzaj cery źle znosi działanie zarówno czynników atmosferycznyc
więcej podobnych podstron