43935 skanuj0089 (15)

86 Ćwiczenia laboratoryjne z chemii żywności
A. Oznaczanie zawartości glukozy i fruktozy w miodzie metodą polarymetryczną
Zasada:
pomiar kąta skręcenia płaszczyzny polaryzacji przez substancje optycznie czynne znajdujące się w miodzie.
Odczynniki i aparatura:
- polarymetr
- roztwór glukozy o stężeniu 0,2 g/cm3
- roztwór fruktozy o stężeniu 0,2 g/cm3
- roztwór miodu o stężeniu 0,2 g/cm3
Wykonanie:
W celu przygotowania wyżej wymienionych roztworów należy do zlewki na 100 cm3 odważyć 10 g glukozy/fruktozy/miodu, a następnie naważkę rozpuścić w 50 cm wody destylowanej.
Po napełnieniu rurki polarymetrycznej badanym roztworem (glukozy, fruktozy, miodu) zmierzyć kąt skręcenia płaszczyzny polaryzacji.
Obliczenia:
1. a właściwe dla roztworu glukozy i roztworu fruktozy:
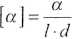
[a] - skręcalność właściwa,
a - skręcalność zmierzona, [°],
d - stężenie glukozy/fruktozy, [0,2 g/cm j,
/ - długość rurki polarymetrycznej, [1 dmj.
2. Stężenie glukozy i fruktozy w miodzie
Sumaryczna zawartość glukozy i fruktozy w miodzie - ok. 80% (tabela 2), czyli w naważce 10 g znajduje się 8 g glukozy i fruktozy.
d =f x/50
dgm = (8 - x)/50
am = [a]8><dgm + [a]fxdrm
am = [a]g x (8 -x) / 50+ [o]r * x/50
am x 50 = [a]g * (8 - x) + [a]f x x
amx 50= [a]g x 8 - [a]gx x + [<x]f x x
am x 50 - [a]g x 8 = - [a]g x x + [a]f x x
a m x 50 - [a]g x 8 = x x ([a]f- [a]g)
x = (am x 50 - [a]g x 8)/([a]r- [a]g)
drm - stężenie fruktozy w miodzie, [g/cm ] d - stężenie glukozy w miodzie, [g/cm ] am — skręcalność zmierzona dla miodu, [°]
[a] - skręcalność właściwa glukozy [a]r - skręcalność właściwa fruktozy
3. Zawartość procentowa glukozy i fruktozy w miodzie % fruktozy = x x 100/10 % glukozy = (8 - x) x 100/10
B. Oznaczanie kwasowości ogólnej Zasada:
zobojętnienie kwaśnych składników miodu mianowanym roztworem wodorotlenku potasu wobec fenoloftaleiny, z wyłączeniem miodów o barwie ciemnej, które miareczkować potencjometrycznie.
Aparatura i sprzęt:
- kolba stożkowa poj. 150 cm3
- biureta
- pH-metr
Odczynniki:
- fenoloftaleina 1%; - wodorotlenek potasu, roztwór mianowany 0,1 mol/dm1 Wykonanie:
10 g miodu odważyć z dokładnością do 0,02 g i rozpuścić w 50 cm3 wody destylowanej w kolbie stożkowej o poj. 150 cm3. Do roztworu dodać 2-3 krople fenoloftaleiny i szybko miareczkować z biurety 0,1 -molowym roztworem wodorotlenku potasu do różowego zabarwienia, utrzymującego się przez około 30 sekund.
W przypadku miareczkowania potencjometrycznego przygotowany jak poprzednio roztwór miareczkować wobec pH-metru do momentu osiągnięcia w miareczkowanym roztworze pH 8,3.
Na podziałce biurety odczytać ilość zużytego wodorotlenku sodowego. Liczba ta jest stopniem kwasowości miodu, wyrażoną ilością cm I-molowego roztworu wodorotlenku potasu potrzebnego do zobojętnienia 100 g miodu.
Wyszukiwarka
Podobne podstrony:
17828 skanuj0090 (15) 88 Ćwiczenia laboratoryjne z chemii żywności C. Oznaczanie zawartości cukrów b
skanuj0091 (14) 90 Ćwiczenia laboratoryjne z chemii żywności Słjliczanie wyniku: Obliczyć średnią a
skanuj0092 (14) 92 Ćwiczenia laboratoryjne z chemii żywności E. Wykrywanie enzymów amylolitycznych w
skanuj0087 (16) 82 Ćwiczenia laboratoryjne z chemii żywności Zasady pomiarów polarymetrycznych Świat
45479 skanuj0093 (14) 94 Ćwiczenia laboratoryjne z chemii żywności 5. Omówić budow
76250 skanuj0085 (16) 78 Ćwiczenia laboratoryjne z chemii żywności i górskich. Miody spadziowe natom
33009 skanuj0088 (16) 84 Ćwiczenia laboratoryjne z chemii żywności Fruktoza (cukier owocowy) jest mo
skanuj0086 (16) o Ćwiczenia laboratoryjne z chemii żywności v tzw. okresach bezpożytkowych. Podany p
więcej podobnych podstron