Ćwiczenie nr 18
Temat: Pomiar ciepła właściwego cieczy o stałym ciśnieniu metodą elektryczną.
I. PODSTAWY TEORETYCZNE
Definicja ciepła właściwego w danej temperaturze T pod stałym ciśnieniem:
![]()
Liczbowo C oznacza ilość ciepła potrzebnego do ogrzania 1 g danego ciała o 1 K. Mierzy się ją w kaloriach na 1g i na 1 K lub w Joulach na kg i na K.
Przyrost ciepła jest inaczej mówiąc przyrostem energii wewnętrznej U ciała wyrażonej wzorem:
![]()
Gdzie wskaźnik n przy Ek i Ep oznacza sumowanie rozciągnięte na n cząsteczkach ciała.
Między przyrostem ciepła ciała, a przyrostem energii wewnętrznej ciała zachodzi związek równoważności:
![]()
Przyrost ciepła Q dostarczonego zależy (przy zmianach temperatury) od:
a)masy ciała m
b)przyrostu temperatury
c)rodzaju ciała
Znajduje to wyraz we wzorze kalorymetrycznym :
![]()
gdzie
c oznacza średnie ciepło właściwe ciała.
Z tego wzoru wyznaczamy wzór na c:
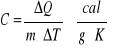
Pojemność cieplną danego ciała lub inaczej , jego równoważnikiem wodnym W nazywamy ilość ciepła potrzebną do ogrzania całej masy o 1 K. Wyraża się to wzorem:
![]()
II. OPIS PRZEPROWADZONEGO DOŚWIADCZENIA
Pomiary ilości ciepła przeprowadzamy w odpowiednio skonstruowanych naczyniach kalorymetrycznych, które zmniejszają do minimum straty ciepła, związane z ucieczką na zewnątrz lub z wnikaniem do wewnątrz. Do naszego doświadczenia użyliśmy kalorymetru wodnego. Składa się on z dwu cylindrycznych naczyń metalowych umieszczonych jedno wewnątrz drugiego. Naczynie wewnętrzne spoczywające na korkach lub innych izolatorach termicznych, ze względu na swe dobre przewodnictwo cieplne - metal - bierze udział w wymianie cieplnej w całej swej masie. Naczynie zewnętrzne o ściankach wypolerowanych zabezpiecza od strat na promieniowanie. W górnej pokrywce, stanowiącej uzupełnienie osłony termicznej, znajdują się otwory na wprowadzenie do wnętrz termometru T i grzałki oporowej.
III. SCHEMAT UKŁADU POMIAROWEGO
IV. WYPROWADZENIE WZORU ROBOCZEGO
Wzór na ciepło Joule'a Q1 wydzielone podczas przepływu prądu ma postać:
![]()
Wzór na ciepło wydzielone podczas doświadczenia przez kalorymetr (straty spowodowane np. promieniowaniem itp.) ma postać:
![]()
Gdy odejmiemy starty ciepła spowodowane budową kalorymetru (rodzaj materiału, struktura itp.) od ciepła wydzielonego przez spiralę grzejną otrzymamy wzór na ciepło właściwe:
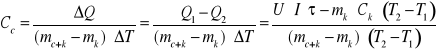
gdzie :
mk - masa pustego i czystego kalorymetru
mc+k - masa kalorymetru z daną cieczą
T1-T2 - różnica temperatur
V. OBLICZENIA I SZACOWANIE NIEPEWNOŚCI
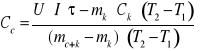
Dla uproszczenia przyjmujemy:
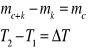
wówczas:
![]()
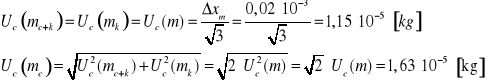
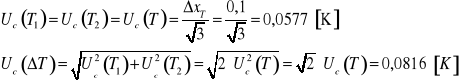
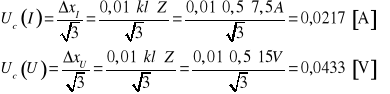
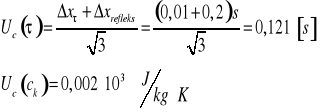
Masa wewnętrznego kalorymetru ![]()
Natężenie prądu płynącego przez grzałkę ![]()
Napięcie na grzałce ![]()
Ciepło właściwe kalorymetru ![]()
a) POMIAR nr 1
Masa kalorymetru wypełnionego badaną cieczą ![]()
Temperatura początkowa ![]()
Temperatura końcowa (po podgrzaniu) ![]()
Czas ogrzewania ![]()
Przyrost temperatury ![]()
Masa cieczy ![]()
![]()
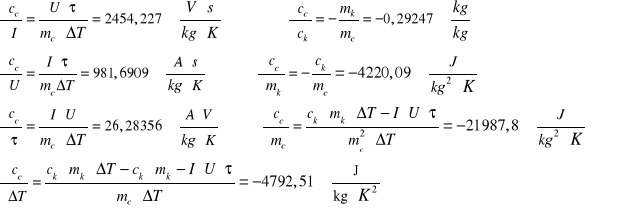
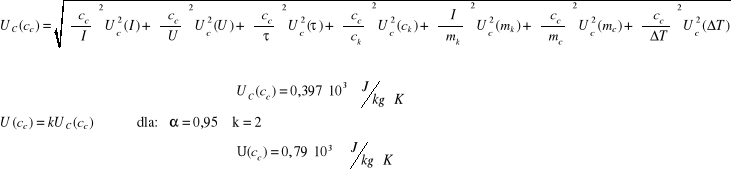
![]()
b) POMIAR nr 2
Masa kalorymetru wypełnionego badaną cieczą ![]()
Temperatura początkowa ![]()
Temperatura końcowa (po podgrzaniu) ![]()
Czas ogrzewania ![]()
Przyrost temperatury ![]()
Masa cieczy ![]()
![]()
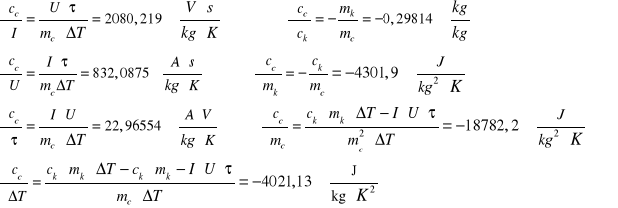
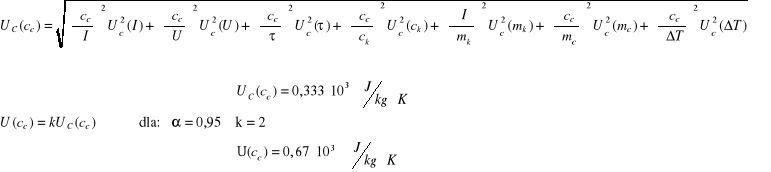
![]()
c) POMIAR nr 3
Masa kalorymetru wypełnionego badaną cieczą ![]()
Temperatura początkowa ![]()
Temperatura końcowa (po podgrzaniu) ![]()
Czas ogrzewania ![]()
Przyrost temperatury ![]()
Masa cieczy ![]()
![]()
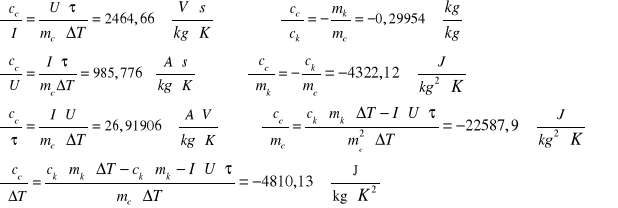
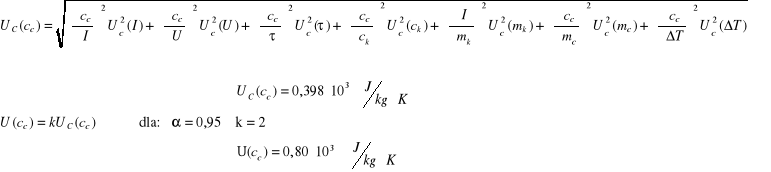
![]()
VI. UWAGI I WNIOSKI
W danym doświadczeniu występują błędy pomiaru, przypadkowe (spowodowane niedokładnością urządzeń pomiarowych) oraz błędy systematyczne. Błąd systematyczny w tym doświadczeniu wynika ze strat cieplnych kalorymetru. Starty te zawsze występują mimo nawet najdokładniejszego przygotowania urządzenia. Ponadto występuje też błąd w wyniku odczytania temperatur.
Po każdym pomiarze po odłączeniu zasilania od układu zaobserwowaliśmy skok temperatury o ok. 0,5 stopnia Celsjusza.
Przyczyną dużej różnicy pomiędzy pomiarami, może być niedokładne zmierzenie wagi kalorymetru napełnionego cieczą przed każdym pomiarem.
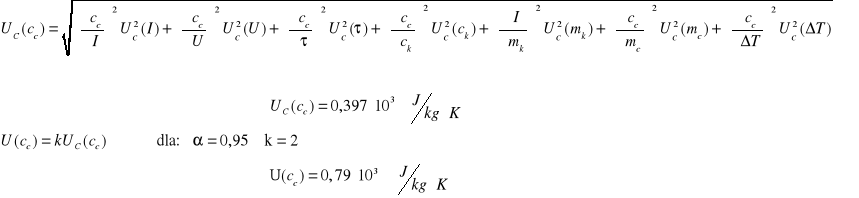
![]()
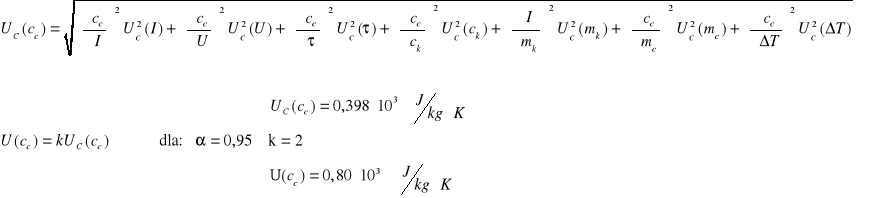
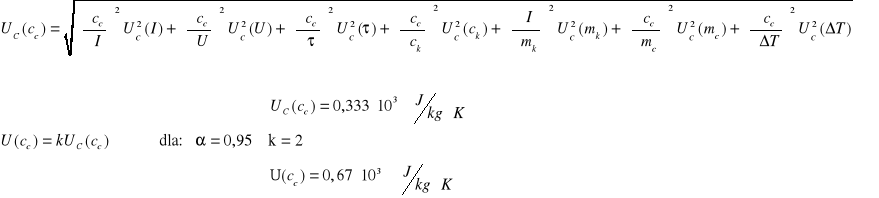
Wyszukiwarka
Podobne podstrony:
18, Cw 18 - Pomiar ciepla wlasciwego cieczy w stalym cisnieniu metoda elektryczna, Jacek Konikowski
WYZNACZANIE CIEPŁA WŁAŚCIWEGO CIECZY METODĄ ELEKTROKALORYMETRU
Wyznaczanie ciepła własciwego cieczy
SPR26, Studia, Pracownie, I pracownia, 26 Wyznaczanie ciepła właściwego ciał stałych metodą kaloryme
Wyznaczenie ciepła własciwego, Studia, Pracownie, I pracownia, 26 Wyznaczanie ciepła właściwego ciał
26 Wyznaczanie ciepła właściwego ciał stałych metodą kalorymetryczną G Szcześniak
, chemia fizyczna, wyznaczanie ciepła parowania cieczy z pomiarów prężności pary metodą izoteniskopo
Wyznaczanie ciepla wlasciwego cial stalych metoda kalorymetryczna
C5 Wyznaczanie ciepła właściwego metodą klorymetryczną
Wyznaczanie ciepła właściwego powietrza metodą rozładowania, Studia, Pracownie, I pracownia
Laboratorium Podstaw Fizyki spr( Wyznaczanie ciepła właściwego ciał stałych metodą kalorymetryczną
38 Oznaczanie ciepła właściwego cieczy metodą kalometryczną
Fizyka laboratorium 4?danie ciepła właściwego cieczy i ciał stałych
wyznaczanie Ciepła właściwego ciał stałych - 1
Wyznaczanie ciepła właściwego ciał stałych, Automatyka i Robotyka Rok I
Ćwiczenie 18, Wyznaczanie stosunku Cp/Cv dla powietrza metodą Clémenta-Desormesa
Wyznaczanie ciepła właściwego ciał stałych, Automatyka i Robotyka Rok I
Ćwiczenie 18, Wyznaczanie stosunku Cp/Cv dla powietrza metodą Clémenta-Desormesa
wyznaczanie ciepła właściego ciał stałych, Transport i Logistyka (AM) 1 (semestr I), Fizyka, fiza la
więcej podobnych podstron