11812
|
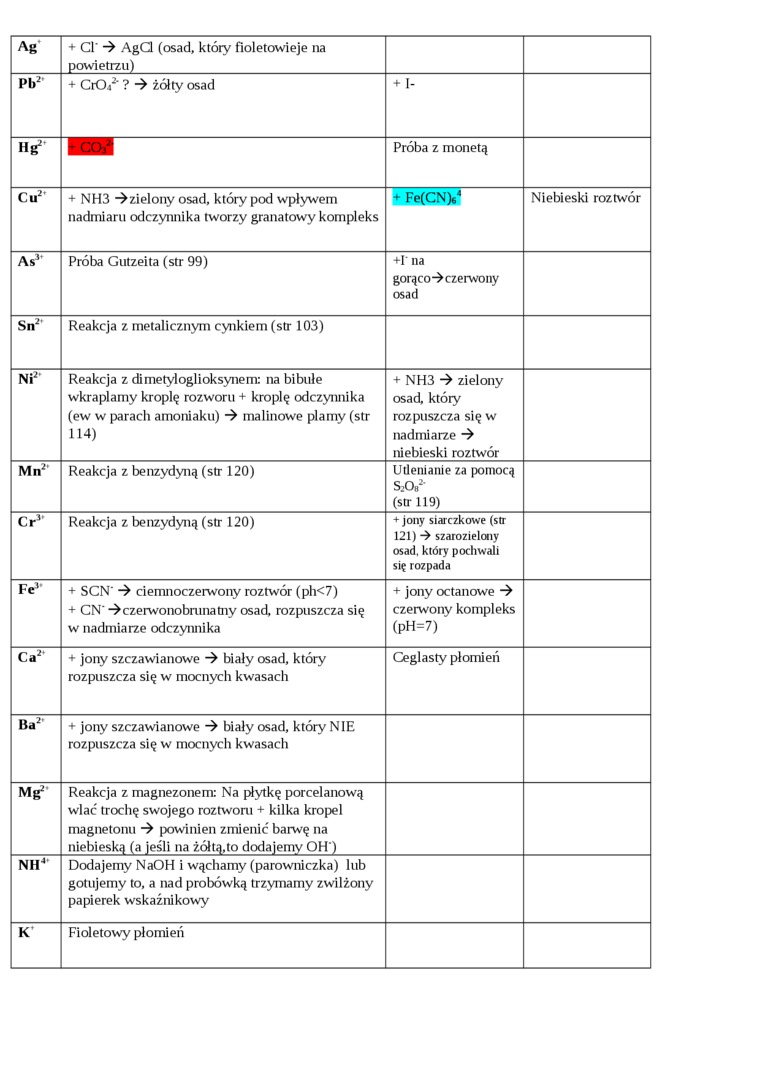
Ag |
+ Cl' -> AgCl (osad, który fioletowieje na powietrzu) | ||
|
Pb2 |
+ CrOj2' ? żółty osad |
+ 1- | |
|
Hg2 |
ta* |
Próba z monetą | |
|
Cu2 |
+ NH3 -dzielony osad, który pod wpływem nadmiaru odczynnika tworzy granatowy kompleks |
|Fe(CNV |
Niebieski roztwór |
|
As3' |
Próba Gutzeita (str 99) |
+1* na gorąco-> czerwony osad | |
|
Sn2 |
Reakcja z metalicznym cynkiem (str 103) | ||
|
Ni2' |
Reakcja z dimetyloglioksynem: na bibule wkraplamy kroplę rozworu + kroplę odczynnika (ew w parach amoniaku) -> malinowe plamy (str 114) |
+ NH3 zielony osad, który rozpuszcza się w nadmiarze -> niebieski roztwór | |
|
Mn2 |
Reakcja z benzydyną (str 120) |
Utlenianie za pomocą S;082' (str 119) | |
|
Cr3 |
Reakcja z benzydyną (str 120) |
+ jony siarczkowe (str 121) -> szarozielony osad. który pochwali się rozpada | |
|
Fe3’ |
+ SCN' ciemnoczerwony roztwór (ph<7) + CN' ->czerwonobrunatny osad, rozpuszcza się w nadmiarze odczynnika |
+ jony octanowe -> czerwony kompleks (pH=7) | |
|
Ca2 |
+ jony szczawianowe -> biały osad, który rozpuszcza się w mocnych kwasach |
Ceglasty płomień | |
|
Ba2 |
♦ jony szczawianowe biały osad, który NIE rozpuszcza się w mocnych kwasach | ||
|
Mg2 |
Reakcja z magnezonem: Na płytkę porcelanową wlać trochę swojego roztworu + kilka kropel magnetonu powinien zmienić barwę na niebieską (a jeśli na żółtą,to dodajemy OH ) | ||
|
NHJ |
Dodajemy NaOH i wąchamy (parowniczka) lub gotujemy to, a nad probówką trzymamy zwilżony papierek wskaźnikowy | ||
|
K |
Fioletowy płomień |
Wyszukiwarka
Podobne podstrony:
Ag4 + Cl* *4 AgCl (osad, który fioletowieje na powietrzu) Pb2* + CrO^2* ? *4 żółty osad +
CCF20111010�027 69 Przebieg reakcji: 69 Ag + Cl" = AgCl 2AgT + CrO^” = Ag2Cr04 W oznaczeniu prz
Czy wytrąci się osad jeżeli zmieszano ról Ag +Cl~ p±AgCI-l (R.1.) **-*,-££ (E- 5.) Rów now aaa ciało
40962 str (155) 5. Który ze składników powietrza działa najbardziej niszcząco na s
skan0285 288 Elektrochemia zatem AG0(Cl~) =AG° + zfG°(AgCl) = -21,46- 109,5 =-131,0 kJ • mor1.
70 (91) — (NH4)2Fe(S04)2-6H20, zwany solą Mohra, który ze względu na swą trwałość na powietrzu znajd
TABLICA ROZPUSZCZALNOŚCI Ag* Cl Osad nierozpuszczalny w H^O, rozpuszczalny w kwasach Osad wytrąca
0000041 (11) układem, który reaguje na (-r) AG, jest trzustka (oraz układ przywspółczulny). Wydziela
75181 skan0285 288 Elektrochemia zatem AG0(Cl~) =AG° + zfG°(AgCl) = -21,46- 109,5 =-131,0 kJ • mor1.
zakres podstawowy S poioU lud poiionnn motu to kofeiny czynnik. który wpływa na zmuny Mnpnalury
img109 (16) .//2.ySlnndhrdowa entalpia swobodna tworzenia AgCl = -110 kj AG dla reakcji: 2 AgCl 2 Ag
arkusz2 6 ZADANIE 17. Obliczyć ruchliwości jonów Ag+ i Cl’, wiedząc, że graniczne przewodnictwo molo
więcej podobnych podstron